Скрининг рака мочевого пузыря: обоснование, ограничения, цели и перспективы
Screening for bladder cancer: rationale, limitations, whom to target, and perspectives.
Larré S, Catto JW, Cookson MS, Messing EM, Shariat SF, Soloway MS, Svatek RS, Lotan Y, Zlotta AR, Grossman HB.
Robert Debré Teaching Hospital, Department of Urology, University of Reims, Reims, France.
Рак мочевого пузыря (РМП) является четвертой по распространенности формой рака у мужчин. Выживаемость при этой болезни за последние 25 лет не улучшилась. Популяционный скрининг теоретически предоставляет лучшие возможности для улучшения исходов агрессивного РМП.
Цель
Проанализировать современную научную литературу относительно эффективности и целесообразности проведения скрининга рака мочевого пузыря.
Доказательная база
Ученые провели несистематический обзор, ограниченный англоязычными статьями и ключевыми словами «опухоль мочевого пузыря», «массовый скрининг», «обязательное тестирование» и «раннее выявление рака». Было обнаружено 184 статьи из которых 22 соответствовали критериям исследования.
Синтез доказательств
Не было обнаружено доказательств уровня 1 (полученных из рандомизированных контролируемых исследований [РКИ]) относительно влияния скрининга на выживание при РМП или стадий опухоли.
Ни в одном из исследований не оценивали диагностическую ценность маркеров в моче в контексте скрининга. Две серии «случай-контроль» предположили преимущества скрининга в выживаемости пациентов, а третий обнаружил недостоверный полезный факт в пользу скрининга. Два исследования предположили недооценку стадии РМП на момент постановки диагноза.
Другие отчеты пришли к выводу, что большинство обнаруженных скринингом опухолей были высокодифференцированными и что нынешнее тестирование мочи не может обнаружить все опухоли. Скрининг, вероятно, будет полезным в группах высокого риска с использованием экономичных высокопроизводительных мочевых биомаркеров. Было отмечено недостаточное количество данных для составления эффективного протокола скрининга.
Выводы
Хотя скрининг РМП теоретически возможен в популяции высокого риска, в настоящее время недостаточно данных, чтобы рекомендовать его из-за недостатка данных для составления эффективного протокола скрининга с выбором соответствующего контингента; отсутствия точных и экономически эффективных мочевых маркеров, способных различить высоко- и низкодифференцированный рак. Необходимы совершенствовать оценку мочевых биомаркеров для улучшения результатов, полученных с помощью КТ.
Рак мочевого пузыря
Предполагается, что в 2004 году в США заболеет раком мочевого пузыря 60240 человек (44640 мужчин и 15600 женщин).
За период с 1975 по 1987 г. был отмечен рост заболеваемости раком мочевого пузыря.
У белых рак диагностируется чаще, чем у черных.
Факторы риска при раке мочевого пузыря
Наличие факторов риска еще не означает, что обязательно возникнет рак. У многих больных раком мочевого пузыря вообще не было выявлено никаких факторов риска. Однако знать о наличии факторов риска необходимо, так как некоторые из них можно изменить или периодически проходить обследование для раннего выявления заболевания.
Влияние профессиональных факторов.
Некоторые химические вещества, использующиеся в промышленности, могут влиять на возникновение рака мочевого пузыря. Например, ароматические амины (бензидин и бетанафтиламин), иногда используемые в красильной промышленности, могут вызывать рак мочевого пузыря.
Повышенный риск рака мочевого пузыря наблюдается у работников ряда промышленных производств (резиновое, кожное, текстильное, печатное и др).
Сочетание курения и факторов, связанных с профессиональной деятельностью, могут усиливать влияние на развитие рака мочевого пузыря.
У белых рак мочевого пузыря возникает в 1,5 раза чаще, чем у афроамериканцев. Причина этого не ясна. У азиатов частота развития рака этой локализации самая низкая.
С возрастом риск рака мочевого пузыря повышается. Средний возраст выявления рака мочевого пузыря составляет 68-69 лет.
Мужчины болеют раком мочевого пузыря в 2-3 раза чаще женщин.
Хроническое воспаление мочевого пузыря.
Мочевая инфекция, наличие камней в почках и мочевом пузыре и другие причины хронического раздражения мочевого пузыря связывают с раком мочевого пузыря (особенно плоскоклеточным раком), но они не обязательно приводят к развитию рака этого органа.
Шистозомы (червь-паразит), попадающие в мочевой пузырь, повышают риск развития рака этой локализации.
Индивидуальный анамнез рака мочевого пузыря.
Рак может развиваться в различных отделах мочевого пузыря. Даже после полного удаления опухоли сохраняется высокий риск возникновения рака в другой части пузыря.
Поэтому больные раком мочевого пузыря требуют тщательного наблюдения и обследования. У людей, в семье которых был или имеется рак мочевого пузыря, риск рака данной локализации повышен.
Врожденные дефекты мочевого пузыря.
До рождения ребенка существует связь между пупком и мочевым пузырем. Это соединение (урахус) в норме после рождения исчезает. При сохранении части урахуса из него может возникнуть рак.
Другим врожденным дефектом является сохранение отверстия в передней брюшной стенке при незаращении кожи, мышц и соединительной ткани, расположенных перед мочевым пузырем. Это приводит к хроническому воспалению мочевого пузыря и в 400 раз повышает вероятность развития рака мочевого пузыря (аденокарциноме).
Противоопухолевые препараты циклофосфамид (цитоксан) и ифосфамид повышают риск развития рака мочевого пузыря. Препарат месна, применяющийся вместе с этими препаратами, защищает слизистую оболочку пузыря от раздражения и снижает риск развития рака мочевого пузыря.
Попадание мышьяка в питьевую воду повышает риск рака мочевого пузыря.
Профилактика рака мочевого пузыря
Избегайте воздействия химических веществ на производстве.
Если Вы имеете дело с химическими веществами под названием ароматические амины, то следуйте инструкциям по безопасности. Обычно эти вещества используются при производстве резиновых изделий, кожи, печатных материалов, текстиля и красок.
Пейте много жидкости.
Потребление большого количества жидкости может снизить риск развития рака мочевого пузыря. Это приводит к более частому мочеиспусканию и разбавлению канцерогенных веществ в моче, а также ограничивает время контакта этих веществ со слизистой оболочкой органа.
Брюссельская и цветная капуста могут снизить риск развития рака мочевого пузыря. Эти овощи содержат фермент, который защищает клетки и предотвращает их превращение в опухолевые клетки.
Возможно ли раннее выявление рака мочевого пузыря?
Иногда рак мочевого пузыря можно обнаружить на ранних стадиях, что повышает вероятность успешного лечения.
Скрининговые исследования применяются с целью выявления рака мочевого пузыря у людей, не имеющих никаких симптомов болезни и у которых ранее не было рака этой локализации.
Обычно скрининг рака мочевого пузыря не проводится, за исключением случаев с выраженными факторами риска (больной ранее лечился по этому поводу; наличие врожденных дефектов мочевого пузыря, контакт с некоторыми химическими веществами). Скрининг заключается в обследовании, включающем анализ мочи или цистоскопию.
Наличие крови в моче или нарушение привычного мочеиспускания могут быть признаками рака мочевого пузыря. Другими признаками могут быть учащенное мочеиспускание или позывы на мочеиспускание.
И хотя эти симптомы могут быть вызваны другими заболеваниями, не игнорируйте их. Необходимо срочно обратиться к врачу.
При подозрении на рак мочевого пузыря будет предложено обследование.
Анамнез и обследование. Врач расспросит о жалобах и уточнит возможные факторы риска.
Цистоскопия. С помощью тонкой трубки, снабженной осветителем (цистоскопа), врач осмотрит мочевой пузырь и при обнаружении подозрительного участка или опухоли возьмет кусочек ткани для исследования (биопсия).
Анализ мочи. При этом исследовании моча или клетки, «вымытые» из мочевого пузыря, изучаются под микроскопом для выявления опухоли или предопухолевых заболеваний.
Бактериологическое исследование мочи позволяет выявить инфекцию, которая может давать симптомы, похожие на рак мочевого пузыря.
Биопсия. Во время цистоскопии берется кусочек ткани для исследования под микроскопом. На основании этого можно судить о наличии рака и его типе.
Изучение маркеров опухолей мочевого пузыря. Исследуются некоторые вещества, выделяемые раковыми клетками в мочу. Однако этот метод используется в основном у больных с уже выявленной опухолью.
Методы визуализации (получения изображения) применяются для получения дополнительной информации об опухоли и ее распространенности. К ним относятся: внутривенная пиелография, компьютерная томография (КТ), магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ), сканирование костей и др.
Лечение рака мочевого пузыря
При лечении больных раком мочевого пузыря применяются хирургический, лучевой, лекарственный и иммунологический методы. Вопрос о лечении решается на основании стадии (степени распространения) заболевания.
ОПЕРАТИВНОЕ ЛЕЧЕНИЕ.
ЛУЧЕВОЕ ЛЕЧЕНИЕ.
При таком методе используется как наружное, так и внутреннее облучение, когда радиоактивный материал вводится непосредственно в опухоль.
Лучевая терапия помогает уничтожить опухоль или сократить ее размеры, что облегчает оперативное вмешательство.
После выполнения частичного удаления мочевого пузыря проведение дополнительного облучения и химиотерапии может дать возможность избежать более радикальной операции.. Облучение, кроме того, позволяет уменьшить симптоматику при распространенном раке.
Побочные явления лучевой терапии (раздражение кожи и мочевого пузыря, тошнота, жидкий стул, слабость) проходят после завершения лечения.
ХИМИОТЕРАПИЯ.
Данный метод лечения показан у больных с распространенным раком. Обычно препараты вводятся в вену или назначаются внутрь. В некоторых случаях противоопухолевые препараты вводятся внутрь мочевого пузыря, однако такой метод показан лишь больным с ранними стадиями рака.
Побочные явления химиотерапии (тошнота, рвота, потеря аппетита, облысение, язвы во рту, повышенная кровоточивость) постепенно проходят после окончания лечения.
ВНУТРИПУЗЫРНАЯ ИММУНОТЕРАПИЯ.
При этом методе чаще всего используется вакцина БЦЖ, применяемая для вакцинации против туберкулеза. Введение вакцины в мочевой пузырь приводит к активизации иммунной системы организма в ее борьбе с опухолевыми клетками. Лечение назначается обычно 1 раз в неделю в течение 6 недель.
В ряде случаев для этой цели применяется интерферон.
Что происходит после окончания лечения рака мочевого пузыря?
После завершения всего лечения рекомендуется динамическое наблюдение и обследование с целью возможного выявления рецидива (возврата) рака или диагностики новой опухоли в мочевой системе.
Обычно после осмотра больного назначают исследование мочи, крови, цистоскопию и рентгенологические методы.
Если Вы курили, то прекратите.
Это улучшит Ваше здоровье и снизит риск возникновения другого вида рака.
Мероприятия 2022 года
Архив мероприятий
Противораковое общество РОССИИ создано по инициативе ученых-онкологов и главных врачей онкологических диспансеров, представляющих более 50 регионов России, с целью претворения в жизнь программы профилактики рака в России
Диагностика и скрининг рака мочевого пузыря. Современный подход
Московский государственный университет им. М.В. Ломоносова
Научно-исследовательский институт урологии, г. Москва
Рак мочевого пузыря (РМП) встречается примерно в 2-5% всех новообразований. В структуре онкологической заболеваемости он занимает седьмое место. Опухоли мочевого пузыря составляют 70% новообразований органов мочевого тракта и около 4% всей онкологической патологии.
Заболеваемость раком мочевого пузыря ежегодно возрастает, особенно в индустриально развитых странах. Вместе с тем результаты лечения больных имеют лишь незначительную тенденцию к улучшению. Это связано со склонностью опухоли к рецидивированию (частота рецидивов после органосохраняющих операций достигает 50—90%) и к первичной множественности поражения (2 очага и более). По данным официальной статистики Минздравсоцразвития за 2010 г. в РФ было зарегистрировано 13 562 больных с раком мочевого пузыря, при этом В России на долю рака мочевого пузыря приходится 4,5% всех злокачественных новообразований. У 60% пациентов рак мочевого пузыря выявляется на I-II стадии, а у 11,3% на IV стадии. 23% всех пациентов с впервые выявленным раком мочевого пузыря умирают в течение первого года с момента выявления рака. Показатель смертности рака мочевого пузыря составляет 8,2%, что составляет 10–е место.
Одним из наиболее значимых факторов прогноза после стадии заболевания, по данным большинства исследователей, является степень дифференцировки опухоли (G) [15]. Существуют критерии для оценки степени дифференцировки различных гистологических вариантов рака определенных локализаций. Уротелиальная карцинома характеризуются структурной и ядерной атипией различной степени выраженности, которая оценивается по шкале от 1 до 3, поскольку степень прогрессии значительно отличается для каждой из трех степеней. Градация опухолей неоднородной структуры (с участками различной степени диффреренцировки) определяется по наименее дифференцированным участкам, т.е. наивысшей степени анаплазии (G), при этом за последние два десятилетия градация степени анаплазии многократно подвергалась изменениям, но тем не менее исследователи и врачи до сих пор пользуются следующей классификацией:
Несмотря на то, что существует тесная связь между категориями TNM, G и выживаемостью больных, эта классификационная система не позволяет учесть динамические характеристики злокачественного процесса, от которых зависит его потенциальная агрессивность [2]. Поэтому в последние годы предпринимаются многочисленные попытки выявления самостоятельных иммуногистохимических (ИМГ) факторов прогноза рака мочевого пузыря.
Ультразвуковое исследование является важным этапом как в уточнении степени распространенности рака мочевого пузыря, так и при динамическом наблюдении [13]. Такие преимущества метода как доступность, безболезненность и отсутствие лучевой нагрузки позволяют проводить многократные исследования при динамическом наблюдении. В целом точность трансабдоминального УЗИ, как самого распространенного варианта УЗИ, составляет 80%, чувствительность – 86%, специфичность – 63%, чувствительность УЗИ определяется также стадией процесса, и она выше на поздних стадиях заболевания. Использование трансабдоминального УЗИ, а также распространенных ректальных и вагинальных датчиков многие специалисты, занимающиеся диагностикой в онкоурологии, тем не менее считают недостаточно эффективными [14].
КТ и МРТ используются для определения степени инвазии опухоли, определения метастазирования. Точность КТ для определения стадии 60-85%, в целом эффективность КТ в определении стадии опухолевого процесса низкая. МРТ сочетает в себе лучшие свойства УЗИ и КТ. Точность при определении распространения опухолевого процесса составляет от 73% (Т3а-b) до 100% (при Т4).
Основным методом диагностики рака мочевого пузыря является цистоскопия, которая позволяет непосредственно визуализировать опухоль. При этом цистоскопия позволяет одномоментно выполнить резекцию мочевого пузыря (по показаниям) или взять материал для гистологического исследования. Постановка диагноза невозможна без морфологической верификации. Цитологическое исследование позволяет правильно установить диагноз в 70-99% случаев, но отрицательный результат не исключает наличия опухоли. Специфичность метода 95-100%, чувствительность 40-51%. Цитологический метод особенно ценен для малодифференцированных опухолей и рака in situ.
Комплексное обследование способно выявлять рак мочевой пузыря на ранней стадии (I по TNM). В качестве методов уточняющей диагностики для определения глубины инвазии опухоли мочевого пузыря преимущественно используют компьютерную томографию, магнитно-резонансную томографию и ультразвуковое исследование датчиками частотой 20 МГц и более [5, 6, 13]. Однако приоритетной задачей диагностики является раннее выявление опухоли. Перечисленные методы не всегда позволяют это сделать на ранней стадии, то есть не все эти методы подходят для скрининга населения. Метод ультразвуковой диагностики и исследование крови на маркеры опухолевого роста представляются наиболее подходящим для скрининга. В настоящий момент разрабатываются новые методы диагностики, подходящие для скрининга. В частности, существует метод регистрации сопротивления электрического тока, пропускаемого через малигнизированные ткани. Было установлено, что высокое сопротивление регистрируется в участках локализации опухолевой ткани. Электрическая спектроскопия является малоинвазивным высокочувствительным методом, позволяющим определить опухоль уже на I стадии [2].
Другим новым направлением скрининга РМП является определение метилированных аллелей генов опухолевых клеток в образце мочи. В настоящее время было проведено исследование, в котором моча 175 пациентов с раком мочевого пузыря была исследована с помощью полимеразной цепной реакции (ПЦР) на наличие метиленовых остатков аллелей 9 генов (APC, p14ARF, CDH1, GSTP1, MGMT, CDKN2A, RARβ2, RASSF1A, и TIMP3). Исследователи доказали, что специфичность этого метода составляет 100%, чувствительность – 69%, что позволяет определить наличие опухоли задолго до появления рентгенологических признаков [3].
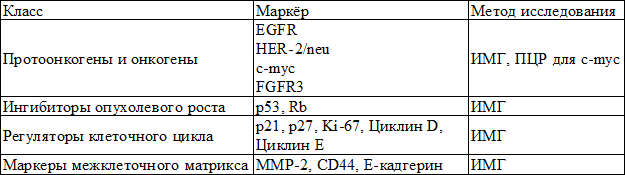
Современным направлением в совершенствовании диагностики рака мочевого пузыря является исследование иммуногистохимических маркеров. Иммуногистохимическое исследование биопсийного материала – это основной прорыв в области молекулярной медицины за последнее десятилетие. Данное исследование проводится во многих центрах мира в обязательном рутинном порядке. Исследование иммуногистохимических маркеров является процедурой, позволяющей определить наличие опухоли, злокачественный потенциал и прогноз, что является перспективным методом диагностики и дополнением к вышеперечисленным методам. Кроме того, достоинством этого метода может быть высокая специфичность и чувствительность [2]. Однако существенным недостатком является то, что этот метод нельзя использовать для скрининга, так как для исследования берется биопсийный материал. Немаловажную роль иммуногистохимическое исследование играет и в уточняющей диагностики. Иммуногистохимические маркеры мочевого пузыря представлены в табл. 1. В частности, наибольшее значение имеют аопоптотические маркеры (р53, р16, р27) и эпидермальный фактор роста (EGFR). Уровень экспрессии р16, р27, EGFR коррелирует со стадией опухолевого процесса. Более подробно особенности экспрессии данных маркеров рассмотрены ниже.
Лечение поверхностного рака мочевого пузыря включает в себя повторные трансуретральные резекции мочевого пузыря при рецидивирования, интравезикулярные инстялляции цитотоксическими препаратами (тиотепа, митомицин С, доксорубицин, гемцитабин, валрубицин, терапия БЦЖ). В целом лечение поверхностного рака не столь агрессивное, как лечение инвазивного рака мочевого пузыря. При прогрессировании и частых рецидивах опухоли встает вопрос о проведении цистэктомии. Учитывая 30-80% частоту рецидивирования процесса, необходимо рано проводить повторное обследование (эндоскопическое исследование). Morris и соавт. в наблюдении за 179 пациентами с поверхностным РМП установили риск возникновения рецидивов в зависимости от времени. При отсутствии рецидива в течении 2, 5 и 10 лет риск рецидирования равен 43, 22, 2% соответственно [12].
Таблица 1. Иммуногистохимические маркеры рака мочевого пузыря [3]
При инвазивном раке мочевого пузыря золотым стандартом лечения является радикальная цистэктомия. Причиной включения химиотерапии в список проводимых процедур, выполняемых до и после радикальной цистэктомии, является предположение о том, что она способна увеличить выживаемость пациентов. Известно, что переходно-клеточная карцинома чувствительна к химиотерапии и у пациентов с метастазами на длительное время может быть достигнута стабилизация заболевания. Неоадъювантная химиотерапия у пациентов с распространенным заболеванием позиционируется как стандартный подход к лечению. Это основано на двух недавно проведенных исследованиях, в которых сообщается о преимуществах этого метода. Самое большое исследование (976 пациентов), проведенное группами MRC и EORTC, было направлено на изучение возможностей неоадъювантной терапии. Вторым подобным исследованием было исследование SWOG-0080. Оба этих исследования показали большое преимущество использования неоадъювантной терапии по сравнению с изолированной радикальной цистэктомией (5-летняя выживаемость при использовании неоадъювантной терапии составила около 40%, при изолированной цистэктомии – 25%). В настоящее время установлено, что у определенной группы пациентов радикальная цистэктомия не является оптимальным способом лечения. То есть получают все большое развитие органосохраняющие вмешательства. Основным преимуществом подобных вмешательств является более высокое качество жизни пациентов и меньший объем оперативного вмешательства, что делает эту операцию более переносимой. Однако большим недостатком подобных операций является постоянная недооценка стадии процесса (30-50% всех проведенных органосохраняющих операций) [14, 9]. При применении органосохраняющих видов терапии 5-летняя выживаемость больных составляет 40%. Местные рецидивы заболевания были отмечены у 28% больных [9].
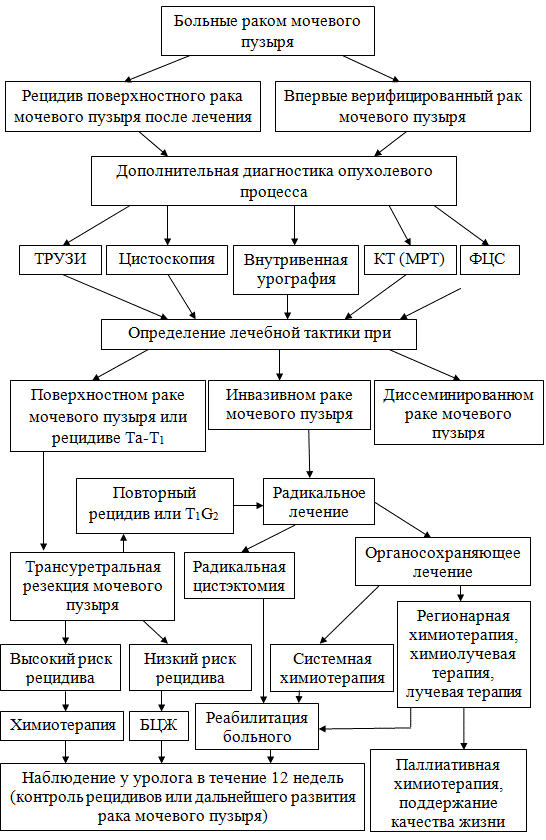
Рис. 1. Общий алгоритм лечения рака мочевого пузыря [1]: ТРУЗИ – трансректальное ультразвуковое исследование, КТ – компьютерная томография, МРТ – магнитно-резонансная томография, ФЦС – флуоресцентная цистоскопия, БЦЖ – вакцина Бацилла Кальметта-Герена
В целом, общепринятый алгоритм диагностики и лечения рака мочевого пузыря, представленный на рис. 1, в ближайшем будущем пополнится новыми методами диагностиками, которые также будут подходящими для скрининга не только рака мочевого пузыря, но и других опухолей.
Список использованных источников:
2. Keshtkar A., Salehnia Z., Keshtkar A., Shokouhi B. Bladder Cancer Detection Using Electrical Impedance Technique (Tabriz Mark 1)// Patholog Res Int. 2012;2012:470101.
3. Blaveri E., Simko J.P., Korkola J.E. Molecular biomarkers in urothelial bladder cancer// Clin Cancer Res 2005; 11: 4044–55.
4. Bernhardt T.M., Schmidi H., Philipp C. et al. Diagnostic potential of virtual cystoscopy of the bladder: MRI vs CT. Preliminary report// Eur. Radiol. 2003. V. 13. № 2. P. 305-312.
5. Beer A., Saar В., Link T.M. et al. Virtual endoscopy of the urinary tract from T2-weighted and gadolinium-enhanced Tl-weighted MR urographic images// Rofo. 2001. V. 173. № 1. P. 997-1005.
6. Bray F., Guerra Yi.M., Parkin D.M. The comprehensive cancer monitoring programme in Europe// Eur J Public Health. 2003 Sep;13(3 Suppl):61-6.
7. Cheng L., Pan C.X., Yang X.J., Lopez-Beltran A., MacLennan G.T., Lin H., Kuzel T.M., Papavero V., Tretiakova M., Nigro K., Koch M.O., Eble J.N. Small cell carcinoma of the urinary bladder: a clinicopathologic analysis of 64 patients// Cancer. 2004 Sep 1;101(5):957-62.
8. Elsobky E., El-Baz M., Gomha M., Abol-Enein H., Shaaban A.A. Prognostic value of angiogenesis in schistosoma-associated squamous cell carcinoma of the urinary bladder// Urology, 2002 Jul;60(1):69-73.
9. Hautmann R.E., Paiss T. Does the option of the ileal neobladder stimulate patient and physician decision toward earlier cystectomy?// J Urol. 1998; 159: 1845-1850.
11. Krüger S., Johannisson R., Kausch I., Feller A.C. Papillary urothelial bladder carcinoma associated with osteoclast-like giant cells// Int Urol Nephrol. 2005;37(1):61-4.
12. Messing E., Teot L., Korman H., Underhill J., Barker E., Stork B., Qian J. et al. Performance of Urine test in patients monitored for recurrence of bladder cancer// J Urol 2005;174:1238-1241
14. Song J.H., Francis I.R., Platt J.F. et al. Bladder tumor detection at virtual cystoscopy// Radiology. 2001. V. 218. № 1. P. 95-100.
15. Tut V.M., Braithwaite K.L., Angus B., Neal D.E., Lunec J., Mellon J.K. Cyclin D1 expression in transitional cell carcinoma of the bladder: correlation with p53, waf1, pRb and Ki67// Br J Cancer. 2001 Jan;84(2):270-5.
В журнале «Врач-аспирант»:
16. Толкач Ю.В., Шестаев А.Ю., Петров С.Б., Schelin S., Костюк И.П., Крестьянинов С.С. Новый способ реконструкции шейки мочевого пузыря во время радикальной простатэктомии: предпосылки эффективности и клинические результаты// Врач-аспирант, №3.4(46), 2011. – С. 532-538.
17. Каримова Б.Н. Патология органов мочевой системы у часто болеющих детей (по данным ретроспективного анализа)// Врач-аспирант, №2(51), 2012. – С. 93-97
18. Миртазаев О.М., Ахмедов Р.Н., Турсунов Р.Б., Нурузова З.А., Мухамеджанова Н.Н. Госпитальные инфекции мочевыводящих путей: мониторинг микрофлоры как средство выбора эффективной терапии// Врач-аспирант, №2(51), 2012. – С. 97-104