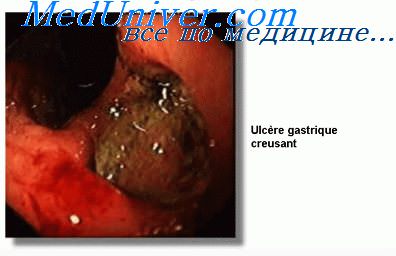
Малигнизация это что такое в желудке
Пилородуоденальные стенозы являются следствием рубцевания при заживлении язвы или плотного инфильтрата в области активной язвы. С клиникой картины стеноза могут протекать также шмиденовские деформации желудка. Наиболее часто стриктура располагается в луковице двенадцатиперстной кишки или в области пилорического канала. В зависимости от степени нарушения эвакуации из желудка различают компенсированные и декомпенсированные стенозы.
Компенсированные стенозы характеризуются умеренным нарушением эвакуации (барий задерживается до 4—6 ч). Вначале может отмечаться даже ускоренная эвакуация из желудка. В этом периоде наблюдается усиленная перистальтика гипертрофированных мышц желудка. За счет этого, несмотря на сужение, хотя и значительно медленнее, желудок еще справляется с эвакуацией пищи. Клинически в этой стадии отмечаются тяжесть после еды в эпигастральной области, иногда видимая на глаз перистальтика. Из-за повышения давления в желудке н гнпермоторики нередко развивается картина недостаточности кардии (изжога, срыгивание пишей, отрыжка). Временами может наблюдаться рвота, но она еще не носит регулярного характера.
Заболевание можно заподозрить уже при опросе больного. Диагноз подтверждается рентгенологическим исследованием, при котором выявляются задержка эвакуации бария и гипермоторпка желудка. Важно тщательно изучить облаете» сужения, определить точное местоположение стриктуры, протяженность ее и по возможности, особенно при наличии выраженного болевого синдрома, указывающего па активную язву, постараться выявить ее.
Декомпенсированный стеноз характеризуется резким нарушением эвакуации из желудка (барии задерживается в желудке свыше 6 часов, в течение суток и более), резким расширением желудка, его атонией, значительным ухудшением общего состояния больных. Пиша в желудке застаивается: нередко в резко растянутом желудке содержится несколько литров застойного, зловонного содержимого, появляется отрыжка с запахом тухлых яиц. Больной жалуется на выраженную тяжесть в эпигастрии, отрыжку тухлым, регулярную рвоту, которая вначале возникает непроизвольно. Позднее, с нарастанием атонии желудка, больной сам вызывает рвоту. Натощак отмечается симптом «шума плеска». Вследствие потери большого количества жидкости, белка и солей больные быстро истощаются. Боли, которые наблюдались ранее, нередко стихают и превалируют симптомы нарушения эвакуации. В других случаях, когда стеноз обусловлен язвенным инфильтратом, болевой синдром может быть резко выражен. Отмечаются сгущение крови, снижение содержании хлоридов и калия в крови, развивается ацидоз. Диурез уменьшается. Кислотность желудочного сока при рП-метрнн обычно повышена.
В терминальной стадии наступают резкое обезвоживание и истощение (кахексия), развивается тяжелый энтероколит, который проявляется диареей, дерматитом, деменцией. В некоторых случаях из-за потери кальция может разниться тетания. Прогноз в таких запущенных случаях определить весьма сложно, но все же благодаря современным реанимационным мероприятиям ряд больных удастся вывести из крайне тяжелого состояния и успешно оперировать.
Обычно диагноз легко установить клинически, исходя из симптомов нарушения эвакуации из желудка и клиники язвенной болезни в анамнезе. При рентгенологическом исследовании определяются нарушение эвакуации из желудка, расширение и атония его. Дифференциальный диагноз следует проводить со злокачественной опухолью, в пользу которой могут говорить короткий анамнез и отсутствие в прошлом классической клиники язвенной болезни. Диагноз уточняют при гастроскопическом исследовании.
Малигнизация язвы
Язвы желудка в 15—20% случаев подвергаются раковой дегенерации. Особо неблагоприятны в этом плане язвы большой кривизны и препилорического отдела желудка. Около 90% язв большой кривизны оказываются злокачественными. Малигнизации чаще подвергаются каллезные язвы у больных старше 40 лет. Язва диаметром более 1,5 см должна рассматриваться как потенциально злокачественная. Малигнизация чаше начинается в крае язвы, реже со дна се.
Совершенно надежных признаков раковой дегенерации нет. Отчетливые симптомы ее, как правило, появляются слишком поздно. И все же некоторые признаки могут помочь врачу установить озлокачествление язвы, во всяком случае заподозрить его и подвергнуть больного тщательному обследованию: 1) локализация язвы (язвы большой кривизны, препилорические и кардиальные следует считать потенциально злокачественными н особенно тщательно обследовать подобных больных); 2) диаметр язвы более 1,5 см; 3) длительный язвенный анамнез; 4) доказанное снижение желудочной кислотности. Последний признак следует принимать во внимание только в том случае, если исследование желудочного сока проведено достаточно надежными способами (рН-метрия, фракционное исследование). Важным указанием на возможность малигнизации служит изменение характера болевого синдрома, которое обычно проявляется исчезновением его периодичности и постоянными тупыми болями. Иногда боли почти полностью исчезают. Во всяком случае следует принимать во внимание любое изменение характера привычных болей, что больные обычно отмечают достаточно отчетливо. Неэффективность 4—6-недельного курса интенсивного лечения также должна вызывать подозрение на малнгнизацию.
Необходимо помнить, что ликвидация язвенной ниши, устанавливаемая при контрольном рентгенологическом исследовании, может наступить вследствие заполнения ее растущей опухолью.
Начальные признаки малигнизации рентгенологически уловить практически не удается. Рентгенологические признаки (подрытость краев язвы, инфильтрация, дефект наполнения) появляются позже. Ведущее значение в диагностике начальной стадии малигнизации принадлежит гастроскопии с биопсией. Для исследования надо брать кусочки ткани из нескольких мест язвы, помня о том, что малигнизация может начинаться в какой-либо одной точке. Отрицательный ответ биопсии еще не означает, что малигнизации нет, поскольку пораженный участок может не попасть в зону биопсии. Если клинически, рентгенологически и эндоскопически у такого больного все же невозможно исключить озлокачествлеиие, эндоскопию и биопсию следует повторить. Если и после повторного исследования остаются сомнения, больного следует оперировать, так как не только доказанная малигнизация, но и обоснованное подозрение на нее служит показанием к оперативному вмешательству. Только такой подход позволит избежать роковых ошибок.
Язва желудка и 12-перстной кишки – угроза жизни! / Врач- хирург И.Ф.Лозовский
Язва желудка и 12-перстной кишки – угроза жизни!
Ежегодно жертвами язвенной болезни становятся сотни тысяч человек. В последнее время в нашем городе и районе участились случаи осложненного течения этого заболевания Эта болезнь распространена повсеместно и встречается тем чаще, чем выше уровень экономического развития региона. Каковы риски связанные с этой болезнью? Чем рискуют люди, страдающие язвой желудка и двенадцатиперстной кишки? В этой статье, обсуждая проблему смертельных осложнений язвы, хочется дать своеобразные советы от противного для того, чтобы стала очевидность серьезности проблемы. Итак, чем опасна для жизни это страдание, каковы смертельные осложнения.
Кровотечение
Язвенная болезнь (или просто язва) желудка и двенадцатиперстной кишки это одна из самых распространенных причин внутреннего кровотечения в органах пищеварительной системы. Сама по себе язва – это постоянно углубляющаяся рана в стенке желудка или кишечника, поэтому при разрастании язвы вполне возможно, что она дойдет до сосуда, питающего ткани желудка и «разъест» его стенки. Нужно сказать, что кровоснабжение желудка отличается интенсивностью, а сосудистая сеть этого органа очень богата, поэтому при отсутствии лечения, язвенная болезнь очень часто осложняется внутренним кровотечением.
Чаще всего кровотечение из язвы возникает внезапно, без видимых на то причин. Однако, если кто-то желает ускорить наступление этого события, то при диагнозе язва желудка ему нужно встать утром и не позавтракав выкурить несколько сигарет и выпив крепкий кофе, отправиться на работу где обязательно нужно несколько раз хорошо понервничать. Будьте уверены, результат не заставит себя ждать!
Симптомы внутреннего кровотечения следующие: внезапное появление ощущения слабости, головокружение, холодный пот, сонливость, чувство страха, учащение пульса. Когда в желудке накопится достаточное количество крови, больного может вырвать. Из-за взаимодействия с соляной кислотой кровь меняет цвет с ярко-красного на темно-коричневый («рвота кофейной гущей»).
В некоторых случаях кровотечение развивается медленно и больной, сам того не ведая, успевает проглотить и переварить изрядное количество собственной крови. В таком случае он должен будет заметить, что его стул стал черным как деготь– это еще один признак кровотечения в желудке или в кишечнике.
Лечением кровотечений из язвы желудка занимаются врачи больниц скорой помощи, каковой является и Гатчинская ЦРКБ. Современные методы лечения с использованием эндоскопической техники позволяют резко снизить количество операций по поводу кровотечения на фоне язвенной болезни, однако, возникшее один раз кровотечение может в любой момент повториться, поэтому у нелеченых больных всегда есть возможность рецидива «смертельного» кровотечения.
Прободная язва
Прободение язвы это частое осложнение быстро развивающейся язвенной болезни. Если больных с кровотечением из язвы сковывает «странная сонливость» и оцепенение, то больные с прободением язвы (даже самые стойкие) в один момент «сгибаются от боли».
Что такое прободение язвы? Представим себе желудок – по сути дела это полый мешок, наполненный некоторым количеством пищи и кислотного желудочного сока. При прободении язвы между полостью желудка и брюшной полостью, в которой он находится, образуется прямое сообщение, то есть, язва углубляется настолько, что пробивает стенку желудка насквозь. При этом из желудка вытекает желудочный сок, сильно раздражающий брюшину – это и вызывает нестерпимую боль.
Это осложнение язвенной болезни также развивается внезапно. Но может наступить и прободение с кровотечением.
Симптомы прободения язвы желудка следующие: больной внезапно сгибается от приступа сильнейшей боли в верхней части живота или в области пупка. Мышцы живота сильно напрягаются, образуя так называемый деревянный живот. При прободении язвы боль постепенно перемещается в подвздошную область («под ложечку»).
Вам нужно знать, что на этом страдания больного с прободением язвы не заканчиваются. Без оказания медицинской помощи он умрет только через несколько дней от перитонита (гнойного воспаления брюшной полости).
Пенетрация
Пенетрация – это одно из частых осложнения язвенной болезни, при которой язвенный процесс приводит к спаиванию стенок желудка с одним из соседних органов (например, кишечник или поджелудочная железа) и постепенному проникновению язвы в этот орган.
Пенетрация гораздо мене опасна прободения, так как при ней язва все-таки остается закрытой, а массивного заражения брюшной полости микробами (перитонит) не происходит. Однако и от пенетрации можно умереть. Наиболее опасна пенетрация в поджелудочную железу.
Этот орган чрезвычайно чувствителен по отношению к разного рода травмам и потому, когда в него врезается язва в считанные часы может развиться острый панкреатит, который сам по себе гораздо опаснее любого из осложнений язвенной болезни. Шансов на пенетрацию больше у хронических больных с язвенной болезнью, которые хоть и предпринимают лечение, но не доводят его до конца, а вот прободение чаще наблюдается у молодых людей с коротким стажем болезни.
Стеноз привратника
Привратник это конечный отдел желудка, соединяющий его с двенадцатиперстной кишкой. В зоне привратника язвы образуются особенно часто, так как именно эта часть желудка наиболее подходит для жизни хеликобактера (бактерия, провоцирующая образование язвы) и именно здесь кислотность желудочного сока максимальна. По анатомическому строению привратник желудка это узкий канал, снабженный мышечными кольцами, способными сокращаться и расслабляться. При сокращении мышц канал привратника закрывается и полость желудка отделяется от полости кишечника. При расслаблении мышц привратника канал расширяется и часть пищи из желудка переходит в двенадцатиперстную кишку для дальнейшего переваривания. Стеноз привратника характеризуется его необратимым сужением и деформацией на фоне хронической язвы, поразившей этот отдел желудка. Фактически, язва превращается в большой жесткий рубец, который деформирует и стягивает канал привратника, из-за чего он теряет способность расширяться, а, следовательно, и пропускать пищу в двенадцатиперстную кишку.
Первые симптомы стеноза привратника могут появиться спустя много лет после начала язвенной болезни. Болезнь начинается с ощущения полноты желудка после приема пищи, тяжести и болей в желудке, кислой отрыжки с неприятным запахом. Также больные жалуются на то, что спустя долгое время после еды слышат, как в желудке «плещется жидкость» и ощущают желудок переполненным.
Действительно, больные со стенозом привратника гибнут от истощения, так как рано или поздно сообщение между желудком и кишечником полностью нарушается из-за разрастания соединительной ткани в области старой язвы.
Лечения стеноза привратника может быть только хирургическим. Обычно в ходе операции пораженная часть желудка удаляется, а здоровая часть органа сшивается с тонким кишечником, для восстановления сообщения.
Рак желудка
Злокачественное перерождение язвы желудка это самое грозное осложнение язвенной болезни. Внешне поверхностные формы рака желудка очень похожи на язву, и потому порой их очень трудно отличить. Язва может дать начало раку, а может развиться на базе опухоли.
Перерождение язвы в рак происходит из-за нарушения процессов размножения и взросления клеток в очаге хронического воспаления, который есть при язве. Гораздо реже уже существующая опухоль дает начало язве.
Рак желудка – это очень агрессивная опухоль, которая трудно поддается лечению и часто приводит к смерти пациента. Малигнизация (озлокачествление) язвы чаще всего наблюдается у больных, страдающих язвой на протяжении многих лет. В таких случаях, рак желудка является завершающим актом развития болезни.
Развитие рака желудка может долгое время оставаться незаметным для больного. Первые симптомы рака это изменение характера болей: если для язвенной болезни характерны голодные боли, успокаивающиеся после приема пищи, то при раке боли перестают зависеть от приема пищи и становятся практически постоянными. Также больные могут заметить непереносимость пищи, потерю веса.
Рак желудка, выявленный на начальных стадиях, полностью излечим хирургическими методами (удаление пораженной зоны желудка). На поздних стадиях рака, при наличии метастаз в других органах лечения рака очень затруднительно и часто не приносит никаких результатов.
В этой статье мы хотели показать читателю насколько опасной может быть язвенная болезнь, если «забросить» ее лечение. При возникновении симптомов язвенной болезни нужно немедленно обратиться к врачу за советом и помощью.
Малигнизация
Малигнизация – процесс трансформации доброкачественных клеток в злокачественные. Может происходить в любых нормальных тканях или тканях доброкачественных опухолей. Сопровождается снижением уровня дифференцировки, изменением морфологических свойств, нарушением функции и бурным размножением клеток, прогрессирующим ростом новообразования и развитием отдаленных метастазов. Малигнизацию подтверждают на основании клинических данных, результатов лабораторных и инструментальных исследований. В процессе лечения опухоли обычно применяют хирургические вмешательства, химиотерапию и радиотерапию. Возможно использование гормонов, иммуностимуляторов и других препаратов.
Общие сведения
Малигнизация (озлокачествление, злокачественное перерождение) – сложный патоморфологический процесс, в ходе которого доброкачественные клетки приобретают свойства злокачественных. Малигнизации могут подвергаться как нормальные клетки, так и уже измененные, но не проявляющие признаков злокачественности. Чаще всего очаги озлокачествления возникают в области язв, полипов и различных доброкачественных опухолей. Причиной малигнизации могут стать генетическая предрасположенность и вредные факторы окружающей среды.
На начальных стадиях малигнизация протекает бессимптомно, поэтому ранняя диагностика злокачественных новообразований сопряжена со значительными затруднениями, однако регулярные профилактические осмотры, использование современных лабораторных и инструментальных методов исследования позволяют частично решить проблему раннего выявления малигнизации. Диагностику и лечение осуществляют специалисты в области онкологии, гастроэнтерологии, пульмонологии, неврологии, дерматологии, отоларингологии, гинекологии, ортопедии и врачи других специальностей (в зависимости от локализации опухоли).
В настоящее время злокачественные опухоли являются второй по распространенности причиной смертности после сердечно-сосудистых заболеваний. В 2012 году от рака умерло более 8 миллионов человек. Вероятность малигнизации увеличивается с возрастом, однако, наряду с людьми преклонных лет, злокачественные опухоли нередко поражают детей и пациентов трудоспособного возраста. Самыми распространенными видами рака являются рак легких, рак желудка, рак молочной железы, рак печени и рак толстого кишечника.
Причины малигнизации
Причиной малигнизации клеток является сочетание нескольких факторов, в числе которых специалисты указывают химические канцерогены, особенности окружающей среды, некоторые вирусы, состояния гормонального дисбаланса, возраст, вредные привычки и неблагоприятную наследственность. При проведении исследований было установлено, что малигнизацию могут провоцировать более 2000 различных химических веществ, однако степень их влияния на процессы злокачественного перерождения клеток может сильно различаться.
В перечень химических соединений, безусловно, вызывающих малигнизацию клеток, входят полициклические ароматические углеводороды (источниками являются транспорт, промышленные предприятия и отопительные системы), нитрозамины (содержатся в сигаретах, некоторых сортах пива и амидопирине), производные гидразина (входят в состав гербицидов и некоторых лекарственных средств), асбест и другие минеральные волокна (источником являются промышленные производства), а также некоторые соединения металлов.
Самым значимым физическим фактором малигнизации является солнечное излучение, от уровня которого напрямую зависит вероятность развития рака кожи. Чем светлее кожа и волосы и чем дольше человек подвергается воздействию солнечных лучей – тем выше риск развития меланомы, базалиомы и плоскоклеточного рака кожи. Кроме того, малигнизацию может стимулировать ионизирующее излучение, провоцирующее возникновение лейкозов, костных опухолей (радиоактивный стронций) и рака щитовидной железы (радиоактивный цезий и йод).
Доказано, что вероятность малигнизации повышается при воздействии на клетки определенных вирусов, в частности – вируса ATLV (вызывает лейкоз), вируса Эпштейна-Барр (провоцирует развитие лимфомы Беркитта), вируса папилломы человека (играет определенную роль в возникновении рака шейки матки) и вируса герпеса II типа. Малигнизации также способствуют нарушения гормонального баланса. Гормоны могут напрямую провоцировать озлокачествление, действовать на клетки опосредованно, стимулируя их пролиферацию, оказывать негативное влияние на иммунитет и изменять метаболизм некоторых канцерогенов.
Существенную роль в процессе малигнизации играет генетическая предрасположенность. Описано множество наследственных заболеваний с высокой вероятностью малигнизации, например, системный полипоз кишечника, при котором у большинства пациентов к 40-50 годам развивается рак толстой кишки, или болезнь Дауна, при которой риск развития лейкоза в 11 раз выше, чем в среднем по популяции. Прослеживается связь между малигнизацией и врожденными пороками развития.
Выявляется зависимость между вероятностью малигнизации тканей определенных органов и полом пациента. Мужчины в 2,4 раза чаще страдают опухолями глаз, в 2,1 раза чаще – новообразованиями желудка, в 2 раза чаще – злокачественными поражениями носоглотки, в 1,7 раза – опухолями костей. У женщин вдвое чаще выявляется малигнизация тканей щитовидной железы. Первое место по распространенности у мужчин занимают опухоли дыхательных путей, у женщин – опухоли половых органов и молочной железы. В большинстве случаев вероятность малигнизации у пациентов обоих полов увеличивается с возрастом, однако некоторые виды новообразований чаще выявляются у детей или молодых людей.
В число привычек, оказывающих наиболее сильное влияние на малигнизацию клеток, входят курение, неправильное питание и прием алкоголя. У курящих рак легких развивается в 11 раз чаще; опухоли полости рта, гортани и глотки – в 7 раз чаще; новообразования мочевого пузыря – в 2,2 раза чаще; опухоли поджелудочной железы – 1,7 раз чаще, чем у некурящих. Основными пищевыми привычками, увеличивающими вероятность малигнизации, являются прием большого количества мясной, жирной, острой и пряной пищи, склонность к пересаливанию и употребление недостаточного количества растительной клетчатки. Алкоголь сам по себе не вызывает малигнизацию, но выступает в роли активатора, усиливая воздействие других факторов.
Стадии и этапы малигнизации
Начальной стадией малигнизации является инициация – мутация клеток под воздействием внутренних или внешних вредных факторов. В геноме клетки появляются клеточные или вирусные онкогены – измененные гены, вызывающие рост и размножение дефектных клеток. В организме человека постоянно образуются дефектные клетки, но в норме процесс малигнизации прерывается на этапе инициации, поскольку такие клетки подвергаются апоптозу – регулируемому процессу клеточной гибели. При одновременном выключении генов, вызывающих апоптоз, и активации генов, препятствующих апоптозу, дефектные клетки не погибают, а продолжают развиваться.
При повторном воздействии на клетки того же или другого вредного фактора наступает вторая стадия малигнизации – промоция. Онкогены активизируются, стимулируя пролиферацию дефектных клеток. Однако, даже этого недостаточно для развития злокачественной опухоли. Рост новообразования становится возможным только после прохождения третьей стадии малигнизации – уклонения дефектных клеток от процесса дифференцировки. Уклонение обычно происходит под влиянием определенных микроРНК.
Кроме того, переход на третью стадию малигнизации может быть обусловлен недостатком цитокининов, способствующих переходу клетки на более высокий уровень дифференцировки. Со временем количество низкодифференцированных клеток увеличивается, возникает микроскопический участок измененной ткани. Клетки с преобладающим набором хромосом формируют так называемую стволовую линию – основу опухоли. Одной из особенностей малигнизации является генетическая нестабильность клеток, из-за которой клеточный состав новообразования постоянно меняется, вместо одной стволовой линии появляются другие.
Измененные клетки, утратившие способность реагировать на внешние воздействия (влияние микросреды, иммунный надзор), продолжают активно делиться. Наступает четвертая стадия развития злокачественного новообразования – опухолевая прогрессия. Ткань, изменившаяся в процессе малигнизации, прорастает соседние органы, разрушает стенки кровеносных и лимфатических сосудов. Клетки новообразования попадают в кровь и лимфу, а затем разносятся по организму, «оседая» в лимфатических узлах и отдаленных органах. Из «осевших» клеток формируются новые очаги опухолевого роста – вторичные новообразования (метастазы).
С точки зрения свойств ткани можно выделить следующие этапы малигнизации: гиперплазия ткани, появление участков очаговой пролиферации, возникновение доброкачественной опухоли, образование участков дисплазии, рак in situ (злокачественная опухоль, не прорастающая окружающие ткани), инвазивное злокачественное новообразование. В ряде случаев этап доброкачественной опухоли может отсутствовать. Этапы очаговой пролиферации, доброкачественной опухоли и дисплазии рассматриваются, как предраковые состояния.
Свойства опухоли после малигнизации
Злокачественные новообразования обладают рядом свойств, отсутствующих у любых нормальных клеток и тканей организма:
Путь клетки «из греков в варяги». Малигнизация: причины и следствия
Малигнизация — один из самых загадочных процессов. Что же на самом деле направляет клетку на тернистый путь перерождения?
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Недуг, прозванный чумой XXI века. В наши дни рак является одним из самых страшных заболеваний. В 2010 году более семи миллионов людей по всему свету умерли от рака. В Соединенных Штатах каждая третья женщина и каждый второй мужчина рано или поздно заболеют раком. По прогнозам ВОЗ, число случаев заболевания будет продолжать расти от 14 миллионов в 2012 году до 22 миллионов в следующие десятилетия. Пугающие числа, от которых невольно бросает в дрожь. Однако процесс ракового перерождения, или малигнизации, не только страшен, но и интересен, и в этой статье мы разберемся, почему же некоторые «избранные» клетки решают свернуть не туда и как это влияет на самого «изменника».
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.
Гончие еще играют во дворе, но дичи не уйти,
как ни мчится она уже сейчас по лесам.
Франц Кафка
На «Биомолекуле» опубликовано немало статей о молекулярных основах канцерогенеза. Но каждая из них, как правило, посвящена какой-то одной стороне этого патологического процесса, в то время как среди наших читателей наверняка есть люди, которые хотели бы, прежде чем углубляться в детали, получить общее представление о раковой клетке. Обзорная статья Анны Батуевой удачно заполняет этот пробел и дает общее представления о ключевых молекулярных механизмах злокачественного перерождения. — Ред.
Под малигнизацией понимают приобретение здоровыми клетками черт злокачественности, которые мы подробно рассмотрим ниже. Процесс злокачественного изменения можно уподобить дичи из цитаты Кафки, ведь клетка, однажды встав на этот путь, не сможет вернуться и получить свое клеточное здоровье обратно. Важную роль в понимании основ перерождения клеток и их дальнейшего функционирования сыграла медицина, а следом за ней и молекулярная биология. Но начнем с истоков истории рака.
Часть 1. Биография рака
Первые упоминания о раке встречаются в папирусе Эдвина Смита, датируемом 16 веком до нашей эры [1]. Там же отмечается, что данное заболевание не поддается лечению.
Во времена Гиппократа, около 400 года до нашей эры, появилось специальное обозначение рака — karkinos. Разросшаяся опухоль напомнила Гиппократу краба, окутывающего все вокруг клешнями. Современное название онкологии произошло от греческого слова onkos, которое греки использовали для описания опухолей. Однако врачи того времени не различали доброкачественные и злокачественные новообразования, и karkinos Гиппократа не имеет ничего общего с истинным раком.
Гиппократ выдвинул гуморальную теорию, суть которой состояла в том, что каждый недуг является следствием переизбытка одного из четырех гуморов: крови, слизи, желтой желчи и черной желчи.
Гален, греческий врач, практиковавший в Риме около 160 года нашей эры, довел теорию Гиппократа до совершенства. Он заявил, что рак образуется из-за переизбытка черной желчи. Гален умер в 199 году нашей эры, но его «черная желчь» еще долго будоражила умы онкологов.
Только спустя пять столетий, в 1538 году, Андреас Везалий опроверг теорию Галена, делая вскрытия в Парижском университете. Окончательно похоронил галенову теорию лондонский анатом Мэтью Бейли, который в 1793 году опубликовал учебник «Патологическая анатомия некоторых наиболее важных частей человеческого тела» [2], в котором представил рисунки и описания раковых опухолей, где не было и следа «черной желчи».
Изобретение микроскопа повлекло за собой первые цитологические исследования рака. В 1801 году французский физиолог Франсуа Биша и в 1838 году Иоганн Мюллер определили, что опухоли имеют клеточную структуру. После этого Жан Крювелье высказал гипотезу «канцероматозной дегенерации», основанную на предположении, что клетка проходит несколько этапов, прежде чем окончательно превратиться в раковую. Немецкий хирург Карл Тирш доказал, что раковая опухоль происходит из эпителиальной ткани, а саркома — из соединительной.
Первая половина XX века породила еще одну теорию канцерогенеза, недалеко ушедшую от истины. В 1911 году Пейтон Раус, работая в Рокфеллеровском университете в Нью-Йорке, открыл вирус, способный вызывать опухоли у кур. Ученые по всему свету бросились искать вирусы, ответственные за рак именно у человека, однако ничего не могли найти. В 1974 году в Medical World News вирус рака у человека ставили в один ряд с НЛО, снежным человеком и лохнесским чудовищем. Вирус СВ-40 и вирус папилломы человека, вызывающие рак у людей, были открыты в 1960 и 1983 годах соответственно.
В 1970 году генетик Говард Темин, работавший в лаборатории Макардла в Висконсине и изучавший вирус саркомы Рауса (ВСР, или VSR), представил свою работу на Десятом Международном онкологическом конгрессе. Он открыл у ВСР обратную транскрипцию — синтез ДНК по РНК — и положил начало изучениям ретровирусов. Позднее он отказался от вирусной теории канцерогенеза, а в 1979 году ученые Майкл Бишоп и Харолд Вармус открыли первый протоонкоген — src (сарк), содержащийся в ВСР. Это положило начало новому этапу в истории онкологии, люди наконец-то поняли, как запускается процесс канцерогенеза. Но этого бы не произошло без изучения раковой клетки и ее странной физиологии.
Часть 2. Что заставляет клетку измениться?
В этой главе мы разберем причины злокачественного перерождения клетки. Первым толчком к началу этого изменения является мутация в ДНК.
Но не всякие повреждения ДНК обязательно приведут к появлению раковой клетки, а лишь те, что затронут определенные гены. Наиболее важную роль в канцерогенезе играют три группы генов: протоонкогены, онкогены и гены — супрессоры опухолей.
Протоонкогены
Протоонкогены — это «здоровые» предшественники онкогенов, которые в результате мутации могут вызвать развитие опухоли. Такими причинами являются различные мутации или суперэкспрессия гена. Как правило, протоонкогены кодируют белки, участвующие в процессах жизненного цикла клетки. В результате мутаций появляются сбои в регуляции клеточного деления и дифференцировки.
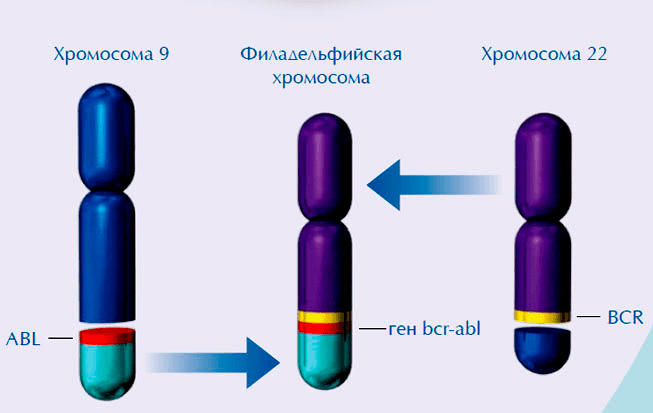
Основные изменения, происходящие с протоонкогенами:
Рисунок 1. Химерный ген BCR-ABL образуется при слиянии участка 9 хромосомы, несущей ген ABL, с участком 22 хромосомы, несущей ген BCR
В некоторых случаях канцерогенез запускается вирусами. Онкогены в геноме вирусов являются ранее захваченными в клетках-хозяевах нормальными генами, которые со временем превратились в злокачественные. Когда такие онкогенные вирусы попадают в клетку, начинается считывание информации с вирусной ДНК или РНК, в цитоплазме накапливаются онкогенные белки и начинается процесс перерождения.
Онкогены
Онкогены — это гены, активность которых стимулирует образование и развитие злокачественной опухоли. Как уже было упомянуто выше, первый вирусный онкоген был открыт в 1979 году.
Биохимические продукты онкогенов
Онкогены кодируют белки с различной структурой и функциями. К основным продуктам деятельности онкогенов относят:
Все вышеперечисленные продукты онкогенов являются сигналами к запуску неконтролируемого клеточного деления. Внешние факторы больше не играют никакой роли в жизни клетки, потому что пролиферацию запускают внутренние сигнальные белки.
Гены и белки — супрессоры
В здоровой клетке существуют защитные механизмы, следящие за процессами и регулирующие клеточный цикл. К таким механизмам относят деятельность белков — супрессоров опухолей: p21, p53, pRb, PTEN и др.
Белок p53 — наиболее изученный белок-супрессор. Он является продуктом гена TP53, мутации которого обнаруживаются в клетках многих опухолей [7]. p53 синтезируется во всех клетках организма, но активируется только при повреждениях ДНК. Этот белок способен остановить клеточный цикл и не допускать дальнейшее деление клетки, пока не произойдет репарация ДНК. При сильных повреждениях он также может запускать процесс апоптоза.
Одной из главных функций p53 является сохранение генетической идентичности всех клеток организма. При неправильной работе этого белка клетка получает возможность делиться даже при поврежденной ДНК, что увеличивает вероятность мутаций и накопления дефектных онкогенов. Важную роль в подавлении p53 играет белок MDM2, который в норме регулирует активность p53. Однако при повышенном синтезе он связывается с p53 и ингибирует его противоопухолевое действие.
Эпигенетические факторы рака
Важными факторами канцерогенеза являются эпигенетические события. Эпигенетика изучает процессы, затрагивающие активность генов, но не изменяющие структуру ДНК. К ним относится изменение метилирования ДНК.
Метилирование — это присоединение метильной группы к нуклеотидам в особых, строго определенных участках генома, называемых CpG-островками. Такое изменение не влияет на структуру молекулы, однако может влиять на экспрессию отдельных генов. В частности, если в участке ДНК много метильных групп, то транскрипция этого участка прекращается.
Особенно активно метилирование проходит в эмбриональный период жизни, а у взрослого человека метилировано около 2% генома. В норме баланс между метилированием и деметилированием строго регулируется и соблюдается, однако в старости начинают преобладать процессы метилирования, что может в итоге привести к канцерогенезу. В процессе онкогенеза происходит гиперметилирование CpG-островков, что приводит к общей геномной нестабильности и накоплению еще большего количества мутаций. В большинстве случаев метилированные участки являются промоторами и влияют на активацию или, наоборот, инактивацию генов, что с виду похоже на действие точечных мутаций.
Однако хотя нарушения в эпигенетической регуляции сопровождают развитие злокачественного перерождения, они, как правило, не являются его первопричиной, а лишь одним из сопутствующих факторов.
По отдельности каждое из вышеперечисленных нарушений не может спровоцировать раковое перерождение. Все они работают совместно и слаженно. Так, онкогенез запускается, только если одновременно активированы онкогены и инактивированы гены-супрессоры в обеих копиях ДНК. Впервые теорию двойного канцерогенеза высказал Альфред Кнудсон, изучавший ретинобластому: «По всей видимости, — писал он, — в возникновении рака у детей ключевую роль играют два типа генов. Первый, онкогены, действует посредством повышенной, аномальной активности. Второй же класс, антионкогены, в онкогенезе рецессивен: рак происходит лишь тогда, когда обе нормальные копии удалены или изменены» [8]. В процессе жизнедеятельности раковая клетка накапливает все большее количество мутаций, поэтому раковый геном часто очень сильно отличается от генома здоровой клетки (рис. 2).
Рисунок 2. Раковый геном. В процессе жизнедеятельности раковая клетка накапливает огромное количество мутаций и нередко характиризуется полиплоидностью.
Часть 3. Физиологические последствия малигнизации
Основное последствие малигнизации — клеточное бессмертие. Оно может поддерживаться несколькими способами: активацией фермента теломеразы, блокировкой регуляторов митохондриального пути апоптоза и в некоторых случаях активацией механизма ALT (alternative lengthening of telomeres, альтернативного удлинения теломер [14]).
Обратная сторона «вечной молодости»
Впервые клеточное бессмертие раковых клеток было продемонстрировано в 1951 году на клеточной линии HeLa, взятой у Генриетты Лакс, вскоре скончавшейся от рака шейки матки (рис. 3) [9].
Рисунок 3. Клеточная линия HeLa — «бессмертная» линия раковых клеток. С 50-х годов прошлого столетия используется для изучения поведения раковых клеток и выявления новых противораковых препаратов.
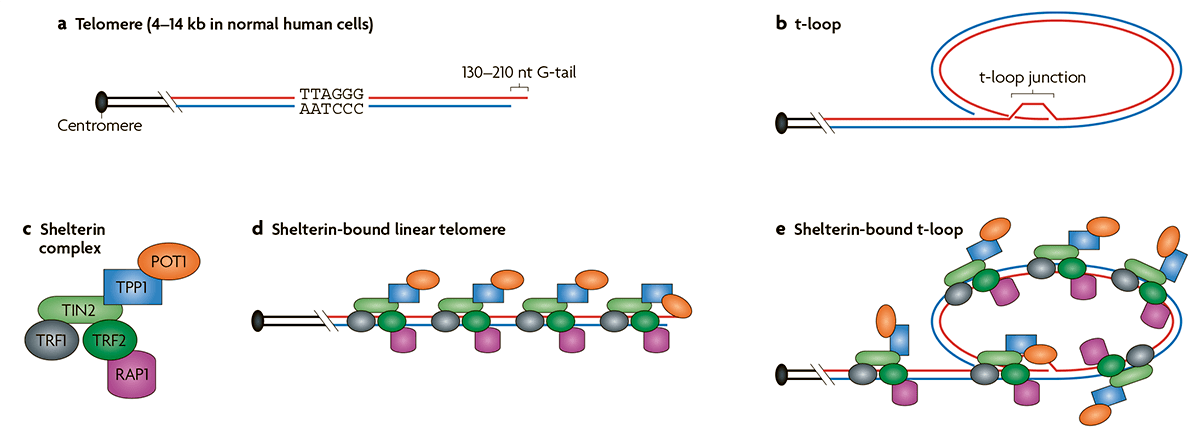
Как правило, малигнизация сопровождается активацией фермента теломеразы. На концах хромосом находятся короткие повторяющиеся участки ДНК, названные теломерами [10]. После каждого деления теломеры укорачиваются, что в итоге приводит к их полному исчезновению и невозможности продолжать деление. Количество возможных делений для клетки названо пределом Хейфлика. Действие теломеразы заключается в восстановлении теломер и превращении клетки в фактически бессмертную, позволяя ей делиться бесконечно долго. Существуют нормальные клетки, в которых также экспрессируется теломераза. Это клетки, которым надо часто делиться: половые, стволовые и клетки эпителия кишечника. Однако теломераза активна в подавляющем большинстве раковых клеток, что играет важную роль в их жизненном цикле.
С другой стороны, в некоторых злокачественных клетках, наравне с активной теломеразой, существует так называемое альтернативное удлинение теломер, или сокращенно ALT [11]. При ALT происходит гомологичная рекомбинация концевых участков хромосом (рис. 4). В норме рекомбинация происходит в процессе мейоза, однако раковые клетки научились достраивать теломеры, используя теломеры другой хромосомы как матрицу [12].
Рисунок 4. Принцип действия ALT, основанный на гомологичном достраивании концов теломер. Такой механизм «бессмертия» является основным для ряда опухолей.
Важно отметить, что раковое бессмертие контролируется не только теломерами, но и ингибированием путей апоптоза, главным из которых является митохондриальный путь. В норме, из митохондрий в цитоплазму выходят митохондриальные белки и образуют апоптотический комплекс — апоптосому, которая и запускает апоптоз. При неправильной работе регуляторных белков, а к ним относятся белки семейства BCL-2, нарушается выход апоптотических белков, что приводит к сбою в процессе апоптоза. В раковых клетках обнаружены нарушения в работе белков BAX и BAK, а также экспрессия ингибиторов клеточной смерти.
Часть 4. Заключение
Ежедневно в нашем организме появляются клетки, вступившие на путь ракового перерождения. Но далеко не все из них дойдут до конца и образуют злокачественную опухоль. С другой стороны, интересно клеточное поведение в процессе малигнизации, когда клетка способна «выключать» отдельные гены, мешающие ее перерождению. Современные исследования в области молекулярной онкологии и раковой геномики дают повод надеяться на окончательное понимание основ малигнизации и физиологии злокачественных клеток. Также в последнее время проводятся разработки новых противораковых препаратов, направленных на исправление дефектных сторон «больных» клеток. Возможно, изучение именно особенностей раковой клетки приведет к созданию лекарства, способного снизить страшные прогнозы Всемирной организации здравоохранения.