Как устроен иммунитет: Объясняем по пунктам
Андрей Смирнов СПИД.ЦЕНТР
«Йогурт для укрепления иммунитета», «Иммуностимулирующие витамины», «Да простудился, наверное, иммунитет упал»… Мы слышим слово «иммунитет» так часто, что уже почти не задумываемся, как он устроен и работает. На уроках биологии нам рассказывали, что иммунитет защищает от микробов, но только ли этим ограничивается его функция и как именно он понимает, от кого нужно нас защищать? СПИД.ЦЕНТР объясняет, как устроена иммунная система.
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
по теме
Мнение
«Иммунитет пациента с ВИЧ похож на иммунитет пожилого человека»
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
Кто отвечает за работу различных видов иммунитета?
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
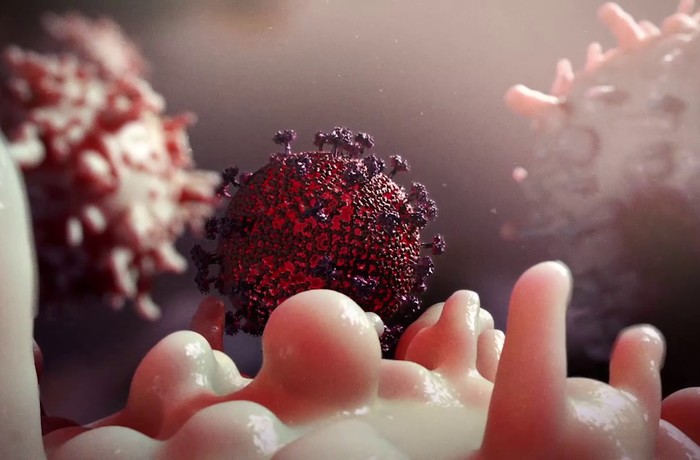
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
по теме
Эпидемия
Учёные выяснили, как вирусы обманывают иммунитет
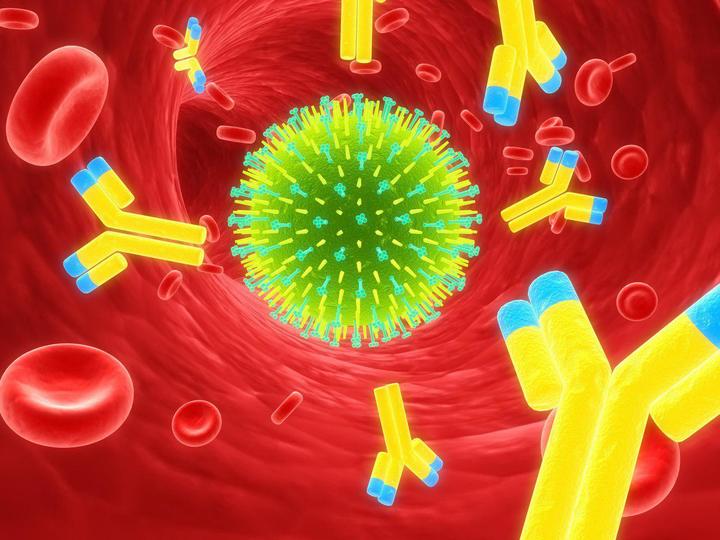
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
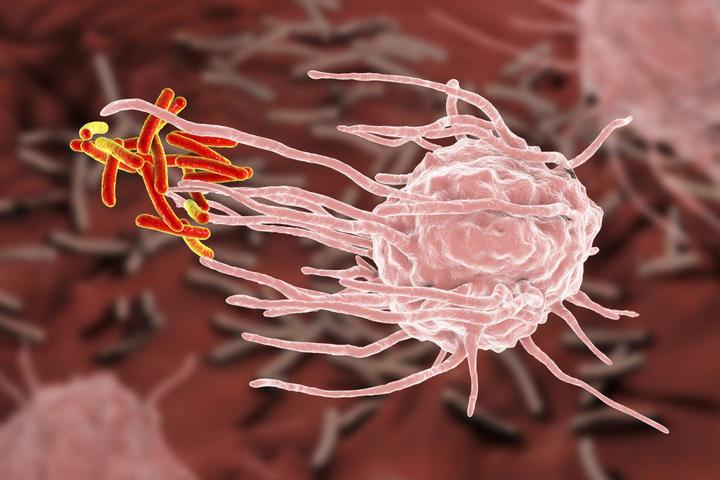
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
Клетки T-reg как иммунные регуляторы
Клетки T-reg как иммунные регуляторы
Регуляторные Т-клетки, существование которых было доказано совсем недавно, удерживают защитные силы организма от нападения на него самого. Манипуляции с этими клетками могут предложить новые методы лечения различных заболеваний, начиная от диабета и заканчивая отторжением органов.
Про клетки Тreg см. также:
«Тяжелейший аутотоксикоз» — такой термин был введен около ста лет назад известным немецким врачом-бактериологом Паулем Эрлихом для описания патологического состояния, при котором иммунная система человека «атакует» его же собственные органы и ткани. Эрлих полагал, что с биологической точки зрения в аутоиммунности (еще одно введенное им определение) нет ничего абсурдного, когда она находится под строжайшим контролем. Однако медицинское сообщество не приняло столь неоднозначной идеи. В самом деле, зачем природе встраивать в организм человека механизм, способный разрушать своего носителя?
Ненадежная система обороны
Многих людей сегодня пугает сознание того, что иммунная система в любой момент может выйти из-под контроля и спровоцировать аутоиммунное заболевание. Неприятнее всего то, что такой «иммунологический дамоклов меч» не так уж трудно привести в действие. Например, при введении мышам белков их собственной центральной нервной системы вместе с каким-нибудь адъювантом (неспецифическим стимулятором иммуногенеза) возникает деструктивная иммунная реакция, которая в основном проявляется как рассеянный склероз, вызывающий разрушение головного и спинного мозга.
Вводя животным их собственные белки разного происхождения, можно вызвать и другие аутоиммунные реакции. Такая же опасность подстерегает и человека. По крайней мере, из крови вполне здоровых людей выделены аутореактивные клетки иммунной системы, которые в пробирке ведут себя крайне агрессивно в отношении тканей своего родного организма.
Почему же при наличии постоянной угрозы со стороны собственной иммунной системы большинство из нас не страдает аутоиммунными заболеваниями? Каким образом наша внутренняя защита отличает опасных микробов от нормальных клеток своего организма? Исследователи обнаружили, что для обеспечения самотолерантности (способности удерживать иммунную систему в рамках) принимается множество мер предосторожности. Первая линия обороны, во всяком случае, в том, что касается Т-клеток, располагается в тимусе. Здесь созревшие Т-клетки проходят серьезный «курс обучения» и настраиваются на крайне слабую реакцию на здоровые клетки организма-хозяина. Клетки, не поддающиеся «дрессировке», отбраковываются. Однако ни одна система не застрахована от ошибок, и некоторое количество аутоагресивных Т-клеток ускользает от контроля. Попадая в кровоток и лимфу, они создают угрозу запуска аутоиммунной реакции.
Кровь и лимфа представляют собой вторую линию обороны. Здесь используется несколько приемов. Некоторые ткани, в том числе головного и спинного мозга, ограждены от аутоагрессивных клеток иммунной системы тем, что к ним ведет небольшое число сосудов, уходящих вглубь этих органов. Однако такая самоизоляция не может быть полной. В силу определенных обстоятельств (например, при повреждении тканей) аутореактивные клетки все же могут проникнуть внутрь. Другие способы защиты носят упреждающий характер. Иммунные клетки, проявляющие подозрительный интерес к здоровым тканям и органам, атакуются другими компонентами иммунной системы и разрушаются или инактивируются ими.
По-видимому, среди «подразделений», участвующим в упреждающих действиях, ключевая роль принадлежит регуляторным Т-клеткам. Большинство из них (а возможно, и все) обучаются мастерству в тимусе, а затем распространяются по всему организму в виде специализированной субпопуляции Т-клеток.
История открытия регуляторных Т-клеток
В 1969 г. Ясуаки Нисидзука (Yasuaki Nishizuka) и Тэруе Сакакура (Teruyo Sakakura) из японского Центра по исследованию рака в г. Нагоя обнаружили, что удаление тимуса у новорожденных мышат женского пола приводит к серьезным последствиям — разрушению яичников. Вначале ученые предположили, что тимус секретирует гормоны, необходимые для развития и сохранения данных органов. Однако позже выяснилось, что ткани яичников у мышат, лишенных тимуса, буквально наводнены иммунными клетками, что свидетельствовало о наличии аутоиммунного заболевания, возникшего в результате выхода из строя какого-то регуляторного механизма. Стоило ввести грызунам нормальные Т-клетки, как болезнь отступала. Все указывало на то, что в популяции Т-клеток имеется система самоконтроля.

Обзор: иммунные регуляторы
Как работают T-reg-клетки?
Механизм подавления аутоиммунной активности клетками T-reg остается загадкой. По-видимому, они способны воздействовать на самые разные клети иммунной системы, блокируя их амплификацию и такие процессы, как секреция сигнальных молекул — цитокинов. Специалисты склонны думать также, что T-reg-клетки активируются прямым межклеточным взаимодействием. Во всем остальном картина остается неясной.

Рис.1. Механизм самотолерантности
Имеются ли какие-либо данные о том, что человеку также необходимы T-reg-клетки? И есть ли они в нашем организме? Исследователи выяснили, что молекулярные особенности, характерные для T-reg-грызунов, присущи также некой субпопуляции Т-клеток человека. На поверхности данных клеток присутствуют молекулы CD25, а внутри содержится необычайно много белка Foxp3. Они обладают иммуносупрессивными свойствами — по крайней мере, таковы результаты опытов in vitro.

Рис. 2. Как T-reg-клетки подавляют аутоиммунную реакцию
Не только самотолерантность
Итак, есть указания на то, что T-reg-клетки действительно предотвращают развитие аутоиммунных заболеваний у человека, однако их роль оказалась еще значительнее. Так, они принимают участие в реакции организма на проникновение микробов.
В 1990-х гг. Фиона Паури (Fiona Powrie) из DNAX, исследовательского института в Пало-Альто, шт. Калифорния, проводила эксперименты по введению популяции Т-клеток, обедненной T-reg, мышам с нефункционирующей иммунной системой. В одной из серий экспериментов у животных развилось острое воспаление кишечника. Но аберрантная иммунная реакция была направлена в первую очередь не на клетки самого органа.
В кишечнике как грызунов, так и человека присутствует множество микроорганизмов. Нередко их число превышает триллион на каждый грамм ткани. Большинство из них не только безвредны, но даже необходимы: они улучшают пищеварение и вытесняют патогенные бактерии (например, сальмонеллы), которые в противном случае заселили бы кишечник. В норме иммунная система никак не реагирует на присутствие полезных, хотя и чужеродных тел. Но у мышей, которые использовала в своих опытах Паури, все было не так. Введенные иммунные клетки атаковали не только микроорганизмы, но и стенки кишечника реципиента. Однако при инъекции клеток T-reg подобных проблем не возникало. И если бы последние вводились вместе с другими Т-клетками с самого начала, то никакого воспалительного процесса в кишечнике не возникло бы. Подводя итоги, можно сказать, что иммунная система представляет собой спусковой механизм, готовый в любую минуту атаковать микрофлору кишечника, и сдерживают ее только T-reg-клетки.
Ответ иммунной системы на болезнетворные чужеродные агенты может контролироваться аналогичным образом. С одной стороны, T-reg-клетки способны блокировать слишком сильную реакцию, с другой — предотвращать уничтожение какого-нибудь инородного тела, позволяя ему существовать в организме хозяина. Есть свидетельство того, например, что невозможность полностью уничтожить обитающую в желудке бактерию Helicobactor pilori, вызывающую язвенную болезнь, связана с «умиротворяющим» действием T-reg-клеток на иммунную систему.
Рис. 3. T-reg сама подавляет активность других T-клеток
Есть указания и на то, что клетки T-reg способствуют нормальному (с иммунологической точки зрения) протеканию беременности, которая всегда оказывается вызовом иммунной системе. Поскольку плод наследует от матери только половину генов, а вторую получает от отца, он генетически не идентичен матери и по существу может считаться имплантированным органом. От отторжения плод защищает целый ряд механизмов, функционирующих в трофобласте (плацентарной ткани, соединяющей зародыш со стенкой матки). Трофобласт — не просто физиологический барьер для содержащихся в материнской крови веществ, вредных для плода: в нем продуцируются молекулы-иммуносупрессанты.
При беременности иммунная система будущей матери претерпевает изменения. Есть данные, что у женщин с таким аутоиммунным заболеванием, как рассеянный склероз, в период беременности T-reg-клетки проявляют большую активность. Недавно получены дополнительные данные: Александр Бетц (Alexander Betz) из Кембриджского университета обнаружил, что у беременных мышей повышено число материнских клеток T-reg. Причем у генетически модифицированных особей, не имеющих T-reg, при вынашивании потомства наблюдается массовое проникновение иммунных клеток через плацентарный барьер. Есть основания полагать, что причиной спонтанных абортов у некоторых женщин оказывается низкая активность T-reg-клеток.
Использование T-reg-клеток в медицине
Итак, T-reg-клетки являются мощным природным регулятором иммунной системы. Научившись влиять на его работу, мы сможем лечить различные заболевания. Ожидать немедленного практического внедрения подобного способа борьбы с недугами, конечно, не приходится, но имеющиеся данные позволяют надеяться, что введение в организм самих T-reg-клеток или препаратов, воздействующих на их активность, уже в скором времени сможет облегчить состояние некоторых больных.
Речь идет, прежде всего, об аутоиммунных заболеваниях. Возможно, с помощью T-reg-клеток удастся справиться также с разными видами аллергии. А легкость, с которой клетки T-reg «усмиряют» иммунную систему, предполагает, что они могут стать незаменимыми при операциях по пересадке органов.
Альтернативный метод мог бы состоять в избирательном устранении определенных компонентов из популяции T-reg-клеток для подавления нежелательной иммуносупресии и, следовательно, для усиления реакции, направленной на нужную мишень. Оптимальным было бы удаление только тех T-reg-клеток, которые блокируют специфическую иммунную реакцию. Такая стратегия может быть незаменима в борьбе с инфекционными заболеваниями, при которых иммунная система, предоставленная самой себе, часто действует не совсем адекватно, например, при туберкулезе и СПИДе.

Рис.4. Будущее трансплантологии
Технические трудности
До сих пор не было никаких попыток создать препараты, увеличивающие или уменьшающие численность популяции T-reg-клеток непосредственно в организме человека. Любые средства, которые можно было бы использовать, должны обладать способностью влиять только на те субпопуляции T-reg-клеток, которые играют роль в развитии конкретного заболевания. Но как распознать такие клетки, специалисты пока не знают.
Диагностика Т-клеточного иммунитета: пандемия как драйвер инновации
Диагностика Т-клеточного иммунитета: пандемия как драйвер инновации
Т-клеточный стартап TScan Therapeutics начал коллаборацию с компанией Qiagen для разработки теста на Т-клеточный иммунитет к COVID-19
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Споры о вакцинах и иммунитете против нового коронавируса кажутся бесконечными! От обсуждения ПЦР-диагностики и тестов на антитела дискуссии постепенно смещаются в сторону стойкости иммунитета: но измерить иммунитет человека по-прежнему сложно. Узнаем о том, как пандемия вдохнула новую жизнь в старую технологию и станет ли диагностика клеточного иммунитета доступной, в статье специалиста по Т-клеткам Софьи Касацкой.
Конкурс «Био/Мол/Текст»-2020/2021

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Вакцинация от коронавирусной инфекции SARS-CoV-2 — одна из самых горячих тем на границе 2020 и 2021 гг. Не утихают споры о безопасности вакцин, разработанных в сжатые сроки, о принципах производства и об основных принципах иммуногенности. Много спорят и о том, стоит ли добровольно прививаться тем, кто уже успел переболеть COVID-19, или, по крайней мере, подозревает об этом. Достаточно ли привиться один раз, а если вирус будет мутировать, как действовать дальше? Достаточно ли переболеть один раз или стоит бояться заболеть одной и той же инфекцией раз в сезон?
Для того чтобы ответить на эти вопросы и понять историю прошлых болезней, нужно изучить иммунную память (также ее называют иммунологической). Как правило, для проверки иммунной памяти на конкретную инфекцию проверяют наличие антител в плазме крови: ИФА-тест на антитела класса IgG (ИФА — иммуноферментный анализ). В этом тесте подсчитывается количество антител, которые сорбируются (прилипают) к стандартизированным антигенам, то есть молекулам, встречающимся именно у возбудителя данной инфекции и нигде больше. Антитела, в особенности класса IgG, поразительно точно и выборочно контактируют с однажды «выбранной» молекулой: мало где в биологии можно найти более точные и постоянные молекулярные контакты. Тем не менее тест на антитела — по большей части дань историческому процессу, а не «золотой стандарт» тестирования иммунной памяти. Пандемия стремительно изменила многие аспекты нашей жизни — может ли она поменять и то, что мы считаем стандартом в диагностике иммунитета?
Увидеть адаптивный иммунитет
«Биомолекула» неоднократно писала об уникальных механизмах, которые обеспечивают работу этой удивительной регуляторной системы — системы адаптивного иммунитета человека [1–3].
Чтобы увидеть Т-клетки и В-клетки разных типов, иммунологи чаще всего используют проточную цитометрию (FACS) [4]. Например, если мы хотим увидеть клетки памяти, то крепим флуоресцентную метку на молекулу, присутствующую только на поверхности клеток иммунной памяти, и подсчитываем клетки, пролетающие по одной через лазер и детектор флуоресценции.
Так можно узнать процент клеток, выполняющих определенную функцию, например, весь объем клеток памяти в крови на все прошлые инфекции. Теперь усложним задачу и выделим только клетки памяти на конкретную инфекцию — например, интересующий всех SARS-CoV-2, — как это сделать? Мы можем увидеть недавно активированные клетки среди клеток памяти. Лимфоциты из образца крови пациента смешиваются и инкубируются с молекулами, принадлежащими вирусу, чаще всего, — с очищенными белками, нарезанными на фрагменты. Т- и В-клетки, способные узнать и связать вирусный антиген, активируются, станут активированными эффекторными клетками, и мы сможем их различить среди всей иммунной памяти на FACS-анализе. Такие тесты проводятся в качестве дополнительных научных исследований.
Тест требует не только несколько часов на выделение клеток и их активацию вирусными белками либо пептидами, но и время дорогостоящего специалиста по проточной цитометрии, у которого прибор для FACS всегда работает и настроен, а не простаивает. Сочетание сразу двух факторов приводит к тому, что метод далеко не массовый. Можно представить метод рутинным в нескольких ведущих медицинских центрах, но сложно распространить: на порядки сложнее, чем внедрить регулярное ПЦР-тестирование.
Антитела или Т-лимфоциты
В качестве гораздо более дешевого и доступного теста, чем FACS, иммунологи смотрят не на сами клетки, а на то, что иммунные клетки производят [5]. Вспомним рецепторы, которые служат для решения задачи точного, прочного и выборочного связывания вирусных белков-антигенов. Т-клетки держат рецепторы на поверхности, на клеточной мембране. А вот В-лимфоциты свои уникальные рецепторы синтезируют как в мембранной, так и в растворимой форме — эти растворимые В-клеточные рецепторы и есть антитела. Получается, что вместо флуоресцентных меток и В-клеток памяти можно просто измерить концентрацию антител? Вдобавок, учебник иммунологии рассказывает, что В-клетки формируют память с помощью Т-клеток. Значит ли это, что если антитела есть, то уже произошло формирование памяти: сначала на уровне Т-клеток, затем на уровне В-клеток?
Да, текущие представления об иммунологии человека говорят: высокий уровень антител подразумевает, что Т-клеточный иммунный ответ тоже есть. Тем не менее известны и неклассические механизмы, при которых В-клетки быстро начинают производить антитела (чаще классов IgD, IgM) вне особых зон лимфоузла и при меньшем контроле со стороны Т-клеток. Обратная логика оказывается неверной: Т-клеточная иммунная память не зависит от наличия антител в крови, формируется независимо и сохраняется дольше.
Интуитивно кажется, что было бы отлично сохранять в крови антитела к коронавирусу после вакцинации или инфекции на всю жизнь. Некоторые инфекции формируют такой иммунный ответ, и это коррелирует с иммунной защитой, то есть вероятностью не заболеть при повторном заражении [6]. Но для других инфекций уровень антител в крови достаточно быстро, за несколько месяцев, снижается. Так происходит потому, что за свою жизнь человек встречает сотни тысяч типов вирусов, и производить антитела на все вирусные антигены просто невозможно. Приходится выбирать, происходит конкуренция с защитой от других инфекций, а также конкуренция с антителами, которые нужны для регуляции собственной физиологии организма. Антитела постепенно снижают концентрацию и пропадают из крови, но сохраняются В-клетки памяти, которые смогут вновь производить нужные антитела при необходимости.
Было бы идеально, чтобы организм производил антитела и держал их в оптимальной концентрации в крови не во время повторной болезни, а чуть заранее: до заражения. Именно для этого существуют сезонные ревакцинации: небольшая бустерная доза антигена поступает заранее и через 9–14 дней иммунитет снова подготовлен к сезонному контакту с большим количеством вирусных частиц вокруг. А постоянное, круглогодичное производство антител на высоком уровне можно оставить тем В-лимфоцитам, которые действительно каждый день сталкиваются с одними и теми же бактериями и вирусами: например, В-лимфоцитам слизистой ЖКТ, работающим с кишечными симбионтами.
ELISPOT: ИФА для Т-клеток?
Антитела оказались удобным для измерения косвенным маркером иммунной памяти, но отсутствие антител еще не говорит об отсутствии Т-клеточной памяти. Специфичную иммунную память Т-клеток, к сожалению, нельзя измерить так же легко, по нескольким миллилитрам плазмы крови. Как упоминалось выше, Т-клетки не секретируют свои рецепторы в растворимом виде. Зато Т-лимфоциты, в соответствии со своей ролью дирижеров всего иммунного ответа, вырабатывают множество сигнальных молекул — цитокинов. Цитокины, в большинстве своем, — тоже растворимые молекулы, и их концентрацию можно измерить в объеме (суммарно), либо «подсветить» с помощью флуоресцентных меток сразу при их секреции из специфичных Т-клеток (и увидеть соответствие клетка—сигнал). На этом принципе основан иммуноферментный анализ на клональных отпечатках Т-клеток, или ELISPOT (enzyme-linked immunosorbent spot).
Как правило, Т-хелперы секретируют сигнальные цитокины, чья основная задача — активировать нужную ветвь иммунного ответа, привлечь клетки врожденного иммунитета и подавить конкурирующие сигналы. Среди функций цитокинов — подача сигналов внутри иммунной системы — от Т-клеток и для Т-клеток для уточнения принятия решений. Подобная информация «для внутреннего использования» передается и от Т-хелперов Т-киллерам, и в обратном направлении. Яркий пример такого сигнала — интерферон-гамма: активированные Т-киллеры секретируют IFNγ наравне с Т-хелперами. Массовая выработка интерферона позволяет быстро распространить информацию на уровне всего организма. На основе измерения продукции IFNγ Т-клетками разработан самый надежный из ELISPOT-тестов на антиген-специфичный Т-клеточный ответ [7], [8].
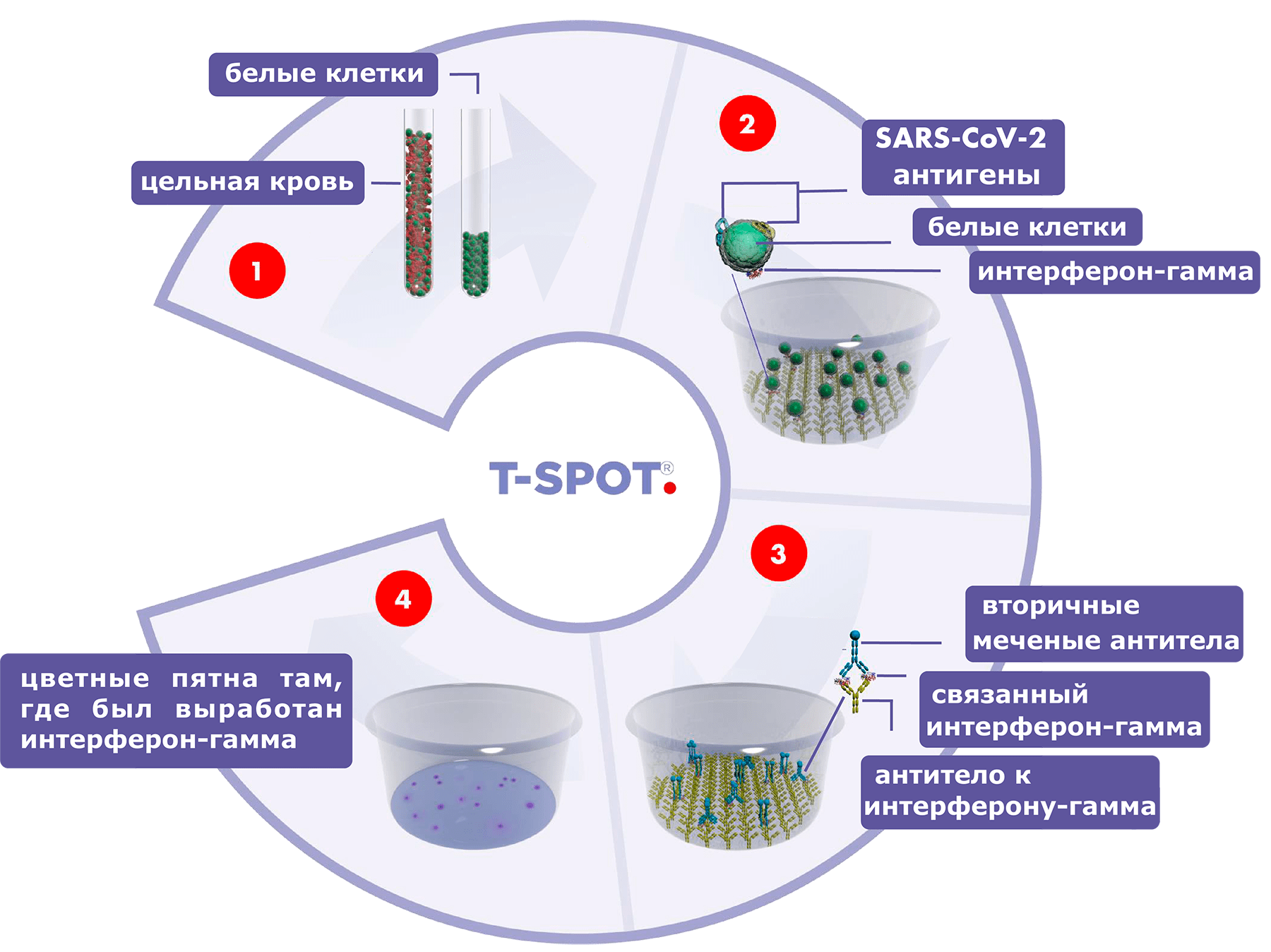
Для ELISPOT живые изолированные Т-клетки периферической крови инкубируются с антигенами, как правило, белковыми либо пептидными. Этот процесс должен имитировать то, как в организме Т-клетки в лимфоузлах узнают антигены и активируются: процесс презентации антигена. Небольшая доля специфичных клеток узнает антигены и производит IFNγ, причем интерферон сразу фиксируется и позже визуализируется в точке секреции. В процессе активации Т-клетки делятся: из одной клетки образуется целый клон антигенспецифичных клеток, все они производят интерферон, и при визуализации «пятно» продукции интерферона растет в диаметре (рис. 1). При ELISPOT сложно точно сказать, сколько антигенспецифичных клонов было изначально в образце до активации, размножения и формирования пятна. Остается неясным, сколько Т-клеток узнают антиген in vivo, но не прореагировали из-за искусственной формы презентации антигена, не похожей на то, как Т-клетки обычно активируются в лимфоузлах. С другой стороны, метод немного проще оптимизировать в лаборатории и проще делать для многих пациентов одновременно, чем более дорогостоящий FACS-анализ; требующиеся приборы и реагенты дешевле.
Рисунок 1. Схема работы теста ELISPOT, определяющего активацию Т-лимфоцитов при взаимодействии с антигенами нового коронавируса SARS-CoV-2
[11], рисунок с изменениями
Поиск коронавирусных Т-клеток. Инновация TScan
ELISPOT используется во всех лабораториях, которые исследуют иммунитет человека. Метод ELISPOT и его модификации на пересекающихся пулах пептидов (наборах фрагментов, на которые нарезается белковый антиген) использовались в исследованиях эффективности вакцин от ВИЧ, и позже медленно распространились на исследования и других вакцин. В диагностических лабораториях метод стал популярен потому, что для более точной диагностики туберкулеза необходимо оценивать Т-клеточный иммунный ответ. Коммерческий тест получил название T-SPOT. Кроме туберкулеза, для других инфекций аналогичная диагностика не применялась — до 2020 года и кризиса, вызванного новой коронавирусной инфекцией SARS-CoV-2. Необходимость широкой диагностики самой инфекции и иммунной памяти к ней подтолкнула одновременно исследователей и производителей диагностических тестов к разработке новых методов и оптимизации старых и привычных. Интерес к быстрому и дешевому измерению Т-клеточной памяти растет параллельно с популярными в медиа опасениями, что у переболевших COVID-19 быстро пропадают антитела в крови.
Очень многие академические коллективы, которые работают на стыке биохимии, иммунологии человека и прикладных биотехнологий, весной 2020 года стали заниматься разработками для борьбы с пандемией, в том числе разрабатывать и налаживать диагностику инфекции. Нельзя не упомянуть пример коллектива Григория Ефимова из НМИЦ гематологии в Москве, активно работающий как над диагностикой Т-клеточного иммунитета к новому коронавирусу на основе FACS, так и в коллаборации по созданию одного из ИФА-тестов для определения антител к антигенам SARS-CoV-2 [9], [10]. Тем не менее вернемся к теме масштабируемого производства быстрых ELISPOT-тестов на Т-клеточный иммунитет: откуда берутся такие разработки, тоже из фундаментальных и клинических академических лабораторий?
Первой ELISPOT-тест на ковид (T-SPOT Discovery SARS-CoV-2 assay) выпустила компания Oxford Immunotec, ранее создавшая одну из самых популярных версий теста на туберкулез [11]. Этот тест использует пул разнообразных антигенов коронавируса и активацию Т-клеток в смеси с другими лейкоцитами периферической крови: иначе говоря, дизайн теста даже несколько упрощен по сравнению с тестом на туберкулез (рис. 1).
Куда более интересную модификацию запустил небольшой биотех-стартап под названием TScan Therapeutics. Этот стартап переориентировался на инфекционную иммунологию во время пандемии. Как и многие другие коллективы, к примеру, BioNTech (разработчик вакцины от коронавируса совместно с Pfizer), до пандемии они занимались онкологией и задачей оптимальной активации противоопухолевого иммунитета.
Осенью 2020 года TScan Therapeutics подписали соглашение о совместной разработке диагностического теста ELISPOT-типа с компанией Qiagen — крупнейшим производителем лабораторных реагентов и универсальных наборов для типовых экспериментов в молекулярной и клеточной биологии [12], [13]. Эта диагностика Т-клеточной памяти во многом отличается от версии Oxford Immunotec, и в первую очередь отличается идеологически: оксфордская компания быстро и практично сделала аналог своего существующего продукта-бестселлера, сохранив всю платформу и протокол метода и изменив только антиген. TScan же демонстрирует почти идеальный инновационный подход: вначале провели исследования Т-клеточного иммунитета, опубликовали выводы в престижном журнале Immunity, затем появилась идея для диагностического теста и, наконец, возможность производства в партнерстве с Qiagen.
Исследование TScan раскрывает детали того, какие молекулы среди белков коронавируса вызывают наибольший «интерес» у Т-клеток человека [14]. Иммунная память Т-киллеров, согласно исследованию, формируется не только и не столько на фрагменты антигена (эпитопы) S-белка коронавируса, на котором сфокусировано большинство вакцин 2020 года [15]. Напротив, эпитопов гораздо больше в нуклеокапсидном основном белке [16]. Далее, специалисты TScan показали отсутствие перекрестного иммунитета: антигены «сезонных» неопасных человеческих коронавирусов формируют память Т-киллеров, но эти Т-киллеры не способны отреагировать на коронавирус SARS-CoV-2. Наоборот, между SARS-CoV-1 (вызвавшим вспышку атипичной пневмонии в 2003 году) и SARS-CoV-2 существует значительная кросс-реактивность Т-клеток (переболевшие атипичной пневмонией могут быть защищены от SARS-CoV-2).
Обнаружение важнейших участков вируса, вызывающих долгую Т-клеточную память — это поиск иммунодоминантных эпитопов. Если активировать Т-клетки именно такими пептидами, можно существенно повысить качество диагностического теста. Уникальные данные TScan позволяют вычесть фон иммунной памяти на родственные и далекие коронавирусы и поднять специфичность диагностики иммунной памяти. При этом используется платформа, сходная с ELISPOT, что позволяет объединять много образцов и делать тест быстрым и широко доступным. Сейчас исследования Т-клеточного иммунитета при коронавирусе проводится либо в рамках научных исследований, либо на коммерческой основе, но точность и интерпретация теста затруднена, клиент получает результат через 1–2 неделю после теста. Партнерство TScan с Qiagen вселяет оптимизм по поводу доступности теста: ведь продукцией этой компанией пользуются буквально в каждой молекулярной и биохимической лаборатории на планете.
Интересна еще одна деталь. Исследователи из TScan брали донорские Т-клетки у доноров с наиболее распространенными в США генотипами других важных иммунных молекул: молекул HLA (молекул главного комплекса гистосовместимости, Human Leukocyte Antigen) подтипов HLA-A*02:01, HLA-A*01:01, HLA-A*03:01, HLA-A*11:01, HLA-A*24:02 и HLA-B*07:02. В зависимости от типа молекул HLA Т-клетки будут распознавать разные эпитопы одного и того же вируса. А поскольку у разных людей максимально вариабельные молекулы HLA, то и иммунный ответ Т-клеток у каждого формируется максимально индивидуально. Именно с этим связаны и сложности/дороговизна изучения Т-клеточного иммунитета, и невозможность «перелить иммунную память» переливанием крови — такой эксперимент может получиться только внутри пары однояйцевых близнецов. С другой стороны, даже в этом огромном разнообразии реакций клеточного иммунитета Т-клетки разных доноров, отвечающие на новый коронавирус, обладают некоторыми общими характеристиками.
Данные об общих параметрах иммунного ответа, которые будут накапливаться в совместных исследованиях TScan/Qiagen, представляют несомненный интерес для оптимизации лечения пациентов и создания методов лечения, таргетно направленного на активный и безопасный Т-клеточный ответ. Здесь проявляется особая черта сильных deeptech-стартапов в области биологии, биоинформатики и биотехнологий: технологическая платформа может быть использована не только для одного применения и быстрого завоевания рынка, а для разных задач, и в процессе, по ходу решения прикладной задачи возникают ценные, качественные и заметные научные открытия. Конечно, новость о сотрудничестве TScan и Qiagen — всего лишь одна из множества историй о биотех-прорывах 2020 года, и легко могла затеряться среди других новостей и инноваций. Но в этой неприметной новости заложен мощный потенциал, способный изменить современные представления о клинической диагностике иммунной памяти.