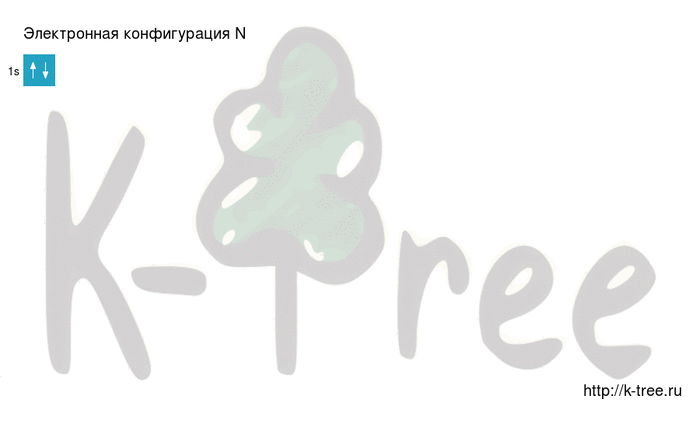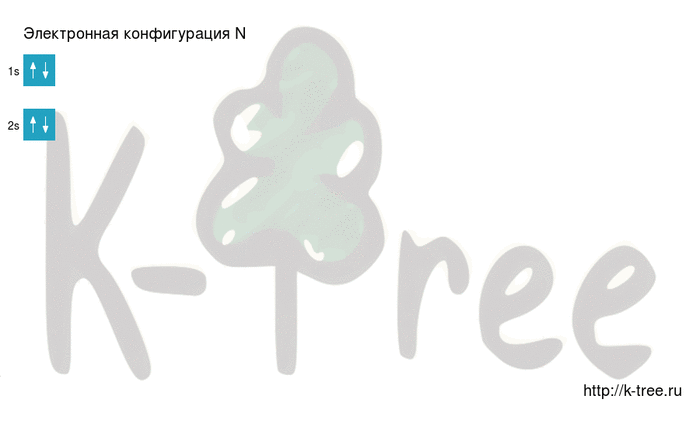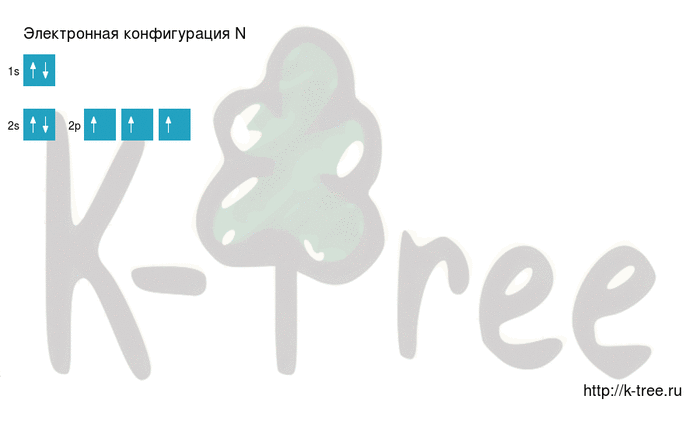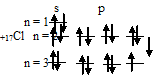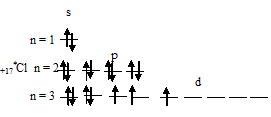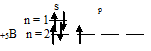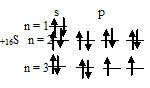Азот N
Азот в таблице менделеева занимает 7 место, в 2 периоде.
| Символ | N |
| Номер | 7 |
| Атомный вес | 14.0064300 |
| Латинское название | Nitrogenium |
| Русское название | Азот |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема азота
Порядок заполнения оболочек атома азота (N) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Азот имеет 7 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
3 электрона на 2p-подуровне
Степень окисления азота
Ионы азота
Валентность N
Атомы азота в соединениях проявляют валентность V, IV, III, II, I.
Валентность азота характеризует способность атома N к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа N
Квантовые числа определяются последним электроном в конфигурации, для атома N эти числа имеют значение N = 2, L = 1, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Соединения азота
| Тип | Формула | Название |
|---|---|---|
| Кислота | HNO3 | Азотная кислота |
| HNO2 | Азотистая кислота | |
| Основание | NH3 | Аммиак |
| Оксид | N2O | Оксид азота (I) |
| NO | Монооксид азота | |
| N2O3 | Азотистый ангидрид | |
| NO2 | Диоксид азота | |
| N2O5 | Азотный ангидрид |
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Графическое заполнение валентных энергетических слоев | Электронные конфигурации атомов
в) Электронная конфигурация 3s 2 верна, потому что на третьем энергетическом уровне (n = 3) находятся s-, p- и d-подуровни. Согласно правилу Хунда, на s-подуровне, состоящем из одной атомной орбитали, может находиться максимальное число электронов равное двум.
г) Электронная конфигурация 2s 2 реализуется, потому что на втором энергетическом уровне (n = 2) содержатся s- и p-подуровни, и на s-подуровне, в его единственной атомной орбитали, может содержаться максимальное число электронов равное двум.
д) Электронная конфигурация 2d5 не реализуется, потому что во втором энергетическом уровне (n = 2) d-подуровень не содержится, в этом слое расположены только s- и p-подуровни.
е) Электронная конфигурация 5d 2 реализуется, потому что на пятом энергетическом уровне (n = 5) содержатся s-, p- d- и f-подуровни. Подуровень d содержит пять атомных орбиталей, в которых может находиться максимальное число электронов равное десяти (5 . 2 = 10). Запись 5d 2 означает, что на 5d-подуровне содержится два неспаренных электрона.
ж) Электронная конфигурация 3f 12 не реализуется, потому что на третьем энергетическом уровне (n = 3) могут находиться только s-, p- и d-подуровни.
з) Электронная конфигурация 2p4 реализуется, потому что на втором энергетическом уровне (n = 2) могут находиться только s- и p-подуровни. Подуровень p состоит из трёх атомных орбиталей, на которых, согласно правилу Хунда, может находиться до шести электронов.
и) Электронная конфигурация 3p7 не реализуется, потому что на p-подуровне, состоящем из трёх атомных орбиталей, согласно правилу Хунда, максимальное число электронов равно 6.
Таким образом, внешний энергетический уровень атома хлора имеет свободные орбитали на 3d-подуровне, что позволяет электронам переходить в возбуждённое состояние (перемещаться на более высокие свободные орбитали). У атома хлора возможно три состояния перемещения электронов на более высокие свободные орбитали, электроны с s- и p-подуровней переходят на 3d-подуровень:
1) При затрате некоторой энергии один из 3p-электронов атома хлора может быть переведён на вакантную 3d-орбиталь, при этом энергия атома возрастает, так что возникающая электронная конфигурация (1s 2 2s22p 6 3s 2 3p 4 3d 1 ) соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
В данном случае 3d-подуровень содержит четыре вакантные орбитали возбуждённого атома хлора.
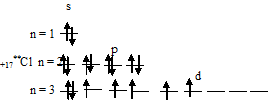
2) При затрате некоторой энергии два из 3p-электронов атома хлора могут быть переведены на вакантные 3d-орбитали, при этом энергия атома возрастает, так что возникает электронная конфигурация (1s 2 2s 2 2p 6 3s 2 3p 3 3d 2 ), которая соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
В таком возбуждённом состоянии атом хлора содержит три вакантные 3d-орбитали.
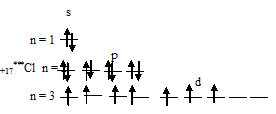
3) При затрате некоторой энергии один из 3s- и два 3p-электронов могут быть переведены на свободные 3d-орбитали, при этом энергия атома возрастает, так что возникающая конфигурация (1s 2 2s 2 2p 6 3s 1 3p 3 3d 3 ) также соответствует одному из возможных состояний хлора:
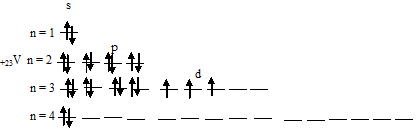
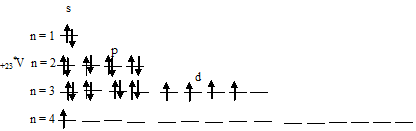
В возбуждённом состоянии атома ванадия один 4s-электрон может быть переведён на свободную 3d-орбиталь, так что возникающая электронная конфигурация валентного уровня (3d 4 4s 1 ) соответствует возбуждённому состоянию атома ванадия, что можно представить в виде схемы:
При возбуждении атома ванадия остаётся вакантной одна 3d-орбиталь.
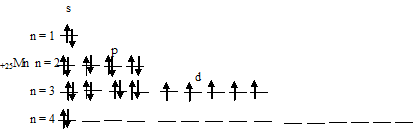
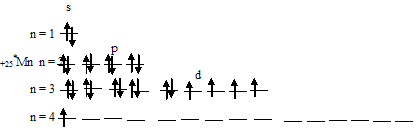
При возбуждении атома марганца один s-электрон переходит на 3d-орбиталь, при этом получается электронная конфигурация валентного уровня (3d 6 4s 1 ) соответствует возбуждённому состоянию атома марганца, что можно представить в виде схемы:
Из схемы вытекает, что при возбуждении атома марганца свободных d-орбиталей нет, так как на 3d-подуровне распределяются два спаренных электрона и четыре неспаренных. Таким образом, атом марганца ни в основном, ни в возбуждённом состоянии не имеет свободных d-орбиталей.
Следовательно, атом бора содержит один неспаренный 2p-электрон.
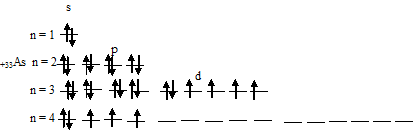
Таким образом, атом мышьяка имеет три неспаренных электрона на 4p-подуровне.
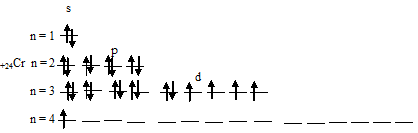
Следовательно, атом хрома в стационарном состоянии содержит шесть неспаренных электронов, из которых пять на 3d-подуровне и один на 4s-подуровне.
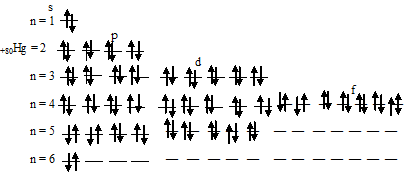
Атом ртути не содержит ни одного неспаренного электрона.
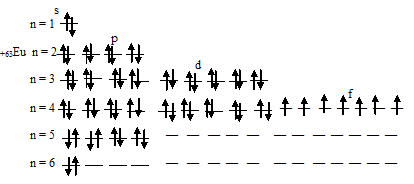
Таким образом, атом европия содержит семь неспаренных 4f-электронов.
Ответ: а) 1; б) 2; в) 3; г) 6; д) 0; е) 7.
Задача 187.
Указать особенности электронных конфигураций меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?
Решение:
Так как число электронов в атоме элемента равно его порядковому номеру, то общее число электронов в атоме меди и хрома соответственно равно 29 и 24.
Последовательность заполнения энергетических уровней и подуровней в атоме элемента определяется правилами Клечковского, согласно которым электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией (меньшая сумма n + l). Порядок заполнения подуровней определяется правилом Хунда. Согласно правилу Хунда, минимальной энергии атома соответствует такое распределение электронов по атомным орбиталям данного подуровня, при котором абсолютное значение суммарного спина атома максимально.
Электронные формулы атомов хрома и меди можно выразить следующим образом:
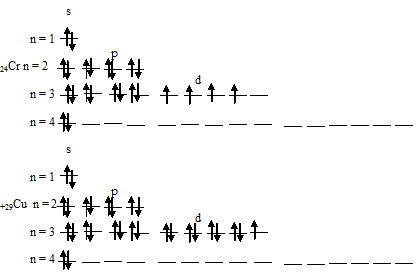
Таким образом, атомы хрома и меди на внешних энергетических уровнях содержат по одному 4-электрону. Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:
Азот N
Азот в таблице менделеева занимает 7 место, в 2 периоде.
| Символ | N |
| Номер | 7 |
| Атомный вес | 14.0064300 |
| Латинское название | Nitrogenium |
| Русское название | Азот |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема азота
Порядок заполнения оболочек атома азота (N) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Азот имеет 7 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
3 электрона на 2p-подуровне
Степень окисления азота
Ионы азота
Валентность N
Атомы азота в соединениях проявляют валентность V, IV, III, II, I.
Валентность азота характеризует способность атома N к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа N
Квантовые числа определяются последним электроном в конфигурации, для атома N эти числа имеют значение N = 2, L = 1, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Соединения азота
| Тип | Формула | Название |
|---|---|---|
| Кислота | HNO3 | Азотная кислота |
| HNO2 | Азотистая кислота | |
| Основание | NH3 | Аммиак |
| Оксид | N2O | Оксид азота (I) |
| NO | Монооксид азота | |
| N2O3 | Азотистый ангидрид | |
| NO2 | Диоксид азота | |
| N2O5 | Азотный ангидрид |
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Тест по теме:» Электронная конфигурация атома» ( формат 2017 года)
« Строение электронных оболочек атомов элементов первых четырёх периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояние атомов»
1) Na 2) K 3) Si 4) Mg 5) C
1) Na 2) K 3) Al 4) Mg 5) C
3. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне пять электронов
1) P 2) N 3) S 4) Al 5) O
4. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона
1) Be 2) Mg 3) Si 4) Cl 5) F
5. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне три электрона.
1) F 2) Ga 3) O 4) B 5) Se
6. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне семь электронов.
1) Kr 2) I 3) As 4) Br 5) P
7. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне один электрон
1) K 2) Br 3) Li 4) Ca 5) Ba
8. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона
1) Cs 2) Ca 3) Bi 4) N 5) Ba
9. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне семь электронов.
1) Sr 2) F 3) C 4) I 5) Sn
10. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона
1) Ne 2) S 3) Ba 4) Be 5) O
11. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне семь электронов
1) Cl 2) Si 3) As 4) Br 5) P
12. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона.
13. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне четыре электрона.
1) Pb 2) Si 3) I 4) At 5) Bi
14. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне четыре электрона.
1) C 2) N 3) Pb 4) Cs 5) Bi
15. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне один электрон.
1) Cs 2) Rb 3) Sr 4) Ba 5) Tl
1) Be 2) S 3) Bi 4) Ba 5) Po
17. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне 5 электронов.
1) As 2) Sb 3) Si 4) Sn 5) Sr
18. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне 6 электронов.
1) O 2) Si 3) Ga 4) Ge 5) Se
19. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне один 6 электронов.
1) S 2) С 3) O 4) N 5) P
20. Определите, атомы каких из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона.
1) P 2) Bi 3) Be 4) At 5) Ba
21. Три неспаренных электрона на внешнем уровне в основном состоянии имеют атомы элементов:1) Al 2)B 3) N 4)As 5)Cr
25. Восьмиэлектронную внешнюю оболочку в основном состоянии имеют частицы:1)Al 3+ 2) C 2+ 3) S 2- 4) F 5) Cl 5+
28. Электронную конфигурацию ls 2 2s 2 2p 6 имеют частицы:
29. Хлорид-ион имеет такую же электронную конфигурацию, как и:
1) катион кальция 2) гидрид-анион 3) атом брома
4) атом натрия 5) сульфид-анион
30. Возбуждённому состоянию отвечают электронные конфигурации:
1) 1s 2 2s 2 2p 2 2) 1s 2 2s 2 2p 6 3s 1 3p 3 3) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2
4) 1s 2 2s 2 2p 6 3s 2 3p 4 4s 1 5)1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2
31. Два неспаренных электрона на внешнем уровне в основном состоянии имеют атомы: 1)Mg 2)C 3) O 4) Fe 5)Cl
1 ) Na 2) К 3) F 4) Li 5) Cl
34. Определите, атомы каких из указанных в ряду элементов содержат во внешнем слое два электрона.1) Ba 2) Na 3) Fe 4) S 5) Si
1) Se 2) O 3) K 4) Te 5) Cs
1) Li 2) Ar 3) Na 4) Ne 5) Cs
1) K 2) S 3) Ar 4) Na 5) Se
1) Mg 2) Cl 3) S 4) Br 5) Ca
40. Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns 1
1) S 2) K 3) O 4) Te 5) Na
1) Li 2) Se 3) K 4) S 5) Cs
1) I 2) N 3) Br 4) P 5) Cl
1) I 2) N 3) Br 4) P 5) Cl
1) N 2) Sb 3) O 4) P 5) S
1) S 2) Na 3) He 4) Cl 5) Se
1) F 2) Br 3) N 4) P 5) I
1) Bi 2) N 3) Br 4) P 5) Cl
1) O 2) N 3) Te 4) S 5) As
50. Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns 2 np 1
1) S 2) Al 3) O 4) B 5) Te
1) Cs 2) He 3) Na 4) Ar 5) Ne
1) Ga 2) S 3) B 4) In 5) Se
1) Mg 2) Bi 3) Ba 4) Sr 5) Al
1) Te 2) Be 3) I 4) Ba 5) Sr
1) Mg 2) Al 3) Sb 4) N 5) P
1) O 2) S 3) N 4) Te 5) P
57. Определите, атомы каких из указанных в ряду элементов имеют на внешнем электронном слое по одному неспаренному электрону.
1) N 2) As 3) Cu 4) P 5) Cr
58. Определите, атомы каких из указанных в ряду элементов имеют 1 неспаренный электрон во внешнем слое в основном состоянии.
1) As 2) Cr 3) Na 4) V 5) Sc
1) N 2) S 3) P 4) Se 5) As
1) Se 2) Ca 3) Br 4) Sr 5) Ba
Среди приведенных частиц выберите те которые имеют такую же электронную конфигурацию как ион n3
Электронная конфигурация соответствует частице
1)
2)
3)
4)
Определить количество электронов по электронной формуле, оно равно сумме верхних индексов — 20. Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У атома кальция количество электронов равно 20.
Определите два элемента, электронные конфигурации ионов которых соответствуют электронной конфигурации атома криптона. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Из указанных в ряду химических элементов выберите три р−элемента. Расположите выбранные элементы в порядке уменьшения их валентности в летучих водородных соединениях. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Из перечня элементов p−элементами являются фосфор, хлор и селен. Валентность химических элементов в их летучих водородных соединениях уменьшается слева направо по периоду. Тогда последовательность химических элементов в порядке уменьшения их валентности в летучих водородных соединениях следующая: фосфор — селен — хлор.
Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в кислородсодержащих анионах может быть одинаковой. Запишите в поле ответа номера выбранных элементов.
Калий и стронций не образуют кислородсодержащих анионов.
Селен образует кислородсодержащие анионы: селенат-анион и селенит-анион
Степени окисления +6 и +4, соответственно, что не характерно для кислородсодержащих анионов фосфора и хлора.
У фосфора и хлора есть кислородсодержащие анионы со степенью окисления хим. элемента +5: фосфат-анион и хлорат-анион
Электронная формула криптона:
1. у атома хлора заполняются три электронных слоя, а в атоме криптона заполнены четыре электронных слоя;
2. —
3. —
4. у атома фосфора заполняются три электронных слоя, а в атоме криптона заполнены четыре электронных слоя;
5. у атома калия 19 электронов в основном состоянии, а у криптона — 36 (получить такой анион калия не представляется возможным).
Электронная конфигурациясоответствует иону
1)
2)
3)
4)
Определить количество электронов по электронной формуле, оно равно сумме верхних индексов — 18. Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У иона серы количество электронов 16+2=18.
Сера ведь имеет заряд +14. Значит 14+2=16
Посмотрите в таблицу Менделева: сера имеет атомный номер 16, поэтому атом серы имеет 16 электронов.
Электронная конфигурация соответствует иону
1)
2)
3)
4)
Определить количество электронов по электронной формуле, оно равно сумме верхних индексов — 18. Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У иона серы 16+2=18.
Электронную конфигурацию инертного газа имеет ион
1)
2)
3)
4)
Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. Для предложенных ионов посчитать количество электронов и сравнить с номерами инертных газов. У иона хлора количество электронов 17+1=18, что соответствует конфигурации инертного газа аргона.
Электронная конфигурация соответствует иону
1)
2)
3)
4)
Определить количество электронов по электронной формуле, оно равно сумме верхних индексов — 18. Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У иона хлора 17+1=18.
Электронную конфигурацию ls 2 2s 2 2p 6 имеет ион
Количество электронов в атоме химического элемента определяется порядковым номером. При образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У иона магния количество электронов 12 − 2 = 10.
Электронная конфигурация 1s 2 2s 2 2p 6 соответствует
1) атому
2) иону
3) иону
4) иону
Указанные атомы и ионы имеют следующее кличество электронов: 6, 10, 18, 18. Даже по количеству электронов видно что электронная конфигурация 1s 2 2s 2 2p 6 соответствует иону кислорода.
Определите, двум атомам каких из указанных элементов до завершения внешнего уровня не хватает двух электронов. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Выберите три элемента, которые в периодической системе находятся в одном периоде, и расположите эти элементы в порядке уменьшения радиуса атома. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Элемент находится вo 2 периоде,
— в 3 периоде,
— во 2 периоде,
— вo 2 периоде,
— в 3 периоде. Таким образом, нужные элементы — это
,
,
. Известно, что атомный радиус уменьшается вверх по группе и вправо по периоду, поэтому последовательность этих атомов в порядке уменьшения атомного радиуса выглядит как
→
→
.
Выберите два элемента, высшая степень окисления которых равна +4. Запишите в поле ответа номера выбранных элементов.
Максимальная положительная степень окисления элемента обычно численно совпадает с номером его группы в периодической системе. и
находятся в 4 группе и имеют высшую степень окисления +4,
и
находятся в 6 группе и имеют степень окисления +6,
— вo 2 группе, и степень окисления +2.
1. Углерод имеет электронную конфигурацию , т. е. до заполнения уровня не хватает еще 4х электронов.
2. Кремний имеет электронную конфигурацию , т. е. до заполнения уровня не хватает еще 4х электронов.
3. Кислород имеет электронную конфигурацию , т. е. до заполнения уровня не хватает еще 2х электронов.
4. Бериллий имеет электронную конфигурацию , т. е. до заполнения уровня не хватает еще 6 электронов на
орбитали.
5. Сера имеет электронную конфигурацию , т. е. до заполнения уровня не хватает еще 2х электронов.
Электронная конфигурация соответствует частице
1)
2)
3)
4)
Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. Для предложенных ионов посчитать количество электронов и сравнить с количеством электронов в предложенной формуле, оно равно сумме всех верхних индексов − 18. У иона фосфора количество электронов 15+3=18.
а почему кислород не подходит?
У иона кислорода было бы 10 электронов.
15.999 почти 16 я просто округлил братан.
Это относительная атомная масса, а не количество электронов.
Электронная конфигурация 1s 2 2s 2 2p 6 3s 2 3p 6 соответствует частице
Количество электронов в атоме химического элемента определяется порядковым номером, при образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. Для предложенных ионов посчитать количество электронов и сравнить с количеством электронов в предложенной формуле, оно равно сумме всех верхних индексов − 18. У иона кальция количество электронов 20-2=18.
Электронную конфигурацию 1s 2 2s 2 2p 6 3s 2 3p 6 имеет ион
Количество электронов в атоме химического элемента определяется порядковым номером. При образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. У иона хлора количество электронов 17 +1 = 18.
18-м элементом таблицы Менделеева является аргон(Ar), а не хлор(Cl)
но там же кислород тоже получается правильный ответ!!
У иона кислорода 10 электронов.
Электронная конфигурация 1s 2 2s 2 2p 6 3s 2 3p 4 соответствует
1) атому
2) иону
3) иону
4) атому
Указанные атомы и ионы имеют следующее количество электронов: 8, 18, 18, 16. Даже по количеству электронов видно что электронная конфигурация 1s 2 2s 2 2p 6 3s 2 3p 4 соответствует атому серы.
Одинаковую электронную конфигурацию имеют
1) атомы и
2) ионы и
3) ион и атом
4) ионы и
Эти частицы будут иметь одинаковую электронную конфигурацию если будут иметь одинаковое количество электронов. Количество электронов в атоме химического элемента определяется порядковым номером. При образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. Поэтому посчитаем сколько электронов на внешней оболочке будут иметь эти ионы (считаем S и P электроны внешнего электронного уровня):
Видно, что правильный ответ №4.
Электронная конфигурация соответствует частице
1)
2)
3)
4)
У этой частицы 2+2+6+2+6=18 электронов.
Количество электронов в атоме химического элемента определяется порядковым номером. При образовании положительно заряженного иона количество электронов уменьшается на величину заряда данного иона, при образовании отрицательно заряженного иона количество электронов увеличивается на величину заряда данного иона. Поэтому посчитаем сколько электронов будут иметь эти ионы:
Значит верный ответ №1.
Определите, атомы каких двух из указанных элементов имеют в основном состоянии один неспаренный электрон. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Выберите три элемента, которые в Периодической системе находятся в одном периоде, и расположите эти элементы в порядке уменьшения элекроотрицательности. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Элементы находятся во 2-ом периоде,
— в 3-ем. Таким образом, нужные элементы — это
. Известно, что уменьшение электроотрицательности идет вниз по группе и влево по периоду, поэтому последовательность этих атомов в порядке уменьшения электроотрицательности выглядит как
→
→
.
Выберите два элемента, которые в соединениях могут иметь степень окисления –1. Запишите в поле ответа номера выбранных элементов.
Металлы не проявляют отрицательную степень окисления, поэтому их можно исключить из данного списка. Остаются кремний, хлор и кислород.
Кремний в соединениях имеет степени окисления: −4; 0; +2; +4.
Хлор : −1; 0; +1; +2; +3; +4; +5; +6; +7.
Кислород : −2; −1; 0; +1; +2.
1. Литий имеет конфигурацию . На
подуровне, где максимум может быть 2 электрона, у него только 1, он же как раз неспаренный.
2. Кремний имеет конфигурацию . На
подуровне, где должно быть 6 электронов, т. е. 3 электронные пары, только 2 электрона, оба по правилу Хунда неспарены.
3. Бериллий имеет конфигурацию . На
орбитали все электроны спарены, на
орбитали их нет.
4. Хлор имеет конфигурацию . На
подуровне, где должно быть 6 электронов, т. е. 3 электронные пары, только 5 электронов, а значит 4 из низ спарены в 2 электронные пары, а один неспарен.
5. Кислород имеет конфигурацию . На
подуровне, где должно быть 6 электронов, т. е. 3 электронные пары, только 4 электрона, по правилу Хунда 2 из них неспарены.