Сопоставляя свойства таких химических элементов как углерод азот водород и кислород можно утверждать
Подробное решение параграф § 6 по биологии для учащихся 10 класса, авторов Пасечник В.В., Каменский А.А., Рубцов A.M. Углубленный уровень 2019
Вопрос 1. Каковы основные положения атомно — молекулярного учения?
1) Все вещества состоят из молекул.
2) Молекулы состоят из атомов. Атомы каждого вида (элемента) одинаковы между собой, но отличаются от атомов любого другого вида.
3) Частицы — молекулы и атомы — находятся в непрерывном движении. Тепловое состояние тел есть результат движения их частиц.
4) При взаимодействии атомов образуются молекулы: гомоядерные — при соединении атомов одного вида (например, H2, O2), образующиеся при этом вещества называются простыми; гетероядерные — при взаимодействии атомов разного вида (например, H2O, H2SO4), образующиеся при этом вещества называются сложными.
5) При физических явлениях молекулы сохраняются, при химических — разрушаются (или образуются новые). Атомы же и при физических, и при химических реакциях остаются неизменными.
6) Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состоят первоначальные вещества.
Вопрос 2. Что такое химические элементы? Как устроены атомы разных химических элементов?
Химический элемент — совокупность атомных частиц (электронейтральных атомов и одноатомных ионов) с одинаково положительным зарядом ядра.
Атомы чрезвычайно малы, их диаметр колеблется в пределах 0,2 — 0,5 нм (1 нм = 10 — 9 м). Массы атомов составляют порядка 10 — 24 — 10 — 22 г. Атомы имеют сложное строение и состоят из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов.
Вопрос 3. Что такое валентные электроны?
Валентные электроны — это такие электроны, которые участвуют в образовании химических связей.
Вопрос 4. Чем различаются свойства химических элементов главных и побочных подгрупп из левой и правой частей таблицы Менделеева?
Главное отличие в особенности заполнения электронами орбиталей и, соответственно, различие химических свойств.
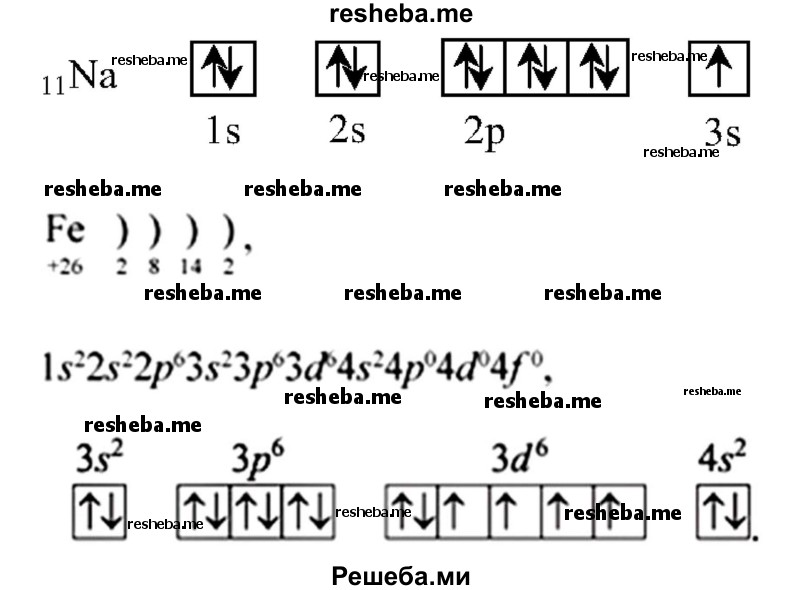
Химические свойства, например, у s — элементов 1 группы — валентность 1, степень окисления — +1. А у d — элементов — переменная валентность и степень окисления, т.к у них есть свободные орбитали для заполнения электронами. К примеру, представлены электронно — графические схемы Na и Fe.
Вопрос 5. Какие химические элементы относят к группе макроэлементов и почему?
К группе макроэлементов относят химические элементы, содержание которых в живых организмах превышает 0,01 %. В значительных количествах встречаются 4 хим. элемента (кислород, углерод, водород и азот) (в сумме около 96 %) и ещё 8: кальций, фосфор, калий, сера, хлор, натрий, магний и железо.
Вопрос 6. Из чего состоят молекулы различных веществ? Что лежит в основе образования их структуры?
Молекулы состоят из атомов различных химических элементов. в основе образования их структуры обеспечивается возникновением химической связи между входящими в их состав атомами. Эти связи возникают вследствие объединения электронных оболочек атомов, которые образуют молекулу.
Вопрос 7. Что лежит в основе разделения веществ на органические и неорганические?
В основе разделения веществ на органические и неорганические лежит происхождение и наличие углерода в составе этих веществ (СО, СО2, Н2СО3 и карбонаты — это неорганические вещества).
Вопрос 8. Какие особенности атомов углерода обусловливают многообразие органических веществ в природе?
Очень важной особенностью атома углерода является его способность образовывать связи сразу с четырьмя другими такими же атомами. Благодаря этой способности атомы углерода могут образовывать каркасы огромного количества разнообразных биологических молекул, что способствует появлению многообразных органических веществ в природе.
Вопрос 9. Какие органические вещества являются биополимерами? Приведите примеры известных вам регулярных и нерегулярных полимеров, гомо — и гетерополимеров.
Биополимеры — высокомолекулярные органические соединения, входящие в состав живых организмов (белки, полисахариды, нуклеиновые кислоты).
Пример регулярных полимеров: крахмал, полисахариды, целлюлоза, гликоген.
Пример нерегулярных полимеров: белки, нуклеиновые кислоты.
Пример гомополимеров: крахмал, полисахариды, целлюлоза, гликоген.
Пример гетерополимеров: белки, нуклеиновые кислоты.
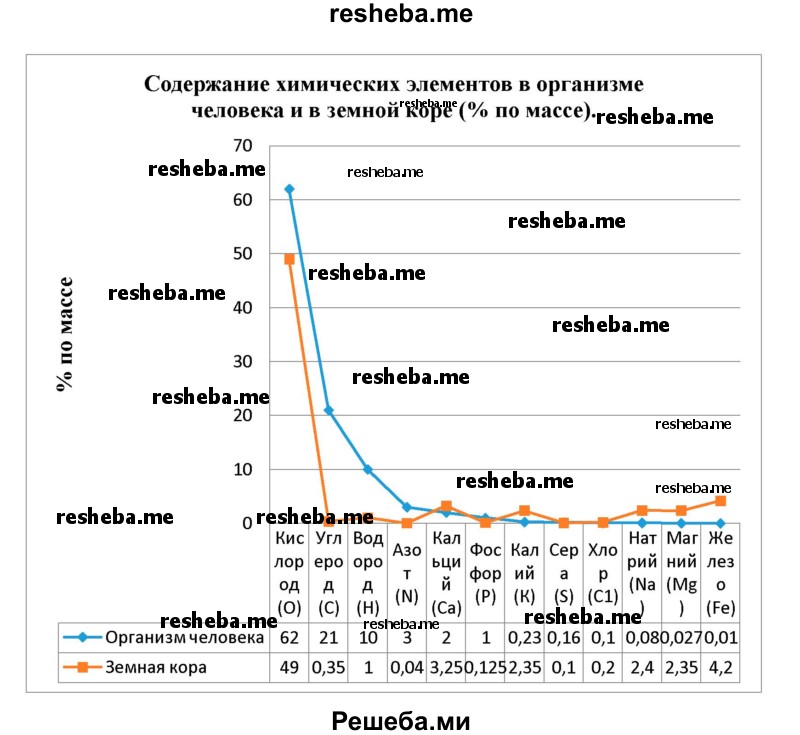
Вопрос 10. Используя данные таблицы 1, постройте диаграмму, отражающую содержание указанных в ней химических элементов в организме человека и в земной коре (% по массе).
Вопрос 11. Прочитайте статью «Химические связи в молекулах веществ». Составьте схему образования молекул известных вам веществ: водорода (Н2), кислорода (02), воды (Н20), хлорида натрия (NaCl) и метана (СН4). Подпишите на схеме названия типов химических связей, участвующих в образовании этих веществ.
В молекуле воды между атомами водорода и кислорода — ковалентная полярная связь. А водородная связь возникает МЕЖДУ МОЛЕКУЛАМИ ВОДЫ (а не В МОЛЕКУЛЕ воды).
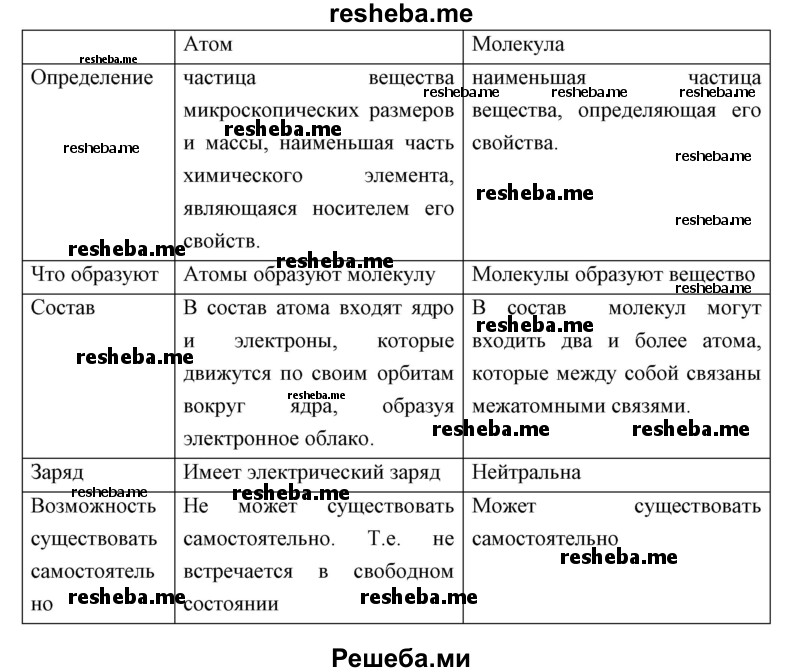
Вопрос 12. Используя материалы Википедии (https://ru.wikipedia.org), обобщите собственные представления о строении атома и молекул. Оформите их в виде таблицы.
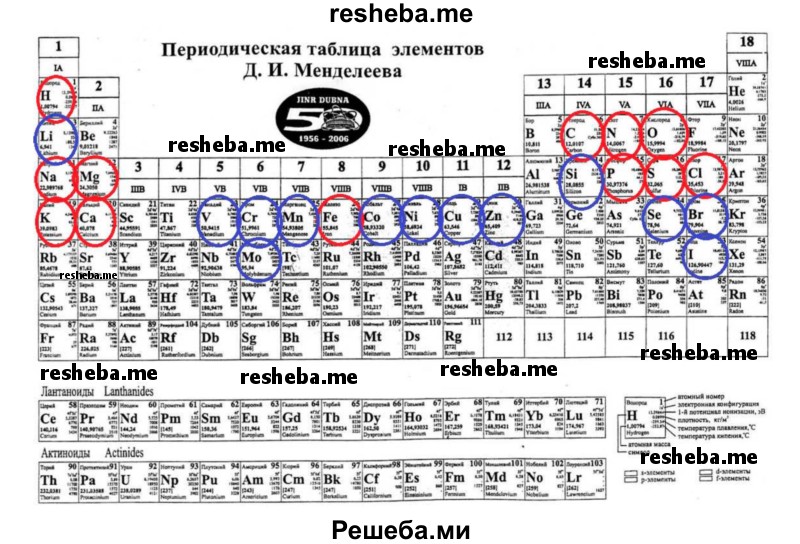
Вопрос 13. Используя доступные информационные источники, найдите и рассмотрите периодическую таблицу химических элементов Д. И. Менделеева. Найдите в ней элементы, относящиеся к микро — и макроэлементам. Атомы нескольких химических элементов обладают строением, сходным со строением атомов углерода. Назовите эти элементы. Могли бы они заменить углерод в структуре органических веществ? Ответ обоснуйте и подкрепите известными вам примерами.
К макроэлементам относятся 12 химических элементов: кислород, углерод, водород и азот, кальций, фосфор, калий, сера, хлор, натрий, магний и железо. Всего в живых организмах найдено более 80 химических элементов, однако содержание большинства из них крайне мало — это микроэлементы (медь, йод, цинк, кобальт, кремний, марганец, литий и др.).
Макроэлементы обозначены красным, а микроэлементы — синим.
Кремний, бор и азот обладают строением, сходным со строением атомов углерода. Но они не могут заменить углерод в структуре органических веществ, потому что:
1. Заполненный внешний электрический слой.
2. Обладает низкой окислительной способностью.
3. Строение атома элемента углерода включает две оболочки, на которых расположено шесть электронов. Валентность углерода, входящего в состав органических веществ, постоянна и равна IV. Это значит, что на внешнем электронном уровне находится четыре электрона, а на внутреннем — два.
4. Возбуждённый атом углерода имеет четыре неспаренных электрона. Его конфигурацию можно выразить формулой 2s12p3. Это даёт возможность образовывать четыре ковалентные связи с другими элементами.
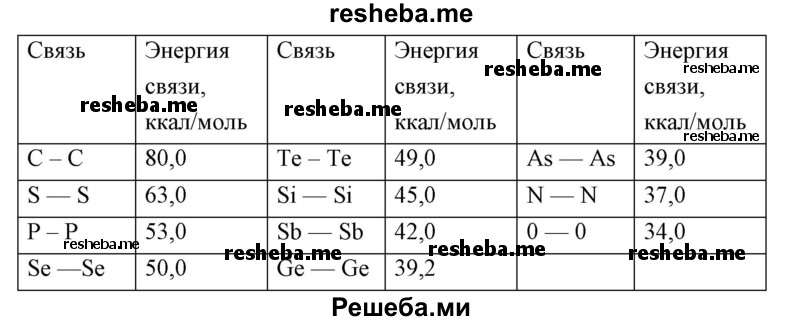
5. Полимерные молекулы способны образовывать в большей степени углерод, сера, фосфор, селен и теллур, а в меньшей — кремний, германий, бор, мышьяк (As), олово (Sn) и сурьма (Sb). Способность образовывать достаточно прочные гомоцепные полимеры зависит от прочности связей атомов данного элемента друг с другом (у углерода этот показатель самый высокий — 80 ккал/моль, смотрите табл.)
Табл. Энергия некоторых связей в гомоцепных полимерах.
Среди всех элементов периодической системы углерод выделяется своей уникальной способностью образовывать необычайно длинные цепи полимеров.
6. Атомы бора, кремния, фосфора и др., также образуют прочные цепи из атомов этих элементов (в элементарном состоянии). Но уникальность углерода обусловлена в значительной степени тем обстоятельством, что образуемые им углерод — углеродные связи прочны и в тех случаях, когда атомы углерода одновременно связаны с другими элементами. Например, углерод — водородные и углерод — фторные соединения высоко стабильны и в химическом отношении относительно мало реакционноснособны, а соответствующие производные бора, кремния, фосфора и т. д. либо не могут быть получены, либо являются крайне реакционноснособными веществами.
7. Атомы углерода могут связываться по — разному, называясь при этом аллотропами углерода.
Вопрос 14. Основные макроэлементы, в первую очередь углерод, водород и азот, присутствуют в живых организмах в больших количествах, чем в неживой природе. Почему? Что из этого следует?
Потому что все органические соединения получены соединением этих элементов. Это связано в основном с их валентностью, равной соответственно 1, 4 и 3, а также с их способностью образовывать более прочные ковалентные связи, нежели связи, образуемые другими элементами той же валентности. Атомы углерода способны образовывать цепочки и кольца, создавая гигантское разнообразие органических молекул. Вода — вещество с уникальными свойствами, способное растворять огромное разнообразие веществ, а также стабилизировать температуру за счет высокой теплоемкости, теплоты замерзания и теплоты испарения. Азот входит в состав аминокислот. Все эти элементы входят в обменные процессы клеток и являются жизненно необходимыми химическими компонентами живых организмов.
Присутствие в живых организмах этих химических элементов в больших количествах, чем в неживой природе, наталкивает на мысль: химические соединения, содержащие углерод, водород, кислород и азот (наиболее распространенные в живой природе элементы) были отобраны из неживой природы в ходе эволюции благодаря их особой приспособленности для участия в процессах жизнедеятельности.
Вопрос 15. Какую проблему необходимо учитывать учёным в связи с разработкой и внедрением в производство новых искусственно созданных органических веществ? Обсудите это с учителем и одноклассниками.
Здесь можно выделить не одну, а несколько проблем.
1. Уменьшение количества отходов с целью уменьшения вредного воздействия на окружающую природу.
В экологическом отношении коксохимическое производство является одним из наиболее опасных. На всех его стадиях выделяется значительная масса загрязнителей. На долю коксохимического производства приходится более 70% канцерогенов от их общего количества, образующегося в металлургии (бензол, каменноугольная смола и др.).
Добыча, переработка и транспортировка нефти сопряжены с загрязнением окружающей среды (в первую очередь загрязнение Мирового океана).
2. Сохранение невозобновляемых источников сырья.
3. Увеличение эффективности переработки сырья.
Например, при переработке нефти выход наиболее ценных продуктов (бензина) недостаточен и обычно не превышает 15%, что не может покрыть все возрастающий спрос народного хозяйства на этот и другие виды моторного топлива. Увеличения их выхода достигают применением химических процессов переработки, резко увеличивающих выход бензина (до 70% массы сырья).
Сопоставляя свойства таких химических элементов как углерод азот водород и кислород можно утверждать
Тип химической связи в соединении N2O5
ковалентная полярная
ионная
ковалентная неполярная
металлическая
Состав нуклеотидов рибонуклеиновой кислоты (РНК):
Тип ответа: Одиночный выбор
аденин, урацил, тимин, цитозин
аденин, урацил, цитозин, тимин
урацил, тимин, цитозин, гуанин
аденин, тимин, цитозин, гуанин
Гомологи имеют … свойства
близкие физические и химические
близкие химические, но разные физические
разные физические и химические
Ациклические ненасыщенные углеводороды – это …
алкены
спирты
алканы
циклоалканы
4.Состав нуклеотидов рибонуклеиновой кислоты (РНК):
аденин, урацил, тимин, цитозин
аденин, урацил, цитозин, тимин
урацил, тимин, цитозин, гуанин
аденин, тимин, цитозин, гуанин
6.Количество протонов, нейтронов и электронов в соединении HNO3.
p = 30, e = 32, n = 32
p = 16, e = 18, n = 15
p = 32, e = 32, n = 31
p = 16, e = 16, n = 16
15.Перманганат калия К2Сг2О7 диссоциирует следующим образом.
2К- + Cr2О72+
2К+ + Cr2O7-
К2+ + Cr2О72-
2К+ + Cr2О72-
25. Изомеры имеют. свойства
близкие физические, но разные химические
разные физические и химические
близкие химические, но разные физические
близкие химические и физические
26. Фосфат натрия Na3PO4 диссоциирует следующим образом.
Na3- + PO43+
3Na+ + PO43-
Na3+-+ PO43-
3Na+ + 3PO4-
27.Правильная последовательность усиления металлических свойств элементов.
натрий, калий, магний
калий, натрий, магний
магний, натрий, калий
натрий, магний, калий
29.Правильная последовательность усиления неметаллических свойств элементов.
хлор, бром., селен
бром, хлор, селен
селен, бром, хлор
хлор, селен, бром
31.Общая формула гомологического ряда карбоновых кислот.
CnH2nO
CnH2n + 1C00H
Cn(H2O)m
CnH2n + 1OH
Растворимость, для которой ΔH > 0, ΔS 0,-.
ограниченная
неограниченная
очень малая
Растворимость, для которой ΔH > 0, ΔS > 0,-.
очень малая
ограниченная
неограниченная
Восстановителем называется элемент, который в ходе реакции …
отдает электроны и окисляется
отдает электроны и восстанавливается
присоединяет электроны и окисляется
присоединяет электроны и восстанавливается
Вещество C6H5OH – это …
кислота
основание
спирт
фенол
Углеводород C7H8 – это …
арен
циклоалкан
алкан
алкен
Гомологи имеют … свойства
близкие физические и химические
близкие химические, но разные физические
разные физические и химические
близкие физические, но разные химические
Ациклические ненасыщенные углеводороды – это …
алкены
спирты
алканы
циклоалканы
Ациклические насыщенные углеводороды – это …
алканы
циклоалканы
спирты
алкены
Функциональная группа органических кислот: …
CH2
COOH
-OH
-CO
Изомеры имеют … свойства
близкие химические, но разные физические
разные физические и химические
близкие химические и физические
близкие физические, но разные химические
Объемная доля – это …
число молей растворенного вещества в 1 кг растворителя
отношение числа молей растворенного вещества к сумме числа молей растворителя и растворенного вещества
число молей растворенного вещества в 1 литре раствора
отношение объема растворенного вещества к сумме исходных объемов растворителя и растворенного вещества
С ростом величины стандартного потенциала металла …
уменьшается и восстановительная активность его атомов и окислительная активность ионов
увеличивается восстановительная активность его атомов и уменьшается окислительная активность ионов
увеличивается и восстановительная активность его атомов и окислительная активность ионов
уменьшается восстановительная активность его атомов и увеличивается окислительная активность ионов
Гомологом C6H6 является …
C6H10
C6H12
C7H8
C5H12
Общая формула алканов: …
C2nH2n
CnH2n-2
CnH2n
CnH2n+2
Молярная доля – это …
число молей растворенного вещества в 1 литре раствора
число молей растворенного вещества в 1 кг растворителя
отношение объема растворенного вещества к сумме исходных объемов растворителя и растворенного вещества
отношение числа молей растворенного вещества к сумме числа молей растворителя и растворенного вещества
При взаимодействии спирта с кислотой образуются …
сложный эфир и вода
соль и сложный эфир
простой эфир и вода
соль и вода
Ациклические насыщенные углеводороды – это …
алканы
циклоалканы
спирты
алкены
Сопоставляя свойства таких химических элементов как углерод азот водород и кислород можно утверждать
Химический состав клетки
В живых организмах содержится большое количество химических элементов. Они образуют два класса соединений — органические и неорганические.
В организме человека обнаружено 86 постоянно присутствующих элементов периодической системы Менделеева. Из них 25 необходимы для поддержания жизнедеятельности, 18 из которых абсолютно необходимы, а 7 — полезны. На долю четырех химических элементов — кислорода, водорода, углерода и азота — приходится около 98% массы клетки. Другие элементы присутствуют в ней в незначительных количествах: серы 0,15-0,2%, цинка 0,003%, а йода — всего 0,000001%.
Основные вещества клетки включают молекулы нуклеиновых кислот, белков, жиров, углеводов, воды, кислорода и углекислого газа. В неживой природе эти вещества нигде не встречаются вместе.
Основные вещества клетки =
= Нуклеиновые кислоты + Белки + Жиры (липиды) + Углеводы + Вода + Кислород + Углекислый газ
В составе клеток человеческого тела преобладают:
Знак химического элемента
В состав живых клеток входят ряд относительно простых соединений, которые встречаются в неживой природе — в минералах, природных водах. Это неорганические соединения.
Вода — одно из самых распространённых веществ на земле. У человека содержание воды в различных тканях и органах варьирует от 20% (в костной ткани) до 85% (в головном мозге). Около 2/3 массы человека составляет вода. Свойства воды настолько важны для живых организмов, что нельзя представить себе жизни без этого соединения водорода с кислородом.
В жидкой воде молекулы подвижны, что немаловажно для процессов обмена веществ. Молекулы воды легко проникают через клеточные мембраны. В воде растворяется больше веществ, чем в любой другой жидкости. Именно поэтому в водной среде клетки осуществляется множество химических реакций. Вода растворяет продукты обмена веществ и выводит их из клетки и организма в целом.
Вода обладает высокой теплопроводностью. Такое свойство создаёт возможность равномерного распределения теплоты между тканями тела.
Химические соединения, основой которых являются атомы углерода, составляют отличительный признак живого. Эти соединения называются органическими. Органические соединения чрезвычайно многообразны, но только четыре класса их имеют всеобщее биологическое значение: белки, нуклеиновые кислоты, углеводы, липиды.
Органическими веществами называют химические соединения, в состав которых входят атомы углерода. Атомы углерода способны вступать друг с другом в прочную ковалентную связь, образуя множество разнообразных цепочечных или кольцевых молекул. Самыми простыми углеродсодержащими соединениями являются углеводороды, соединения, которые содержат только углерод и водород. Однако в большинстве органических соединений содержатся и другие элементы (кислород, азот, фосфор, сера).
Углеводы широко распространены в живых клетках. В состав молекулы углеводов входит углерод, водород и кислород. Общая формула углеводов Cn(H2O)m. Примером углеводов может служить глюкоза.
Её формула C6H12O6.
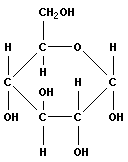
Структурная формула и модель молекулы глюкозы
Глюкоза является простым сахаром. В состав молока входит дисахарид, который состоит из остатков двух простых сахаров. Тысячи остатков простых сахаров образуют молекулы полисахаридов. В составе живых организмов много полисахаридов. Полисахариды относятся к биополимерам («био» — жизнь, «поли» — много).
У растений — это крахмал, у животных — это гликоген. Они состоят из тысяч молекул глюкозы.
Липиды.
Липиды разнообразны по структуре. Всем им присуще одно общее свойство — они неполярные. К липидам относятся жиры, жироподобные вещества. В клетке при окислении жиров образуется большое количество энергии, которая используется на различные процессы. Жиры могут накапливаться в клетках и служить запасом энергии.
Белки.
Белки — обязательная составная часть всех клеток. В состав этих биополимеров входят 20 типов мономеров. Такими мономерами являются аминокислоты. Аминокислоты получили своё название потому, что содержат и аминогруппу (–NH2), и кислотную карбоксильную группу (–COOH).
Образование линейных молекул белков происходит в результате соединения аминокислот друг с другом. Карбоксильная группа одной аминокислоты сближается с аминогруппой другой, и при отщеплении молекулы воды между аминокислотными остатками возникает прочная ковалентная связь, называемая пептидной. Соединение, состоящее из большого числа аминокислот, называется полипептидом. Каждый белок по своему составу является полипептидом.
Выделяют первичную, вторичную, третичную и четвертичную структуры белков.
Первичная структура определяется порядком чередования аминокислот в полипептидной цепи. Двадцать аминокислот можно уподобить 20 буквам химического алфавита, из которых составлены «слова» длиной в 300–500 букв. С помощью 20 букв можно написать безграничное множество таких длинных слов. Известно, что замена даже одного аминокислотного звена другим в белковой молекуле изменяет её свойства.
В живой клетке многие молекулы белков или их отдельные участки представляют собой не вытянутую нить, а спираль с одинаковыми расстояниями между витками. Такая спираль представляет собой вторичную структуру белковой молекулы. Между группами N–H и C=O, расположенными на соседних витках, возникают водородные связи. Они намного слабее ковалентных, но, повторённые многократно, скрепляют регулярные витки спирали.
В результате взаимодействия различных остатков аминокислот спирализованная молекула белка образует клубок — третичную структуру. Для каждого вида белка характерна своя форма клубка с изгибами и петлями. Третичная структура зависит от первичной структуры, т.е. от порядка расположения аминокислот в цепи.
Наконец, некоторые белки, например гемоглобин, состоят из нескольких цепей, различающихся по первичной структуре. Объединяясь вместе, они создают сложный белок, обладающий не только третичной, но и четвертичной структурой.
Нуклеиновые кислоты.
В клетках имеются два типа нуклеиновых кислот: дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК). Эти биополимеры состоят из мономеров, называемых нуклеотидами. Мономеры-нуклеотиды ДНК и РНК сходны в основных чертах строения. Каждый нуклеотид состоит из трёх компонентов, соединённых прочными химическими связями.
Одно из четырёх органических соединений, называемых азотистое основание
Аденин (А)
Гуанин (Г)
Цитозин (Ц)
Тимин (Т)
Одно из четырёх органических соединений, называемых азотистое основание
Аденин (А)
Гуанин (Г)
Цитозин (Ц)
Урацил (У)
Остаток ортофосфорной кислоты
Остаток ортофосфорной кислоты
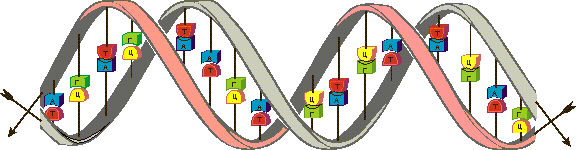
Модель молекулы ДНК
Порядок расположения нуклеотидов в молекулах ДНК определяет порядок расположения аминокислот в линейных молекулах белков, то есть их первичную структуру. Молекулы ДНК хранят сведения о свойствах белков и передают их поколениям потомков, то есть являются носителями информации.
Основные виды РНК.
Наследственная информация, хранящаяся в молекулах ДНК, реализуется через молекулы белков. Информация о строении белка передаётся в цитоплазму особыми молекулами РНК, которые называются информационными РНК (иРНК).
Информационная РНК строится комплиментарно одной из нитей ДНК, а в цитоплазме с помощью специальных органоидов рибосом идёт синтез белка.
В синтезе белка принимает участие и другой тип РНК – транспортная РНК (тРНК), которая подносит аминокислоты к месту образования белковых молекул — рибосомам, своеобразным фабрикам по производству белков.
В состав рибосом входит третий вид РНК, так называемая рибосомная РНК (рРНК), которая определяет структуру и функционирование рибосом.
Каждая молекула РНК в отличие от молекулы ДНК представлена одной нитью; вместо дезоксирибозы содержит рибозу и вместо тимина — урацил.
Итак, нуклеиновые кислоты выполняют в клетке важнейшие биологические функции. В ДНК хранится наследственная информация обо всех свойствах клетки и организма в целом. Различные виды РНК принимают участие в реализации наследственной информации через синтез белка.
Аденозинтрифосфорная кислота (АТФ).
Особо важную роль в биоэнергетике клетки играет адениловый нуклеотид, к которому присоединены два остатка фосфорной кислоты, называемое аденозинтрифосфорная кислота (АТФ). В химических связях между остатками фосфорной кислоты молекулы АТФ запасена энергия, которая освобождается при отщеплении фосфата:
где АДФ — аденозиндифосфорная кислота, Ф — фосфат, Е — освобождающаяся энергия.
Энергию АТФ все клетки используют для процессов биосинтеза, движения, производства тепла, нервных импульсов, то есть для всех процессов жизнедеятельности. АТФ — универсальный биологический аккумулятор энергии. Световая энергия Солнца и энергия, заключённая в потребляемой пище, запасаются в молекулах АТФ.
Плоды шиповника, чёрная смородина, листья салата, картофель, яблоки, лимон, лук, капуста.
Печень, куриные яйца, плоды шиповника, лук, горох, морковь, помидоры, сливочное масло, листья салата, рыбий жир.
Злаки (пшеница, рожь, овёс), капуста, куриные яйца, морковь, лук, яблоки.