Существуют ли различия между нестероидными противовоспалительными препаратами? В центре внимания нимесулид
В данной работе представлены различия нестероидных противовоспалительных препаратов, применяемых для лечения заболеваний, сопровождающихся острой болью.
This paper describes different non-steroid anti-inflammatory preparations used for treatment of diseases accompanied with acute pain.
Распространенность заболеваний, сопровождающихся острой болью и требующих применения обезболивающих препаратов, в современном мире постоянно растет. К ним относятся, в частности, ревматические болезни, воспалительные и дегенеративные заболевания опорно-двигательного аппарата, головная боль. Примерно 40% визитов к врачу общей практики обусловлены слабой и умеренной острой болью, а более 70% посещений отделений неотложной помощи происходит из-за наличия у пациента интенсивной острой боли [1]. В структуре общей заболеваемости населения Российской Федерации болезни костно-мышечной системы и соединительной ткани (БКМС) занимают 3-е место после болезней системы кровообращения и органов дыхания [2]. Агентство National Health Interview Survey демонстрирует следующие данные: в 2011 г. 28,4% взрослых американцев сообщали о боли в нижней части спины (БНС) в течение предыдущих опросу 3 месяцев [3].
Эффективность нестероидных противовоспалительных препаратов (НПВП) при острой боли не подвергается сомнению. НПВП обладают противовоспалительной, обезболивающей и жаропонижающей активностью. Входящие в состав НПВП вещества относятся к различным химическим классам, поэтому обладают разными фармакокинетическими и фармакодинамическими свойствами.
Обзор клинической эффективности НПВП показывает, что различные препараты данной группы обладают примерно схожей терапевтической активностью. В данной работе будут представлены различия НПВП и особое внимание будет уделено представителю НПВП нимесулиду.
Фармакологические свойства НПВП
Ингибирование синтеза простагландинов
В начале 70-х годов Vane высказал предположение, что в основе противовоспалительного действия Аспирина и аналогичных ему препаратов лежит способность ингибировать биосинтез простагладинов, путем ингибирования ответственного за их синтез фермента циклооксигеназы (ЦОГ). Лишь 20 лет спустя эта гипотеза получила свое подтверждение, и стало известно, что за синтез простагландинов отвечают две изоформы ЦОГ (ЦОГ-1 и ЦОГ-2), а НПВП можно разделять с учетом селективности в отношении разных изоформ ЦОГ.
ЦОГ-1 отвечает в основном за синтез простагландинов, участвующих в процессах гомеостаза в жизненно важных органах. Именно с ингибированием ЦОГ-1 связывают хорошо известные желудочно-кишечные побочные эффекты традиционных неселективных НПВП.
Ингибирование ЦОГ-2 обеспечивает противовоспалительный эффект НПВП, так как она участвует в синтезе воспалительных простагландинов.
Неселективные НПВП ингибируют обратимо или необратимо как ЦОГ-1, так и ЦОГ-2. Большинство токсических эффектов этих препаратов связано с их способностью блокировать синтез физиологических простагландинов, необходимых для обеспечения гомеостаза в почках, желудке и тромбоцитах за счет ингибирования ЦОГ-1.
Появление на рынке в конце 90-х годов селективных ингибиторов ЦОГ-2 (коксибов) давало клиницистам надежду на то, что эта группа НПВП обеспечит высокую фармакологическую эффективность при более низком уровне желудочно-кишечных осложнений. Однако ожидания были оправданы не в полной мере, в частности, получены доказательства того, что применение коксибов сопровождается увеличением частоты тромбоэмболических осложнений, что привело к выводу с рынка во всем мире таких препаратов, как рпсиофекоксиб и валдекоксиб. Кроме того, применение валдекоксиба связывают с частым развитием нежелательных кожных реакций. Кардиотоксичность коксибов объясняют блокированием синтеза простациклинов, опосредованного ЦОГ-2, что нивелирует их защитные эффекты в отношении тромбогенеза, гипертензии и атерогенеза in vivo.
НПВП классифицируют по степени селективности в отношении изоформ ЦОГ (рис. 1). Селективность в отношении ЦОГ определяется химической структурой НПВП. Аминокислотная структура ЦОГ-1 и ЦОГ-2 является достаточно стабильной, однако рентгеновские кристаллографические исследования ЦОГ показали, что активная область связывания с НПВП у ЦОГ-2 позволяет связываться с большим количеством субстратов, чем центр связывания у ЦОГ-1. Этот активный канал является гидрофобным, у ЦОГ-2 возможно открытие бокового гидрофильного кармана, который у ЦОГ-1 закрыт изолейцином.
Так, флурбипрофен, который относят к неселективным НПВП, взаимодействует с ЦОГ-1 посредством связывания фенильной группы с гидрофобным каналом и карбоксильной группы с аргинином в 120-м положении. Взаимодействие флурбипрофена с ЦОГ-2 сходно с вышеописанным, однако, связываясь с аргинином в 120-м положении, карбоксильная группа блокирует активный центр ЦОГ-2, не позволяя ему взаимодействовать с субстратом. Напротив, селективные ингибиторы ЦОГ-2 не могут войти в активный канал ЦОГ-1 и не имеют карбоксильной группы для связывания с аргинином в 120-м положении.
Нимесулид — единственный представитель класса сульфонанилидов, преимущественно ингибирующим ЦОГ-2. Активность нимесулида в отношении ЦОГ-2 в 5–50 раз превосходит активность в отношении ЦОГ-1. В исследованиях in vivo использование нимесулида в терапевтической дозе (100 мг 2 раза в сутки) продемонстрировало значительное снижение концентрации простагландина E2 в плазме крови. Нимесулид не оказывает влияния на агрегацию тромбоцитов, что было доказано при оценке индуцированной активности ЦОГ-1, и не влияет на образование в желудке простагландина E2 и простагландина I2, а также ЦОГ-1 зависимых эффектов.
Фармакокинетический профиль
На основании периода полувыведения НПВП могут быть разделены на две большие группы: с коротким периодом полувыведения (менее 6 часов) и с длительным периодом полувыведения (более 10 часов). Группа НПВП с коротким периодом полувыведения включает Аспирин, диклофенак, ибупрофен, флурбипрофен, индометацин, лумиракоксиб* и нимесулид. Группа препаратов с длительным периодом полувыведения включает целекоксиб, напроксен, сулиндак, рофекоксиб, оксапрозин*, пироксикам. Достижение равновесной концентрации препарата в плазме крови происходит после его применения в течение периода, превосходящего период полувыведения в 3–5 раз, поэтому достижение пиковой концентрации в плазме крови и максимального клинического эффекта НПВП с коротким периодом полувыведения происходит быстрее, чем препаратов с длительным периодом полувыведения.
Нимесулид: фармакологический профиль
Нимесулид оказывает быстрое обезболивающее действие, что подтверждают следующие исследования. Применение нимесулида у пациентов с острым артритом характеризуется быстрым началом действия и ранним ингибированием образования простагландина E2 (маркера активности ЦОГ-2). В клинических исследованиях у пациентов с остеоартритом коленных суставов были получены доказательства быстрого начала действия нимесулида. У данной категории больных нимесулид вызывал достоверно более значимое облегчение боли, связанной с ходьбой, и эффект наступал быстрее, чем при применении целекоксиба и рофекоксиба. Начало обезболивающего действия нимесулида фиксировалось уже через 15 минут после приема. Согласно недавним исследованиям, эффективные концентрации нимесулида в плазме крови и синовиальной жидкости обнаруживаются уже через 30 минут после его приема.
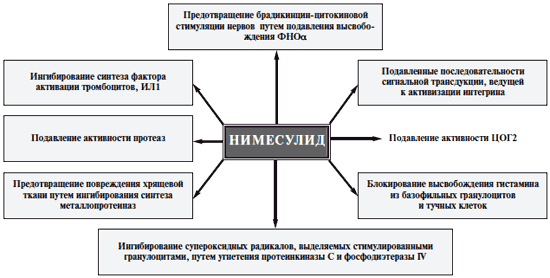
НПВП могут обладать противовоспалительными свойствами, которые не зависят от ЦОГ. Было показано, что нимесулид, помимо периферического ингибирующего воздействия на ЦОГ, может ингибировать высвобождение фактора некроза опухолей (ФНО), гистамина, образования активных форм кислорода (АФК), высвобождения матриксных металлопротеаз (ММП) и гибели хондроцитов (рис. 2).
 Влияние нимесулида на медиаторы воспаления
Влияние нимесулида на медиаторы воспаления
ФНО-α играет ведущую роль в воспалительном процессе, что делает его идеальной целью при терапии ревматоидного артрита. В исследованиях на крысах, которым вводили липополисахариды для увеличения уровня ФНО-α, нимесулид эффективно ингибировал его высвобождение.
Выработка фагоцитами супероксида и высвобождение лактоферрина из нейтрофилов были исследованы у восьми добровольцев до и после приема нимесулида внутрь. В качестве активирующих стимулов были использованы фактор хемотаксиса N-формил-метионил-лейцил-фенилаланин и частицы опсонизированного зимозана. Нимесулид значимо ингибировал образование АФК N-формил-метионил-лейцил-фенилаланином и активированными за счет воздействия опсонизированных частиц зимозана фагоцитами (ингибирование до 67,6% и 36,8% соответственно) (рис. 3). Он не оказывал влияния на высвобождение лактоферрина нейтрофилами, что позволило авторам предположить, что нимесулид не оказывает влияния на механизмы, происходящие при экзоцитозе специфичных гранул.
В ходе воспалительной реакции для предупреждения повреждения тканей требуется поддержание баланса между протеиназами (преимущественно эластазами, выделяемыми мигрировавшими в очаг нейтрофилами) и антипротеазами (в основном эластаз-специфическим альфа-1-ингибитором протеиназ; A1PI). Нейтрофильные клетки способны инактивировать A1PI с помощью серии окислительных реакций с участием хлорноватистой кислоты, что позволяет эластазе свободно разрушать соединительную ткань. Возможным способом регулирования активности нейтрофильной эластазы является фармакологическая защита A1PI от окислительной инактивации под действием хлорноватистой кислоты нейтрофилов. В доклинических исследованиях было показано, что нимесулид предотвращал инактивацию A1PI под действием выделяемой нейтрофилами хлорноватистой кислоты, что позволяет осуществлять опосредованный A1PI контроль гистотоксической функции эластазы. Полученные данные позволяют предполагать, что защитное влияние нимесулида на A1PI может иметь значение в реализации его противовоспалительного действия.
В другом исследовании морским свинкам предварительно вводили нимесулид или индометацин, после чего ацетальдегидом провоцировали выброс гистамина и бронхоспазм (рис. 4). В контрольной группе, получавшей только ацетальдегид, концентрация гистамина в крови была равна 195 ± 12 мг/л, в группе, получавшей нимесулид, при использовании дозы 0,1 мг/кг она была равна 154 ± 10 мг/л (p
О. В. Котова, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Боли в спине
Подбор лекарственных средств для лечения болей в спине

Доктор Перец ® — 100 % натуральное тепло для облегчения мышечных и суставных болей 1
Перцовый пластырь № 1 в России по объемам продаж 2
100 % натуральные экстракты красного перца и красавки 2
Основа, позволяющая коже дышать 3
1 Согласно ТУ Доктор Перец ®. Данное утверждение относится только к активным компонентам пластыря, оказывающим тепловой воздействие.
2 Лидер рынка перцовых пластырей по объему продаж в стоимостном и количественном выражении за период июль 2020‑июль 2021 на основе данных ООО «Айкьювиа Солюшнс»
3 Согласно ТУ Доктор Перец ®
Список лекарств от боли в спине
Форма выпуска
таблетки, покрытые пленочной оболочкой, порошок для приготовления суспензии для приема внутрь
«Дексалгин», «Дексалгин 25»
таблетки, покрытые оболочкой, раствор для внутривенного и внутримышечного введения
«Биоран», «Дикловит», «Флотак», «Раптен рапид», «Раптен Дуо», «Диклофенак ретард Оболенское», «Диклофенак-УБФ», «Табук-Ди», «Наклофен», «Наклофен СР», «Диклофенак-АКОС», «Диклофенак-ФПО», «Диклофенак-Эском»
таблетки пролонгированного действия, покрытые оболочкой, капсулы с модифицированным высвобождением, суппозитории ректальные, раствор для внутримышечного введения
таблетки, покрытые оболочкой
«Ибупрофен», «Бруфен СР», «Солпафлекс», «Ибупром Макс»,
таблетки, покрытые оболочкой, таблетки шипучие, таблетки для рассасывания,
капсулы пролонгированного действия, гранулы для приготовления раствора для приема внутрь, суспензия,
суппозитории ректальные (для детей), суспензия для приема внутрь (для детей)
раствор для внутривенного введения
Ибупрофен + кодеина фосфата гемигидрат
таблетки, покрытые оболочкой
таблетки, покрытые оболочкой
таблетки диспергируемые (для детей)
Ибупрофен + питофенон + фенпивериния бромид
таблетки, покрытые оболочкой
капсулы, таблетки, суппозитории ректальные, для внутримышечного введения
гранулы для приготовления раствора для приема внутрь
таблетки, раствор для внутривенного и внутримышечного введения
«Ксефокам», «Ксефокам рапид»
таблетки, покрытые оболочкой, лиофилизат для приготовления раствора для внутривенного и внутримышечного введения
«Матарен», «Мелоксикам», «Мовасин», «Мовикс», «Мовалис»,
таблетки, раствор для внутримышечного введения + суспензия для приема внутрь (Мовалис), суппозитории ректальные
таблетки, гранулы для приготовления суспензии для приема внутрь, суспензия для приема внутрь
раствор для внутримышечного введения
Миорелаксанты
Мильгамма композитум, Полиневрин®
«Мидокалм-Рихтер», «Толперизон с лидокаином-Ферейн»
раствор для внутривенного и внутримышечного введения
«Сирдалуд», «Тизанил», «Тизанидин-Тева», «Тизалуд»
капсулы с модифицированным высвобождением
таблетки, покрытые пленочной оболочкой, раствор для внутримышечного введения
NB! Ибупрофен в таблетках может быть как рецептурного, так и безрецептурного назначения, в отличие от других НПВП, у которых безрецептурными являются только наружные формы!
Форма выпуска
крем для наружного применения
Глюкозамин (глюкозамина сульфат, глюкозамина сульфата натрия хлорид)
таблетки, таблетки покрытые пленочной оболочкой, раствор для внутримышечного введения, порошок для приготовления раствора для приема внутрь
Хондроксид ® Максимум, «Фармаскин ТГК»
крем для наружного применения
Глюкозамин + ибупрофен + хондроитина сульфат
капсулы, таблетки покрытые пленочной оболочкой
гель для наружного применения
мазь для наружного применения
Глюкозамин + хондроитина сульфат + витамин Е
аэрозоль для наружного применения
крем для наружного применения
мазь для наружного применения
спрей для наружного применения дозированный
«Диклофенак», «Диклонат П», «Наклофен»,
гель для наружного применения
трансдермальная терапевтическая система, пластырь трансдермальный
гель для наружного применения
крем для наружного применения
гель для наружного применения
крем для наружного применения
аэрозоль для наружного применения
раствор для местного применения
гель для наружного применения
гель для наружного применения
трансдермальная терапевтическая система
Хондроксид ® Форте (мелоксикам+хондроитина сульфат&)
крем для наружного применения
мазь для наружного применения
гель для наружного применения
мазь для наружного применения
«Ваньтун Артиплас», «Перцовый пластырь Доктор перец с обезболивающим действием», «Перцовый пластырь» (белладонны листьев экстракт + перца стручкового плодов экстракт)
Витамины группы B
Дополнением к базовой анальгетической терапии может служить применение как «разогревающих», так и локальных «охлаждающих» средств, в частности трансдермальных систем на основе местных анестетиков (лидокаина и т. п.), блокирующих распространение болевых импульсов.
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
Подходы к лечению боли с учетом механизмов ее развития
Г.Р. Имаметдинова, Н.В. Чичасова, Е.В. Иголкина
ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздрава России, Москва
Рассмотрены проблемы лечения острой и хронической боли у больных с ревматическими заболеваниями. Показана роль воспаления и мышечного спазма в патогенезе острой и хронической боли. Представлены результаты клинических исследований и использования в клинической практике нимесулида (Найз ® ) и тизанидина (Сирдалуд ® ) при лечении острой и хронической боли.
Ключевые слова: боль, воспаление, мышечный спазм, нимесулид (Найз ® ), тизанидин (Сирдалуд ® ).
Approaches to treating pain in terms of the mechanisms of its development G.R.
Imametdinova, N.V. Chichasova, E.V. Igolkina
I.M. Sechenov First Moscow State Medical University, Ministry of Health of Russia, Moscow
The paper considers problems in the treatment of acute and chronic pain in patients with rheumatic diseases and shows the role of inflammation and muscle spasm in the pathogenesis of acute and chronic pain. It gives the results of clinical trials and the clinical use of nimesulide (Nise ® ) and tizanidine (Sirdalud ® ) in the treatment of acute and chronic pain.
Key words: pain, inflammation, muscle spasm, nimesulide (Nise ® ), tizanidine (Sirdalud ® ).
Самой распространенной причиной, заставляющей пациента обратиться к врачу, является боль. Боль сопровождает около 70% всех известных заболеваний. Распространенность хронической боли в популяции колеблется от 2 до 49% [1]. Наиболее часто боль возникает в различных структурах опорно-двигательного аппарата и является одним из основных симптомов ревматических заболеваний (РЗ), к которым относят воспалительные, дегенеративные заболевания суставов, позвоночника и периартикулярных тканей. В различные периоды жизни боль в связи с поражением компонентов опорно-двигательного аппарата встречается хотя бы 1 раз у 20-45% населения земного шара, чаще у женщин, чем у мужчин, и чаще в старших возрастных группах [2, 3].
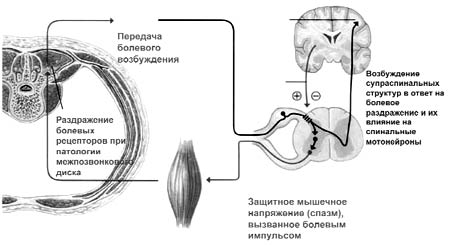
Рис. 1. Механизм развития порочного круга
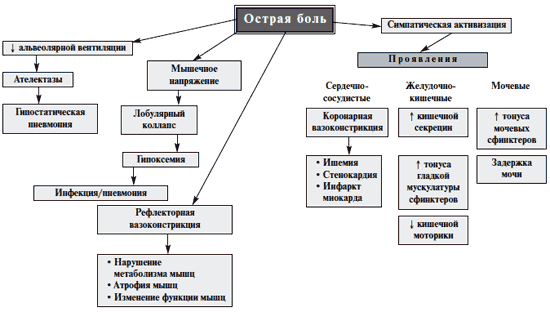
Боль является значимой медицинской проблемой. Острая и хроническая боль может приводить к функциональным нарушениям сердечно-сосудистой, дыхательной, пищеварительной, мочевыделительной систем 11 (рис. 2). Возникнув вследствие того или иного повреждения, боль приводит к серьезным нарушениям в системе регуляции болевой чувствительности, вызывает психологические расстройства, формирует у пациента особый тип болевого поведения [14].
Рис. 2. Висцеральные эффекты острой боли
Боль в структурах опорно-двигательного аппарата требует комплексного фармакологического подхода. Расширение представлений о генезе боли обусловливают новые подходы к проводимой терапии. Медикаментозная терапия включает использование нестероидных противовоспалительных препаратов (НПВП) и вспомогательных анальгетических средств (миорелаксанты) [4].
НПВП относятся к числу наиболее широко применяемых в клинической практике лекарственных средств. Основными показаниями к их назначению являются воспалительные процессы различного генеза, боль, лихорадка, необходимость профилактики тромбозов [15].
Таким требованиям соответствует селективный ингибитор ЦОГ2 нимесулид. Он является одним из наиболее широко используемых в России препаратов группы селективных НПВП. По анальгетическому, противовоспалительному и жаропонижающему действию нимесулид не уступает неселективным НПВП, а по некоторым данным, даже несколько их превосходит [20].
Рис. 3. Механизмы действия нимесулида
Нимесулид относится к короткоживущим НПВП. Период полувыведения составляет от 1,8 до 4,7 ч, что способствует снижению частоты побочных эффектов препарата. При пероральном приеме нимесулид быстро и практически полностью абсорбируется независимо от приема пищи. Нимесулид отличается быстрым достижением максимальной концентрации. Уже через 30 мин после перорального приема концентрация препарата в плазме крови и синовиальной жидкости достигает 25-80% от максимальной, что обусловливает высокую скорость наступления анальгетического эффекта. Благодаря биохимическим свойствам нимесулид легко попадает в очаг воспаления. Концентрация свободного нимесулида непосредственно в очаге воспаления (особенно в ткани сустава), где рН среды более низкий, может быть намного выше, чем его плазменная концентрация [33, 34]. Препарат выводится с мочой и калом.
По данным мировой литературы, частота побочных явлений при лечении нимесулидом колеблется в пределах 6,8-36% с четкой зависимостью от дозы и длительности приема препарата. В частности, при анализе результатов нескольких клинических испытаний, включавших 22 938 больных ОА, леченных нимесулидом в дозе 100-400 мг в течение 5-21 дня (в среднем 12 дней), общая частота побочных реакций составила 8,2% [34]. В другом многоцентровом исследовании, в котором участвовало 12 607 пациентов с различными РЗ и ортопедическими заболеваниями, на фоне лечения нимесулидом 400-200 мг/сут в течение 21 дня частота развития побочных эффектов составила 6,8%. При специальном анализе вошедших в эти 2 исследования 8354 пациентов старше 60 лет оказалось, что частота побочных эффектов равнялась 8,9% и не отличалась от таковой в общей популяции больных [35].
По данным отечественных и зарубежных авторов, нимесулид крайне редко вызывает усиление бронхоспазма у больных, страдающих бронхиальной астмой и гиперчувствительностью к ацетилсалициловой кислоте или другим НПВП, так как не обладает перекрестной реактивностью с этой кислотой и неселективными НПВП в отношении индукции обострения астмы и является одним из препаратов выбора (среди селективных НПВП) для этих больных [25, 36].
Отличительной особенностью нимесулида является отсутствие отрицательного действия на хрящ, что обусловлено механизмом его действия: способностью влиять на апоптоз хондроцитов [28], ингибировать ИЛ 1|3 в культуре синовиальных фибробластов [27] и металлопротеаз. Это дает возможность применять его у пациентов с ОА.
Результаты многочисленных исследований, выполненных отечественными и зарубежными авторами, подтверждают высокую эффективность нимесулида при лечении как острой, так и хронической боли. Высокая анальгетическая эффективность нимесулида показана при острых травмах, после хирургических вмешательств, при острой боли в нижней части спины [37, 38], а также при заболеваниях опорно-двигательного аппарата, головной боли, дисменорее. По анальгетической активности нимесулид не уступает индометацину, диклофенаку, пироксикаму [39].
Более быстрый и выраженный эффект нимесулида по сравнению с диклофенаком был продемонстрирован при купировании острого подагрического артрита и поражении периартикулярных тканей [37, 40].
Результаты работ отечественных исследователей, посвященных применению нимесулида у больных ОА, указывают на его высокую эффективность и хорошую переносимость при отсутствии отрицательного влияния на хрящ.
Как свидетельствуют многочисленные исследования, нимесулид характеризуется высокой гастроэнтерологической безопасностью [3]. Весьма интересным является тот факт, что низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [41].
Следует отметить, что пациенты, страдающие ОА, подвержены высокому риску развития ЖКТ-осложнений в связи с возрастом, частым развитием сосудистой, кардиальной, ренальной патологии и необходимостью прибегать к сопутствующей терапии. Нимесулид (Найз ® ) использовался у этой категории больных в суточной дозе 200 мг, что обеспечивало достижение клинического эффекта у 87-93% больных [47, 48] при хорошей переносимости в отношении ЖКТ Это подтверждено и данными зарубежных контролируемых исследований [49, 50], а также постмаркетингового изучения переносимости нимесулида в 17 странах у 11 831 385 больных [35, 51].
В течение 6 мес проводилось сравнительное исследование эффективности и переносимости нимесулида в суточной дозе 200 мг и диклофенака в суточной дозе 150 мг у 279 больных ОА. Эффективность обоих препаратов была сопоставимой при лучшей переносимости нимесулида: развитие побочных реакций со стороны ЖКТ было зафиксировано у 36 и 47% пациентов соответственно (р ® ) у больных ОА с артериальной гипертензией (АГ) показало отсутствие у него негативного влияния на течение АГ как по уровню среднесуточного артериального давления (АД), так и по потребности в антигипертензивной терапии [53]. Аналогичные результаты продемонстрированы в исследовании, включавшем 40 больных РА, которые получали нимесулид (Найз ® ) в течение 6 мес. По результатам суточного мониторинга не отмечено негативного влияния на АД, а также отсутствовала иная отрицательная динамика со стороны сердечно-сосудистой системы, что было подтверждено ЭКГ-мониторингом и эхокардиографией [54]. По данным анализа, проведенного A. Helin-Salmivaara и соавт., значение относительного риска инфаркта миокарда для нимесулида составило 1,69, что было сопоставимо с аналогичным показателем для мелоксикама, набуметона и неселективных НПВП [55].
Данные, полученные в результате метаанализа, показали, что нимесулид не вызывает побочные реакции со стороны почек. Оказалось, что на 100 тыс. пациентов, принимавших нимесулид, за 10 лет отмечено только 11 случаев возможной связи почечных осложнений с приемом препарата, из которых только в четырех проводилась монотерапия нимесулидом [57, 58].
Анализ данных литературы указывает на то, что гепатотоксичность нимесулида не выше, чем у многих других представителей класса НПВП [59]. Так, при назначении нимесулида коротким курсом (не более 30 дней) повышение уровня АЛТ и АСТ в 2 раза и более отмечается лишь у 0,4% больных, а при длительном многомесячном приеме частота подобных изменений не превышает 1,5% [60, 61]. В исследовании G. Traversa и соавт. частота серьезных осложнений со стороны печени при использовании нимесулида составила 35,3 на 100 тыс. человеко-лет, что меньше в сравнении с диклофенаком (39,2), кеторолаком (66,8), ибупрофеном (44,6) [62].
Особый интерес представляет работа отечественных авторов, посвященная изучению влияния нимесулида на функцию печени при лечении подагрического артрита. Как известно, для пациентов с подагрой часто характерны метаболические нарушения и высокая частота злоупотребления алкоголем, что способствует развитию побочных реакций со стороны печени. На фоне использования нимесулида в суточной дозе от 100 до 400 мг отсутствовала отрицательная динамика биохимических показателей крови, свидетельствующих о поражении печеночных клеток или холестазе [63].
Таким образом, быстрота развития и выраженность анальгетического, противовоспалительного эффекта в сочетании с хорошей переносимостью позволяют использовать нимесулид при лечении острой и хронической боли и определяют возможность его применения в течение длительного времени.
Между тем в ряде случаев применение НПВП не дает оптимального анальгетического эффекта. Одной из причин этого может служить наличие стойкого мышечного спазма в области поражения [64].
Дополнительными препаратами для лечения острой и хронической боли при заболеваниях опорно-двигательного аппарата являются центральные миорелаксанты. Эти препараты устраняют мышечный спазм как один из важных компонентов боли или уменьшают его выраженность. Применение миорелаксантов способствует облегчению боли, предотвращению образования контрактур, улучшению функциональной способности опорно-двигательного аппарата [65].
Одним из наиболее эффективных современных миорелаксантов является тизанидин (Сирдалуд ® ). Тизанидин относится к миорелаксантам центрального действия (α2-адренергическим агонистам) и реализует свой эффект на спинальном и супраспинальном уровнях. Стимулируя пресинаптические α2-рецепторы, он подавляет высвобождение возбуждающих аминокислот, которые стимулируют НМДА-рецепторы. Это приводит к угнетению полисинаптических рефлексов головного мозга, ответственных за гипертонус мышц, и подавлению передачи возбуждения через них, что вызывает снижение повышенного тонуса и ослабление болезненных мышечных спазмов. В дополнение к миорелаксирующим свойствам тизанидин дает центральный анальгетический эффект (за счет снижения высвобождения возбуждающих нейромедиаторов в головном мозге) [66, 67].
При пероральном приеме препарат быстро и практически полностью абсорбируется. Максимальная концентрация в плазме крови достигается через 1-2 ч. Период полувыведения составляет 3-5 ч. Прием пищи не влияет на фармакокинетику препарата. С белками плазмы крови тизанидин связывается не более чем на 30%. Экскреция препарата и его метаболитов осуществляется с мочой [68].
Установлено, что Сирдалуд ® хорошо переносится. Как при краткосрочном, так и при длительном применении малых доз препарата, к которым обычно прибегают в ревматологии, нежелательные явления возникают редко и купируются при отмене препарата [69]. Побочные реакции со стороны сердечно-сосудистой системы при использовании тизанидина в дозах, вызывающих миорелаксирующий эффект, выражены слабо и носят преходящий характер [69]. Наиболее частыми побочными эффектами являются сонливость, заторможенность (пациентам следует рекомендовать воздержаться от видов работ, требующих концентрации внимания и быстрой реакции), головокружение, сухость во рту. Препарат дает гипотензивный эффект, который значительно усиливается при одновременном применении с сильными ингибиторами CYP1A2, такими как некоторые антиаритмические препараты, фторхинолоны. Необходимо принимать во внимание, что при сочетанном применении тизанидина с антигипертензивными препаратами и диуретиками возможны выраженная гипотония и брадикардия, поэтому одновременное использование тизанидина с этими препаратами не рекомендуется. Повышение уровня печеночных трансаминаз наблюдается редко [66, 68].
Список использованной литературы
.gif)
.gif)
.gif) Влияние нимесулида на медиаторы воспаления
Влияние нимесулида на медиаторы воспаления