Системный мастоцитоз
Системный мастоцитоз (системная болезнь тучных клеток) — это редкое заболевание, характеризующееся чрезмерной выработкой и накоплением тучных клеток в тканях и органах (коже, костном мозге, ЖКТ, селезенке, печени).
Тучные клетки (мастоциты, лаброциты) — иммунные клетки соединительной ткани, локализуются в коже, дыхательных путях, ЖКТ, костном мозге, лимфатических узлах. Участвуют в развитии воспаления, играют важную роль в иммунном ответе, защите организма от патогенов, формировании гематоэнцефалического барьера. Реакцией тучных клеток на проникновение в организм патогенов или антигенов является выделение целого ряда биологически активных веществ (гистамина, гепарина, цитокинов, факторов роста). При системном мастоцитозе, т. е. чрезмерном накоплении тучных клеток в коже, костном мозге или желудочно-кишечном тракте у человека могут наблюдаться такие клинические проявления, как покраснение и зуд кожи, спазмы в животе, мышечные боли, тошнота, рвота, диарея, снижение артериального давления, учащенное сердцебиение, шок. Триггерами могут стать алкоголь, перепады температуры, острая пища, некоторые лекарства.
Существует 5 типов системного мастоцитоза, различающихся по степени тяжести течения, признакам и симптомам:
К легким типам СМ относятся вялотекущий и тлеющий. Они связаны с благоприятным прогнозом. Вялотекущий СМ наиболее распространен у взрослых. Агрессивный системный мастоцитоз, СМ, ассоциированный с гематологическим новообразованием, и лейкоз тучных клеток относятся к наиболее тяжелым типам заболевания и связаны с серьезным сокращением продолжительности жизни.
Распространенность системного мастоцитоза — 1 случай заболевания на 10 000-20 000 человек во всем мире.
Причины
Большинство случаев возникновения СМ носят спорадический характер и связаны с соматической мутацией гена KIT, кодирующего рецептор фактора роста тучных и стволовых клеток (протоонкоген c-kit).
Симптомы
Диагностика
Диагноз системный мастоцитоз устанавливается на основании симптомов и жалоб пациента, результатов лабораторных и инструментальных (УЗИ, рентгенография, КТ) диагностических исследований, биопсии костного мозга, биопсии кожи или органов (по показаниям), генетического тестирования. Таким образом определяется уровень тучных клеток и выделяемых ими веществ (триптазы, гистамина, лейкотриенов, простагландина), степень и стадия заболевания. Основным диагностическим критерием СМ, установленным ВОЗ, является наличие многоочаговой инфильтрации тучными клетками костного мозга, тканей и органов.
Дифференциальный диагноз включает другие причины синдромов активации тучных клеток (первичные и вторичные), разные формы мастоцитоза, эндокринные нарушения (опухоли надпочечников, синдром Вернера — Моррисона, синдром Золлингера — Эллисона), некоторые желудочно-кишечные патологии, аллергии, другие миелопролиферативные заболевания, поражающие костный мозг, гистиоцитоз, гиперэозинофильный синдром и макроглобулинемию Вальденстрема.
Лечение системного мастоцитоза
Лечение системного мастоцитоза направлено на определение конкретных факторов, вызывающих симптомы заболевания (продукты питания, укусы насекомых, лекарства, изменение температуры) и их контроль. Пациенту могут быть назначены антигистаминные препараты, аспирин, ингибиторы протонной помпы, стабилизаторы мембран тучных клеток и другие препараты, воздействующие на вещества, выделяемые тучными клетками (кортикостероиды, антагонисты лейкотриенов).
При повышенном риске анафилактического шока пациенту рекомендуется иметь при себе автоинжектор адреналина и уметь им пользоваться. В некоторых случаях (при агрессивной форме СМ, на поздних стадиях заболевания или в качестве промежуточного лечения перед аллогенной трансплантацией гемопоэтических стволовых клеток) пациентам может предлагаться лечение химиотерапевтическими препаратами.
Прогноз заболевания зависит от типа системного мастоцитоза.
Особенности и преимущества лечения системного мастоцитоза в клинике Рассвет
Врачи Рассвета специализируются на сложных диагнозах, редких болезнях и синдромах. Мультидисциплинарный подход и принципы доказательной медицины лежат в основе работы нашей клиники. При проявлении признаков и симптомов системного мастоцитоза вы можете записаться на консультацию к терапевту Рассвета. В зависимости от клинической картины заболевания, к диагностическому поиску и рассмотрению вариантов лечения подключатся аллерголог, гепатолог, гастроэнтеролог, эндокринолог и другие специалисты клиники. Мы проводим лечение по международным протоколам, назначаем только необходимые диагностические исследования.
Триптаза: маркер грозных проявлений аллергии
Классические симптомы аллергии, в большинстве своем, знакомы каждому. Но не всем известно, что патология может протекает в более «хитрой» и опасной – отечной форме. Итак, что такое ангионевротический отек? И каковы его признаки?
Что такое ангионевротический отек
В широком смысле, ангионевротический отек (АНО), известный также, как «отек Квинке» – это разновидность аллергической реакции, но реализующаяся в более «глубоких» слоях тканей. А основу такой реакции составляет гиперреактивность некоторых представителей иммунитета, а именно – тучных клеток (мастоцитов).
При контакте с аллергеном эти клетки молниеносно выбрасывают в «целевые» ткани целый ряд биологически активных веществ, которые также стремительно провоцируют:
Что «наглядно» проявляется как отек. И, в зависимости от «точки приложения» и степени выраженности, он может носить относительно безопасный или угрожающий жизни характер.
Как «выглядит» АНО
Наибольшее скопление тучных клеток наблюдается в «местах» непосредственного контакта тканей организма с окружающей средой, что, в норме, служит одним из звеньев иммунного «надзора».
Поэтому наивысшая концентрация мастоцитов отмечается на уровне кожи и слизистых оболочек, особенно дыхательной и пищеварительной систем. И АНО развивается именно в этих областях.
Провокатором отека может стать абсолютно любой аллерген, однако достоверно чаще – лекарственные средства и анестетики, укусы насекомых и химические вещества (красители для перманентного макияжа и прочие).
А характерными чертами АНО является:
«Под удар» тучных клеток может попасть лицо (чаще губы и веки), конечности, половые органы, гортань и бронхи, а также органы пищеварения.
При этом, если в случае кожи, АНО редко представляет угрозу для жизни, то на уровне дыхательных путей – может закончиться удушьем.
На уровне пищеварительной системы ангионевротичекий отек сопровождается спастической болью в животе, диареей, тошнотой и даже рвотой, чем может напоминать некоторые хирургические (аппендицит и прочие) или инфекционные патологии.
При этом, без лечения и угрозы для жизни, симптомы АНО бесследно исчезают в течение 8-72 часов.
Когда стоит провериться
«Полноценный» ангионевротический отек на лице и конечностях, как правило, сомнений не вызывает. И лабораторная диагностика служит только для подтверждения диагноза.
Однако, нередки случаи, когда АНО носит стертый характер и/или имитирует ряд других заболеваний.
Проверить кровь на уровень триптазы (один из наиболее стабильных ферментов тучных клеток) следует, если:
При этом, стоит помнить, что уровень триптазы в крови довольно быстро возвращается в «исходное положение», поэтому сдавать анализ необходимо именно в момент появления указанных симптомов или непосредственно отека.
Повышение уровня триптазы говорит об аллергической природе симптомов и требует консультации аллерголога.
А в некоторых случаях может также свидетельствовать о мастоцитозе (аномальном увеличении численности тучных клеток).
Боль в животе после еды объяснили работой тучных клеток
Javier Aguilera-Lizarraga et al. / Nature, 2020
Биологи выяснили, что ключевую роль в развитии болей в животе после еды у мышей с кишечной инфекцией играет работа тканевых агентов воспаления — тучных клеток. Такой иммунный ответ активирует гистаминовые рецепторы H1, которые и вызывают боль. Иммунный ответ наблюдался и у людей с синдромом раздраженного кишечника после инъекций глютена, пшеницы, сои и молока в кишечник. Статья опубликована в журнале Nature.
Иммунная система кишечника способна поддерживать баланс между ответом на патогенные микроорганизмы и безвредные бактерии и пищевые антигены. Поскольку в кишечнике содержится множество полезных микроорганизмов, а с пищей поступают безвредные для организма вещества, важно предотвратить избыточное воспаление в ответ на такие антигены. Поэтому иммунная система кишечника толерантна ко многим агентам и чаще всего не активна после приема пищи.
На толерантность иммунной системы к антигенам, которые поступают с пищей, влияют инфекции. Они повышают риск развития синдрома раздраженного кишечника — заболевания, при котором пациенты часто испытывают боль в животе и другие нарушения пищеварения. Более десяти процентов людей подвержены этому заболеванию и вынуждены сталкиваться с хроническими болями. Однако причины возникновения болей при синдроме раздраженного кишечника до сих пор изучены были слабо.
Исследователи из Католического университета Левена под руководством Хавьера Агилера-Лизарраги (Javier Aguilera-Lizarraga) и Моргана Флоренса (Morgane V. Florens) предположили, что боли при синдроме раздраженного кишечника вызваны снижением толерантности к пищевым антигенам и, как следствие, усиленным воспалением. Они заразили мышей возбудителем кишечного воспаления Citrobacter rodentium, смешав его с яичным белком овальбумином в качестве пищевого антигена. Через месяц — когда инфекция уже прошла — мышей повторно накормили овальбумином и проверили их иммунную реакцию.
Оказалось, что у мышей возрос уровень специфических антител IgE к альбумину в толстой кишке (p = 0,05). Более того, мыши испытывали больше боли после повторного поедания яичного белка, что было связано с повышением проницаемости кишечника. Биологи также наблюдали в толстой кишке усиление работы гена-маркера тканевых агентов воспаления — тучных клеток. Этот результат свидетельствует об активации этих клеток в ответ на антиген при заражении. Тогда исследователи провели дополнительные эксперименты и «заблокировали» тучные клетки у мышей при помощи геномного редактирования, после чего также заразили их и накормили овальбумином. У таких ГМО-мышей повышения воспалительного ответа на белок не наблюдалось.
У мышей также исследовали чувствительность висцеральных нервов, которые передают болевые сигналы из кишечника. Оказалось, что после инфекции эти нервы сильнее реагировали на механическую стимуляцию (p
LTP: маленькие виновники больших неприятностей
Грустный ребенок, которому нельзя есть апельсин
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Аллергию называют болезнью XXI века. Иммунитет призван защищать организм, но в этом случае он дает сбой. В чем причина? Статья знакомит с одним из сильнейших пищевых аллергенов — растительными липид-транспортирующими белками, их структурой и функциями.
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
Введение
Как вы отреагируете на сообщение, что в мире возникла новая «эпидемия»? По данным ВОЗ, от нее страдает 20% населения Европы. Это заболевание занимает третье место по распространенности в мире. Наверное, вы уже догадались, что речь идет об аллергии. Если открыть учебник по биологии и посмотреть определение данного недуга, то сразу станет ясно, что причина аллергии скрывается в некоем сбое иммунной системы. Иммунная система является главным защитником нашего организма от вирусов, бактерий, простейших, гельминтов — одним словом, от патогенов. Основными игроками иммунитета являются специальные клетки организма — лейкоциты.
Лейкоциты подразделяются на несколько групп [1]:
Собственно в первом приближении борьба иммунной системы с патогеном выглядит так: при попадании патогена в организм происходит активация первой линии защиты — нейтрофилов и макрофагов. Макрофаги, а также дендритные клетки способны активировать лимфоциты, которые начинают направленно убивать патогенов-чужаков. Более подробно с лимфоцитами и иммунным ответом можно ознакомиться в статье «Иммунитет: борьба с чужими и. своими» [1].
Строение и классификация антител
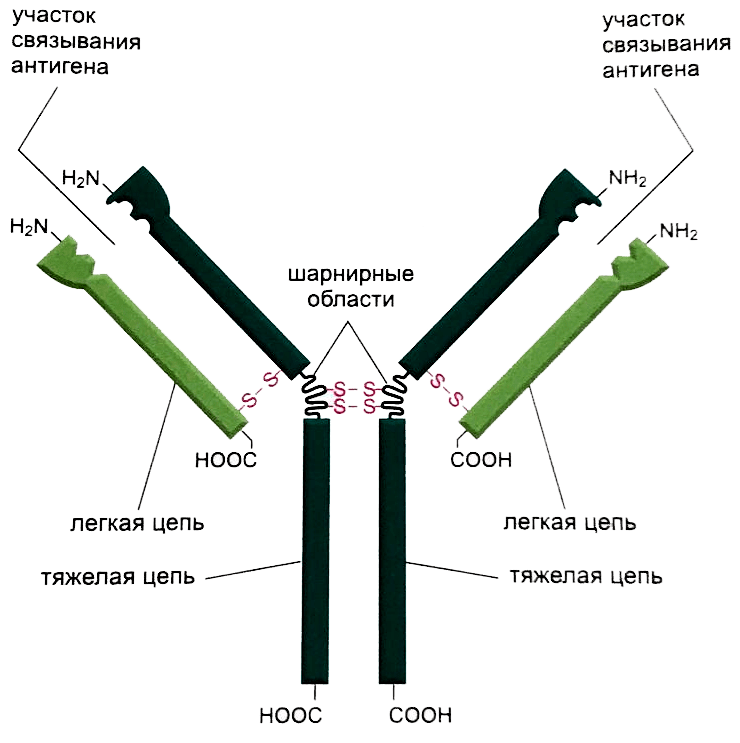
Антитела — это Y-образные молекулы из суперсемейства белков иммуноглобулинов, содержащие два участка связывания с антигеном [3].
Антиген — это молекула на поверхности патогена, способная к связыванию с антителом.
Антитело состоит из четырех полипептидных цепей: двух идентичных легких цепей и двух идентичных тяжелых (рис. 1). Между собой цепи соединены с помощью электростатических, ван-дер-ваальсовых и ковалентных дисульфидных связей [3]. Не связанная с легкими цепями часть тяжелых цепей образует шарнирные области и хвост (Fc-фрагмент) антитела.
Рисунок 1. Строение антитела
Шарнирная область — это достаточно гибкое место молекулы, за счет которого расстояние между двумя связывающими антиген участками может изменяться, что значительно повышает эффективность взаимодействия с антигеном [3].
У млекопитающих выделяют пять классов антител: IgA, IgD, IgE, IgG, IgM. Каждый класс имеет свой тип тяжелой цепи, а значит свой уникальный Fc-фрагмент, что придает молекулам одного класса характерные свойства. Строение хвостовой части антитела влияет на такие свойства, как связывание с фагоцитирующими клетками, пересечение плацентарного барьера и другие. Специальные Fc-рецепторы, расположенные на мембране лейкоцитов распознают Fc-фрагмент антитела определенного класса и затем связываются с ним. Другими словами, для каждого типа антител будет свой Fc-рецептор [3]. Таким образом, получается, что разные классы антител эффективны в различных ситуациях. Но для аллергии наибольшее значение представляют IgE.
IgE — это класс антител, которой практически отсутствует в свободном виде в крови здорового человека. Хвостовая часть молекулы имеет высокое сродство к Fc-рецепторам, расположенным на поверхности тучных клеток, базофилов и эозинофилов. Считается, что IgE защищают организм человека от паразитов, а также обусловливают аллергические реакции [3]. Более подробно ознакомиться с антителами можно в статье «Антитело: лучший способ распознать чужого» [19].
Существует теория, что аллергия — это сверхинтенсивная реакция организма на борьбу с паразитами. Такие симптомы, как зуд, чихание, интенсивное выделение слизи и других секретов — не что иное, как механизмы, помогающие избавиться от них.
В современном мире переход к соблюдению норм гигиены предотвращает контакт организма со многими антигенами [4]. Нагрузка на иммунную систему снижается. В таком случае организм начинает реагировать на «безобидные антигены», и возникает аллергия (видео 1) [5]. Антигены, вызывающие аллергию, называют аллергенами. Часто меру аллергической настроенности организма определяют по количеству IgE в крови.
Видео 1. Теория происхождения аллергии
Механизм возникновения аллергической реакции, типы аллергенов
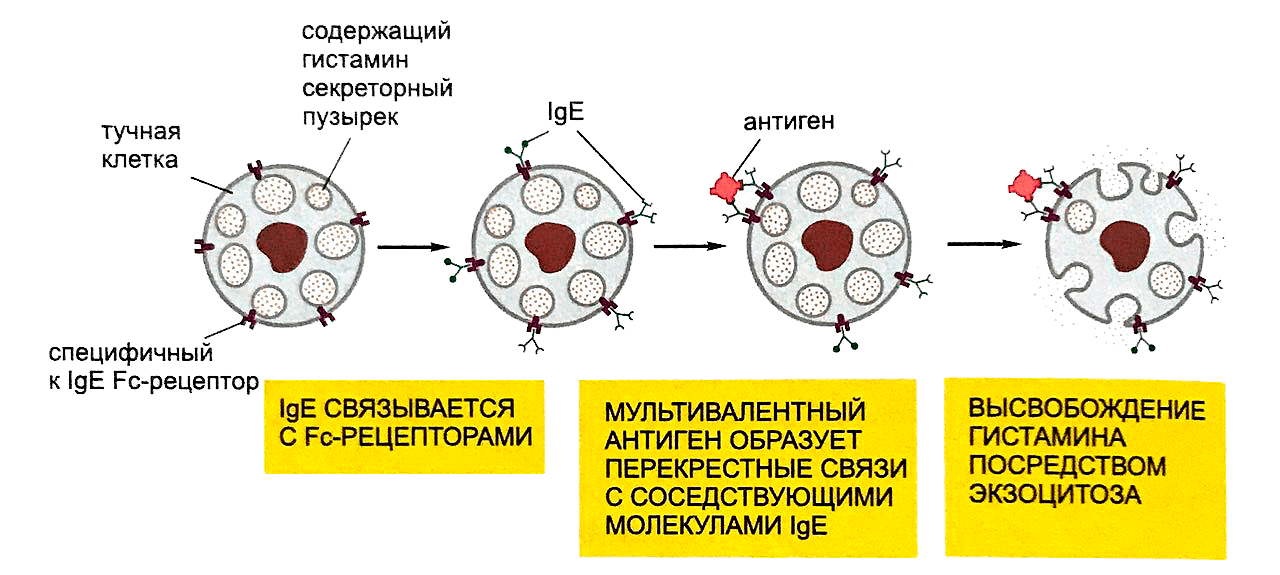
Первая встреча аллергена с иммунной системой стимулирует выработку IgE в кровоток. Эти антитела связываются хвостовой частью с Fc-рецепторами тучных клеток и базофилов. При повторной встрече аллерген связывается с IgE на поверхности тех же самых тучных клеток и базофилов, вызывая их активацию и дегрануляцию (рис.2) [3].
Рисунок 2. Механизм возникновения аллергической реакции
Таким образом тучные клетки и базофилы выделяют в организм человека биологически активные вещества, в том числе гистамин [3]. Гистамин — это биоорганическая молекула, производное аминокислоты гистидина. Гистамин обладает комплексным действием. При попадании в межклеточную среду он сразу же воздействует на стенки капилляров, увеличивая их проницаемость, понижает артериальное давление и вызывает спазм гладкой мускулатуры. Из кровяного русла жидкость выходит в ткани и накапливается там. Образуется отек. Если аллергическая реакция возникла в дыхательных путях, то высвобождение гистамина приведет к резкому спазму бронхов, что является причиной возникновения астмы [3].
В других случаях это приводит к отеку слизистой носа, различных кожных высыпаний, конъюнктивиту. Гистамин также влияет на процесс воспаления, то есть является медиатором воспаления — защитной реакции организма, направленной на устранение патогена и его продуктов жизнедеятельности.
Аллергия может возникнуть практически на любое вещество. Поэтому, для удобства аллергены можно подразделять на группы по происхождению. Это бытовые, лекарственные, эпидермальные (клетки эпидермиса и его производные человека и животных), грибковые, пыльцевые, пищевые и так далее [4].
Одними из сильнейших аллергенов являются представители липид-транспортирующих белков (Lipid Transfer Proteins, LTP) растений. LTP вызывают развитие иммунных реакций на пыльцу и растительные пищевые продукты. Считается, что эти белки играют одну из важнейших ролей в жизнедеятельности растений [6].
Строение и функции LTP
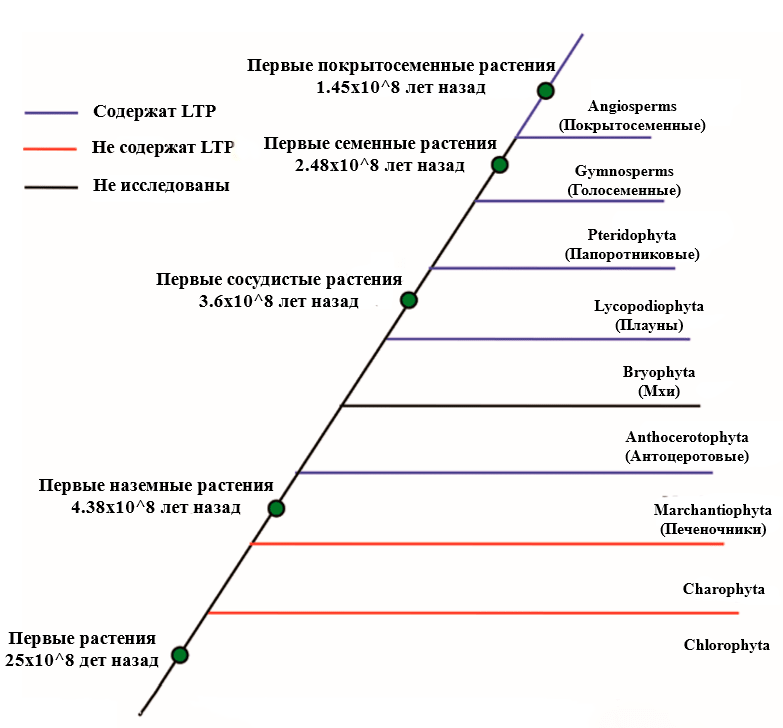
LTP были открыты в 1992 году группой испанских ученых под руководством Рамона Ллеонарта (Ramon Lleonart). Эти маленькие положительно заряженные белки весом около 7–10 кДа обнаружены только у высших растений [6]. У водорослей же они отсутствуют. Возможно, что появление именно этих белков помогло растениям выйти на сушу (рис. 3) [7].
Рисунок 3. Филогенетическое древо, на котором показано наличие или отсутствие LTP в различных группах растений
Выход на сушу и LTP
Выход на сушу требовал развития новых органов, приспособлений и механизмов, чтобы выжить и спокойно существовать в наземной среде. Для ее освоения растениям требовалось решить основную проблему: как защититься от потерь воды. Они нашли выход в виде различных гидрофобных полимеров, формирующих защитный слой на поверхности эпидермальных клеток. Этот слой называется кутикулой. Она защищает от обезвоживания, радиации и даже в какой-то мере от поедания травоядными животными. Образование кутикулы требует транспортировки липидов к месту синтеза на поверхности клетки. Сейчас предполагают, что LTP внесли большой вклад в возникновение и эволюцию кутикулы [8].
Все LTP имеют гидрофобную полость, в которой расположен сайт связывания с гидрофобными молекулами, такими как жирные кислоты, фосфолипиды и др [9].
Помимо гидрофобной полости, структура LTP содержит четыре дисульфидных мостика. Эти четыре связи между атомами серы поддерживают стабильность молекулы в пространстве, придавая ей прочность. Они делают это настолько хорошо, что даже ни ферменты желудочно-кишечного тракта, ни термическая обработка до 100 градусов не могут разрушить белок полностью [9].
Существует несколько типов классификации LTP.
LTP кодируются в растениях мультисемейством генов, в состав которого входят три кластера (3–8 генов в каждом). Белки, кодируемые каждым кластером, характеризуются специализацией по тканям, синтезом на определенной стадии онтогенеза и различием по функциям. Синтез LTP в клетках активируется под влиянием стрессовых факторов и фитогормонов. Стрессовыми факторами могут быть УФ-излучение, осмотический шок, отсутствие влажности, низкие температуры, вторжение различных патогенов [9].
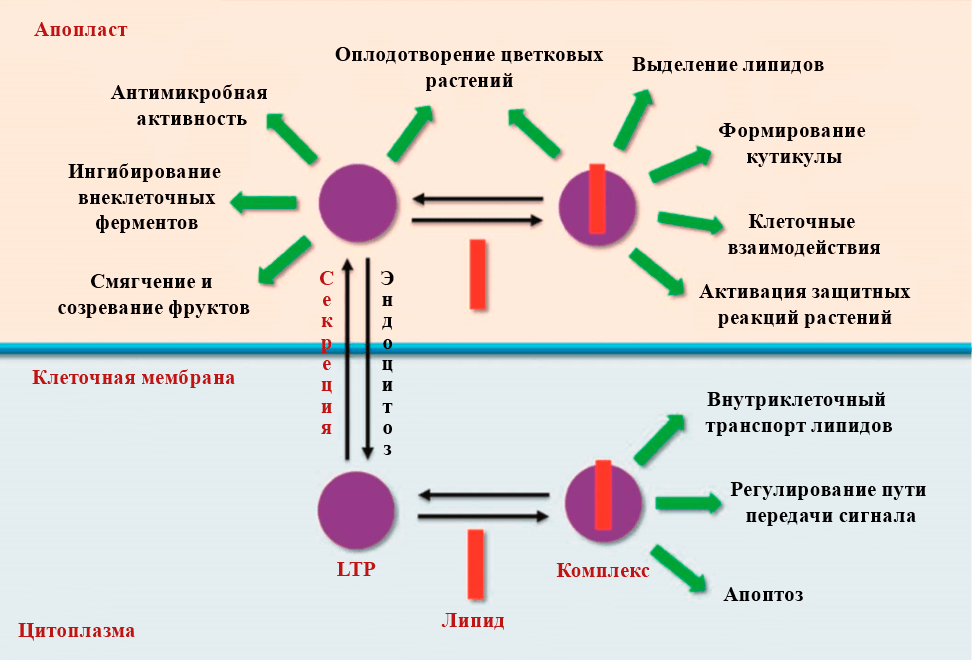
Теперь перейдем к функциям LTP в растениях. Большинство из них основано на проявленных ими активностях в экспериментах in vitro (рис. 4).
Рисунок 4. Функции растительных липид-транспортирующих белков
Было установлено, что LTP способны связывать и переносить липиды через биомембраны в лабораторных экспериментах. Собственно, из этого вытекает одна из предполагаемых функций — перенос гидрофобных молекул, участие в метаболизме липидов [6], [7]. LTP содержатся в высокой концентрации в покровных тканях растений, и это безусловно наталкивает на мысль об их вовлеченности в синтез поверхностного кутикулярного слоя (рис. 5) [9]. У мутантов растений Brassica napus с повышенным синтезом белка BrLTPd1 наблюдается нарушение секреции воска [8].
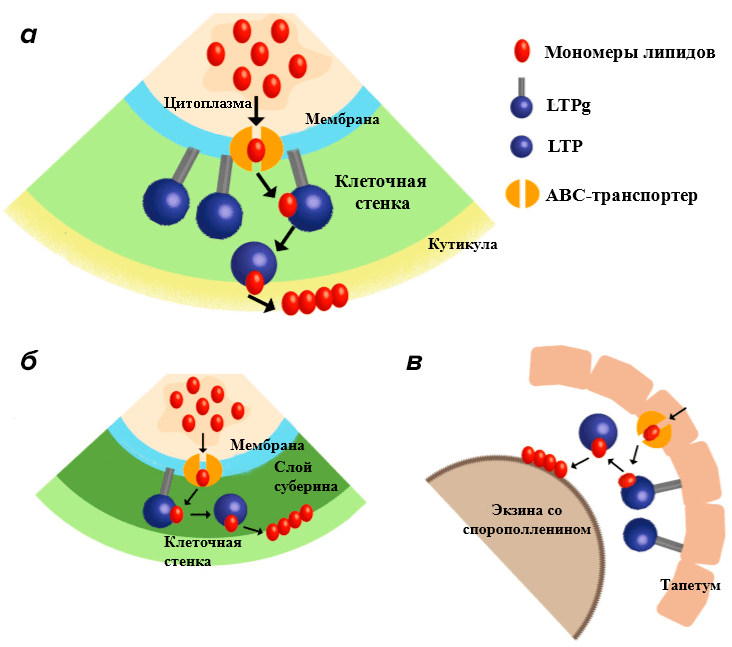
Рисунок 5. Предполагаемый механизм переноса липидов через мембрану и их участие в синтезе кутикулы. а — В зеленых тканях. б — В корнях. в — В пыльце.
Это происходит так: мономеры липидов через специальный ABC-транспортер попадают в пространство клеточной стенки. Там происходит их связывание с прикрепленными к наружней стороне мембране LTPg. Те, в свою очередь, передают липид на свободный LTP, который транспортирует гидрофобную молекулу в место синтеза кутикулы. Но до сих пор остается неясным механизм переноса липида по клеточной стенке [9].
Многие LTP препятствуют росту патогенных бактерий и грибов. Чаще всего такие взаимодействия являются избирательными, скорее всего, это связано с разным составом липидов в клеточных мембранах бактерий, грибов, млекопитающих и растений. Также некоторые исследования отмечают, что LTP из перца и кофе подавляют активность грибов рода Candida, которые являются патогенами человека. Механизм такой антимикробной активности не ясен. Возможно, он обеспечивается за счет электростатических взаимодействий с мембранами патогенов. Есть данные, что при разрушении дисульфидных мостиков антимикробная активность пропадает, поскольку нарушается процесс связывания белков с липидами. В то же время, антимикробная активность никак не связана с процессами взаимодействия с гидрофобными молекулами [9].
LTP в пищевой промышленности
Свойство LTP связываться с гиброфобными молекулами активно используется в пивоварении. LTP ячменя обладает поверхностно-активными свойствами, однако до термообработки и пастеризации пива этот белок демонстрирует слабые свойства вспенивания. После пастеризации пива LTP ячменя модифицируется по неисследованному механизму и становится пенообразующим [10]. При пастеризации его антимикробная активность не нарушается, в результате чего увеличивается срок хранения, поскольку LTP способен подавлять рост дрожжей. LTP также связывает жиры, что в лучшую сторону сказывается на формировании пены (рис. 6) и на вкусе пива [9].
Рисунок 6. Пена
И еще одно интересное свойство у определенных LTP, не связанное с аллергией, выявленное в ходе экспериментов, — это наличие противораковой активности [9]. Проведенные исследования показали, что LTP из полевой капусты и нарцисса препятствуют размножению и пролиферации раковых клеток in vitro, а также подавляют активность респираторно-синцитиального вируса человека и ВИЧ (механизм остается неизвестным) [11]. Остальные функции LTP (рис. 4) изучены очень слабо и в этой статье рассматриваться не будут.
LTP — аллергены
LTP обладают аллергенностью — способностью вызывать аллергию, что напрямую связано с особенностями их структуры. Четыре дисульфидных мостика обеспечивают устойчивость к разрушению ферментами желудочно-кишечного тракта. Получается, что LTP попадают в неизменном виде в тонкий кишечник и затем через ворсинки всасываются в кровь, где встречаются с иммунной системой человека [9]. В отличие от других аллергенов, 40% поверхности LTP способно связываться с иммуноглобулинами. Часто у страдающих пищевой аллергией на LTP может проявляться LTP-синдром, заключающийся в перекрестных аллергических реакциях на LTP различных видов растений, в том числе и таксономически далеких [12].
Был описан интересный случай на одном из складов в Европе. Работа сотрудников требовала ежедневного контакта с персиками. Известно, что кожура персиков содержит высокую концентрацию растительных липид-транспортирующих белков, а LTP Pru p 3 — это один из самых распространенных пищевых аллергенов. Через какое-то время один из служащих начал страдать ринитами. А через шесть месяцев у него возникла тяжелая пищевая аллергия на персики, сливы, фундук, арахис и т.д. Исследователи сделали вывод, что контакт пациента с кожурой персика мог спровоцировать возникновение аллергической чувствительности через дыхательные пути и дальнейшее развитие пищевой аллергии [12].
По данным Европейской академии аллергии и клинической иммунологии, 150 миллионов европейцев страдают от хронической аллергии. Из них у семи миллионов обнаруживается пищевая аллергия, а 100 миллионов в той или иной степени столкнулись с аллергическими ринитами [13]. В Испании 11% людей имеют аллергию на пыльцу. Из них от 10% до 40% также имеют аллергию на LTP персика [14].
В Северной Европе аллергия на LTP чаще всего представлена в виде оральной аллергии на входящий в состав пыльцы березы белок Bet v 1. А от пищевой аллергии на LTP больше страдают жители Средиземноморья [12].
Такое неравномерное географическое распределение до сих пор обсуждается, поскольку растительные продукты в Северной Европе также имеют высокое содержание LTP, однако частота возникновения аллергии на них значительно ниже. Возможное объяснение — это разные диетические привычки и способы термической обработки продуктов [12].
Методы лечения аллергии
Одним из самых простых и действенных методов борьбы с аллергией является, конечно же, ограничение контакта с аллергеном. В случае аллергии на пыль необходимо использовать воздушные фильтры для очистки воздуха, в случае пищевой аллергии — перестать употреблять продукт.
Для того чтобы не заставлять больного полностью исключать аллергенный продукт из рациона, можно методами генной инженерии разработать его гипоаллергенные аналоги. Так, уже созданы генномодифицированные томаты с LTP, измененные с помощью методов сайт-направленного мутагенеза и химических модификаций. Модифицированные белки снизили аллергическую реакцию при кожных тестах у пациентов [12].
Для избавления от симптомов аллергии, в том числе вызванных LTP, применяют фармакотерапию. Используемые для этого средства можно разделить на три группы.
К первой относится лечение антигистаминными препаратами. Действующие вещества блокируют рецепторы, с которыми связывается гистамин и, следовательно, препятствуют развитию аллергической реакции. Они не подходят для лечения аллергии в долгосрочной перспективе. Антигистаминные препараты обладают побочными эффектами, например, сонливостью, негативно влияют на сердечную мышцу [15].
Другая группа препаратов воздействует на мембраны тучных клеток, блокируя выброс везикул с гистамином. Это устраняет отеки слизистой носа и предупреждает появление астмы. Но опять же механизм работы направлен на блокирование симптомов, что не решает проблему полностью.
При серьезных случаях для быстрого облегчения острых симптомов принимают препараты на основе глюкокортикоидов — гормонов надпочечников. Глюкокортикоиды обладают противовоспалительной активностью [15].
Однако на данный момент одним из самых эффективных методов борьбы с аллергией является аллергенспецифическая иммунотерапия. Этот метод основан на продолжительном введении одного аллергена пациенту для постепенного уменьшения восприимчивости [16]. Его применяют при аллергии на LTP арахиса, персика, фундука, вишни и т.д. [17]. Подробности механизма действия, эффективность работы описаны в статье «Как победить аллергию за четыре инъекции?» [16].
Эффективность данной терапии налицо, но доказано, что такое лечение сопровождается анафилактическими побочными эффектами. Для их предотвращения в случае LTP разрабатывают замены экстрактов LTP на гипоаллергенные рекомбинантные аналоги [17].
Также врачи в качестве лечения назначают сублингвальную терапию. Данная терапия очень похожа по принципу действия на аллергенспецифическую, а отличие в том, что здесь используются не один, а несколько аллергенов [17], [18]. В этом методе пациенту индивидуально подбирают «коктейль» из аллергенов, которые наносится под язык каждый день по нескольку капель в течение продолжительного времени (3–5 лет). В результате спустя какое-то время организм пациента перестает остро реагировать на контакт с этими аллергенами [17], [18]. С помощью этой терапии борются с аллергией на LTP персиков, абрикосов, груш, слив и др. [12].
Растительные липид-транспортирующие белки, без сомнения, интересный биологический объект для изучения аллергической реакции, как с фундаментальной, так и с практической точки зрения. Бóльшая часть механизмов их действия на организм человека до сих пор не исследована, а точные функции в растениях не установлены. Количество людей, страдающих от аллергии на LTP, увеличивается с каждым годом, что указывает на необходимость их активного изучения. Кто знает, к каким новым открытиям могут привести эти маленькие катионные белки!