Синдром Стивенса-Джонсона
Общая информация
Краткое описание
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ БОЛЬНЫХ СИНДРОМОМ СТИВЕНСА-ДЖОНСОНА / ТОКСИЧЕСКИМ ЭПИДЕРМАЛЬНЫМ НЕКРОЛИЗОМ
Шифр по Международной классификации болезней МКБ-10
Синдром Стивенса-Джонсона – L51.1
Токсический эпидермальный некролиз – L51.2
ОПРЕДЕЛЕНИЕ
Синдром Стивенса-Джонсона / токсический эпидермальный некролиз – эпидермолитические лекарственные реакции (ЭЛР) – острые тяжелые аллергические реакции, характеризующиеся обширными поражениями кожи и слизистых оболочек, индуцированные приемом лекарственных препаратов.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
В зависимости от площади пораженной кожи выделяют следующие формы ЭЛР:
— синдром Стивенса-Джонсона (ССД) – менее 10% поверхности тела;
— токсический эпидермальный некролиз (ТЭН, синдром Лайелла) – более 30% поверхности тела;
— промежуточная форма ССД/ТЭН (поражение 10–30% кожи).
Этиология и патогенез
Наиболее часто синдром Стивенса-Джонсона развивается при приеме лекарственных препаратов, однако в некоторых случаях причину заболевания выяснить не удается. Среди лекарственных препаратов, при приеме которых чаще развивается синдром Стивенса-Джонсона, выделяют: сульфаниламиды, аллопуринол, фенитонин, карбамазепин, фенибутазол, пироксикам, хлормазанон, пенициллины. Реже развитию синдрома способствует прием цефалоспоринов, фторхинолонов, ванкомицина, рифампицина, этамбутола, теноксикама, тиапрофеновой кислоты, диклофенака, сулиндака, ибупрофена, кетопрофена, напроксена, тиабендазола.
Заболеваемость ЭЛР оценивается как 1–6 случаев на миллион человек. ЭЛР могут возникать в любом возрасте, риск развития заболеваний возрастает у лиц в возрасте старше 40 лет, у ВИЧ-позитивных лиц (в 1000 раз), больных системной красной волчанкой и онкологическими заболеваниями. Чем старше возраст пациента, серьезнее сопутствующее заболевание и обширнее поражение кожи, тем хуже прогноз заболевания. Смертность от ЭЛР составляет 5–12%.
Для заболеваний характерен скрытый период между приемом препарата и развитием клинической картины (от 2 до 8 недель), необходимый для формирования иммунного ответа. Патогенез ЭЛР связан с массовой гибелью базальных кератиноцитов кожи и эпителия слизистых оболочек, вызванных Fas-индуцированным и перфорин/гранзим-опосредованным апоптозом клеток. Программируемая гибель клеток происходит в результате иммуноопосредованного воспаления, важную роль в развитии которого играют цитотоксические Т-клетки.
Клиническая картина
Cимптомы, течение
При синдроме Стивенса-Джонсона отмечается поражение слизистых оболочек как минимум двух органов, площадь поражения достигает не более 10% всего кожного покрова.
Синдром Стивенса-Джонсона развивается остро, поражение кожи и слизистых оболочек сопровождается тяжелыми общими расстройствами: высокой температурой тела (38. 40°С), головной болью, коматозным состоянием, диспепсическими явлениями и др. Высыпания локализуются преимущественно на коже лица и туловища. Клиническая картина характеризуется появлением множественных полиморфных высыпаний в виде багрово-красных пятен с синюшным оттенком, папул, пузырьков, мишеневидных очагов. Очень быстро (в течение нескольких часов) на этих местах формируются пузыри размером до ладони взрослого и больше; сливаясь, они могут достигать гигантских размеров. Покрышки пузырей сравнительно легко разрушаются (положительный симптом Никольского), образуя обширные ярко-красные эрозированные мокнущие поверхности, окаймленные обрывками покрышек пузырей («эпидермальный воротник»).
Иногда на коже ладоней и стоп появляются округлые темно-красные пятна с геморрагическим компонентом.
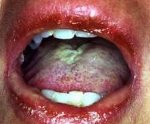
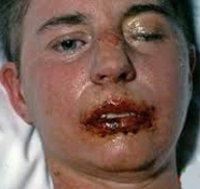
Наиболее тяжелое поражение наблюдается на слизистых оболочках полости рта, носа, половых органов, коже красной кайме губ и в перианальной области, где появляются пузыри, которые быстро вскрываются, обнажая обширные, резко болезненные эрозии, покрытые сероватым фибринозным налетом. На красной кайме губ часто образуются толстые буро-коричневые геморрагические корки. При поражении глаз наблюдается блефароконъюнктивит, возникает риск развития язвы роговицы и увеита. Пациенты отказываются от приема пищи, предъявляют жалобы на боль, жжение, повышенную чувствительность при глотании, парестезии, светобоязнь, болезненное мочеиспускание.
Диагностика
Диагноз синдрома Стивенса-Джонсона основывается на результатах анамнеза заболевания и характерной клинической картине.
При проведении клинического анализа крови выявляется анемия, лимфопения, эозинофилия (редко); нейтропения является неблагоприятным прогностическим признаком.
При необходимости проводят гистологическое исследование биоптата кожи. При гистологическом исследовании наблюдаются некроз всех слоев эпидермиса, образование щели над базальной мембраной, отслойка эпидермиса, в дерме воспалительная инфильтрация выражена незначительно или отсутствует.
Дифференциальный диагноз
Синдром Стивенса–Джонсона следует дифференцировать с вульгарной пузырчаткой, синдромом стафилококковой ошпаренной кожи, токсическим эпидермальным некролизом (синдромом Лайелла), для которого характерна отслойка эпидермиса более чем 30% поверхности тела; реакцией «трансплантат против хозяина», многоформной экссудативной эритемой, скарлатиной, термическим ожогом, фототоксической реакцией, эксфолиативной эритродермией, фиксированной токсидермией.
Лечение
— улучшение общего состояния пациента;
— регресс высыпаний;
— предупреждение развития системных осложнений и рецидивов заболевания.
Общие замечания по терапии
Лечение синдрома Стивенса-Джонсона проводит врач-дерматовенеролог, терапию более тяжелых форм ЭЛР осуществляют другие специалисты, врач-дерматовенеролог привлекается в качестве консультанта.
При выявлении эпидермолитической лекарственной реакции, врач, независимо от его специализации, обязан оказать больному неотложную медицинскую помощь и обеспечить его транспортировку в ожоговый центр (отделение) либо в реанимационное отделение.
Немедленная отмена приема препарата, спровоцировавшего развитие ЭЛР, увеличивает выживаемость при коротком периоде его полувыведения. В сомнительных случаях следует отменить прием всех препаратов, не являющихся жизненно необходимыми, и в особенности тех, прием которых был начат в течение последних 8 недель.
Необходимо учитывать неблагоприятные прогностические факторы течения ЭЛР:
1. Возраст > 40 лет – 1 балл.
2. ЧСС > 120 в мин. – 1 балл.
3. Поражение > 10% поверхности кожи – 1 балл.
4. Злокачественные новообразования (в т.ч. в анамнезе) – 1 балл.
5. В биохимическом анализе крови:
— уровень глюкозы > 14 ммоль/л – 1 балл;
— уровень мочевины > 10 ммоль/л – 1 балл;
— бикарбонаты 5 баллов (90%).
Показания к госпитализации
Установленный диагноз Синдрома Стивенса-Джонсона / токсического эпидермального некролиза.
Схемы лечения
Системная терапия
1. Глюкокортикостероидные препараты системного действия:
— преднизолон (В) 90–150 мг в сутки внутримышечно или внутривенно [1]
или
— дексаметазон (В) 12–20 мг в сутки внутримышечно или внутривенно [2].
2. Инфузионная терапия (допустимо чередование различных схем):
— калия хлорид + натрия хлорид + магния хлорид (C) 400,0 мл внутривенно капельно, на курс 5–10 вливаний
или
— натрия хлорид 0,9% (C) 400 мл внутривенно капельно на курс 5–10 вливаний
или
— кальция глюконат 10% (C) 10 мл 1 раз в сутки внутримышечно в течение 8–10 дней;
— тиосульфат натрия 30% (C) 10 мл 1 раз в сутки внутривенно на курс 8–10 вливаний.
Также является оправданным проведение процедур гемосорбции, плазмафереза (C) [3].
3. При возникновении инфекционных осложнений назначают антибактериальные препараты с учетом выделенного возбудителя, его чувствительности к антибактериальным препаратам и тяжести клинических проявлений.
Наружная терапия
заключается в тщательном уходе и обработке кожных покровов путем очищения, удаления некротической ткани. Не следует проводить обширное и агрессивное удаление некротически измененного эпидермиса, поскольку поверхностный некроз не является преградой для реэпителизации и может ускорять пролиферацию стволовых клеток посредством воспалительных цитокинов.
Для наружной терапии используют растворы антисептических препаратов (D): раствор перекиси водорода 1%, раствор хлоргексидина 0,06%, раствор перманганата калия (D).
Для обработки эрозий применяют раневые покрытия, анилиновые красители (D): метиленовый синий, фукорцин, бриллиантовый зеленый.
При поражении глаз требуется консультация офтальмолога. Не рекомендуется использовать глазные капли с антибактериальными препаратами в связи с частым развитием синдрома «сухого глаза». Целесообразно использовать глазные капли с глюкокортикостероидными препаратами (дексаметазоном), препараты искусственной слезы. Требуется механическая деструкция ранних синехий в случае их формирования.
При поражении слизистой оболочки полости рта проводят полоскания несколько раз в день антисептическими (хлоргексидин, мирамистин) или противогрибковыми (клотримазол) растворами.
Особые ситуации
Лечение детей
Требует интенсивного междисциплинарного взаимодействия педиатров, дерматологов, офтальмологов, хирургов:
— контроль за жидкостным балансом, электролитами, температурой и артериальным давлением;
— асептическое вскрытие еще упругих пузырей (покрышку оставляют на месте);
— микробиологический мониторинг очагов на коже и слизистых оболочках;
— уход за глазами и полостью рта;
— антисептические мероприятия, для обработки эрозий у детей применяют анилиновые красители без спирта: метиленовый синий, бриллиантовый зеленый;
— неадгезивные раневые повязки;
— помещение больного на специальный матрац;
— адекватная обезболивающая терапия;
— осторожная лечебная гимнастика для предупреждения контрактур.
Требования к результатам лечения
— клиническое выздоровление;
— предупреждение развития рецидивов.
ПРОФИЛАКТИКА
Профилактика рецидивов синдрома Стивенса–Джонсона заключается в исключении препаратов, вызвавших данное заболевание. Рекомендуется носить опознавательный браслет с указанием препаратов, вызвавших синдром Стивенса–Джонсона.
Информация
Источники и литература
Информация
Персональный состав рабочей группы по подготовке федеральных клинических рекомендаций по профилю «Дерматовенерология», раздел «Синдром Стивена-Джонсона»:
1. Заславский Денис Владимирович – профессор кафедры дерматовенерологии ГБОУ ВПО «Санкт-Петербургский государственный педиатрический университет» Минздрава России, профессор, доктор медицинских наук, г. Санкт-Петербург.
2. Горланов Игорь Александрович заведующий кафедрой дерматовенерологии ГБОУ ВПО «Санкт-Петербургский государственный педиатрический университет» Минздрава России, профессор, доктор медицинских наук, г. Санкт-Петербург.
3. Самцов Алексей Викторович – заведующий кафедрой кожных и венерических болезней ФГБВОУ ВПО «Военно-медицинская академия им С.М. Кирова», доктор медицинских наук, профессор, г. Санкт-Петербург.
4. Хайрутдинов Владислав Ринатович – ассистент кафедры кожных и венерических болезней ФГБВОУ ВПО «Военно-медицинская академия им С.М. Кирова», доктор медицинских наук, г. Санкт-Петербург.
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
· Консенсус экспертов;
· Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).
Рейтинговая схема для оценки силы рекомендаций:
| Уровни доказательств | Описание |
| 1++ | Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок |
| 1+ | Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок |
| 1- | Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок |
| 2++ | Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2+ | Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2- | Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 3 | Неаналитические исследования (например: описания случаев, серий случаев) |
| 4 | Мнение экспертов |
Методы, использованные для анализа доказательств:
· Обзоры опубликованных мета-анализов;
· Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций:
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
· Внешняя экспертная оценка;
· Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами.
Комментарии, полученные от экспертов, систематизированы и обсуждены членами рабочей группы. Вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не были внесены, то зарегистрированы причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совершенствовании рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы.
Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.
Синдром Стивенса-Джонсона ( Злокачественная экссудативная эритема )
Синдром Стивенса-Джонсона — это острое буллезное поражение слизистых и кожи аллергической природы. Протекает на фоне тяжелого состояния заболевшего с вовлечением слизистой полости рта, глаз и мочеполовых органов. Диагностика синдрома Стивенса-Джонсона включает тщательный осмотр пациента, иммунологическое исследование крови, биопсию кожи, коагулограмму. По показаниям проводится рентгенография легких, УЗИ мочевого пузыря, УЗИ почек, биохимический анализ мочи, консультации других специалистов. Лечение осуществляется методами экстракорпоральной гемокоррекции, глюкокортикоидной и инфузионной терапией, антибактериальными препаратами.
МКБ-10
Общие сведения
Данные о синдроме Стивенса-Джонсона были опубликованы в 1922 году. Со временем синдром получил название в честь впервые описавших его авторов. Заболевание является тяжело протекающим вариантом многоформной экссудативной эритемы и имеет второе название — “злокачественная экссудативная эритема”. Вместе с синдромом Лайелла, пузырчаткой, буллезным вариантом СКВ, аллергическим контактным дерматитом, болезнью Хейли-Хейли и др. клиническая дерматология относит синдром Стивенса-Джонсона к буллезным дерматитам, общим клиническим симптомом которых является образование пузырей на коже и слизистых.
Синдром Стивенса-Джонсона наблюдается в любом возрасте, наиболее часто у лиц 20-40 лет и крайне редко в первые 3 года жизни ребенка. По различным данным распространенность синдрома на 1 млн. населения составляет от 0,4 до 6 случаев в год. Большинство авторов отмечает более высокую заболеваемость среди мужчин.
Причины
Развитие синдрома Стивенса-Джонсона обусловленно аллергической реакцией немедленного типа. Выделяют 4 группы факторов, которые могут спровоцировать начало заболевания: инфекционные агенты, лекарственные препараты, злокачественные заболевания и не установленные причины.
В детском возрасте синдром Стивенса-Джонсона чаще возникает на фоне вирусных заболеваний: простого герпеса, вирусного гепатита, аденовирусной инфекции, кори, гриппа, ветряной оспы, эпидемического паротита. Провоцирующим фактором могут быть бактериальные (сальмонеллез, туберкулез, иерсиниоз, гонорея, микоплазмоз, туляремия, бруцеллез) и грибковые (кокцидиомикоз, гистоплазмоз, трихофития) инфекции.
У взрослых синдром Стивенса-Джонсона, как правило, обусловлен введением медикаментов или злокачественным процессом. Из медикаментозных препаратов роль причинного фактора в первую очередь отводится антибиотикам, нестероидным противовоспалительным, регуляторам ЦНС и сульфаниламидам. Ведущую роль среди онкологических заболеваний в развитии синдрома Стивенса-Джонсона играют лимфомы и карциномы. Если конкретный этиологический фактор заболевания установить не удается, то говорят о идеопатическом синдроме Стивенса-Джонсона.
Симптомы
Синдром Стивенса-Джонсона характеризуется острым началом со стремительным развитием симптоматики. В начале отмечается недомогание, подъем температуры до 40°С, головная боль, тахикардия, артралгии и боли в мышцах. Пациента может беспокоить боль в горле, кашель, диарея и рвота. Уже через несколько часов (максимально через сутки) на слизистой рта наблюдается появление довольно больших пузырей. После их вскрытия на слизистой образуются обширные дефекты, покрытые бело-серыми или желтоватыми пленками и корками из запекшейся крови. В патологический процесс вовлекается красная кайма губ. Из-за тяжелого поражения слизистой при синдроме Стивенса-Джонсона пациенты не могут есть и даже пить.
Поражение глаз в начале протекает по типу аллергического конъюнктивита, но часто осложняется вторичным инфицированием с развитием гнойного воспаления. Для синдрома Стивенса-Джонсона типично образование на конъюнктиве и роговице эрозивно-язвенных элементов небольшой величины. Возможно поражение радужной оболочки, развитие блефарита, иридоциклита, кератита.
Поражение слизистой органов мочеполовой системы наблюдается в половине случаев синдрома Стивенса-Джонсона. Оно протекает в виде уретрита, баланопостита, вульвита, вагинита. Рубцевание эрозий и язв слизистой может приводить к образованию стриктуры уретры.
Поражение кожи представлено большим количеством округлых возвышающихся элементов, напоминающих волдыри. Они имеют багровую окраску и достигают в размере 3-5 см. Особенностью элементов кожной сыпи при синдроме Стивенса-Джонсона является появление в их центре серозных или кровянистых пузырей. Вскрытие пузырей приводит к образованию ярко-красных дефектов, покрывающихся корками. Излюбленная локализация сыпи — кожа туловища и промежности.
Период появления новых высыпаний синдрома Стивенса-Джонсона длится примерно 2-3 недели, заживление язв происходит в течение 1,5 месяцев. Заболевание может осложниться кровотечением из мочевого пузыря, пневмонией, бронхиолитом, колитом, острой почечной недостаточностью, вторичной бактериальной инфекцией, потерей зрения. В результате развившихся осложнений погибает около 10% больных с синдромом Стивенса-Джонсона.
Диагностика
Диагностировать синдром Стивенса-Джонсона клиницист-дерматолог может на основании характерных симптомов, выявляемых при тщательном дерматологическом осмотре. Опрос пациента позволяет определить причинный фактор, вызвавший развитие заболевания. Подтвердить диагноз синдрома Стивенса-Джонсона помогает биопсия кожи. При гистологическом исследовании наблюдается некроз эпидермальных клеток, периваскулярная инфильтрация лимфоцитами, субэпидермальное образование пузырей.
В клиническом анализе крови определяются неспецифические признаки воспаления, коагулограмма выявляет нарушения свертываемости, а биохимический анализ крови — пониженное содержание белков. Наиболее ценным в плане диагностики синдрома Стивенса-Джонсона является иммунологическое исследование крови, которое обнаруживает значительное повышение Т-лимфоцитов и специфических антител.
Диагностика осложнений синдрома Стивенса-Джонсона может потребовать проведения бакпосева отделяемого эрозий, копрограммы, биохимического анализа мочи, пробы Зимницкого, УЗИ и КТ почек, УЗИ мочевого пузыря, рентгенографии легких и др. При необходимости пациента консультируют узкие специалисты: окулист, уролог, нефролог, пульмонолог.
Дифференцировать синдром Стивенса-Джонсона необходимо с дерматитами, для которых типично образование пузырей: аллергическим и простым контактным дерматитом, актиническим дерматитом, герпетиформным дерматитом Дюринга, различными формами пузырчатки (истинной, вульгарной, вегетирующей, листовидной), синдромом Лайелла и др.
Лечение синдрома Стивенса-Джонсона
Терапия проводится высокими дозами глюкокортикоидных гормонов. В связи с поражением слизистой рта введение препаратов зачастую приходится осуществлять инъекционным способом. Постепенное снижение дозы начинают только после стихания симптомов заболевания и улучшения общего состояния больного.
Для очищения крови от образующихся при синдроме Стивенса-Джонсона иммунных комплексов применяются метода экстракорпоральной гемокоррекции: каскадная фильтрация плазмы, мембранный плазмаферез, гемосорбция и иммуносорбция. Производится переливание плазмы и белковых растворов. Важное значение имеет введение в организм пациента достаточного количества жидкости и поддержание нормального суточного диуреза. В качестве дополнительной терапии применяются препараты кальция и калия. Профилактика и лечение вторичной инфекции проводится при помощи местных и системных антибактериальных препаратов.
Синдром Лайелла
Реаниматолог Александр Черновоб острой патологии с иммунным механизмом развития и высоким процентом летальных исходов
К сожалению, до сих пор есть заболевания, которые за считанные часы доводят, казалось бы, совершенно здорового человека до критического состояния и имеют крайне неблагоприятный прогноз.Одним из таких заболеваний является синдром Лайелла (L51.2 по МКБ-10).
В СМИ широко обсуждался скандальный случай смерти от данной патологии — гибель в июле 2003 года журналиста, депутата Государственной Думы третьего созыва Юрия Щекочихина.
Свидетели отмечали необъяснимое резкое ухудшение его состояния: «за две недели превратился в глубокого старика, волосы выпадали клоками, с тела сошла кожа, практически вся, один за другим отказывали внутренние органы» («Новая газета», выпуск № 20 от 24 марта 2008 г.).
По факту смерти депутата было заведено уголовное дело по статье 105 УК РФ ч. 1 — «Убийство». Родственники и подхватившая ажиотаж пресса твердили об отравлении, в частности таллием. Семь месяцев проводились соответствующие экспертизы, эксгумировали тело депутата. Лишь к марту 2004 года были установлены обстоятельства стремительного ухудшения состояния Щекочихина. Диагноз и причина смерти — синдром Лайелла, острая сердечно-сосудистая недостаточность.
Из истории синдрома
Впервые эту патологию описал в 1956 году шотландский дерматолог Алан Лайелл. Он систематизировал 11 сообщений о 14 случаях этого заболевания, 4 из которых наблюдал лично.
Лайелл заменил принятое ранее обозначение «острый пемфигус» на «токсический эпидермальный некролиз» (ТЭН).Дело в том, что у всех пациентов отмечалась сыпь, «имеющая сходство с ошпариванием кожи объективно и субъективно». Сыпь и послужила основным диагностическим признаком для выделения новой нозологической единицы. Термин «токсический» Лайелл ввел, полагая, что заболевание вызывается токсемией — циркулирующим в организме определенным токсином. «Некролиз» — медицинский неологизм, придуманный самим Лайеллом, скомбинировавшим в нем основной клинический признак — «эпидермолиз» и гистопатологический признак — «некроз».
Также Лайелл отметил тяжесть поражения слизистых оболочек и необычную слабость воспалительных процессов в дерме — «дермальное безмолвие».
В научном мире заболевание получило имя своего первооткрывателя еще при жизни Лайелла — в 60‑е годы. Однако сам дерматолог всегда использовал обозначение ТЭН.
В 1967 году, проведя целевой опрос коллег по всей Великобритании, Лайелл представил самое обширное на сегодняшний день обобщение по ТЭН — 128 случаев заболевания. В том же году он описал 4 формы ТЭН, соответствующие определенной этиологии: стафилококковая, лекарственная, смешанная и идиопатическая.
В настоящее время стафилококковая форма синдрома Лайелла выделена в отдельную нозологическую единицу: стафилококковый синдром ошпаренной кожи (staphylococcal scalded skin syndrome, SSSS, L00 по МКБ-10).
Эпидемиология
С 70‑х годов в медицине ведется ежегодный учет распространенности синдрома Лайелла. По данным разных авторов, показатели колеблются в пределах 0,4–1,3 случая на 1 млн населения в год. Показатели смертности составляют 20–60 % от числа заболевших, в зависимости от состояния системы здравоохранения региона. Таким образом число смертей от данной патологии по всему миру за год исчисляется тысячами. Среди аллергических реакций немедленного типа по показателю смертности синдром Лайелла уступает лишь анафилактическому шоку. В общей структуре лекарственных аллергий доля синдрома Лайелла составляет 0,3 %. Чаще болеют женщины: соотношение с пациентами-мужчинами 1,5:1. Прямой зависимости риска заболевания от возраста не выявлено. Группой риска считаются пациенты, ранее перенесшие синдром Лайелла, особенно в детском возрасте.
Самая распространенная форма синдрома — лекарственная, до 80 % всех случаев.После лекарственной, второй по частоте причиной выступают злокачественные новообразования (особенно лимфомы). Частота идиопатических случаев синдрома составляет 5–10 %.
У детей Лайелла синдром чаще — до 60 % случаев — имеет инфекционную этиологию. Особая группа риска проявления болезни среди детей — это перенесшие в раннем возрасте ОРВИ и прошедшие в связи с этим курс лечения НПВП.
Этиология
Дискуссии об этиологии и патогенезе синдрома Лайелла продолжаются. Наиболее изучена лекарственная форма заболевания, которая развивается из‑за нарушения способности организма к обезвреживанию реактивных промежуточных лекарственных метаболитов. Данные метаболиты взаимодействуют с тканями, в результате формируется антигенный комплекс, иммунный ответ на который и инициирует развитие болезни.
Фактически доказана и генетическая предрасположенность к данной патологии, в частности у лиц с рядом антигенов комплекса гистологической совместимости HLA: A2, А29, В12, В27, DR7. Наличие в организме хронических очагов инфекции (синусит, тонзиллит, холецистит и т. п.), приводящих к снижению иммунитета, — увеличивает риск заболевания. Особую группу риска составляют ВИЧ-инфицированные пациенты: у них риск развития синдрома Лайелла в 1000 раз выше, чем в общей популяции.
Диагностика
Для дифференциальной и лабораторной диагностики провокационные пробы не проводятся, поскольку высок риск неконтролируемых осложнений. Наиболее распространены внеорганизменные диагностические пробы, основанные на реакциях клеток крови пациента на сенсибилизировавшее организм вещество. К ним относятся: тест дегрануляции базофилов по Шелли, реакция агломерации лейкоцитов по Флеку, реакция бластной трансформации лимфоцитов, гемолитические тесты.
Апоптоз кератиноцитов — один из первых тканевых морфологических признаков синдрома Лайелла. Всё большее распространение приобретает пункционная биопсия с использованием замороженных срезов кожи. При этом выявляются отсутствие типичных акантолитических клеток, тотальный эпидермальный некролиз, под- и внутриэпидермальные пузыри.
Течение
По характеру течения выделяют три варианта клиники синдрома Лайелла:
У подавляющего числа пациентов — более 90 % — присутствуют эрозивные изменения слизистых оболочек. Типичны жалобы на болезненность по ходу уретры при мочеиспускании и светобоязнь.
Характерен положительный симптом Никольского: отслойка эпидермиса на внешне неизмененной коже при скользящем надавливании и отслойка околопузырного эпидермиса при потягивании за обрывок пузырной покрышки. При особо тяжелых формах наблюдается тотальная отслойка эпидермиса при трении по всей поверхности тела пациента.
Синдром Стивена — Джонсона или синдром Лайелла?
Один из главных прогностических факторов при синдроме Лайелла — площадь некролизированной поверхности. Поэтому очень важна правильная оценка ее протяженности. Для этого используются те же правила, что и в комбустиологии: правило «девятки» — когда руки, грудь и живот считаются по 9 % поверхности тела, а спина и ноги — по 18 %; и правило «однопроцентной ладони». Для более точной оценки рекомендуется измерять площадь отделенного и отделяемого эпидермиса не только на участках с выраженными эритематозными изменениями, но и на отдаленных от «эпицентра» участках тела.В зависимости от площади пораженной некролизом поверхности выделяют клинические отличия синдрома Лайелла от синдрома Стивена — Джонсона.
В последние годы набирает популярность теория, что эти синдромы являются двумя вариантами тяжелого исхода эпидермолитической кожной реакции на медикаменты и отличаются лишь степенью отслойки кожного покрова.
Системная терапия
К сожалению, единых клинических рекомендаций при диагностированном синдроме Лайелла не существует. Это связано прежде всего с полиорганностью поражений, что предполагает в первую очередь разнонаправленную посимптомную терапию.Для лечения синдрома Лайелла правило «отмены последнего» назначенного медикамента чаще всего неэффективно, так как время проявления заболевания варьирует от нескольких часов до нескольких суток. Поэтому рекомендуется отмена всех ранее назначенных медикаментов и экстренная симптоматическая терапия. Подтверждено, что быстрая и тотальная отмена всех медикаментов при невозможности четкого выявления определенного аллергена — улучшает прогноз заболевания на 30 %. В рамках специфического лечения аллергического синдрома Лайелла большинством исследователей однозначно рекомендованы:
Лечение поражений кожного покрова и слизистых проводят по принципам терапии ожогов. Соблюдается режим парентерального питания. Коррекция инфузий осуществляется в зависимости от состояния пациента.
В период нахождения в стационаре обязательны регулярные — не реже одного раза каждые 72 часа — осмотры урологом, окулистом, стоматологом, отоларингологом, чтобы вовремя выявить и назначить соответствующую терапию при поражении слизистых оболочек.
Прогноз
С 2011 года на Западе распространена SCORTEN шкала оценки тяжести синдрома Лайелла. В ней учитываются следующие прогностические факторы:
Наличие каждого фактора увеличивает риск летального исхода. Так, примерный риск смерти составляет: при наличии 1 фактора — до 3,2 %; 2‑х факторов — 12,1 %; 3‑х факторов — 35,3 %; 4‑х факторов — 58,3 %; 5 и более факторов — 90 %.
Клинический случай
В 2009 году в Донецке я стал свидетелем редчайшего для Донбасса (всего 6 случаев в Донецкой области за период с 1991 по 2013 годы!) случая синдрома Лайелла. Пациентка: 37 лет. Аллергический и инфекционный анамнезы — не отягощены. За трое суток до поступления заболела простудным заболеванием. Лечилась «знакомыми» лекарствами: таблетки от кашля, глазные, носовые капли, витамины. С вечера второго дня появились зуд, высыпания. Самостоятельно принимала супрастин. После кратковременного облегчения — состояние ухудшилось. Вечером на третьи сутки, после обморока доставлена БСМП в городскую больницу, в течение нескольких часов переведена в областную клинику.
Поступила женщина с гиперемированной кожей на грудной клетке, плечах, внутренних поверхностях бедер. На третий день появились наполненные мутноватым содержимым пузыри. Объем иных достигал 100 мл. На протяжении всего периода сохранялась гиперемия век, склер, слизистых оболочек ротовой полости, перианальной области.
С третьих суток комбустиологом неоднократно предпринимались попытки закрыть раневую поверхность ксенокожей. Однако кратковременные периоды спокойствия сменялись у пациентки психомоторным возбуждением, что приводило к смещению повязок и ксенокожи. Ни один лоскут не прижился. На протяжении двух недель в реанимационном отделении пациентка более половины времени провела в вынужденном медикаментозном сне. А с шестых суток, когда состояние пациентки стало критическим, ее перевели на постоянную ИВЛ.
В данном случае синдром Лайелла диагностирован в течение двух суток после поступления пациентки в стационар; течение заболевания было не молниеносным, а скорее острым; проводилась посимптомная терапия, но спасти женщину не удалось.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.