Акушерство: синдром возобновленного кормления (Obstetrics & Gynecology, май 2019)
Обзор

09 мая 2019 г. в журнале Obstetrics & Gynecology опубликована статья: «Потеря плода во втором триместре у пациентки с гиперемезис беременных, осложненной синдромом возобновленного кормления».
Синдром возобновленного кормления это сочетание электролитных нарушений после возобновления поступления глюкозы в организм во время адаптационной фазы голодания и нарушения питания, что приводит к дисбалансу жидкости, повреждению органов мишеней и потенциально к смерти.
Большинство литературных данных касаются синдрома возобновленного кормления у пациентов с нервной анорексией, раком, синдромами мальабсорбции, послеоперационных осложнений, неконтролируемый сахарный диабет и алкоголизм.
Беременные и плод имеют уникальную уязвимость к катастрофическим эффектам синдрома возобновленного кормления.
В представленной статье авторы описывают случай синдрома возобновленного кормления у беременной с гиперемезис беременных. Описываются патология в лабораторных тестах при поступлении. В первый день в больнице вводят в/в 1 литр физ.раствора со 100 мг тиамина, 2 г магнезии и 1 мг фолиевой кислоты, а также в/в зофран 4 мг и ранитидин 50 мг. Делают УЗИ, нормальный плод с надлежащей амниотической жидкостью и ЧСС.
Через 3 часа делают вторую инфузию 1 литр физ. раствора с мультивитаминами (в таблице 2 в статье), 100 мг тиамина, 2 г магнезии, и дают калий перорально 40 mEq. В течение первого дня мочи получили 0,5 мл/кг/час.
На 2й день в 3:00 утра фетальная активность норма, но электролитные нарушения сохраняются. Выделение мочи выросло до 3,1 мл/кг/час. В 7:00 утра пациентка отмечает улучшение тошноты и смогла скушать завтрак. В это же время впервые вводят в/в декстрозо-содержащий раствор, смотрят допплером и не слышат сердцебиение плода. Срочно УЗИ, где подтверждено отсутствие сердечной деятельности у плода. Далее делают родоразрешение. Общий осмотр рожденного плода: фенотипически нормальный плод женского рода, вес 102 грамма, плацентарная гистология без признаков инфекции или тромбомботических событий. Устанавливают диагноз синдром возобновленного кормления.
Далее авторы обсуждают несколько случаев синдрома возобновленного кормления у беременных, и что возобновление приема глюкозы в ситуациях голодания и нарушения питания у беременных вызывает каскад реакций, приводящих к синдрому возобновленного кормления у беременных.
Авторы предполагают, что их пациентка после длительного периода голодания и нарушенного питания, приняла очень сладкий без нутриентов напиток, который стал катализатором каскада синдрома возобновленного кормления.
Авторы советуют проводить дополнительное обучение беременных с гиперемезис беременных о риске синдрома возобновленного кормления и об необходимости избегать чрезмерного употребления сахара без надлежащего восстановления электролитов и нутриентов.
Рефидинг-синдром у пациентов хирургического профиля. Анализ клинических случаев
Полный текст:
Аннотация
Введение. Рефидинг-синдром — это состояние, в основе которого лежат метаболические нарушения, возникающие в результате возобновления питания у пациентов после длительного голодания. Истинная частота потенциально опасного для жизни синдрома повторного кормления неизвестна. В этой связи целью настоящей работы является демонстрация на примере клинического случая клинической картины и методов разрешения рефидинг-синдрома.
Материалы и методы. На примере пациентки с острым панкреатитом средней тяжести продемонстрирована клиническая картина рефидинг-синдрома с выраженной неврологической и кардиологической симптоматикой при возобновлении энтерального питания. Представлен обзор доступной литературы на данную тему.
Результаты и обсуждение. Диагностический поиск проводился в широком диапазоне —исключались острая коронарная и неврологическая патологии. По данным дополнительных лабораторных методов исследования было сформировано предположение о развитии рефидинг-синдрома, проведена коррекция лечения. Применялось парентеральное введение фосфатсодержащих препаратов, а также энтеральное питание, в составе которого имеются фосфаты. Пациентка переведена на долечивание в неврологическое отделение. Выписана на 53-е сутки с полным регрессом неврологической симптоматики.
Заключение. Ключевым клиническим маркером рефидинг-синдрома является гипофосфатемия — очень низкий уровень фосфора в крови. Однако пониженное содержание калия, кальция, магния и витамина В1 в крови также может сыграть свою роль. Высокий риск развития рефидинг-синдрома отмечается у пациентов с хронической алиментарной недостаточностью и/или не принимающих пищу более 10 дней. Повторное кормление следует начинать при низком уровне замещения энергии. Прием витаминов следует начинать с повторного кормления и продолжать в течение не менее 10 дней. Исправление дисбаланса электролитов и жидкости перед кормлением не требуется; это следует делать вместе с кормлением.
Ключевые слова
Для цитирования:
Нартайлаков М.А., Салимгареев И.З., Пантелеев В.С., Нагаев Ф.Р., Погадаев В.В., Резяпов В.В., Иванов И.И. Рефидинг-синдром у пациентов хирургического профиля. Анализ клинических случаев. Креативная хирургия и онкология. 2019;9(2):118-124. https://doi.org/10.24060/2076-3093-2019-9-2-118-124
For citation:
Nartailakov M.A., Salimgareev I.Z., Panteleev V.S., Nagaev F.R., Pogаdaev V.V., Rezyapov V.V., Ivanov I.I. Refeeding Syndrome in Surgical Patients. A Clinical Case Analysis. Creative surgery and oncology. 2019;9(2):118-124. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-2-118-124
Введение
Рефидинг-синдром — это состояние, в основе которого лежат метаболические нарушения, возникающие в результате возобновления питания у пациентов после длительного голодания 3. Следует отметить, что данное состояние является потенциально смертельно опасным, однако среди хирургов общего профиля существует ограниченное понимание синдрома, отчасти из-за отсутствия общепринятых принципов диагностики и лечения. В этой связи целью настоящей работы является демонстрация на примере клинического случая клинической картины и методов разрешения рефидинг-синдрома.
Клинический случай
Пациентка Г., 52 года, поступила в хирургическое отделение с диагнозом: острый панкреатит средней тяжести. Осложнения: сдавление двенадцатиперстной кишки воспалительным инфильтратом с формированием дуоденальной непроходимости, парапанкреатический инфильтрат.
Из данных анамнеза: в течение последних 2 месяцев беспокоят незначительные боли в животе, тошнота, рвота, потеря массы тела до 20 кг.
Проводилась дифференциальная диагностика с опухолью головки поджелудочной железы. Онкомаркеры: СА 19-9 30,9 Ед/мл. РЭА 2,02 нг/мл.
По данным компьютерной томографии с в/в контрастированием данных за злокачественное новообразование нет. Больше данных за псевдотуморозный панкреатит, последствия панкреонекроза, формирующаяся псевдокиста поджелудочной железы.
Пациентке был установлен питательный зонд и начата нутритивная поддержка.
На 10-е сутки выполнено оперативное вмешательство: лапаротомия, секвестрнекрэктомия, позадиободочная задняя горизонтальная гастроеюностомия с брауновским соустьем на длинной петле.
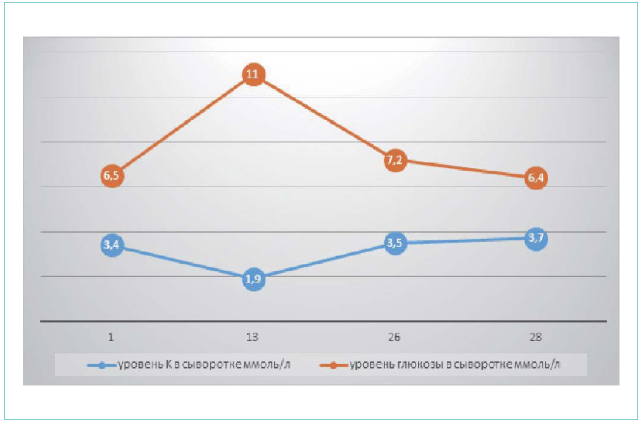
На рисунке 1 приведена динамика изменения уровня сывороточного калия, глюкозы в крови.
Рисунок 1. Динамика изменения уровня сывороточного калия, глюкозы в крови
Figure 1. Dynamics of the plasma potassium and blood glucose change
В 1-е послеоперационные сутки у пациентки по данным ЭКГ отмечено: формирующийся зубец q- в V2, повышение сегмента S-T в V2-V3, отрицательные зубцы Т V4-V5.
Расценен как острый коронарный синдром с подъемом сегмента S-T.
Проведена ЭхоКГ: полости сердца не расширены, левый желудочек шарообразной формы. Гипертрофия миокарда межжелудочковой перегородки (МЖП) в базальном отделе, ее толщина 14 мм. Толщина МЖП в медиальном отделе 7 мм. Акинез переднеперегородочной стенки медиального и апикального сегментов (миокард истончен — формирующаяся аневризма верхушки левого желудочка). Гипокинез боковой, передней, нижней стенок левого желудочка медиального и апикального сегментов. Систолическая функция левого желудочка снижена, ФВ 31 %. Уплотнение восходящего отдела аорты. Сепарация листков перикарда за задней стенкой 3 мм. Д-ЭхоКГ: МР1+, ТР1+. Диастолическая функция левого желудочка нарушена по 1-му типу.
Проведена в экстренном порядке коронарография. Замедление продвижения контраста по левой коронарной артерии до 5-6 кардиоциклов. Замедление продвижения контраста по правой коронарной артерии до 6 кардиоциклов.
Ферменты КФК МВ, КФК в пределах нормы, тропонин отрицательный весь период пребывания в стационаре. На 2-е послеоперационные сутки проводится ЭхоКГ в динамике. Полости сердца не расширены, левый желудочек шарообразной формы. Гипертрофия миокарда МЖП в базальном отделе, ее толщина 14 мм. Толщина МЖП в медиальном и апикальном отделе 7 мм — истончена. Гипокинез переднеперегородочной и нижней стенок медиального и апикального сегментов. Систолическая функция левого желудочка снижена, ФВ 41 %. Уплотнение восходящего отдела аорты. Сепарация листков перикарда за задней стенкой 2,2 мм. Д-ЭхоКГ: МР1+, ТР1+. Диастолическая функция левого желудочка нарушена по 1-му типу. Слабоположительная динамика, улучшение систолической функции левого желудочка.
На 7-е послеоперационные сутки у пациентки развивается клиническая картина проксимального парапареза, атаксический синдром.
Проводится компьютерная томография (КТ) L-S отделов позвоночника. Правосторонняя обызвествленая грыжа диска L5-S1. КТ признаки остеохондроза, деформирующего спондилоатроза L-S отделов позвоночника.
Электронейромиография (ЭНМГ): на момент исследования убедительных данных за полинейропатию не выявлено. Признаки умеренного аксонального поражения малоберцовых нервов, с большой вероятностью вертеброгенного генеза (дисфункция проведения на уровне L4-L5-S1).
На 10-е послеоперационные сутки у пациентки появляется бульбарный синдром и тетрапарез.
По данным КТ головного мозга (г/м): картина атрофических изменений больших полушарий и мозжечка на фоне хронической цереброваскулярной недостаточности. Патологические изменения орбит не выявлены. Патологические изменения придаточных пазух носа не выявлены. Патологические изменения височных костей не выявлены.
МРТ г/м. На момент исследования убедительных данных за очаговую патологию г/м не выявлено. На DWI и ADC картах патологический МР-сигнал не выявлен. Диагностический поиск проводился в широком диапазоне. Консультация гематолога, невролога, терапевта, психотерапевта. Определялся уровень в моче порфобилиногена и уробилиногена. Показатели в пределах нормы.
На 17-е сутки взят анализ на фосфат в сыворотке крови. Гипофосфатемия: 1.03 мг/дл. Самый низкий показатель фосфата в сыворотке крови приходился на 13-й день. Расценено как проявление рефидинг-синдрома.
На 25-е сутки данные ЭхоКГ. Заключение: уплотнение восходящего отдела аорты, фиброзных колец аортального и митрального клапанов. Незначительная гипертрофия миокарда левого желудочка. Асинергия МЖП и нижней стенки ЛЖ, ФВ 60 % (по Тейхольцу). Диастолическая дисфункция левого желудочка 1-го типа. Полости сердца не расширены.
Клинически нарастание неврологического дефицита. Проведена коррекция лечения. Парентеральное введение фосфатсодержащих препаратов, а также энтеральное питание, в составе которого имеются фосфаты. Пациентка переведена на долечивание в неврологическое отделение. Выписана на 53-е сутки с положительной неврологической динамикой в виде появления активных движений в конечностях.
Результаты и обсуждение
Синдром повторного кормления был сначала описан у заключенных, освобожденных из концентрационных лагерей во время Второй мировой войны, которые начали получать кормление после длительного голодания, что привело к сердечной недостаточности, неврологическим осложнениям, включающим кому, судороги, и в конечном счете к летальному исходу [3]. Патофизиология синдрома повторного кормления на сегодняшний день известна. В период голодания организм переходит от использования углеводов к использованию жиров, секреция инсулина уменьшается в ответ на снижение поступления углеводов. Метаболические превращения направлены на сведение к минимуму расщепления белка и аминокислот. При этом в печени из ацетил-КоА активируется синтез кетоновых тел (Р-оксибутирата и ацетона), которые служат источником энергии для многих тканей, в том числе и для мозга. Это приводит к уменьшению скорости распада белков и снижению потребности в глюкозе 6.
В период длительного голодания содержание некоторых внутриклеточных минералов значительно снижается, особенно фосфата. Однако концентрации этих минералов в сыворотке могут оставаться нормальными. Это происходит потому, что минералы в основном находятся во внутриклеточном депо. Кроме того, наблюдается снижение почечной экскреции [7].
Обычно биохимические нарушения возникают в первые 3-4 суток после начала кормления. При возвращении к нормальному питанию резкое насыщение углеводами приводит к внезапной перестройке организма с жирового на углеводный обмен. Увеличивается секреция инсулина. Глюкоза становится основным источником энергии. Инсулин стимулирует возвращение магния и калия в клетку, способствует гликогенезу и синтезу жира и белка. Эти анаболические процессы требуют фосфорилирования промежуточных веществ и, следовательно, высоких затрат внутриклеточных фосфатов. Внутриклеточное депо этих электролитов пополняется за счет быстрого уменьшения их концентрации в плазме крови [8, 9].
Истощение запасов фосфата является чрезвычайно опасным состоянием, при котором нарушаются почти все клеточные физиологические процессы. Фосфат играет важную роль в процессах клеточного дыхания, поскольку его первый этап, гликолиз, включает фосфорилирование глюкозы. Фосфат принимает участие в поддержании функции внутриклеточных ферментов, включая синтез 2,3-дифосфоглицерата, который регулирует диссоциацию кислорода и гемоглобина, участвует в буферной системе кислото- основания.
Общий уровень фосфатов в сыворотке крови составляет 3,0-5,0 мг/дл [8, 10].
Легкая гипофосфатемия: 2,5-3,0 мг/дл.
Умеренная гипофосфатемия: 1,0-2,5 мг/дл.
Либо при наличии двух или более из следующих условий:
Профилактика
Чтобы обеспечить адекватную профилактику, NICE рекомендует провести тщательную оценку питания перед началом повторного кормления. Следует установить недавнее изменение веса, рацион питания, потребление алкоголя, а также социальные и психологические проблемы. Плазменные электролиты (особенно фосфат, натрий, калий и магний) и глюкоза должны быть измерены на базовом уровне перед кормлением, а любые недостатки должны быть исправлены во время кормления с тщательным мониторингом [20].
Для пациентов с высоким риском развития рефидинг- синдрома пополнение энергии должно начинаться медленно (максимум 0,042 МДж/кг/24 часа) и должно быть адаптировано к каждому пациенту. Затем энергетическая доставка может быть увеличена для удовлетворения или превышения полных потребностей в течение четырех-семи дней. У пациентов с недостаточным питанием (индекс массы тела 1. Миронов Л.Л., Крастелёва И.М., Каско И.Б., Панов А.П., Курдюкова Д.Ю. Рефидинг-синдром. Здравоохранение (Минск). 2018;(9):17–23.
2. Dewar H., Horvath R. Refeeding syndrome. In: Todorovic V.E., Micklewright A., editors. A pocket guide to clinical nutrition. 2nd ed. British Dietetic Association; 2001.
3. Rio A., Whelan K., Goff L., Reidlinger D.P., Smeeton N. Occurrence of refeeding syndrome in adults started on artificial nutrition support: prospective cohort study. BMJ Open. 2013;3(1):e002173. DOI: 10.1136/ bmjopen-2012-002173
4. Knochel J.P. The pathophysiology and clinical charactertistics of severe hypophosphatemia. Arch Intern Med. 1977;137:203–20. PMID: 836118
5. Crook M.A., Hally V., Pantelli J.V. The importance of the refeeding syndrome. Nutrition. 2001;17(7-8):632–7. PMID: 11448586
6. Friedli N., Stanga Z., Sobotka L., Culkin A., Kondrup J., Laviano A., et al. Revisiting the refeeding syndrome: Results of a systematic review. Nutrition. 2017;35:151–60. DOI: 10.1016/j.nut.2016.05.016
7. Nasir M., Zaman B.S., Kaleem A. What a trainee surgeon should know about refeeding syndrome: a literature review. Cureus. 2018;10(3):e2388. DOI: 10.7759/cureus.2388
8. Hayek M.E., Eisenberg P.G. Severe hypophosphatemia following the institution of enteral feedings. Arch Surg. 1989;124(11):1325–8. DOI: 10.1001/archsurg.1989.01410110087016
9. Koletzko B. Nutrition rehabilitation in eating disorders. World Rev Nutr Diet. 2015;113:259–65. DOI: 10.1159/000375192
10. Klein C.J., Stanek G.S., Wiles C.E. Overfeeding macronutrients to critically ill adults: metabolic complications. J Am Diet Assoc. 1998;98(7):795–806. DOI: 10.1016/S0002-8223(98)00179-5
11. Malczyk Ż., Oświęcimska J.M. Gastrointestinal complications and refeeding guidelines in patients with anorexia nervosa. Psychiatr Pol. 2017;51(2):219–29. DOI: 10.12740/PP/65274
12. Lee Z.Y., Heyland D.K. Determination of nutrition risk and status in critically ill patients: what are our considerations? Nutr Clin Pract. 2019;34(1):96–111. DOI: 10.1002/ncp.10214
13. Marik P.E., Bedigan M.K. Refeeding hypophosphataemia in an intensive care unit: a prospective study. Arch Surg. 1996;131(10):1043–7. DOI: 10.1001/archsurg.1996.01430220037007
14. Martinez M.J., Matrinez M.A., Montero M., Campelo E., Castro I., Inaraja M.T. Hypophosphatemia in postoperative patients on total parenteral nutrition:influence of nutritional support teams. Nutr Hosp. 2006;21(6):657–60. PMID: 17147062
15. Perrault M.M., Ostrop N.J., Tierney M.G. Efficacy and safety of intravenous phosphate replacement in critically ill patients. Ann Pharmacother. 1997;31(6):683–8. DOI: 10.1177/106002809703100603
16. Solomon S.M., Kirby D.F. The refeeding syndrome: a review. J Parenter Enteral Nutr. 1990;14(1):90–7. DOI: 10.1177/014860719001400190
17. Tan M.C.Y., Chien J.M.F., Khor L.Y., Chea Y.W., Wong T.H. Acute presentation of post-operative kwashiorkor and refeeding syndrome complicated by chronic Strongyloides infection in an elderly patient. ANZ J Surg. 2018;88(9):E692. DOI: 10.1111/ans.14769
18. Reuler J.B., Girard D.E., Cooney T.G. Wernicke’s encephalopathy. N Engl J Med. 1985;312(16):1035–9. DOI: 10.1056/ NEJM198504183121606
19. Weinsier R.L., Krumdieck C.L. Death resulting from overzealous total parenteral nutrition: the refeeding syndrome revisited. Am J Clin Nutr. 1980;34(3):393–9. DOI: 10.1093/ajcn/34.3.393
20. Rizzo S.M., Douglas J.W., Lawrence J.C. Enteral nutrition via nasogastric tube for refeeding patients with anorexia nervosa: a systematic review. Nutr Clin Pract. 2019;34(3):359–70. DOI: 10.1002/ ncp.10187
Об авторах
Нартайлаков Мажит Ахметович — д.м.н., член-корреспондент РАЕН, профессор, зав. кафедрой общей хирургии с курсом лучевой диагностики ИДПО, директор НИИ новых медицинских технологий
Салимгареев Ильдар Зуфарович — к.м.н., зав. отделением гастрохирургии
Пантелеев Владимир Сергеевич — д.м.н., зав. отделением лазерной хирургии
Погадаев Вадим Валерьевич — врач-хирург отделения гастрохирургии
Резяпов Вадим Вакилевич — врач-хирург отделения гастрохирургии
Иванов Иван Иванович — врач-хирург отделения гастрохирургии
Для цитирования:
Нартайлаков М.А., Салимгареев И.З., Пантелеев В.С., Нагаев Ф.Р., Погадаев В.В., Резяпов В.В., Иванов И.И. Рефидинг-синдром у пациентов хирургического профиля. Анализ клинических случаев. Креативная хирургия и онкология. 2019;9(2):118-124. https://doi.org/10.24060/2076-3093-2019-9-2-118-124
For citation:
Nartailakov M.A., Salimgareev I.Z., Panteleev V.S., Nagaev F.R., Pogаdaev V.V., Rezyapov V.V., Ivanov I.I. Refeeding Syndrome in Surgical Patients. A Clinical Case Analysis. Creative surgery and oncology. 2019;9(2):118-124. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-2-118-124
Гипофосфатемия и рефидинг-синдром при возобновлении питания у пациентов в критических состояниях (обзор литературы)
Для корреспонденции: Конаныхин Василий Дмитриевич, лаборант отделения анестезиологии и реаниматологии НИИ клинической хирургии Российского национального исследовательского медицинского университета им. Н.И. Пирогова; e-mail: v.konanykhin@ya.ru
Для цитирования: Ярошецкий А.И., Конаныхин В.Д., Степанова С.О., Резепов Н.А. Гипофосфатемия и рефидинг-синдром при возобновлении питания у пациентов в критических состояниях (обзор литературы). Вестник интенсивной терапии имени А.И. Салтанова. 2019;2:82–91. DOI: 10.21320/1818-474X-2019-2-82-91
Реферат
Синдром возобновления питания, или рефидинг-синдром (РФС) — жизнеугрожающее состояние, которое возникает при возобновлении питания у пациентов с исходной нутритивной недостаточностью. Впервые РФС был описан более 70 лет назад, но до сих пор мало исследован. Основа патогенеза РФС — выраженные водно-электролитные и метаболические нарушения, провоцируемые возобновлением питания, на фоне истощения запасов калия, магния, фосфора, приводящие к полиорганной недостаточности.
Гипофосфатемия является основным диагностическим критерием РФС, при этом у пациентов отделения реанимации и интенсивной терапии (ОРИТ) существует множество других причин гипофосфатемии, что значительно затрудняет диагностику. Большинство исследований, посвященных РФС, проведены среди пациентов с нервной анорексией. В ОРИТ встречается около 34 % случаев РФС, но до сих пор все рекомендации по ведению этих больных были перенесены из практики лечения нервной анорексии и были основаны на мнениях экспертов. За последние годы появилось несколько крупных работ, которые доказали эффективность гипокалорийного подхода в лечении пациентов с РФС у пациентов в критических состояниях.
Настоящий обзор посвящен проблеме РФС у пациентов с нервной анорексией и пациентов ОРИТ, дифференциальной диагностике и подходам к лечению этого состояния.
Ключевые слова: рефидинг-синдром, рефидинг-гипофосфатемия, синдром возобновления питания, нутритивная поддержка, парентеральное питание
Поступила: 03.03.2019
Принята к печати: 26.03.2019
Введение
Рефидинг-синдром (РФС) — это комплекс жизнеугрожающих метаболических нарушений, возникающих при возобновлении питания у пациентов с исходной нутритивной недостаточностью [1]. Клиническим проявлением синдрома является органная дисфункция:
Провоцирующим фактором может быть любое питание: пероральное, энтеральное и парентеральное.
Впервые проявления РФС были описаны у освобожденных узников концентрационных лагерей времен Второй мировой войны, а также у голодающих жертв вооруженных конфликтов, когда возобновление питания приводило к полиорганной недостаточности [2]. В 1980-х гг. на РФС вновь было обращено внимание в связи с развитием полиорганной недостаточности у недокормленных пациентов, которым проводили полное парентеральное питание [3].
Гипофосфатемия сопровождает РФС в 96 % случаев, однако существует множество других причин гипофосфатемии, что затрудняет дифференциальную диагностику [4].
РФС исторически считали проблемой пациентов с нервной анорексией и длительным голоданием, пока не обратили внимание на то, что у некоторых групп пациентов частота гипофосфатемии после возобновления питания составляет 20 %, а у пациентов отделения реанимации и интенсивной терапии (ОРИТ) может достигать 59 % [5]. В последние годы началось изучение эпидемиологии РФС у пациентов ОРИТ, а также наметилась стратегия для оптимизации диагностики и лечения синдрома возобновления питания у пациентов в критических состояниях [6, 7].
Эпидемиология
Исследование эпидемиологии РФС у пациентов в критических состояниях осложняет отсутствие единых общепризнанных критериев и высокоспецифичных маркеров этого состояния [8].
Также по шкале NICE высокий риск развития РФС существует при наличии двух из следующих факторов («малые» критерии):
Помимо этого, рутинно применяют шкалы MUST и NRS 2002, которые очень похожи на шкалу NICE [15, 16]. Данные критерии используют для определения риска РФС у пациентов с нервной анорексией, однако в исследованиях, проведенных у пациентов в критических состояниях, они не показали своей эффективности [17]. Это может быть объяснено тем, что у пациентов в критических состояниях риск РФС обусловлен не длительным голоданием, а стресс-индуцированным катаболизмом. Так, в единственном рандомизированном клиническом исследовании, проведенном Doig G. et al., средний индекс массы тела (ИМТ) составлял 28 кг/м2 [6], тогда как при нервной анорексии низкий ИМТ практически во всех работах свидетельствует о риске гипофосфатемии [12, 18–20].
Хотя проведенные среди пациентов ОРИТ исследования не выявили предикторов развития РФС, а так- же не показали эффективности шкал, применяющихся у пациентов с нервной анорексией, пациента с клиническими признаками нутритивной недостаточности и истощения, низким индексом массы тела, вероятно, следует отнести к категории высокого риска [14].
Патогенез рефидинг-синдрома
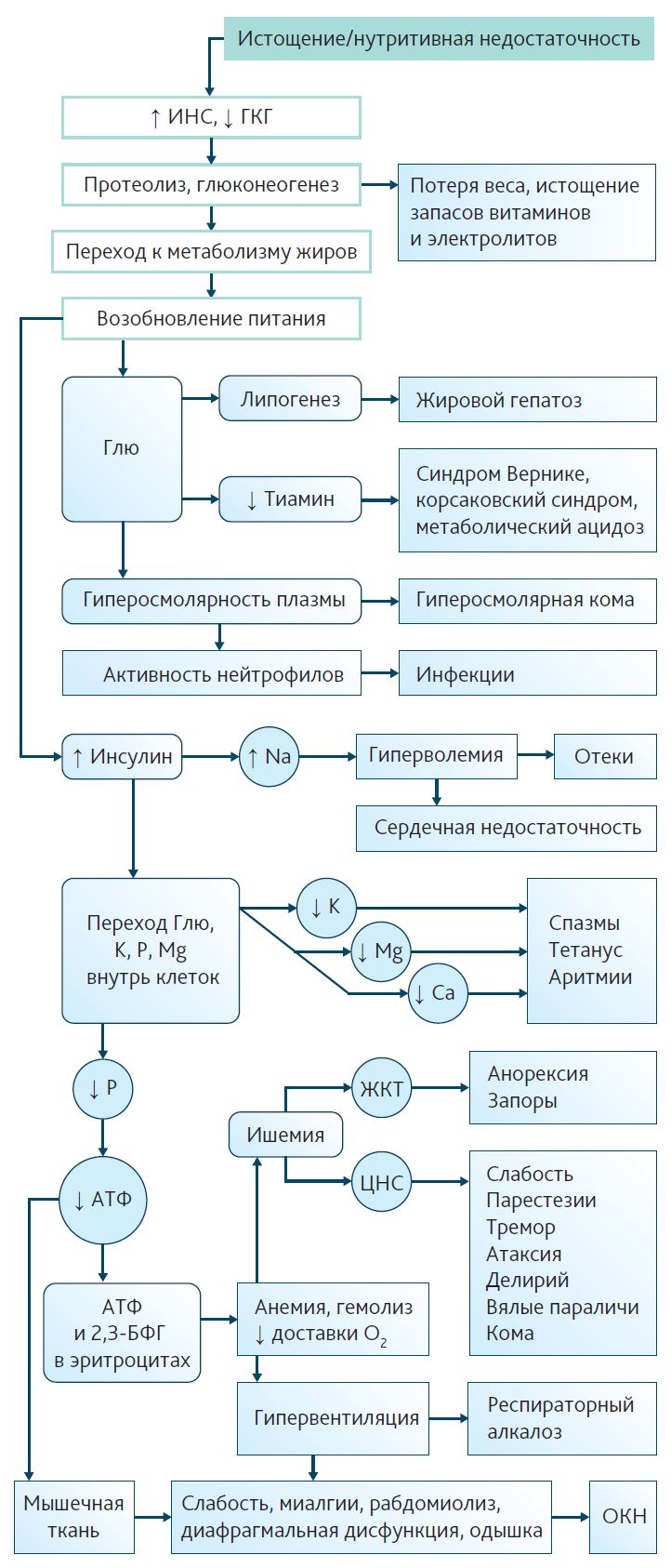
Патогенез РФС может быть представлен следующим образом (рис. 1).
Рис. 1. Патогенез рефидинг-синдрома 2,3-БФГ — 2,3-бифосфоглицерат; Ca — кальций; K — калий; Mg — магний; P — фосфор; АТФ — аденозинтрифосфат; ГКГ — глюкагон; Глю — глюкоза; Инс — инсулин; ОКН — острый канальцевый некроз
При длительном голодании повышается секреция контринсулярных гормонов, снижается секреция инсулина, происходит переход анаболического состояния к катаболическому [21]. Основным источником энергии становятся кетоновые тела и аминокислоты, получаемые в процессе катаболизма мышечной и жировой ткани [22]. Питание глюкозозависимых тканей поддерживается за счет глюконеогенеза в печени, в дальнейшем уровень базального метаболизма значительно снижается, замедляется глюконеогенез [23]. Это необходимо для экономии белка и поддержания тощей массы тела, т. к. аминокислоты используются для «наполнения» цикла трикарбоновых кислот [24]. В процессе голодания снижается внутриклеточный объем, происходит потеря основных внутриклеточных ионов (фосфора, калия, магния), истощаются запасы витаминов, в том числе тиамина [25]. При возобновлении питания происходит повышение плазменной концентрации глюкозы, стимулируется секреция инсулина, происходит переключение на гликолиз [26]. При повышении концентрации инсулина происходит транспорт ионов внутрь клеток, вследствие чего возникают гипофосфатемия, гипомагниемия, гипокалиемия, а также снижается экскреция натрия, увеличивается задержка жидкости, возникают отеки [27].
При возникновении РФС характерно появление инсулинорезистентности: гипергликемия, метаболизм кетоновых тел, снижение дыхательного коэффициента (RQ) [26, 28]. Персистирующая гипергликемия значимо увеличивает летальность, что обусловливает важность ее контроля и коррекции [29, 30].
Неорганические фосфаты PO4 3- являются одними из основных внутриклеточных электролитов; они необходимы для синтеза высокоэнергетических фосфатов (АТФ), 2,3-бифосфоглицерата, регулирующего сродство гемоглобина к кислороду, нуклеотидов, входящих в состав ДНК и РНК. Кроме того, неорганический фосфат — субстрат ферментов фосфокиназ и фосфатаз, играющих ключевую роль в клеточных сигнальных системах, а также компонент буферной системы регуляции кислотно-щелочного равновесия [31]. Гипофосфатемия может вызывать острую дыхательную, сердечную, почечную недостаточность, задержку отлучения от респиратора, мышечную слабость, рабдомиолиз, гемолиз, нарушение хемотаксиса лейкоцитов, отек головного мозга [1].
Гипокалиемия приводит к нарушению возбудимости кардиомиоцитов, ухудшению проведения нервных импульсов, возникновению жизнеугрожающих аритмий и является независимым предиктором внутрибольничной летальности [32].
Магний является кофактором более 300 ферментов, в том числе обеспечивает биологическую активность АТФ. У пациентов ОРИТ дефицит магния встречается в 18–65 % случаев при поступлении и связан с ростом летальности, увеличением длительности ИВЛ, увеличением времени нахождения в ОРИТ [33].
Тиамин является кофактором в реакциях пентозофосфатного пути, а также превращения пирувата в ацетил-КоА [34]. При этом тиамин не синтезируется в организме человека, а его запасы ограничены коротким периодом полураспада, что делает его зависимым от поступления с пищей. У пациентов с исходной нутритивной недостаточностью внутриклеточные запасы тиамина зачастую истощены. Проведенное обсервационное исследование выявило дефицит тиамина у 39,7 % пациентов ОРИТ [35]. Несмотря на то что тиамин является кофактором, в ходе превращения пирувата в лактат происходит его гидролиз, что приводит к дальнейшему уменьшению запасов тиамина при возобновлении питания, нарушению аэробного метаболизма углеводов и недостаточному синтезу АТФ, повышению концентрации лактата за счет перехода на анаэробный гликолиз.
Гипофосфатемия у пациентов в критических состояниях
Плазменная концентрация фосфатов в норме составляет 0,85–1,45 ммоль/л, при этом легкая (0,6–0,85 ммоль/л) и среднетяжелая (0,3–0,6 ммоль/л) гипофосфатемия обычно протекают бессимптомно, а тяжелая гипофосфатемия 2,5 г/кг/сут) и калорий (> 60 ккал/кг/сут). На тот момент стабильные жировые эмульсии не были доступны, поэтому небелковые калории доставлялись за счет растворов углеводов [39].
С точки зрения современного представления о РФС это были пациенты очень высокого риска — истощенные больные, питание за счет парентеральных растворов глюкозы, высокий калораж питания.
В своих работах исследователи отмечали частое развитие гипофосфатемии, поэтому парентеральное питание всегда сопровождалось замещением дефицита фосфора [41]. Нередко встречались острая задержка жидкости и прогрессирующая сердечная недостаточность, хотя эти явления неудивительны, учитывая большую инфузионную нагрузку (до 5 л в сутки, которые затем компенсировали стимуляцией диуреза). Концепция парентеральной гипералиментации была широко популяризирована Dudrick S. и его учениками, но она не подтвердила своей эффективности в большинстве современных исследований [42–46].
Гипофосфатемия
Хотя гипофосфатемия играет важную роль в патогенезе РФС, доказательств о необходимости коррекции бессимптомной гипофосфатемии нет, т. к. в небольших исследованиях это не улучшило клинический исход у пациентов с риском РФС [47]. Тем не менее из-за потенциального риска жизнеугрожающих осложнений многочисленные рекомендации по ведению пациентов с РФС, основанные в целом на экспертном мнении, говорят об обязательной коррекции гипофосфатемии [14, 27, 37]. Фосфаты входят в состав современных смесей для парентерального и энтерального питания, но их количества недостаточно для восполнения дефицита фосфатов при РФС. Препараты фосфора в РФ, к сожалению, не зарегистрированы. В других странах они доступны в виде таблеток и растворов для инфузий, в виде фосфатов натрия или калия. Отсутствие на российском рынке добавок фосфатов для энтерального и парентерального питания значительно осложняет лечение таких больных.
Рекомендации по лечению гипофосфатемии [27, 48]
Коррекция электролитов
До возобновления питания должны быть оценены концентрации фосфора, калия, магния в плазме крови, за- тем необходим ежедневный мониторинг в первую неделю [14]. Все пациенты с риском развития РФС должны получать магний и фосфор для поддержания их повышенной потребности при возобновлении питания. В зависимости от степени дефицита дозировку необходимо корректировать. Также необходимо избегать гипокалиемии. При этом не следует откладывать возобновление питания на время коррекции электролитных нарушений. На данный момент не существует доказательной базы по режимам замещения дефицита электролитов при РФС у пациентов в критическом состоянии, поэтому все рекомендации основаны на мнениях экспертов.
Рекомендации по замещению дефицита электролитов при рефидинг-синдроме [27, 48]
Тиамин
Для профилактики развития энцефалопатии Вернике и Корсаковского синдрома перед началом питания следует назначить 200–300 мг тиамина, затем ежедневно вводить комплекс витаминов группы B в течение первых 10 сут возобновления питания [27, 48].
Особенности интенсивной терапии у пациентов с нервной анорексией
Наиболее исследованной группой пациентов с риском РФС являются больные нервной анорексией. Нервная анорексия — одно из самых опасных заболеваний в области психиатрии, а восстановление массы тела — обязательный этап в лечении таких пациентов, но слишком агрессивное введение питания может спровоцировать развитие РФС, особенно при парентеральном питании [49]. Это нашло отражение в рекомендациях по лечению нервной анорексии, согласно которым питание у пациентов с риском развития РФС необходимо начинать с минимальных объемов (500 ккал/сут) и постепенно расширять калораж [37].
Пример восстановления питания у пациентов с нервной анорексией
Ниже представлены примеры расчета при сипинге и зондовом питании пациента с нервной анорексией массой 35 кг (табл. 2, 3). Следует отметить, что стандартные энтеральные смеси не содержат достаточного количества фосфатов, чтобы покрыть потребности пациентов после длительного голодания.
Таблица 2. Пример питания пациента 35 кг при помощи сипинга [48, 50]
Пищевая смесь 1,5 ккал/мл
1–3-й дни, мл
4–5-й дни, мл
6–8-й дни, мл
9–10-й дни, мл
11-й день
Увеличивать по 300 ккал/день до увеличения массы тела 0,5–1 кг в неделю
Таблица 3. Пример питания пациента массой 35 кг через зонд [48, 50, 51]
Энтеральная смесь с пищевыми волокнами, 1 ккал/мл
Калораж, ккал
750 мл 31 мл/ч за 24 ч
1000 мл 42 мл/ч за 24 ч
1250 мл 52 мл/ч за 24 ч
1500 мл 63 мл/ч за 24 ч
Увеличивать по 300 ккал/день до увеличения массы тела 0,5–1 кг в неделю
Следуя таким рекомендациям, врач оберегает пациента, снижая риск развития РФС, но при этом существенно снижается набор веса и увеличивается длительность госпитализации. Также появляется риск недокормить пациента с исходно тяжелой нутритивной недостаточностью — это состояние получило название underfeeding syndrome [37].
За последние годы был проведен ряд работ, оценивающих влияние более агрессивных подходов к лечению РФС. Первое исследование, в котором применялся агрессивный подход к возобновлению питания у пациентов с нервной анорексией, опубликовали в 2010 г. Whitelaw M. et al. Возобновление питания начинали с 1900 ккал/сут (около 45 ккал/кг/сут), при этом не было выявлено клинических случаев РФС [18]. Вслед за этой работой последовали более крупные. Redgrave G. et al. проанализировали рефидинг у 331 пациента с нервной анорексией, у которых применяли высококалорийную стратегию: питание начинали с 1200–1500 ккал/сут и постепенно расширяли до 3500 4000 ккал/сут [19]. Только в двух работах сравнивались две группы пациентов: с консервативным и агрессивным подходом к питанию [12, 52]. Ни в одном из приведенных выше исследований не было выявлено клинических случаев РФС, а увеличенный калораж питания позволил быстрее набрать целевую массу тела и сократить сроки госпитализации, хотя и не влиял на итоговую массу тела.
Хотя ни в одном исследовании не было выявлено случаев РФС, единственным показателем, предсказывавшим развитие гипофосфатемии, являлся ИМТ [12, 52, 53]. При этом необходимо учитывать, что средний ИМТ в этих работах был достаточно высоким (> 16 кг/м2), а проведенный Redgrave et al. анализ подгруппы с крайне низкой массой тела (ИМТ 0,16 ммоль/л, до уровня