Нарушения переработки пуринов
, MD, Sidney Kimmel Medical College of Thomas Jefferson University
Пурины являются ключевыми компонентами клеточных энергетических систем (например, АТФ, НАД), передачи сигналов (например, ГТФ, цАМФ, цГМФ) и вместе с пиримидинами – синтеза РНК и ДНК.
Пурины могут быть синтезированы de novo или переработаны в «реутилизационном» пути нормального катаболизма.
Конечный продукт полного катаболизма пуринов – мочевая кислота.
синдром Леша-Найхана
Это редкое, Х-сцепленное рецессивное Сцепленные с Х-хромосомой рецессивные Генетические нарушения, вызванные изменениями в одном гене («Менделевские нарушения»), являются самыми простыми для анализа и наиболее хорошо поняты. Если экспрессия признака требует только. Прочитайте дополнительные сведения расстройство, вызванное дефицитом гипоксантин гуанинфосфорибозилтрансферазы (HPRT); степень дефицита (и, следовательно, проявлений) зависит от конкретных мутаций. HPRT-дефицит приводит к нарушению пути реутилизации гипоксантина и гуанина. Вместо этого пурины деградируют до мочевой кислоты. Кроме того, уменьшение инозитол монофосфата и гуанозил монофосфата приводит к усилению конверсии 5-фосфорибозил-1-пирофосфата (PRPP) в 5-фосфорибозиламин, что еще больше усиливает перепроизводство мочевой кислоты. Гиперурикемия предрасполагает к развитию подагры и ее осложнений. Пациенты также имеют ряд когнитивных и поведенческих нарушений, этиология которых неясна; считается, что они не связаны с мочевой кислотой.
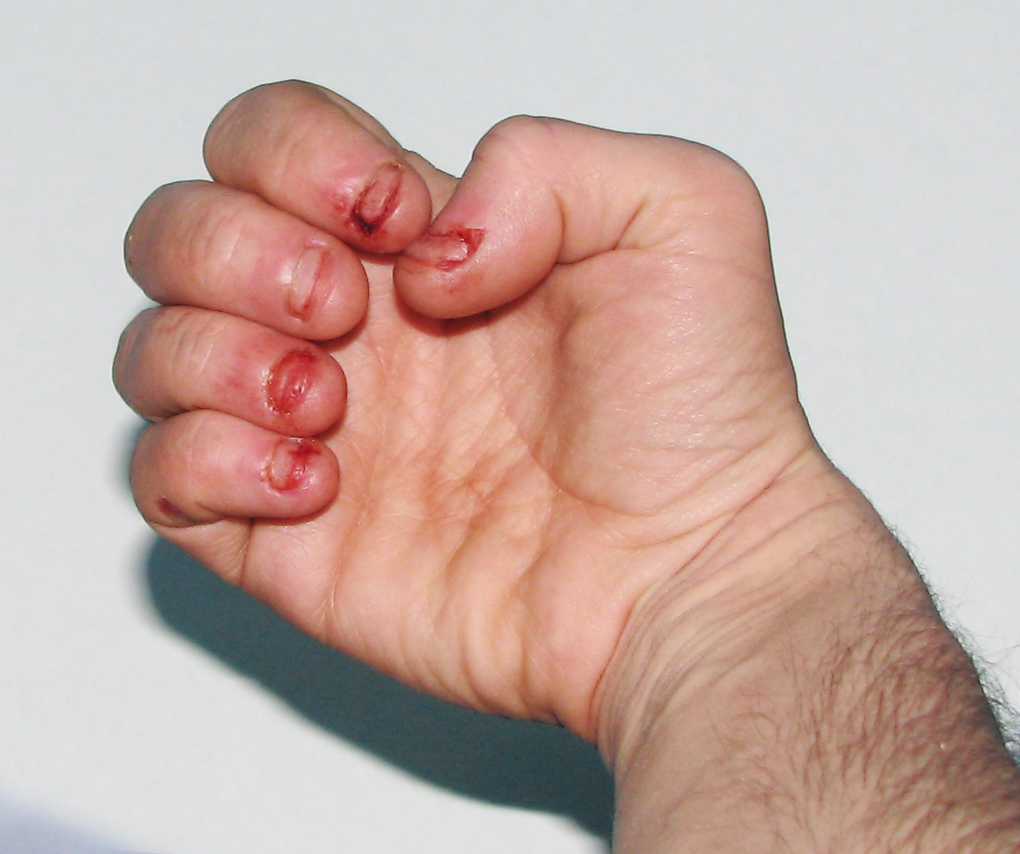
Заболевание обычно проявляется в возрасте 3–12 месяцев с появлением оранжевых песчинок (ксантин) в моче; оно прогрессирует до поражения центральной нервной системы с умственной отсталостью, спастическим церебральным параличом, непроизвольными движениями и самокалечащим поведением (в частности, укусами). Позже хроническая гиперурикемия вызывает симптомы подагры (например, мочекаменную болезнь, нефропатию, подагрический артрит, тофусы).
Диагноз Леша-Найхана предполагают при сочетании дистонии, умственной отсталости и членовредительства. Уровни мочевой кислоты в сыворотке крови, как правило, повышены, и это подтверждается с помощью ДНК анализа.
Способы лечения нарушений функций центральной нервной системы неизвестны; ведение поддерживающее. Самокалечение может потребовать принятия физических мер, удаления зубов, а иногда и лекарственной терапии; применялись различные препараты. Гиперурикемию лечат с применением диеты с низкими дозами пуринов (например, избегая мясные продукты, бобы, сардины) и аллопуринола, ингибитора ксантин оксидазы (последний фермент пути катаболизма пуринов). Аллопуринол предотвращает превращение накопления гипоксантина в мочевую кислоту, потому что гипоксантин хорошо растворим, он выделяется.
Дефицит аденин фосфорибозилтрансферазы
Это редкое аутосомно-рецессивное Аутосомно-рецессивные Генетические нарушения, вызванные изменениями в одном гене («Менделевские нарушения»), являются самыми простыми для анализа и наиболее хорошо поняты. Если экспрессия признака требует только. Прочитайте дополнительные сведения заболевание, приводящее к неспособности реутилизировать аденин для синтеза пуринов. Накопленный аденин окисляется до 2,8-дигидроксиаденина, который осаждается в мочевыводящих путях, что приводит к возникновению таких же проблем, что и при вызванной мочевой кислотой нефропатии (например, почечных колик, частых инфекций, и если диагноз установлен поздно, почечной недостаточности). Болезнь может возникнуть в любом возрасте.
Диагностику недостаточности аденинфосфорибозилтрансферазы проводят путем выявления повышенного уровня 2,8-дигидроксиаденина, 8-гидроксиаденина и аденина в моче; диагноз подтверждают по данным анализа ДНК, содержание в сыворотке мочевой кислоты при этом нормальное.
Лечение состоит в диетическим ограничении пуринов, приеме большого количества жидкости и предотвращении подщелачивания мочи. Аллопуринол может предотвратить окисление аденина; трансплантация почки может быть необходима при терминальной стадии почечной болезни.
Синдром Леша-Нихана
Внимание! Информация носит ознакомительный характер и не предназначена для постановки диагноза и назначения лечения. Всегда консультируйтесь с профильным врачом!
Что такое синдром Леша-Нихана?
Синдром Леша-Нихана (или Нехена) представляет собой редкую врожденную ошибку метаболизма пурина, характеризующуюся отсутствием или дефицитом активности фермента гипоксантин-гуанин фосфорибозилтрансферазы (ГГФТ или англ. HPRT). Пурины являются азотсодержащими соединениями, содержащимися во многих продуктах питания (например, органическое мясо, мясо домашней птице и бобовые).
В отсутствие HPRT пурины гипоксантин и гуанин не встраиваются в нуклеотиды. У людей с синдромом Леша-Нюхана аномально высокое содержание мочевой кислоты, а кристаллы урата натрия могут ненормально накапливаться в суставах и почках.
Синдром Леша-Нихена наследуется как Х-сцепленное рецессивное генетическое заболевание, которое, за редким исключением женщин, чаще всего поражает мужчин. Симптомы синдрома Леша-Нихана включают в себя нарушение функции почек, острый подагрический артрит и самоуничижительное поведение, такое как прикус губ и пальцев и/или удары головой.
Признаки и симптомы
Симптомы синдрома Леша-Нихана могут проявиться уже в возрасте 6 месяцев. Более раннее образование кристаллов урата в результате аномально повышенного уровня мочевой кислоты в моче приводит к наличию отложений оранжевого цвета («оранжевый песок») в подгузниках у детей с этим расстройством. Это может быть первым проявлением синдрома Леша-Нихана, но оно редко распознается в раннем детстве.
В результате чрезмерного количества мочевой кислоты, которая выделяется в виде урата натрия в почках младенцев с синдромом Леша-Нихена могут развиваться мочевые конкременты (камни). Эти камни могут вызвать появление крови в моче (гематурию) и увеличить риск инфекций мочевыводящих путей. Кристаллы урата также могут быть обнаружены в суставах, но, как правило, только в позднем подростковом возрасте или во взрослом возрасте нелеченные пациенты с синдромом Леша-Нихана испытывают повторяющиеся эпизоды боли и отека суставов, как у взрослых с подагрой. Эти эпизоды могут становиться все более частыми после их начала.
У детей старшего возраста с этим заболеванием отложения урата натрия могут накапливаться в хрящевых тканях суставов и ушей; в ушах они образуют видимые «выпуклости», называемые тофус. Этот симптом также широко известен как подагрический тофус.
Неврологические симптомы, связанные с синдромом Леша-Нихена, обычно начинаются в возрасте до 12 месяцев. Они могут включать в себя непроизвольные извивающиеся движения рук и ног (дистонию) и бесцельные повторяющиеся движения (хорею), такие как сгибание пальцев, подъем и опускание плеч и/или корченье гримас на лице. Младенцы, которые раньше могли сидеть прямо, обычно теряют эту способность. Первоначально мышцы могут быть мягкими и приводить к затруднению удержания головы в вертикальном положении. Пострадавшие дети могут не достичь вех в развитии, таких как ползание, сидение или ходьба (т.е. испытывают задержки в развитии). В конце концов, большинство детей с синдромом Леша-Нихана испытывают аномально повышенный мышечный тонус (гипертонию) и ригидность мышц (спастичность). Глубокие сухожильные рефлексы повышены (гиперрефлексия). Интеллектуальная инвалидность также может возникнуть и обычно умеренная. Однако точная оценка интеллекта может быть затруднена из-за плохо сформулированной речи (дизартрии). У некоторых пациентов нормальный интеллект.
Самая поразительная особенность синдрома Леша-Нихана, которая наблюдается примерно у 85 процентов пациентов, — это самоповреждение. Такое поведение чаще всего начинается в возрасте от двух до трех лет. Тем не менее, они также могут развиваться в течение первого года жизни или значительно позже в детстве. Самоповреждение может включать в себя повторяющиеся прикусы губ, пальцев и/или рук и повторяющиеся удары головой о твердые предметы. Некоторые дети могут поцарапать свое лицо несколько раз. Тем не менее, люди с синдромом Леша-Нихана не чувствительны к боли. Дополнительные поведенческие нарушения включают агрессивность, рвоту и плевки. Регулярное самоповреждение приводит к потере тканей.
Дети с синдромом Леша-Нихена могут испытывать затруднения при глотании (дисфагию) и могут испытывать трудности при кормлении. Рвота встречается часто, и большинство пораженных детей имеют недостаточный вес для своего возраста. Дополнительные симптомы могут включать раздражительность или крик. У некоторых детей с синдромом Леша-Нихана также может развиться редкая анемия, известная как пернициозная анемия.
Другим симптомом синдрома Леша-Нихана может быть тяжелый мышечный спазм, который вызывает сильное сгибание спины и наклон головы и пятки назад (опистотонус). Пострадавшие дети могут также испытывать вывих бедра, переломы, ненормальное искривление позвоночника (сколиоз) и/или постоянную фиксацию нескольких суставов в согнутом положении (контрактуры).
Женщины-носители обычно не имеют симптомов расстройства, но могут развить подагру в более позднем возрасте в результате нелеченного избытка мочевой кислоты в крови (гиперурикемии).
Причины
Единственный ген, о котором известно, что он связан с синдромом Леша-Нихана, расположен в Х-хромосоме и называется HPRT1. Нарушения (мутации) в гене HPRT1 приводят к отсутствию или дефициту фермента гипоксантин-гуанин-фосфорибозилтрансферазы (ГГФТ или англ. HPRT) и ненормальному накоплению мочевой кислоты в крови.
Синдром Леша-Нихена наследуется по Х-сцепленной схеме. Х-связанные генетические расстройства — это состояния, вызванные ненормальным геном на Х-хромосоме и проявляющиеся в основном у мужчин. Женщины с ненормальным геном, присутствующим в одной из их Х-хромосом, являются носителями этого расстройства. Женщины-носители обычно не проявляют симптомов, потому что у женщин есть две Х-хромосомы, и только одна несет аномальный ген. У мужчин есть одна Х-хромосома, которая унаследована от матери, и если мужчина унаследует Х-хромосому, которая содержит ненормальный ген, он разовьет болезнь.
Женщины-носители расстройства, связанного с Х, имеют 25% риск с каждой беременностью родить дочь-носительницу, подобную себе, 25% риск родить дочь, не являющуюся носителем, 25% вероятность родить сына, пораженного этой болезнью, и 25% риск иметь незатронутого здорового сына.
Если мужчина с Х-связанным расстройством способен к размножению, он передаст аномальный ген всем своим дочерям, которые будут носительницами. Мужчина не может передать X-связанный ген своим сыновьям, потому что мужчины всегда передают свою Y-хромосому вместо своей X-хромосомы потомству мужского пола.
Затронутые группы населения
Синдром Леша-Нихана — это редкое заболевание, которое поражает в мужчин. Редко женщины могут быть затронуты расстройством. Тем не менее, в большинстве случаев женщины могут быть носительницами гена заболевания, но бессимптомными. Согласно одной из оценок, заболевание встречается примерно у 1 из 380 000 живорожденных.
Близкие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы синдрома Леша-Нихена в том смысле, что может возникнуть самоповрежденческое поведение. Сравнения могут быть полезны для дифференциальной диагностики:
Диагностика
Диагноз синдрома Леша-Нихена может быть подтвержден тщательной клинической оценкой, включающей подробную историю болезни и специальные анализы крови. Дети с этим расстройством имеют аномально высокие концентрации мочевой кислоты в крови. Отсутствие фермента HPRT в клетках любой ткани подтверждает диагноз. Для определения конкретной вызывающей заболевание мутации также доступен молекулярно-генетическое тестирование на ген HPRT1.
Пренатальная диагностика и предимплантационная генетическая диагностика возможны, если у пострадавшего члена семьи была выявлена мутация гена HPRT1, вызывающая заболевание. Пренатальная диагностика также может быть сделана с помощью ферментного анализа.
Стандартные методы лечения
Лечение синдрома Леша-Нихана направлено на конкретные симптомы, которые проявляются у каждого человека. Лечение может потребовать скоординированных усилий команды специалистов. Педиатрам, специалистам по диагностике и лечению скелетных нарушений (ортопедам), физиотерапевтам и другим медицинским работникам может потребоваться систематическое и всестороннее планирование лечения пострадавшего ребенка.
Для контроля избыточного количества мочевой кислоты, связанной с синдромом Леша-Нихана, и контроля симптомов, связанных с избыточным количеством мочевой кислоты используется препарат аллопуринол. Однако это лечение не влияет на неврологические или поведенческие симптомы, связанные с этим расстройством.
При наличии камней в почках их можно лечить экстракорпоральной ударно-волновой литотрипсией (ЭУВЛ). Во время этой процедуры пациент погружается в воду и ударные волны высокой энергии направляются на тело в области почечного камня. Камень распадается на мелкие кусочки, и эти мелкие кусочки выходят с мочой.
Никакое продолжительное лечение или медикаментозная терапия не оказались столь же эффективными для лечения неврологических проблем, связанных с синдромом Леша-Нихана. Баклофен или бензодиазепины были использованы для лечения спастичности. Также и диазепам может быть полезен.
Сообщалось, что люди с синдромом Леша-Нихана извлекают выгоду из методов модификации поведения, разработанных для уменьшения самоповрежденческого поведения, но реальный успех необычен. Детям с синдромом Леша-Нихена обычно требуется физическая сдержанность в области бедер, груди и локтей, чтобы они не травмировали себя. Подлокотники удерживают руки свободными. Укус пальцев и/или губ, который может привести к необратимому извращению, может быть предотвращен путем использования защитного средства для рта (орального протезирования) или удаления зубов. Многие пострадавшие люди сами требуют ограничений. По мере взросления самоповрежденческое поведение некоторых пострадавших может улучшиться или прекратиться.
У некоторых пациентов для лечения поведенческих нарушений, связанных с синдромом Леша-Нихана использовались лекарства. К ним относятся Апилепсин, Депакин, Орфирил, Конвулекс, Энкорат (Вальпроевая кислота), Габапентин, Баклофен и Карбамазепин. Бензодиазепины также могут быть полезны при лечении симптомов тревоги, иногда связанных с синдромом Леша-Нихана.
Прогноз
Пациенты могут умереть от аспирационной пневмонии или осложнений от хронического нефролитиаза и почечной недостаточности. При оптимальном уходе немногие пациенты живут за 40 лет, и большинство из них ограничены инвалидной коляской.
Высшее образование (Кардиология). Врач-кардиолог, терапевт, врач функциональной диагностики. Хорошо разбираюсь в диагностике и терапии заболеваний дыхательной системы, желудочно-кишечного тракта и сердечно-сосудистой системы. Закончила академию (очно), за плечами большой опыт работ.
Специальность: Кардиолог, Терапевт, Врач функциональной диагностики.
Синдром Леша-Нихана
Синдром Леша-Нихана — это наследственное заболевание, которое возникает при нарушении обмена пуринов, избыточном накоплении мочевой кислоты в организме. Развивается вследствие генетической мутации, вызывающей дефицит фермента ГФРТ. Проявляется приступами подагры, тяжелым неврологическим дефицитом, самоповреждающим поведением. Диагностика болезни проводится путем биохимических анализов, генетического исследования, методов нейровизуализации. Лечение синдрома симптоматическое: подбор диеты, противоподагрические средства, психотропные препараты и комплексная нейрореабилитация.
МКБ-10
Общие сведения
Синдром назван в честь американского педиатра и генетика Вильяма Нихана и его студента Майкла Леша, которые в 1964 г. первыми описали типичную клиническую картину у двух братьев с подагрой, поражением ЦНС, самоагрессией. С учетом особенностей транскрипции в русскоязычных источниках встречаются вариации названия «синдром Леша-Нихена», «Леша-Найхана». Заболевание регистрируется с частотой 1 случай на 235-380 тыс. населения, болеют преимущественно мужчины. Несмотря на редкость, проблема актуальна в современной генетике, что связано со сложностями ее диагностики, затруднениями в подборе терапии.
Причины
Заболевание возникает вследствие мутаций гена HPRT1, который отвечает за образование фермента гипоксантин-гуанинфосфорибозилтрансферазы (ГФРТ). Описано более 400 вариантов дефектов генетического кода, вызывающих болезнь Леша-Нихана. Мутация расположена на Х-хромосоме в локусе Xq26.2-q26.3. Наследование синдрома происходит по Х-сцепленному типу, поэтому практически все пациенты – представители мужского пола, а женщины в основном являются бессимптомными носителями гена.
Патогенез
Главную роль в патогенезе болезни играет повышенное образование мочевой кислоты. Она синтезируется из гуанина и гипоксантина, которые накапливаются внутри клеток вследствие дефицита ГФРТ, а затем подвергаются биохимическим превращением под действием фермента ксантиноксидазы. Ведущим в развитии синдрома является усиленное образование новых пуринов, что в сочетании с нарушениями реутилизации существующих пуриновых соединений утяжеляет состояние больного.
Механизм появления неврологических нарушений при болезни Леша-Нихана пока не раскрыт. Экспериментальные исследования позволяют предположить поражение ЦНС из-за нарушений обмена нейромедиаторов — дофамина, серотонина, аденозина. Особенно важное значение в патогенезе синдрома играет поражение базальных мозговых ганглиев, где расположено большое число дофаминергических нейронов.
Симптомы
В практике условно выделяют 3 формы синдрома соответственно степени остаточной активности энзима ГФРТ. При показателе меньше 1,5% развивается полный спектр расстройств, включающий тяжелые нарушения пуринового обмена и неврологические симптомы. Значение 1,5-8% соответствует менее интенсивным неврологическим проявлениям, а при уровне ГФРТ больше 8% преобладают расстройства обмена мочевой кислоты при нормальном функционировании ЦНС.
Первые признаки синдрома Леша-Нихана появляются у 3-6 месячных младенцев. Наблюдается снижение мышечного тонуса, вялые движения руками и ногами, задержка психомоторных навыков (улыбка, фиксация взгляда, удерживание головы). Во втором полугодии жизни младенца начинаются непроизвольные движения конечностями, головой, туловищем. После 1 года формируется выраженный гиперкинез с сопутствующей мышечной гипотонией.
Двигательные расстройства неуклонно прогрессируют. При попытке ребенка научиться сидеть или стоять зачастую отмечается дугообразное прогибание туловища и шеи, которому сопутствует тремор. Внешне такие симптомы напоминают судорожный припадок. При тяжелом дефиците ГФРТ больные утрачивают способности к целенаправленным движениям, самостоятельному передвижению. Клиническая картина сходна с симптоматикой ДЦП.
Синдром обязательно сопровождается аутоагрессивным поведением, когда пациент наносит травмы самому себе. Обычно это проявляется в виде постоянного прикусывания губ, кусания собственных пальцев, попыток травмировать глаза. Изредка агрессия проецируется на других людей: больные пытаются ударить окружающих, употребляют нецензурные выражения в речи.
Неотъемлемой составляющей клинической картины является гиперурикемия и гиперурикозурия. У детей раннего возраста родители могут замечать желтый осадок на памперсах, который представляет собой кристаллы мочевой кислоты. Для синдрома Леша-Нихана характерны развитие уратной нефропатии, случаются эпизоды микро- или макрогематурии. В тяжелых случаях возникает нефролитиаз, острая почечная недостаточность.
Осложнения
У всех больных с синдромом Леша-Нихана есть интеллектуальные нарушения по типу легкой или среднетяжелой умственной отсталости. Самой главной проблемой является дефицит внимания, вследствие чего такие дети крайне сложно обучаются. Вследствие тяжелых нарушений двигательных функций происходит ранняя инвалидизация пациентов, они большую часть времени пребывают на специальных колясках с фиксацией.
В редких случаях патология осложняется гастроэзофагеальным рефлюксом и частой рвотой, что затрудняет кормление. Также при болезни Леши-Нихана возможно появление мегалобластной или микроцитарной анемии. У некоторых больных бывают врожденные пороки развития: деформация ушных раковин, атрезия ануса, отсутствие яичек. Иногда возникают приступы апноэ, которые могут быть ассоциированы с синдромом внезапной смерти.
Диагностика
Первичное обследование проводится у детского невролога или педиатра, после чего назначается консультация генетика. Заподозрить болезнь удается по признакам гиперурикемии, которая сочетается с эпизодами аутоагрессии, задержкой психомоторного развития, гиперкинезами. Для подтверждения диагноза синдрома Леша-Нихана применяются следующие методы диагностики:
Лечение синдрома Леша-Нихана
Поддерживающая терапия начинается со специальной диеты для ограничения поступления пуринов в организм. Из рациона исключаются мясные и рыбные бульоны, копчености, консервы, также пациентам запрещено давать шоколад, кофе, соленые сыры. Основу питания составляют овощи, молочные продукты, правильный питьевой режим (отвары сухофруктов, щелочные минеральные воды). Медикаментозная терапия синдрома Леша-Нихана включает:
Большое значение при синдроме Леша-Нихана имеет правильный уход. Дома нужно создать безопасную обстановку, покрыть мягкими материалами острые углы в зоне доступности ребенка, убрать травмоопасные предметы. При двигательных нарушениях используется специальное инвалидное кресло с широкими ремнями-фиксаторами, чтобы оградить больного от самоповреждения. Для защиты губ и языка от прикусывания на зубы надеваются специальные пластины.
Поскольку у многих пациентов с болезнью Нихана сохраняется речевое развитие и способность к запоминанию, возможно обучение таких детей. Учитывая выраженный дефицит внимания, требуются занятия по специальной программе с коррекционными педагогами. Реабилитация дополняется программами ЛФК, массажем для коррекции гипертонуса, физиотерапевтическими методиками.
Прогноз и профилактика
Синдром Леша-Нихана относится к неизлечимым заболеваниям, поэтому прогноз относительно неблагоприятный. Продолжительность жизни коррелирует с уровнем ГФРТ: пациенты с содержанием фермента менее 1,5% и развернутой клинической картиной зачастую погибают в возрасте 20-30 лет. При более высоком содержании энзима больные живут дольше. Профилактика синдрома заключается в медико-генетическом консультировании семей с отягощенной наследственностью.
Синдром Леша–Нихана
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Наследственное заболевание, характеризующееся метаболическими расстройствами, в основе которого лежит избыточное образование мочевой кислоты, расстройствами нервно-психических функций, напоминающими по симптоматике ДЦП, аномалиями поведения, проявляющимися в склонности к самоповреждениям и навязчивой агрессивности в сочетании с умственной отсталостью получила название синдрома Леша–Нихана.
Это не слишком распространенное заболевание привлекало к себе внимание издавна, его первое описание относят к середине XIII столетия. И только в 1964 году студент-медик М.Леш и его преподаватель У. Нихан, описав это заболевание как самостоятельное, увековечили свои фамилии в его названии. А спустя три года группа ученых установила, что его вызывает отсутствие ферментативной активности катализатора метаболизма пуринов.

Код по МКБ-10
Эпидемиология
Эпидемиология данного заболевания в классической форме оценивается как один случай из 200 – 380 тысяч популяции. Частота вариаций синдрома неизвестна. Практически все эпизоды зарегистрированы у мужчин, редкостные эпизоды синдрома среди женщин поясняют неслучайной инактивацией Х-хромосомы. В настоящее время известны более 600 случаев мутации гена ГФРТ.

Причины синдрома Леша–Нихана
Это заболевание определяется патологией обменного процесса пуриновых нуклеотидов, вызванной наследственным ферментативным недостатком ГФРТ (второй фосфорибозилтрансферазы), катализирующей вторичное превращение гуанина и гипоксантина в соответственные мононуклеотиды.
Ген ГФРТ раположен на длинном плече Х-хромосомы, передается мужчинам последующих поколений от матери, т.е. факторы риска – эпизоды данного синдрома в предшествующих поколениях.
Отсутствие гипоксантин-гуанин фосфорибозилтрансферазы – главный момент патогенеза этого заболевания. В таких условиях происходит разложение пуринов и выделение их в форме мочевой кислоты. Организм включает компенсаторный механизм, ускоряющий синтез пуриновых оснований, чтобы восполнить потери от их разрушения. Скорость биосинтеза пуринов превосходит скорость процесса их разрушения, что является основной причиной перепроизводства мочевой кислоты и приводит к перенасыщению плазмы крови уратами натрия.
В результате они кристаллизуются в разных органах и тканях организма с формированием тофусов (подагрических образований). Кристаллы мочевой кислоты, оказываясь в суставах, вызывают воспаление и подагрический артрит.
Почки также реагируют на гиперурикемию ускорением экскреции мочевой кислоты, что может привести к образованию уратных образований. Это может быть не только песок, а и камни, способные перекрыть выведение мочи и спровоцировать гематурию и инфицирование мочевыделительной системы.

Патогенез
В части патогенеза нарушений нервной системы и поведения при синдроме Леша-Нихана еще немало вопросов. Химические и визуализационные изучения нейропроцессов свидетельствуют: у больных наблюдаются значительные уменьшения (до 90%) уровня дофамина в базальных ядрах – связующем звене между участками коры головного мозга, отвечающими за ассоциативное мышление и координацию движений. Этим можно пояснить возникновение двигательных расстройств и поведенческих отклонений.
Биохимические процессы, возникающие в результате отсутствия гипоксантин-гуанин фосфорибозилтрансферазы и влияющие на базальные ядра и, в частности, на дофамин, пока не выяснены. Из-за ферментативного дефицита в спинномозговой жидкости концентрируется не мочевая кислота, а, гипоксантин. Кислота же в тканях мозга не синтезируется и не попадает сквозь гематоэнцефалический барьер. Аномалии поведения, по-видимому, не вызваны перенасыщением плазмы крови уратами натрия или концентрацией гипоксантина. Тут имеют место иные обстоятельства, так как частичная потеря активности фермента вызывает только подагру, а развитие синдрома Леша-Нихана происходит при абсолютном отсутствии ферментативной активности ГФРТ.

Симптомы синдрома Леша–Нихана
У значительной части больных уже в первый год жизни обнаруживаются расстройства моторики, от 0,5 до 1,5 лет у них становятся заметными нескоординированные непроизвольные движения, характерные для экстрапирамидных нарушений. Опираясь на клиническую картину, малышам нередко ошибочно диагностируют детский церебральный паралич.
Небольшое количество больных с данной патологией имеют симптоматику, указывающую на повышенное вырабатывание мочевой кислоты. Мамы малышей могут видеть в пеленках «оранжевый песок», то есть выпадение в осадок солей мочевой кислоты (кристаллурия) либо эритроциты в моче (микрогематурия). Первые признаки данного синдрома могут выражаться полной или частичной дисфункцией почек или гематурией из-за образования камней в мочевыводящей системе.
В младенческом возрасте агрессия к самому себе почти не наблюдается, однако, с возрастом этот симптом характерен для всех пациентов. По наличию самоагрессии в сочетании с интеллектуальной отсталостью и гиперурикемией и ставят диагноз данного заболевания.
Внешние симптомы, позволяющие диагностировать эту генетическую патологию, классифицируются в следующие группы:
Начальная стадия заболевания характеризуется психомоторной отсталостью, впоследствии добавляются мышечный гипертонус и комбинация гиперкинеза и гипокинеза. С появлением зубов становится выраженной склонность к самоповреждениям. Аутоагрессия проявляется в обкусывании губ, ногтей, пальцев, расцарапывании кожи лица до крови. Болевой порог не снижен, поэтому членовредительство сопровождается воплями, вызванными болью. Больные на этой стадии агрессивны не только к себе, но и к окружающим людям, животным, вещам.
Клинические виды синдрома Леша-Нихана классифицируют по степени активности гипоксантин-гуанин фосфорибозилтрансферазы. Классический вид заболевания наблюдается при отсутствии ферментативной активности ГФРТ.
При ее частичном дефиците (1,5-2% нормы), преобладает симптоматика со стороны центральной нервной системы.
Если недостаточность превышает 8% нормы, то умственные способности практически без отклонений, но этот вид сопровождается тяжелыми проявлениями подагры.
Аутоагрессия для стертых вариантов заболевания не характерна, но иногда у больных наблюдается небольшая дистония.
Осложнения и последствия
Последствия и осложнения синдрома в классическом виде связаны с множеством психологических и неврологических проблем, пациенты лишены возможности самостоятельно передвигаться, не могут заниматься самообслуживанием, чаще всего находятся в психиатрических стационарах. Физическое состояние неудовлетворительное (подагра, камни в почках), продолжительность жизни низкая.

Диагностика синдрома Леша–Нихана
Диагностируется заболевание по клинической триаде: гиперурикемия, расстройства нервной системы; умственная отсталость в комплексе с аномальным поведением. Для установления диагноза требуются консультации невролога, ревматолога, генетика.
Обследуется соответствие физического развития возрасту больного. Для синдрома характерно отставание в росте, половом развитии, которое может вообще не наступить. Обычно при проверке физического состояния обнаруживаются следы травм у большей части больных – шрамы, рубцы, ампутации частей губ, языка, пальцев. Больные демонстрируют навязчивое нерациональное поведение, переходящее в агрессию к неживым предметам и к другим людям.
Наблюдаются нарушения интеллекта (IQ≈60), неврологических функций – при нормальной чувствительности заметны расстройства координации, нейроциркуляторная дистония, судорожные сокращения мышц, хореоатетические движения. Степень тяжести расстройств нервной системы лишает больных возможности самостоятельно передвигаться.
Больным в рамках диагностических мероприятий назначаются клинические анализы мочи и крови, биохимия крови – для установления уровня мочевой кислоты. Основная инструментальная диагностика – исследование почек ультразвуком.
Диагностика синдрома на ранней стадии представляет затруднения, потому что все три особенности еще не проявились. Заподозрить его наличие можно, заметив физическую и интеллектуальную отсталость, которая сопровождается гиперпродукцией мочевой кислоты, приводящей к нефролитиазу или гематурии. Позже, когда прорезываются зубы, самотравмирование больного может натолкнуть на мысль о синдроме Лёша-Нихена. Но поскольку аутоагрессия характерна и для других психических патологий, приходит очередь дифференциальной диагностики.

Дифференциальная диагностика
От других синдромов, для которых характерны нанесения самому себе травм, эту патологию отличают локализации ранений – искусанные пальцы, губы, слизистая оболочка полости рта. Факты самоповреждений обязательно сопровождаются гиперурикемией и расстройствами нервной системы, сходными по клинике с детским церебральным параличом. Дифференциальная диагностика позволяет по совокупности симптомов достаточно точно отличить синдром Леша-Нихена от других заболеваний.
Решающую точку в диагностических мероприятиях ставит генетическое исследование – установление уровня ГФРТ и распознавание мутаций его гена.
К кому обратиться?
Лечение синдрома Леша–Нихана
Больных с классической формой заболевания рекомендуется помещать в стационар. При лечении данного заболевания основное внимание уделяется нормализации синтеза мочевой кислоты с целью предотвращения негативных последствий со стороны мочеполовой системы и воспалительных процессов в суставах. При этом применяются медикаментозные препараты, замедляющие процесс перепроизводства мочевой кислоты, и компенсируют потери жидкости, особенно в периоды ее интенсивной потери, например, при часто повторяющейся рвоте.
При гиперурикозурии камни удаляют медикаментозно или с помощью хирургического вмешательства. При подагрическом артрите применяют нестероидные противовоспалительные средства.
Лекарственное лечение обязательно сочетают с соблюдением беспуриновой диеты, при этом больные должны пить как можно больше чистой воды. Как дополнительный фактор может использоваться только растительное питание, которое способствует подщелачиванию мочи и растворению кристаллов мочевой кислоты.
Для снижения уровня мочевой кислоты и, как следствие, уменьшения воспалительных процессов в подагрических узлах и отложения солей, заметный эффект дает терапия Аллопуринолом. Это лекарство, расстраивающее процесс перепроизводства мочевой кислоты. Уростатический эффект достигается благодаря его способности ингибировать ферментативную активность ксантиноксидазы – катализатора реакции окисления гипоксантина. Препятствуя выработке мочевой кислоты, Аллопуринол уменьшает ее содержание в крови и содействует растворению ее солей. Длительность и схему лечения назначает врач в зависимости от уровня содержания мочевой кислоты.
Среднесуточная дозировка Аллопуринола от 100 до 300мг, ее можно принимать одноразово. Рекомендованная начальная дозировка 100мг/сутки, ее корректировку производят не чаще одного раза в неделю по необходимости. Суточная дозировка, поддерживающая уровень мочевой кислоты, в среднем от 200мг до 600мг, при лечении высокими дозировками – от 600мг до 800мг. Когда дозировка более 300мг/сутки, препарат принимают равными частями (один прием не превышает 300мг).
Корректировка дозирования в сторону увеличения предполагает контроль за уровнем оксипуринола в плазме крови (основного метаболита Аллопуринола).
Детям от 15 лет в сутки назначают препарат из расчета 10-20мг на 1кг веса (разделить на три приема). Наибольшая детская дозировка – 400мг/сутки.
Аллопуринол не назначают при тяжелых патологиях почек и печени, аллергиях, в период обострения подагры, с осторожностью – при болезнях сердца и гипертензии.
Этот препарат, в основном, не вызывает побочных действий, однако их исключать нельзя со стороны любых органов и систем организма.
Как альтернативу Аллопуринолу (при его непереносимости) назначают Пробенецид, препятствующий обратному поглощению мочевой кислоты, что увеличивает ее экскрецию.
В случаях хронического течения подагры к терапии Пробенецидом приступают с дозировки по 250мг дважды в день на протяжении месяца. Спустя неделю после начала лечения дозировку можно увеличить до 500мг дважды в день. Наибольшая дозировка 2000мг/сутки. При условии, что в течение ½ года приема Пробенецида у больного не случилось обострения подагры, а также, содержание мочевой кислоты в плазме крови не более допустимого уровня, дозировку снижают каждые полгода на 500мг до наименьшей действующей. Пробенецид назначают детям с двух лет, терапию начинают с дозировки 25мг/кг веса с увеличением до 40мг/кг, принимают с перерывами не менее 6 часов.
Необходимо учитывать, что действие Пробенецида, приводящее к высвобождению мочевой кислоты, может вызвать подагрический пароксизм. Также этот препарат препятствует экскреции с мочой некоторых лекарств, например, антибиотиков, НПВС, производных сульфонилмочевины, увеличивая их накопление в плазме крови.
Пробенецид не назначают при подагрических пароксизмах; камнях, особенно уратных; порфирии; патологии кроветворения; в возрасте до двух лет; вторичной гиперурикемии в результате новообразований либо химиотерапии; аллергии.
Больным с почечнокаменной болезнью, нужно поддерживать большой объем мочи с нейтральным уровнем кислотности. В этом случае применяют сбалансированные смеси солей, например, Polycitra.
Значимость нейтрального уровня кислотности мочи доказывается тем, что при кислой моче (например, рН≈5,0) способность мочевой кислоты растворяться составляет 0,15г/л, а при нейтральном – 2г/л.
Гиперурикемию обязательно нужно корректировать, поскольку при приеме Пробенецида корректировка не происходит, но перепроизводство мочевой кислоты хорошо тормозится Аллопуринолом.
Неврологические нарушения лечат, опираясь на симптоматику, например, алпразолам, баклофен или диазепам могут снизить проявления беспокойства, устранить судороги, уменьшить расстройства двигательной функции.
Алпразолам – психотропное средство, оказывающее умеренный снотворный эффект, снимающее проявления депрессии, обладающее легким противосудорожным действием.
У больных, принимающих этот препарат, наблюдается снижение тревожности и чувства страха, а также стабилизация эмоционального состояния.
Воздействие Алпразолама на сердечно-сосудистую и дыхательную системы у пациентов без данных патологий не наблюдается.
Лечение взрослых больных начинают с дозировки 0,1-0,2мг два или три раза в день. По истечении недели с момента начала терапии дозировку при необходимости начинают повышать с вечернего приема. Средняя суточная дозировка – от 3-х до 6мг, наибольшая – 10мг.
Длительность лечения в острых случаях – от трех до пяти дней, максимально можно принимать не более трех месяцев.
Для отмены препарата дозировку снижают каждые три дня на 0,5 мг, поскольку резкое прекращение лечения приводит к формированию синдрома отмены. В начале лечения наблюдается сонливость, вялость, упадок сил, снижение концентрации внимания и психомоторики и другие негативные реакции. Препарат не назначается в случаях непереносимости лактозы, с дисфункциями органов дыхания, печени и почек.
Диазепам – транквилизатор бензодиазепинового ряда, способствует мышечной релаксации, снимает судорожную готовность, оказывает выраженное успокаивающее действие, усиливает действие γ-аминомасляной кислоты, реализовывающей функцию медиатора торможения ЦНС.
Диазепам увеличивает стабильность тканей нервной системы при кислородном голодании, тем самым повышая болевой порог, угнетает вегетативные приступы.
Оказывает зависимое от принятой дозировки воздействие на ЦНС: до 15мг в сутки стимулирующее, более 15мг – гипноседативное.
Вследствие приема препарата у больных уменьшается тревожность, чувство страха, эмоциональное напряжение. Изредка наблюдается снижение аффектации.
Как психотропный препарат применяют от 2,5 до 10мг два, три или четыре раза в день. В психиатрии при дисфорических состояниях дозируют от 5 до 10мг два – три раза в день. Если есть необходимость, суточную дозировку поэтапно увеличивают до максимума (60мг).
В педиатрии при лечении реактивных и психосоматических нарушений, а также спастических состояниях детям до 3-х лет рекомендуют парентеральное введение (дозируют индивидуально), старше 3-х лет – перорально с 2,5мг в сутки. В случаях необходимости дозировку поэтапно увеличивают, при этом состояние ребенка контролируется медперсоналом.
Диазепам в большинстве случаев переносится хорошо, но при лечении нужно учитывать вероятность нежелательных последствий его употребления как упадок сил, спутанное сознание, сонливость, эмоциональные, зрительные, двигательные, речевые расстройства. Препарат может вызывать привыкание.
Диазепам не рекомедуется принимать лицам, склонным к суициду, при патологической мышечной утомляемости, с эпилепсией. Не применяется при нарушениях внешнего дыхания, глаукоме, атаксии, порфирии,
сердечной недостаточности.
С аномалиями поведения, главным образом, с самоагрессией, справиться труднее всего, наиболее эффективно действуют комплексные методики, включающие поведенческую и лекарственную терапии. Применяют габапентин и бензодиазепины, при наиболее тяжелых вариантах можно применить нейролептики, их используют для снятия обострения.
В комплексной терапии обязательно присутствуют витамины и микроэлементы, при гиперурикемии назначают витамины группы В, витамин С, калий, нейропротекторы – витамин А, D, фолиевая кислота, биотин.
Практически во всех случаях генетических патологий в комплексе лечебных мероприятий применяется физиотерапевтическое лечение. При синдроме Леша-Нихана применяются очень разнообразные физиотерапевтические методы лечения – электросон, гальванизация, массажи, хвойные ванны. С целью предупреждения подагрических приступов рекомендована физиобальнеотерапия, в особенности, хороший урикозурический эффект оказывают радоновые ванны. Для снятия воспаления используются грязевые аппликации, а также парафино-озокеритолечение.
Для выведения мочевой кислоты и профилактики образования камней рекомендуется приём внутрь слабоминерализованных минеральных вод, имеющих щелочные значения pH.
В общий комплекс лечения включается и лечебная гимнастика.
Народное лечение
В дополнение к медикаментозной, физиологической и психологической терапии можно, посоветовавшись с лечащим врачом, применить народные средства и воспользоваться некоторыми советами:
В диетическом питании молибден и медь предпочтительно употреблять вместе, они словно созданы друг для друга. Медью богаты – орехи, ржаной хлеб, простокваша, желтки яиц (сырые), листья шпината и салата, спаржа, петрушка, картофель.
В народной медицине применяются различные не очень сложные отвары и настои, удаляющие отложение солей.
Например, отвар из сельдерея и петрушки: взять по 100г стеблей с листьями и корнями данных растений на пол-литра воды, прокипятить смесь не менее пяти минут, отставить на полчаса, потом процедить и отжать; добавить сок одного лимона и две столовые ложки меда; выпить все в течение дня.
Продолжительность лечения – один месяц, повторить с интервалом в одну неделю.
Или отвар из стручков фасоли: хорошо измельченные сухие стручки (одну столовую ложку) заварить одним литром кипятка и два часа кипятить на водяной бане. Процедить и пить по одной столовой ложке трижды в сутки.
Яблоки есть в продаже круглый год. Три крупных или пять более мелких яблок нарезать ломтиками (кожуру не счищать). Залить водой, кипятить четверть часа под крышкой. Отвар должен настояться 4 часа, его нужно выпить маленькими порциями в течение суток.
Ванночки из трав: 200г цветов ромашки, календулы или шалфея заварить 1,5л кипятка, настоять не менее двух часов, процедить и добавить в ванну для ног с температурой 34ºС, снизить температуру до 26ºС, опустить ноги и принимать ванну 20 минут. Процедуры хорошо проводить перед сном, рекомендованная длительность курса 20 дней, спустя 20 дней курс процедур повторить.
Очищение от солей для ленивых. Купить 1кг меда и изюма. Утром натощак съесть горсть изюма и два часа больше ничего не пить и не есть. На следующий день с утра натощак съесть одну столовую ложку меда и два часа больше ничего не пить и не есть. И так – каждый день, пока мед с изюмом, не закончатся.
Только лечение травами, конечно, не сможет победить такой серьезный генетический дефект как синдром Леша-Нихана. И не всякая трава может сочетаться с комплексом медикаментов, поэтому консультация врача перед применением обязательна

Гомеопатия
Часть медицинской науки, как и современная традиционная медицина, а не один из видов народной медицины, гомеопатия подчиняется определенным принципам лечения.
Врач-гомеопат, как и любой другой, должен выяснить, что происходит с пациентом и назначить лечение. Обследование делается традиционным путем – сбор анамнеза, осмотр и оценка результатов диагностических процедур. Эти данные сравниваются с лекарственным патогенезом – чем больше сходства патогенеза препарата с данными диагностики, тем больший эффект может оказать избранный препарат.
Назначение гомеопатического препарата происходит, исходя из суммы патологических проявлений с их индивидуальным течением в совокупности с конституцией, учитывая образ жизни и наследственность пациента. Врач-гомеопат должен определить индивидуальный препарат для конкретного организма.
Правильно подобранный гомеопатический препарат помогает существенно улучшить состояние здоровья и избавиться хронических болезней. Терапевтический эффект от лечения гомеопатией наступает, как правило, в интервале от трех месяцев до двух лет.
В гомеопатии есть препараты для состояний, описание которых сходно синдромом Леша-Нихана. Наиболее подходящий препарат Литиум карбоникум (Lithium carbonicum ):
Карбонат лития попал в гомеопатическую аптеку, как противоподагрический. Соли лития превращают соли мочевой кислоты в растворимые, затем они экскретируются из организма. У больного деформированные суставы с подагрическими узлами, болезненные, отекшие, чувствительные к прикосновениям. Во всех суставах, в особенности, коленных и мелких на пальцах ног, ощущается скованность почти паралитическая. Артрит, острый и хронический.
Также препарат применяется при мочекаменной болезни (оксолаты и ураты). Калькулезные колики, частая боль в зоне сердца, особенно по утрам. Проходит после посещения туалета. В симптоматике указывается головная боль, снижение остроты и четкости зрения, быстрое утомление глаз.
В зависимости от симптоматики можно подобрать и другие препараты, например:
Дозировки и схемы лечения назначаются только индивидуально, рекомендованных доз препарата, как в традиционной медицине, в классической гомеопатии нет.
Оперативное лечение
Хирургические операции производятся таким больным по поводу мочекаменной болезни в случаях неэффективного терапевтического лечения. Показаниями к операции служат: прекращение поступления мочи в мочевой пузырь из-за закупорки мочеточника камнем, септицемия, вызванная калькулезным пиелонефритом; частые пароксизмы почечной колики при отсутствии тенденции к самостоятельному выходу камней; гематурия, угрожающая жизни.
Оперативное лечение включает как открытые хирургические вмешательства, так и инструментальные, в том числе дробление камней в мочевом пузыре цистолитотриптором, лазером, ультразвуком, эндоскопом.