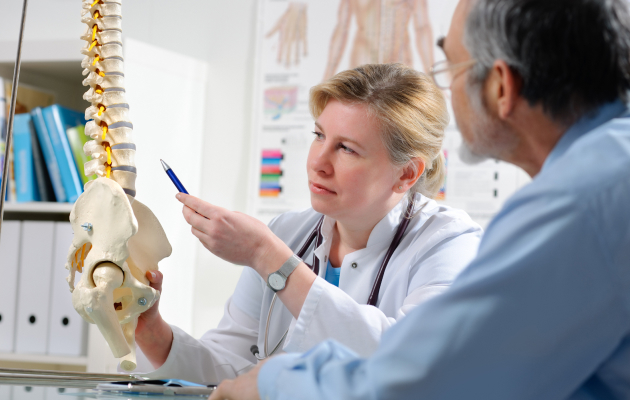
Гипермобильный синдром
Гипермобильность суставов определяется как превышение объема движений в одном или нескольких суставах по сравнению со среднестатистической нормой. И хотя это состояние описано нашим соотечественником А.Черногубовым более 100 лет тому назад и в последние 30 лет интенсивно изучается, вопрос о том, что принимать за среднестатистическую норму объема движений и что относить к гипермобильности, окончательно не разрешен. Это особенно трудно определить у детей, поскольку им свойственна физиологическая гипермобильность ввиду незрелости соединительной ткани.
Критерии гипермобильности суставов.
1. Пассивное сгибание пястно-фалангового сустава 5-го пальца в обе стороны;
2. Пассивное сгибание 1-го пальца в сторону предплечья при сгибании в лучезапястном суставе;
3. Переразгибание локтевого сустава свыше 10о;
4. Переразгибание коленного сустава свыше 10о;
5. Наклон вперед при фиксированных коленных суставах, при этом ладони достигают пола.
Вторичная гиперподвижность суставов может развиться при любом воспалительном процессе с суставной локализацией вследствие ослабления капсулы и связок. Она зафиксирована при некоторых неврологических, эндокринных заболеваниях и т.д.
Олигосимптоматическая форма встречается много чаще и отличается менее выраженной и менее генерализованной симптоматикой. Эта группа включает и гипермобильный синдром.
Т.Милковска-Дмитрова и А.Каракашов рассматривают также отдельные виды врожденной неполноценности соединительной ткани в зависимости от преимущественной локализации в той или иной системе. Ими выделены следующие формы: суставная, глазная, экхимозная, легочная, лаксационная, почечная, сердечно-сосудистая, периодонтальная, пролапс митрального клапана, абдоминальная, сколиозная.
Приводим краткую их характеристику.
Глазные аномалии: голубые склеры, косоглазие, повышенная подвижность глазных яблок, вывих и эктопия хрусталика, гипертелоризм, гипер- и гипометропия, глаукома, гиперэластичность кожи век, эпикант. С возрастом многие из глазных симптомов прогрессируют.
Дыхательная система: трахеобронхомегалия, спонтанный пневмоторакс, эмфизема легких, рецидивирующие бронхопневмонии, обструктивный бронхит.
Желудочно-кишечный тракт: грыжи, дивертикулез желудка и кишечника, увеличение отдельных его отделов, птоз внутренних органов, перфорации, кровотечения.
Мочеполовая система: аномалии, поликистоз, дивертикулез мочевого пузыря. Показано сочетание наследственных заболеваний органов мочеполовой системы с множественными признаками дизэмбриогенеза соединительных тканей. Интересно, что при врожденных и наследственных болезнях мочеполовой системы выявлен чаще других HLA-B35 (как генетический маркер). Он же обнаружен М.Ондрашиком у больных с гипермобильностью суставов.
Зубы: аномальное расположение, неправильное формирование, гипоплазия эмали, резорбция десен, выпадение зубов, множественный кариес и пр.
Наблюдаются нервно-вегетативные проявления и психические отклонения.
Т.Милковска-Дмитрова и А.Каракашов предлагают следующие критерии диагностики врожденной неполноценности соединительных тканей. Главные: плоскостопие, расширение вен, готическое нёбо, растягивающиеся суставы, глазные изменения и костно-связочные симптомы (кифоз, сколиоз, гиперлордоз). Второстепенные: аномалии ушных раковин, суставные боли, птеригиум, зубные аномалии, грыжи, гипертелоризм и пр.
Определенное количество главных и второстепенных признаков позволяет установить степень дисплазии соединительной ткани.
Наиболее полно, с нашей точки зрения, признаки дисплазии соединительной ткани и их значимость в баллах представлены Л.Фоминой. В течение последних 5 лет ею обследовано более 1000 детей по единой схеме и с использованием статистических методов. В суммарном виде данные приведены в таблице.
Таблица
Значимость фенотипических признаков, характерных для дисплазии соединительной ткани (ДСТ) в баллах
|
Делаются попытки поисков генетического маркера, что помогло бы в дифференциальной диагностике отдельных форм соединительнотканной недостаточности. По данным того же автора, гипермобильный синдром сочетается с В35-антигеном гистосовместимости (у 47,5 проц. при 18,3 проц. в контроле). Дальнейшие исследования в этом направлении продолжаются.
Итак, врач имеет дело с гетерогенной группой наследственных заболеваний соединительной ткани, основным клиническим признаком которых является повышенная подвижность суставов. Клинико-генетическая гетерогенность создает значительные трудности в ограничении отдельных форм, входящих в эту группу. А происходящие в процессе роста и развития изменения и функциональные расстройства в опорно-двигательном аппарате и других органах и системах у этих детей обеспечивают дополнительные дифференциально-диагностические затруднения, в том числе и в отграничении от различных воспалительных и дегенеративных заболеваний суставов, позвоночника, сердца и т.п. Необходимость в их дифференциальной диагностике представляется весьма актуальной.
Проведенные в клинике артрологии НИИ педиатрии РАМН исследования различных нозологических форм артритов (ревматоидный, реактивный, ювенильный хронический, псориатический, анкилозирующий спондилоартрит и др.) показало особенности суставного синдрома при наличии у ребенка гипермобильного синдрома и прочих признаков ДСТ. Они выражались в следующем: перерастяжение суставной сумки экссудатом с локализацией в различных суставах; образование единичных и множественных бурситов, главным образом в области лучезапястных, голеностопных суставов, а также подколенных кист; частый рецидив суставного выпота; меньшая склонность к формированию контрактур и функциональных нарушений. Возникающая у больных тем или иным артритом на фоне выраженного гипермобильного синдрома инконгруэнтность суставных поверхностей ввиду слабости капсулы и связочного аппарата, а также рецидив воспалений создают предпосылки для формирования раннего артроза. При выявлении у больного с артритом синдрома гипермобильности возникает необходимость назначения дополнительных лечебных мер.
Не менее актуальным является диагностика этого синдрома и ДСТ (в более широком понимании) и при других заболеваниях в плане построения рациональной терапии.
Лечение детей с гипермобильным синдромом проводится дифференцированно в зависимости от степени его выраженности. При слабой степени (на грани с физиологической нормой) отсутствии жалоб лечение не проводится. Этим детям назначают комплекс санитарно-гигиенических мер, применяемых в педиатрии для здоровых с целью предупреждения плоскостопия, нарушений осанки, функции зрения и пр.
При умеренной и особенно же выраженной гипермобильности суставов и других признаков ДСТ помимо общегигиенических проводят меры по устранению уже возникших функциональных и анатомических изменений. Обычно это лечение ортопедического плана, назначаемое для каждого ребенка индивидуально в зависимости от выявленной патологии. У всех детей показано ограничение физической нагрузки, особенно на суставы ног: ношение тяжестей, занятие непосильным физическим трудом, нагрузочными и травмирующими видами спорта, участие в соревнованиях, связанных с перегрузкой суставов и т.д. Возможность занятия тем или иным видом спорта и физкультурой в школе определяется индивидуально врачом в зависимости от состояния суставов, сердца и других органов. Наиболее показанными у этой категории больных являются плавание, лыжи, велосипед, настольный теннис, коньки, танцы. При появлении тех или иных жалоб на фоне занятий спортом они временно прекращаются. При необходимости (сильные боли, признаки воспаления и пр.) показана кратковременная иммобилизация и назначение нестероидных противовоспалительных препаратов в возрастной дозе (бруфен, ортофен, вольтарен и др.). Для устранения болевого синдрома показана физиотерапия: фонофорез с гидрокортизоном, лекарственный электрофорез, импульсная коротковолновая диатермия, амплипульс на соответствующие суставы или паравертебрально. Используют также лечебную физкультуру, гидрокинезотерапию, массаж. С целью предупреждения посттравматического синовита детям запрещают ползать и играть на полу на коленях.
В зависимости от клинических проявлений со стороны опорно-двигательного и (или) других систем дети находятся под наблюдением ревматолога, ортопеда, окулиста, стоматолога и других специалистов.
С возрастом некоторые симптомы исчезают или сглаживаются, другие, наоборот, нарастают или появляются новые. Прогноз различен, он хуже у детей с генерализованной ДСТ и зависит также от развивающихся на этом фоне заболеваний и их течения.
Гипермобильность суставов
Специалисты ЦМРТ более 15 лет специализируются на диагностике и лечении заболеваний суставов. Читайте подробнее на странице Лечение суставов.
Синдром гипермобильности суставов означает патологическую подвижность или нестабильность суставных сочленений. Характеризуется артралгией и миалгией, плоскостопием и вальгусными проявлениями, возможно раннее развитие варикоза. Диагностируют на основании жалоб пациента, осмотра, проведения тестов критериев Бейтона по шкале в 9 баллов. Для исключения похожих заболеваний суставной ткани назначают МРТ обследование.
Рассказывает специалист ЦМРТ
Дата публикации: 14 Сентября 2021 года
Дата проверки: 30 Ноября 2021 года
Содержимое статьи
Причины гипермобильности суставов
Гипермобильность суставов у детей и взрослых развивается по следующим причинам.
Генетическая предрасположенность — наследственное нарушение синтеза коллагена, сопровождающееся признаками дисплазии соединительной ткани. Например, несовершенный остеогенез, синдромы Элерса–Данлоса, Марфана. Практически в каждом клиническом случае врач при сборе семейного анамнеза определяет семейный характер патологии.
Продолжительные физические нагрузки или травмы, приобретенные заболевания ОДА, связанные со спортом, тяжелой физической работой с повтором однообразных движений.
Снижение тонуса мышц вследствие продолжительной болезни, малоподвижного образа жизни (возникает из-за отсутствия физической деятельности или инсульта).
У женщин чаще встречаются все формы гипермобильности, нежели чем у мужчин. Также локальная форма патологии может возникать в период беременности.
Симптомы
Рассмотрим характерные признаки:
Синдром гипермобильности суставов у детей встречается чаще, чем у взрослых. Основные признаки, по которым распознают патологическую гибкость:
Классификация гипермобильности суставов
По принятой в медицине классификации выделяют следующие формы патологии:
Как диагностировать
Среди всех травматических патологии шеи на долю ротационного подвывиха первого шейного позвонка приходится около 30% случаев.
К сожалению, только лишь по тревожащей симптоматике трудно понять, о какой именно патологии идет речь. Кроме того, подвывихи могут сочетаться с разрывом/растяжением связок и мышц, разрывом суставной капсулы, повреждениями сосудов и нервных волокон и т.д.
Для выявления патологической подвижности применяют:
Для выявления сопутствующих патологий, оценки состояния суставной ткани, степени воспалительного процесса используют МРТ исследование — наиболее результативный и предпочтительный метод. При возникновении неприятных симптомов, частой мышечной и суставной боли, иных признаков ГМС необходимо записаться на прием к врачу и пройти обследование в одной из клиник ЦМРТ.
К какому врачу обратиться
Лечением патологического состояния занимается врач-ортопед. В части случаев необходима консультация ревматолога, кардиолога, флеболога. Также потребуется профессиональная помощь мануального терапевта, физиотерапевта и массажиста.
Чем опасна гипермобильность суставов
Артроз и артрит – не единственные проблемы суставов, с которыми сталкиваются люди в пожилом или среднем возрасте. Иногда ортопед озвучивает и другой диагноз – «свободные суставы». Так говорят о ситуации, когда диапазон движений выходит за рамки нормального и приносит человеку определенные неудобства, а порой и серьезные ухудшения здоровья.
Гипермобильность суставов в детстве – это вариант нормы
Всегда ли опасна ли гипермобильность
Более диапазонные, чем необходимо, движения суставов характерны в основном для детей, а с возрастом эта проблема постепенно исчезает. В таких случаях лечение не требуется и осложнений не бывает. Причина – в развитии суставной ткани и росте хрящей. Если же проблема остается с человеком и во взрослом возрасте, это может свидетельствовать о патологии – деформации суставов и изменении структуры сосудов.
Пластика и гибкость в детском возрасте порой зашкаливают! Ниже представлена подборка самых гибких детей в мире:
Какие проблемы могут возникнуть на фоне гипермобильности суставов
Если свободные суставы сопровождаются болевыми ощущениями, это создает предпосылки для вывихов и растяжений. Стабилизирующие связки – слишком слабые и склонные к деформациям, поэтому у таких людей чаще остальных происходят травмы. Еще один симптом синдрома доброкачественной гипермобильности – вторичный остеоартроз коленного сустава, локтевого, плечевого или любого другого.
5 специфических признаков гипермобильности суставов
Эти признаки ортопеды используют для оценки степени гипермобильности пациентов согласно шкале Бейтона. Максимальная оценка – 9 баллов. Если опрос показал 4 балла или больше по отношению к четырем или более суставам, при этом человек жалуется на боль в течение последних нескольких месяцев, ему диагностируют синдром доброкачественной гипермобильности.
К сожалению, аналогичного теста для диагностирования остеоартроза тазобедренного сустава или коленного еще не разработали, поэтому это заболевание со скрытой симптоматикой обнаруживают слишком поздно.
Чтобы определить гипермобильность суставов, ортопеды проводят тест Бейтона
Тактика лечения
Как и в случае с лечением остеоартроза, здесь необходим комплексный подход. Суставы не существуют отдельно от других систем организма, поэтому воздействовать необходимо с разных сторон. Чаще всего терапия включает такие методы:
Гипермобильность суставов – явление неприятное, но зачастую не опасное
Очень редко гипермобильность является следствием серьезного заболевания. К таковым относятся, к примеру, синдром Элерса-Данлоса («гиперэластичность кожи»), синдром Марфана (аутосомно-доминантная патология соединительной ткани наследственного характера).
К счастью, в большинстве случаев гипермобильность не несет потенциальной опасности и не приводит к инвалидности. Поэтому главная задача терапии – устранить болевой синдром и помочь человеку психологически принять этот диагноз. Не менее важно научить пациента беречь себя, чтобы избегать травм, поскольку частые травмирования могут спровоцировать дегенеративные заболевания в суставах, посттравматический артроз и новые проблемы.
Гипермобильный синдром: клинические проявления, дифференциальный диагноз, подходы к терапии
Н.Г. Правдюк, Н.А.Шостак
Кафедра факультетской терапии им. А.И. Нестерова, Российский государственный медицинский университет, Москва Дисплазия соединительной ткани (ДСТ) представляет собой уникальную онтогенетическую аномалию развития организма, которая относится к числу сложных вопросов современной медицины. Рассматриваются основные подходы к дифференциальной диагностике различныхформ ДТС. Ведущее место отводится клинической оценке, подходам к терапии одного из вариантов недифференцированной формы ДТС – гипермобильному синдрому.
Ключевые слова: дисплазия соединительной ткани, гипермобильный синдром, гипермобильность суставов.
РФК 2008;3:70-75
Hypermobility syndrome: clinical manifestations, differential diagnosis, therapy approaches N.A. Shostak, N.G. Pravdyuk
Chair of Faculty Therapy named after A.I. Nesterov, Russian State Medical University, Moscow Connective tissue dysplasia (CTD) represents special ontogenetic abnormality which is a complex problem of contemporary medicine. The principles of differential diagnosis of various forms of CTD are considered. A clinical estimation and therapy approaches are discussed with focus on hypermobility syndrome as one of undifferentiated form of CTD.
Key words: connective tissue dysplasia, hypermobility syndrome, joint hypermobility.
Rational Pharmacother. Card. 2008;3:70-75
Группа наследственных заболеваний соединительной ткани и скелета была впервые выделена американским генетиком Mc Kusick в 1955 году. К тому времени она объединяла лишь некоторые нозологические формы: несовершенный остеогенез, синдром Марфана, синдром Элерса-Данло, эластическую псевдоксантому и гаргоилизм. [1] В течение последующих трех десятилетий благодаря достижениям генетики были описаны и классифицированы свыше 200 заболеваний соединительной ткани и скелета наследственного характера.
Клинические проявления дисплазий соединительной ткани
Дисплазия соединительной ткани (ДСТ) – генетически детерминированное нарушение развития соединительной ткани, приводящее к изменению ее структуры и функций и реализующееся в клиническом многообразии фенотипических признаков и органных проявлений. В настоящее время предложено подразделение ДСТ на дифференцированный и недифференцированный синдромы [2].
Дифференцированные дисплазии характеризуются установленным генным или биохимическим дефектом с определенным типом наследования и клинической картиной заболевания (синдром Марфана, синдром Элерса-Данлоса, несовершенный остеогенез, эластическая псевдоксантома и др.).
Недифференцированные дисплазии соединительной ткани диагностируются в случаях, когда наборфенотипических признаков не соответствует ни одному из дифференцированных синдромов.
Соединительнотканная дисплазия, затрагивая все органы и системы, проявляется комплексом фенотипических признаков. Весьма характерным для ДСТ является генерализованная гипермобильность суставов (ГМС), которая может быть ведущим признаком как недифференцированной ДСТ, так и частью дифференцированных синдромов.
Для объективной оценки генерализованной гипермобильности суставов используются критерии Бейтона [3] (табл. 1).
Таблица 1. Признаки гипермобильности суставов (критерии Бейтона)
Научный и практический интерес к ГМС возник еще в конце 19 века, когда были описаны наследственные синдромы, в клинической картине которых ГМС являлась одним из ведущих симптомов (синдром Марфана, синдром Элерса-Данло, несовершенный остеогенез). Влияние ГМС на состояние здоровья имеет самые разнообразные аспекты. Первое описание ГМС было сделано в 1967 году Kirk, Ansell и Bywaters. [4]. Авторами был предложен термин «гипермобильный синдром» (ГС), отражающий феномен гипермобильности суставов, сочетающийся с дисфункцией опорно-двигательного аппарата (подвывихи, артралгии). Позже стало известно, что ГМС ассоциируется с внешними фенотипическими признаками ДСТ, сходными с маркерами дисплазии при дифференцированных синдромах, а «гипермобильный синдром» стал рассматриваться в рамках нозологической формы. Однако генетическая основа ГС до настоящего времени остается неизвестной.
Клинические проявления ГС многообразны и включают как суставные, так и внесуставные признаки, отраженные в критериях ГС. Диагностические критерии ГС представлены в табл. 2 и именуются Брайтоновскими критериями [5].
Малые критерии ГС были дополнены в ходе работ А.Г. Беленького [6] и включают пролапс митрального клапана, полую стопу, браходактилию, деформацию грудной клетки, сандалевидную щель стопы, сколиоз, Hallux valgus. ГС диагностируется при наличии 2 больших критериев, 1 большого и 2 малых критериев или 4 малых. Достаточно 2 малых критериев, если родственник 1 линии родства имеет признаки ДСТ.
Таблица 2. Диагностические критерии ГС (Brighton, 1998г)
Малые критерии:
Основным клиническим проявлением ГС является поражение опорно-двигательного аппарата в виде артралгий (полиартралгий), ассоциированных с физической нагрузкой. Наиболее часто в процесс вовлекаются коленные и голеностопные суставы. Причиной болевого синдрома в этом случае является чувствительность к нагрузке опорных суставов и умеренные ортопедические аномалии (дисплазия тазобедренных суставов, продольное и поперечное плоскостопие). Дебют артралгий приходится на молодой возраст, преимущественно у лиц женского пола. Подвывихи суставов (в основном, голеностопных и коленных) типичны для пациентов с ГС. Рецидивирующий выпот в суставе, как проявление ГМС, является нечастой, но наиболее сложной диагностической ситуацией. Характерной особенностью синовита при ГМС является непосредственная связь с травмой, невоспалительный характер синовиальной жидкости и быстрое обратное развитие. В последующему этих пациентов может развиться стойкая артралгия травмированного коленного сустава, связанная с постравматической менископатией. Дорсалгии, нередко сочетающиеся со сколиозом и спондилолистезом, встречаются у пациентов с ГС в любом возрасте. Периартикулярные поражения (тендиниты, эпикондилит, другие энтезопатии, бурситы, туннельные синдромы) встречаются у пациентов с ГС и возникают в ответ на необычную (непривычную) нагрузку или минимальную травму. Наиболее полная картина клинических проявлений и потенциальных осложнений ГС (в том числе со стороны опорно-двигательного аппарата) представлена в табл. 3.
Таблица 3. Клинические проявления и потенциальные осложнения ГС [1]
Хронические (нетравматические)
ГМС требует тщательного клинического анализа и дифференцированного диагностического подхода. Немаловажную роль в диагностике ГС играет оценка фенотипических маркеров ДСТ. При наличии сопутствующей гиперрастяжимости кожи (диагностируемой при толщине кожной складки над ключицами > 2 см), атрофичных рубцов, повышенной ранимости кожи, в первую очередь, следует думать о классическом варианте синдрома Элерса-Данло (СЭД) (I/II подтип по классификации Villefranche, 1997). Наличие же врожденного вывиха суставов свидетельствует в пользу артрохалазического типа (VII подтип). Обширные кровоподтеки на коже и/или семейный анамнез сосудистых или кишечных разрывов или внезапной смерти являются признаками сосудистого подтипа СЭД (IV). Если умеренная гипермобильность суставов сочетается с характерным внешним обликом, подвывихом хрусталика и/или дилатацией аорты или аневризмой, необходимо думать о синдроме Марфана. Та же клиническая комбинация без глазных и кардиальных проявлений свидетельствует в пользу гипермобильного подтипа СЭД (III). В настоящее время не определены генетические и нозологические границы между гипермобильным типом СЭД и ГС. Кроме того, было показано, что у пациентов с III подтипом СЭД и ГС имеются мутации в генах, кодирующих неколлагеновые молекулы Tenascin-X, при этом отмечается снижение уровня сывороточного Tenascin-X в обеих группах гетерозиготных лиц женского пола [7]. Идентификация мутаций генов Тenascin-X является важной моделью изучения генетической основы ГС.
Клиническая картина несовершенного остеогенеза характеризуется повышенной ломкостью костей, переломы возникают при небольших нагрузках или спонтанно. Клиническая картина заболевания не ограничивается патологией скелета. Синие склеры, низкий рост, разрушение дентина зубов, прогрессирующая тугоухость в детском и юношеском возрасте, контрактуры, мышечная гипотония и повышенная частота пупочных и паховых грыж, врожденных пороков сердца и нефролитиаза – характерный комплекс патологических изменений при несовершенном остеогенезе. Другие характерные признаки в сочетании с ГМС могут указывать на наличие псевдоахондроплазии (PSACH), синдрома Ларсена, мышечной дистрофии Ульриха и др.
Биохимические и генетические нарушения при ДСТ
Наряду с клинической оценкой ДСТ в диагностике заболевания важную роль играют биохимические методы исследования. Они позволяют оценить состояние обмена соединительной ткани, уточнить диагноз, прогнозировать течение заболевания. Наиболее информативным является определение уровня оксипролина и гликозоаминогликанов в суточной моче, а также лизина, пролина, оксипролина в сыворотке крови. Генетические дефекты синтеза коллагена приводят к уменьшению его поперечных связей и возрастанию количества легкорастворимых фракций. Именно поэтому у больных с врожденной дисплазией соединительной ткани отмечается достоверное повышение оксипролина в суточной моче, степень которого коррелирует с тяжестью патологического процесса. О катаболизме межклеточного вещества судят по величине экскреции гликозоаминогликанов [8].
Для наследственных заболеваний соединительной ткани характерно изменение соотношения коллагенов разных типов и нарушение структуры коллагенового волокна. Типирование коллагена проводится методом непрямой иммунофлюоресценции по Sternberg L.A. при помощи поликлональных антител кфибронектину и коллагену [8]. Современной и перспективной является молекулярно-генетическая диагностика (ДНК-диагностика) дисплазии соединительной ткани, предполагающая применение молекулярных методов выявления генных мутаций. Молекулярный анализ гена fibrillin1 (FBN1) при подозрении на синдром Марфана может быть выполнен на геномной ДНК, извлеченной из лейкоцитов крови. В случаях диагностики СЭД или несовершенного остеогенеза проводится биопсия кожи с последующим биохимическим анализом коллагена типов I, III и V. В зависимости от клинической и биохимической оценки дальнейший молекулярный анализ проводится на ДНК, извлеченной из культивируемых фибробластов.
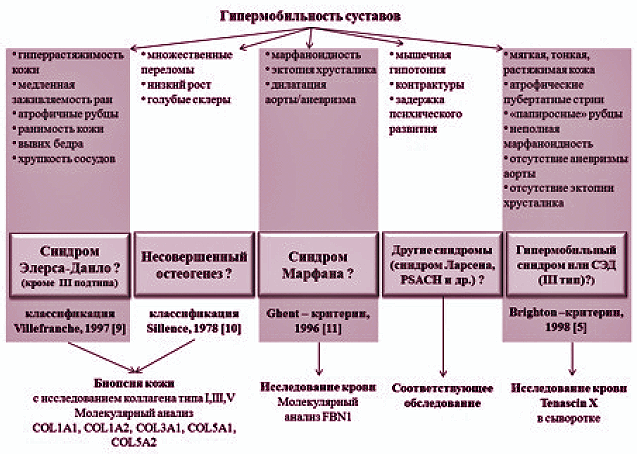
Алгоритм обследования пациента с гипермобильностью суставов представлен на рис. 1.
Рисунок 1. Алгоритм диагностики гипермобильности суставов
Возможности лечения ДСТ
Лечение ГМС при отсутствии жалоб не требует специальных мероприятий. При умеренных артралгиях показано ограничение физических нагрузок. Необходимо свести к минимуму возможности травм, что включает профессиональную ориентациюи исключение игровых видов спорта. При упорных болях в одном или нескольких суставах используют эластичные ортезы, обеспечивающие искусственное ограничение объема движений. Немаловажную роль играет укрепление окружающих болезненный сустав мышц с помощью изометрических упражнений, обеспечивающих оптимизацию локальной биомеханики и как следствие – исчезновение болей. В качестве симптоматической медикаментозной терапии при болевом синдроме показан прием нестероидных противовоспалительных препаратов и анальгетиков. С учётом патогенетической основы несостоятельности соединительной ткани и системного характера проявлений ГС основным направлением терапии является коррекция нарушенного метаболизма коллагена. Это позволяет предотвращать возможные осложнения ДСТ. К средствам, стимулирующим коллагенообразование, относят аскорбиновую кислоту, препараты мукополисахаридной природы (хондроитинсульфат, глюкозаминсульфат), витамины группы В (В1, В2, В3, В6) и микроэлементы (медь, цинк, магний). Последние являются кофакторами внутри- и внеклеточного созревания молекулы коллагена и других структурных элементов соединительной ткани [8].
Особая роль в регуляции метаболизма соединительной ткани отводится магнию. В условиях его недостатка происходит усиление деградации коллагеновых и, возможно, эластиновых волокон, а также полисахаридных нитей гиалуронана. Это обусловлено инактивацией гиалуронансинтетаз и эластаз, а также повышением активности гиалуронидаз и матричных металлопротеиназ. На клеточном уровне дефицит магния приводит также к увеличению числа дисфункциональных молекул т-РНК, замедляя, тем самым, скорость белкового синтеза. Кроме того, определенную роль в деградации соединительной ткани играют аутоиммунные реакции, обусловленные присутствием аллеля Bw35 системы HLA. Активация Т-клеточного иммунитета к компонентам соединительной ткани, содержащим рецепторы, соответствующие антигену Вw35, приводит к деградации соединительнотканного матрикса, что сопряжено с неконтролируемой потерей магния [12]. Повышенная экспрессия этого антигена отмечена у пациентов с первичным пролапсом митрального клапана, который является фенотипическим маркером ГС. В ряде исследований показана принципиальная возможность замедления процессов дегенерации соединительной ткани при лечении препаратами магния. Это достигается посредством усиления биосинтетической активности фибробластов, ответственных за нормализацию волокнистых структур соединительнотканного матрикса [13].
Необходимо отметить, что ДСТ имеет, как правило, прогрессирующий характер и лежит в основе формирования соматической патологии. Последняя нередко выходит на первый план и определяет прогноз основного заболевания. Своевременная метаболическая терапия играет важную роль в лечении и профилактике потенциальных осложнений ДСТ, в том числе ГС.