Если при ультразвуковом исследовании найдены маркеры хромосомной патологии плода
Если при ультразвуковом исследовании были найдены маркеры (признаки) хромосомной патологии плода, то это еще не означает, что у плода есть хромосомная патология, и надо обязательно прерывать беременность. Всем женщинам, у которых были найдены ультразвуковые маркеры хромосомной патологии плода, предлагается инвазивная пренатальная диагностика – хорионбиопсия/плацентобиопсия с целью взятия клеток плода и их тонкого микроскопического анализа.
Хорионбиопсия – это взятие нескольких ворсинок из хориона плода под ультразвуковым контролем и подсчет количества хромосом в его клетках. Хорион – орган плода, из которого потом образуется плацента. Его клетки идентичны клеткам плода. Поэтому если количество и структура хромосом в клетках хориона нормальны, то хромосомные болезни у плода исключаются с вероятностью более 99%.
Как проводится хорионбиопсия
Тонкой иглой через переднюю брюшную стенку делается укол, игла проходит в хорион и в нее попадает несколько ворсинок хориона. Процедура проводится в амбулаторных условиях, используются одноразовые перчатки и стерильные иглы, поэтому риск инфицирования во время процедуры практически отсутствует.
Каковы риски проведения хорионбиопсии
Любая процедура, даже простейший анализ крови, имеет риск осложнений. При проведении хорионбиопсии тоже есть риск – риск прерывания беременности. Однако, при соблюдении всех правил проведения процедуры этот риск не превышает 1%. Поэтому в тех случаях, когда индивидуальный риск хромосомной патологии плода достаточно высок, должна быть выполнена эта процедура.
На сегодняшний день в мире не разработано другого метода, позволяющего получить для исследования клетки плода, не выполняя внутриматочного вмешательства. В то же самое время, исключить или подтвердить диагноз болезни Дауна или другой хромосомной патологии можно только при исследовании клеток плода, которые были получены при внутриматочном вмешательстве.
Когда проводится хорионбиопсия
Хорионбиопсия выполняется до 14 недель беременности, после этого срока на месте хориона образуется плацента и тогда проводится уже плацентобиопсия. Техника выполнения и риск при плацентобиопсии принципиально не отличаются от хорионбиопсии.
Мы надеемся, что эта информация поможет Вам лучше понять, для чего мы проводим эти исследования, и преодолеть тот естественный страх перед процедурой, который вызывает неизвестность и те непрофессиональные сведения, которые иногда печатаются в немедицинских источниках.
В нашем центре вы можете пройти инвазивную диагностику хромосомных болезней плода и получить полный ответ уже через 3-4 дня (в некоторых случаях – через 24 часа).
Хромосомные аномалии плода
Наличие идеальных анализов и замечательное самочувствие беременной, ее юный возраст и безупречный анамнез (информация о перенесенных заболеваниях, условиях жизни, операция, травмах, хронической патологии, наследственности и под.) еще не являются 100% гарантией, что у ребенка нет хромосомных аномалии.
Хромосомные аномалии плода. Признаки
Признаки наличия хромосомной аномалии (ХА) плода во время беременности:
Каждый из этих признаков в отдельности и даже все вместе могут быть вариантами нормы.
Диагностика ХА
Из обычных анализов наиболее информативен первый скрининг или двойной тест. Его надо делать строго на сроке 12 недель. Он состоит из УЗИ плода (особенно важен замер шейной складки) и анализа крови на АФП, РАРР-А и ХГЧ.
Анализ не дает точного ответа на вопрос о наличии или отсутствии ХА. Его задача — рассчитать риски в зависимости от результатов, а также возраста и анамнеза беременной. Второй скрининг, так называемый «тройной тест», не информативен для выявления ХА. Узнать точно, есть ли у будущего ребенка ХА, можно только при помощи инвазивных методов — биопсии хориона, забора пуповинной крови, анализа амниотической жидкости. Цель этих анализов — определение кариотипа плода. Точность — 98%. Риск выкидыша — 1-2%. ХА не лечатся. После выявления ХА все, что может предложить медицина, — прерывание беременности.
Делать этот анализ или нет?
При принятии решения необходимо ответить на следующие вопросы:
Причины возникновения хромосомных аномалий
Однозначных причин возникновения ХА не известно. Повышенный риск существует, если:
Механизм возникновения ХА
ХА возникает у плода в момент образования зиготы, т.е. при слиянии яйцеклетки и сперматозоида. Материнская и отцовская клетка несут по 23 хромосомы (23 от мамы и 23 от папы). Обе клетки могут уже нести в себе «ломаные» хромосомы (даже если мама и папа абсолютно здоровы). Сбой может произойти и в момент слияния двух абсолютно здоровых родительских клеток. В этом случае «расходятся» неверно хромосомы плода. Этот процесс еще не изучен и не поддается контролю.
ХА — хромосомные синдромы
Изучено и описано более 300 хромосомных синдромов.
Учитывая, что у человека 23 парных хромосомы и существует несколько видов аберрации, количество хромосомных синдромов, не описанных в литературе и возникающих вновь, не ограничено.
Аберрации могут быть разные: полные и частичные трисомии, делеции, моносомии, мозаицизм транслокации и т.д. Выраженность признаков при хромосомном синдроме зависит от вида аберрации. Самый благоприятный вид — сбалансированная транслокация. Люди с такими изменениями ничем не отличаются от обычных, их особенность может быть выявлена только путем кариотипирования, однако у них повышен риск рождения детей с хромосомными синдромами — от 10 до 50% (средний риск в популяции — 5%).
Следующий наименее «травматичный» вид аберрации — мозаицизм, при котором хромосомное нарушение проявляется не во всех клетках и/или органах. Частичные трисомии и делеции дают уже значительные пороки развития, порой не совместимые с жизнью.
Самый тяжелый вид — полная трисомия или моносомия хромосомы.
Большая часть беременностей с хромосомной патологией плода отторгается самим организмом на самых ранних сроках или на сроке 20-23 недели, так как при хромосомной патологии плода велика вероятность различных патологий беременности (невынашивание, угроза выкидыша, гипертонус матки, преждевременное старение плаценты, токсикоз, гестоз, гипоксия плода и т.д.). Также многие малыши не доживают до года ввиду множественных пороков развития. Средняя продолжительность жизни людей с ХА — 30 лет, но есть описанные случаи пациентов с ХА доживших до 60 лет и более.
Развитие людей с ХА
Люди с хромосомными синдромами могут быть как тяжелыми инвалидами, так и абсолютно полноценными членами общества, получившими полноценное образование и имеющими обычную работу. Все зависит от вида аберрации, общего состояния организма и труда родных и близких. В большинстве случаев люди с хромосомными синдромами могут себя обслуживать, общаться, выполнять посильную работу. Интеллект снижен, есть хронические заболевания органов и систем организма.
Наличие эхо маркеров ха что это значит
Если у Вашего плода найдены ультразвуковые маркёры
Если при ультразвуковом исследовании найдены маркеры хромосомной патологии плода
Самые часто встречающиеся ультразвуковые маркеры хромосомной аномалии:
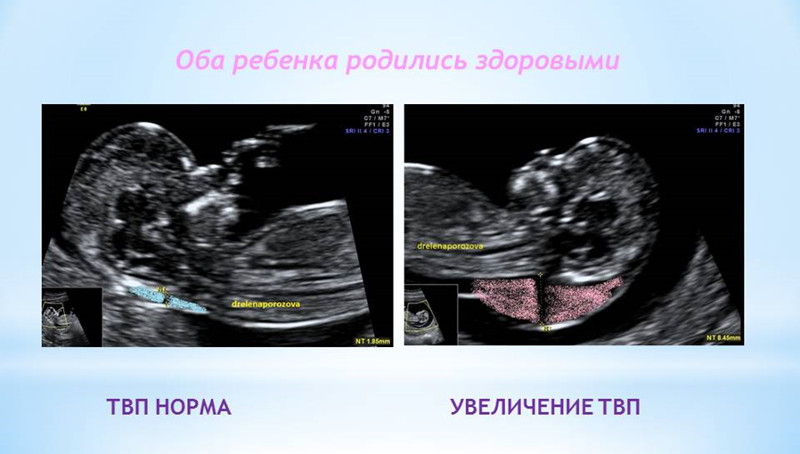
1. Увеличение ТВП.
Оценка этого параметра проводится в первое скрининговое УЗИ (11-14 недель)
ТВП (толщина воротникового пространства) может оказаться больше нормы по нескольким причинам.
Почему у плода может выявляться увеличение ТВП?
Родители бывают крайне взволнованы и хотят сразу же получить ответы на все, возникающие у них вопросы – с чем связано, что делать и многие другие. Вопросы, на которые невозможно ответить сразу. Ведь причин увеличения ТВП множество. Данная находка может встречаться у абсолютно здоровых плодов, это не порок развития, это лишь сигнал к более глубокому обследованию, потому что такая особенность может иметь место у плодов с хромосомной патологией, аномалиями сердца либо другими врожденными или наследственными заболеваниями. При увеличении максимального порога ТВП ВАЖНО, чтобы врач оценил все остальные ультразвуковые маркеры (признаки), а также провел детальную оценку анатомии плода. Возможно, причина увеличения ТВП кроется в нарушении развития плода (например, аномалии строения сердца).
Что делать при выявлении увеличения ТВП у плода?
Если у вашего плода обнаружили расширение ТВП, Вас обязательно направят на консультацию к врачу генетику, который собрав анамнез, оценив все риски, даст рекомендации по дополнительным методам исследования (инвазивная диагностика). Далее потребуется экспертное УЗИ плода на сроке 20 недель для детальной оценки анатомии. Если по всем этим исследованиям отклонений не выявлено, то шансы родить здорового ребенка велики даже при значительной величине ТВП.
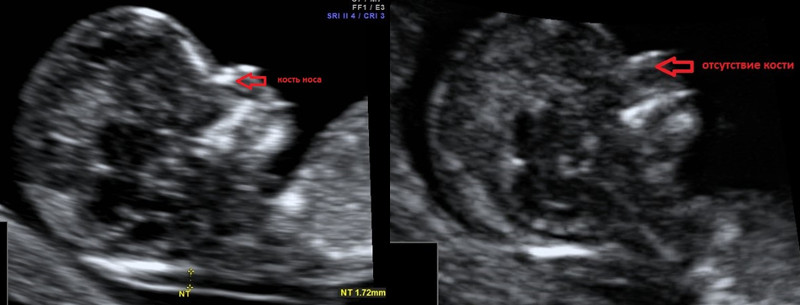
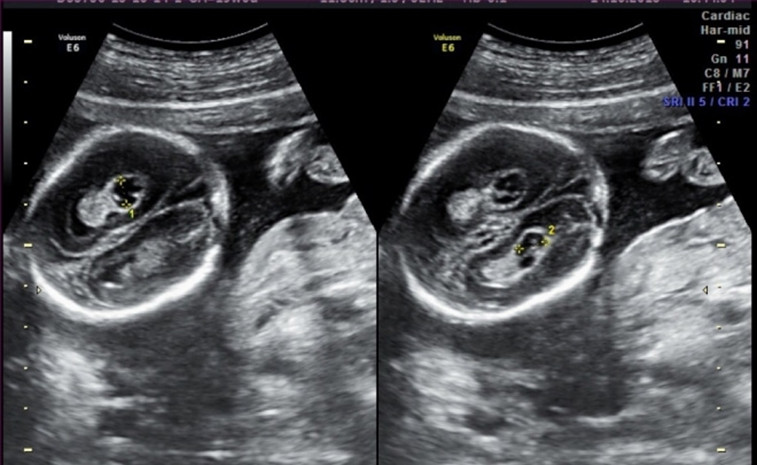
2. Гипоплазия\аплазия костей носа.
Гипоплазия костей носа – уменьшение размеров косточки носа в зависимости от КТР вашего малыша.
Аплазия костей носа – отсутствие визуализации косточки носа у вашего малыша.
Отсутствие видимости костной части спинки носа у плода или ее недоразвитие (недостаточно яркая) на первом скрининге связана с задержкой отложения кальция. Такая ситуация несколько чаще может встречаться у плодов с синдромом Дауна, однако важно, что:
3. Гиперэхогенный кишечник.
Это термин, говорящий о повышенной эхогенности (яркости) кишечника на ультразвуковом изображении. Выявление гиперэхогенного кишечника НЕ является пороком развития кишечника, а просто отражает характер его ультразвукового изображения. Необходимо помнить, что эхогенность нормального кишечника выше, чем эхогенность соседних с ним органов (печени, почек, легких), но такой кишечник не считается гиперэхогенным. Гиперэхогенным называется только такой кишечник, эхогенность которого сравнима с эхогенностью костей плода.
Почему кишечник у плода может быть гиперэхогенным?
Иногда гиперэхогенный кишечник выявляется у абсолютно нормальных плодов, и при УЗИ в динамике этот признак может исчезать. Повышенная эхогенность кишечника может быть проявлением хромосомных болезней плода, в частности, синдрома Дауна. В связи с этим при обнаружении гиперэхогенного кишечника проводится тщательная оценка анатомии плода. Однако при выявлении гиперэхогенного кишечника можно говорить лишь о повышенном риске синдрома Дауна, так как подобные изменения могут встречаться и у совершенно здоровых плодов. Иногда гиперэхогенный кишечник может быть признаком внутриутробной инфекции плода. Гиперэхогенный кишечник часто обнаруживается у плодов с задержкой внутриутробного развития. Однако при этом будут обязательно выявляться отставание размеров плода от срока беременности, маловодие и нарушение кровотока в сосудах плода и матки. Если ничего из вышеперечисленного не выявлено, то диагноз задержки развития плода исключен.
Что делать при выявлении гиперэхогенного кишечника у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты биохимического скрининга и даст необходимые рекомендации по дальнейшему ведению беременности.
4. Гиперэхогенный фокус в желудочке сердца.
Это термин, говорящий о повышенной эхогенности (яркости) небольшого участка сердечной мышцы на ультразвуковом изображении. Выявление гиперэхогенного фокуса в сердце НЕ является пороком развития сердца, а просто отражает характер его ультразвукового изображения. Гиперэхогенный фокус возникает в месте повышенного отложения солей кальция на одной из мышц сердца, что не мешает нормальной работе сердца плода и не требует никакого лечения.
Почему у плода может выявляться гиперэхогенный фокус в сердце?
Иногда гиперэхогенный фокус в сердце выявляется у абсолютно нормальных плодов, и при УЗИ в динамике этот признак может исчезать. Наличие гиперэхогенного фокуса в сердце плода может быть проявлением хромосомных болезней плода, в частности, синдрома Дауна. В связи с этим при обнаружении гиперэхогенного фокуса проводится тщательная оценка анатомии плода. Однако этот маркер относится к «малым» маркерам синдрома Дауна, поэтому выявление только гиперэхогенного фокуса в сердце не повышает риск наличия синдрома Дауна и не является показанием к проведению других диагностических процедур.
Что делать при выявлении гиперэхогенного фокуса в сердце плода?
Если у плода выявлен ТОЛЬКО гиперэхогенный фокус в сердце, то никаких дополнительных обследований не требуется; риск болезни Дауна не увеличивается. На плановом УЗИ в 32-34 недели еще раз будет осмотрено сердце плода. В большинстве случаев гиперэхогенный фокус в сердце исчезает к этому сроку беременности, но даже если он продолжает оставаться в сердце, это никак не влияет на здоровье плода и тактику ведения беременности.
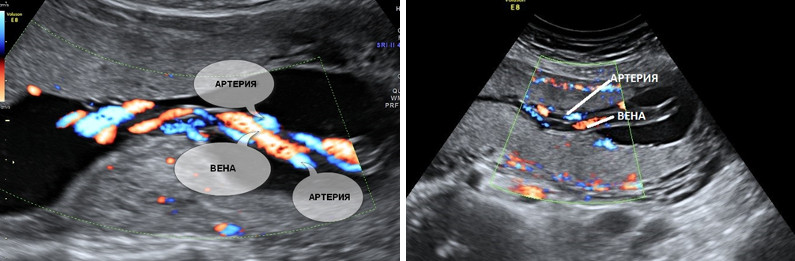
5. Единственная артерия пуповины.
Нормальная пуповина состоит из трех сосудов – две артерии и одна вена. Иногда вместо двух артерий в пуповине формируется только одна артерия и одна вена, таким образом, в пуповине определяется всего два сосуда. Данное состояние считается пороком развития пуповины, однако этот порок не оказывает никакого влияния на послеродовое состояние ребенка и его дальнейшее развитие.
Почему у плода может определяться единственная артерия пуповины?
Иногда единственная артерия пуповины выявляется у абсолютно нормальных плодов; после рождения ребенка данный факт не оказывает никакого влияния на его дальнейшее развитие. Иногда единственная артерия пуповины сочетается с пороками сердечно-сосудистой системы плода, поэтому при выявлении единственной артерии пуповины проводится детальный осмотр анатомии плода и, в частности, сердечно-сосудистой системы. При отсутствии других пороков развития единственная артерия пуповины в состоянии обеспечить адекватный кровоток плода. Несколько чаще единственная артерия пуповины выявляется у плодов с синдромом Дауна и другими хромосомными болезнями. Однако этот маркер относится к «малым» маркерам синдрома Дауна, поэтому выявление только единственной артерии пуповины не повышает риск наличия синдрома Дауна и не является показанием к проведению других диагностических процедур. Единственная артерия пуповины иногда приводит к возникновению задержки внутриутробного развития плода. В связи с этим при обнаружении единственной артерии пуповины рекомендуется дополнительное УЗИ в 26-28 недель беременности, и плановое в 32-34 недели. Если отставание размеров плода от срока беременности или нарушение кровотока в сосудах плода и матки не выявлено, то диагноз задержки развития плода исключен.
Что делать при выявлении единственной артерии пуповины у плода?
Выявление только единственной артерии пуповины не повышает риск наличия синдрома Дауна и не является показанием к консультации генетика и проведению других диагностических процедур. Необходимо контрольное УЗИ в 26-28 и 32 недели беременности для оценки темпов роста плода и оценки его функционального состояния.
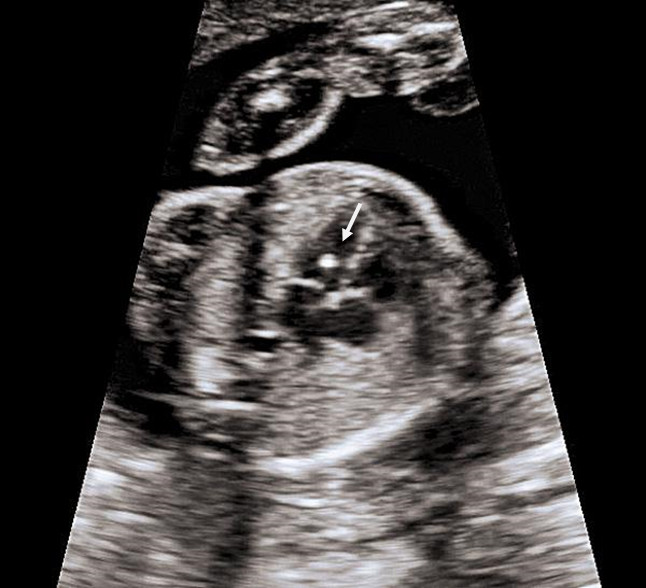
6. Кисты сосудистых сплетений (КСС).
Часто ли встречаются кисты сосудистых сплетений?
В 1-2 % всех нормальных беременностей плоды имеет КСС, в 50 % случаев обнаруживаются двусторонние кисты сосудистых сплетений, в 90 % случаев кисты самопроизвольно исчезают к 26-ой неделе беременности, число, размер, и форма кист могут варьировать, кисты также найдены у здоровых детей и взрослых. Несколько чаще кисты сосудистых сплетений выявляются у плодов с хромосомными болезнями, в частности, с синдромом Эдвардса (трисомия 18, лишняя 18 хромосома). Однако, при данном заболевании у плода всегда будут обнаруживаться множественные пороки развития, поэтому выявление только кист сосудистого сплетения не повышает риск наличия трисомии 18 и не является показанием к проведению других диагностических процедур. При болезни Дауна кисты сосудистых сплетений, как правило, не выявляются. Риск синдрома Эдвардса при обнаружении КСС не зависит от размеров кист и их одностороннего или двустороннего расположения. Большинство кист рассасывается к 24-28 неделям, поэтому в 28 недель проводится контрольное УЗИ. Однако, если кисты сосудистых сплетений не исчезают к 28-30 неделям, это никак не влияет на дальнейшее развитие ребенка.
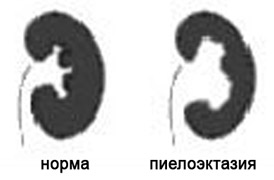
7. Расширение почечных лоханок (пиелоэктазия).
Почечные лоханки это полости, где собирается моча из почек. Из лоханок моча перемещается в мочеточники, по которым она поступает в мочевой пузырь.
Пиелоэктазия представляет собой расширение почечных лоханок. Пиелоэктазия в 3-5 раз чаще встречается у мальчиков, чем у девочек. Встречается как односторонняя, так и двухсторонняя пиелоэктазия. Легкие формы пиелоэктазии проходят чаще самостоятельно, а тяжелые иногда требуют хирургического лечения.
Причина расширения почечных лоханок у плода.
Если на пути естественного оттока мочи встречается препятствие, то моча будет накапливаться выше данного препятствия, что будет приводить к расширению лоханок почек. Пиелоэктазия у плода устанавливается при обычном ультразвуковом исследовании в 18-22 недели беременности.
Опасна ли пиелоэктазия?
Умеренное расширение почечных лоханок, как правило, не влияет на здоровье будущего ребенка. В большинстве случаев при беременности наблюдается самопроизвольное исчезновение умеренной пиелоэктазии. Выраженная пиелоэктазия (более 10 мм) свидетельствует о значительном затруднении оттока мочи из почки. Затруднение оттока мочи из почки может нарастать, вызывая сдавление, атрофию почечной ткани и снижение функции почки.
Кроме того, нарушение оттока мочи нередко сопровождается присоединением пиелонефрита – воспаления почки, ухудшающего ее состояние. Несколько чаще расширение лоханок почек выявляется у плодов с синдромом Дауна. Однако этот маркер относится к «малым» маркерам синдрома Дауна, поэтому выявление только расширения почечных лоханок не повышает риск наличия синдрома Дауна и не является показанием к проведению других диагностических процедур. Единственное, что нужно сделать до родов – пройти контрольное УЗИ в 32 недели и еще раз оценить размеры почечных лоханок.
Нужно ли обследовать ребенка после родов?
У многих детей умеренная пиелоэктазия исчезает самопроизвольно в результате дозревания органов мочевыделительной системы после рождения ребенка. При умеренной пиелоэктазии бывает достаточно проводить регулярные ультразвуковые исследования каждые три месяца после рождения ребенка. При присоединении мочевой инфекции может понадобиться применение антибиотиков. При увеличении степени пиелоэктазии необходимо более детальное урологическое обследование.
В случаях выраженной пиелоэктазии, если расширение лоханок прогрессирует, и происходит снижение функции почки, бывает показано хирургическое лечение. Хирургические операции позволяют устранить препятствие оттоку мочи. Часть оперативных вмешательств может с успехом выполняться эндоскопическими методами – без открытой операции, при помощи миниатюрных инструментов, вводимых через мочеиспускательный канал. В любом случае вопрос об оперативном лечении решается после рождения ребенка и полного его обследования.
Что делать при выявлении ультразвуковых маркеров хромосомной патологии у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты ультразвукового исследования и биохимического скрининга, рассчитает риск индивидуально для вашего случая и даст необходимые рекомендации по дальнейшему ведению беременности.
© 2021 краевое государственное бюджетное учреждение здравоохранения «Красноярский краевой медико-генетический центр» (КГБУЗ «ККМГЦ»)
Наличие эхо маркеров ха что это значит
Московский областной НИИ акушерства и гинекологии
Медико-генетическое отделение Московского областного НИИ акушерства и гинекологии
Курс пренатальной диагностики при кафедре медицинской генетики ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва, Россия
Московский областной НИИ акушерства и гинекологии
Медико-генетическое отделение Московского областного НИИ акушерства и гинекологии
Пренатальные маркеры частых хромосомных синдромов. Оценка прогностической значимости
Журнал: Российский вестник акушера-гинеколога. 2016;16(6): 47-53
Жученко Л. А., Андреева Е. Н., Голошубов П. А., Калашникова Е. А., Одегова Н. О. Пренатальные маркеры частых хромосомных синдромов. Оценка прогностической значимости. Российский вестник акушера-гинеколога. 2016;16(6):47-53.
Zhuchenko L A, Andreeva E N, Goloshubov P A, Kalashnikova E A, Odegova N O. Prenatal markers for common chromosomal syndromes. Estimation of prognostic value. Russian Bulletin of Obstetrician-Gynecologist. 2016;16(6):47-53.
https://doi.org/10.17116/rosakush201616647-53
Московский областной НИИ акушерства и гинекологии
Пренатальная диагностика патологических состояний является современным методом диспансеризации плода, позволяет определить медицинский и социальный прогноз для жизнеспособности и здоровья будущего ребенка. Поиск и практическое использование знаний о достоверных пренатальных признаках частых врожденных заболеваний определяют эффективность скрининговых программ. Основной целью настоящего исследования явилась оценка значимости известных и поиск новых ультразвуковых признаков, улучшающих диагностику частых хромосомных анеуплоидий для оптимизации скринингового обследования беременных в сроках беременности 11—14 нед. Материал и методы. Материалом для исследования послужили результаты ультразвукового обследования 266 779 беременных, жительниц Московской области, за период 2011—2015 гг., проведенного в рамках раннего пренатального скрининга в сроки беременности 11—14 нед (строго при показателе копчико-теменного размера плода от 45 до 84 мм). Одновременно проводились биохимический скрининг для выявления патологических пренатальных маркеров и расчет индивидуального риска выявления хромосомных анеуплоидий на основе единого программного обеспечения. Результаты. Были выявлены 433 плода с трисомией 21, 166 плодов с трисомией 18, 64 плода с трисомией 13. Впервые в российской популяции установлены медианы известных пренатальных ультразвуковых признаков трех частых хромосомных анеуплоидий (трисомии 21, 18 и 13): толщины воротникового пространства, частоты сердечных сокращений и состояния носовой кости. Изучена распространенность ряда врожденных пороков развития и особенностей фенотипа плода. Заключение. В перечень дополнительных пренатальных ультразвуковых маркеров могут входить следующие: патология лимфатической системы и дефекты межжелудочковой перегородки при трисомии 21; врожденный порок сердца, микрогнатия, расщелины лица, патологическое положение кистей плода при трисомии 18; пороки развития центральной нервной системы, врожденные пороки сердца, пороки развития и особенности строения лицевого черепа, полидактилия при трисомии 13. Авторы информируют об отсутствии конфликта интересов.
Московский областной НИИ акушерства и гинекологии
Медико-генетическое отделение Московского областного НИИ акушерства и гинекологии
Курс пренатальной диагностики при кафедре медицинской генетики ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва, Россия
Московский областной НИИ акушерства и гинекологии
Медико-генетическое отделение Московского областного НИИ акушерства и гинекологии
Спорадически возникающие врожденные дефекты развития у детей в настоящее время могут быть диагностированы при использовании доказательно эффективной системы ранней дородовой диагностики в рамках нового подхода при решении задач медицинского и социального прогноза в семье. Акушерская тактика при наблюдении за течением беременности должна определяться достоверным пренатальным диагнозом нарушений состояния плода, постановка которого реальна уже в сроки 11—14 нед беременности. При этом особое значение в системе пренатального скрининга имеют летальные и неизлечимые болезни, определяемые с помощью различных пренатальных методов. Поиск и изучение маркерных признаков патологических состояний плода и оценка их прогностической ценности составляют основу важнейшего направления медицины плода — пренатальной диагностики (ПД).
Цель исследования — оптимизация дородовой диагностики частых хромосомных синдромов как нового подхода к медико-социальному прогнозу исхода беременности посредством изучения прогностической значимости известных ультразвуковых маркеров и поиска новых достоверных ультразвуковых признаков хромосомных анеуплоидий (ХА) на основании их распространенности.
В задачи исследования входило изучение закономерностей изменения таких известных эхомаркеров ХА, как толщина воротникового пространства (ТВП), состояние носовой кости (НК), частота сердечных сокращений (ЧСС) при наиболее частых анеуплоидиях (трисомиях по 21, 18, 13-й хромосомам), а также поиск новых достоверно значимых ультразвуковых маркеров: врожденных пороков развития (ВПР) и особенностей фенотипа плода для диагностики наиболее частых генетических синдромов хромосомной этиологии.
Материал и методы
В рамках современного акушерского мониторинга в России проводится массовый ранний пренатальный скрининг (РПС) беременных на частые ХА, трисомии по хромосомам 21, 18, 13 и рано манифестирующие пороки развития у плода. Алгоритм РПС основан на международном стандарте, разработанном независимой врачебной организацией «Фонд медицины плода» и признанном в большинстве стран мира [1]. В сроки 11—14 нед беременности на экспертном уровне ПД одновременно проводятся ультразвуковое исследование (УЗИ) и биохимический скрининг (БХС) для выявления патологических пренатальных маркеров, а также расчет индивидуального риска выявления ХА на основе единого программного обеспечения, позволяющего вести базу данных и проводить внутренний индивидуальный аудит всех пренатальных измерений с оценкой качества РПС в регионе в целом.
Источником данных для проведения настоящего исследования явились сведения об обследованиях, проведенных в рамках РПС в Московской области за 5 лет, с 2011 по 2015 гг. Всего были обследованы 270 087 беременных, взято в анализ 266 779 случаев одноплодных беременностей в связи с имеющимся различием подходов к расчету рисков и к интерпретации результатов при многоплодных беременностях.
В программе РПС были созданы базы данных, куда вводились результаты УЗИ (в том числе наличие и описание маркеров ХА и ВПР), показатели биохимического исследования материнских сывороточных маркеров ХА (РАРР-А и свободная β-субъединица ХГч) [11], расчетные риски ХА с учетом порогового значения cut-off 1:100, результаты медико-генетического консультирования (МГК), инвазивной пренатальной диагностики (ИПД): виды манипуляций и лабораторные данные по анализу плодного материала, а также исходы беременности у женщин, прошедших РПС.
ИПД (аспирация ворсин хориона, амниоцентез) для постановки окончательного диагноза была проведена в 3053 случаях: в 61% наблюдений — аспирация ворсин хориона, в 39% — амниоцентез. По результатам лабораторного исследования плодного материала, выполненного посредством молекулярно-цитогенетических, цитогенетических исследований, было выявлено 916 различных хромосомных аномалий при общей эффективности пренатального кариотипирования 30%. Структура пренатально установленных за период исследования ХА представлена на рис. 1. Число включенных в исследование частых анеуплоидий (трисомий по хромосомам 21, 18 и 13) составило 663.

Результаты и обсуждение
Основным, самым важным и статистически значимым ультразвуковым маркером для пренатальной оценки индивидуального риска развития хромосомной патологии является ТВП. Распространенность хромосомных или других дефектов зависит от величины, а не от внешнего вида воротникового пространства [1—3]. Аномальное увеличение ТВП ассоциируется с трисомией 21 и другими частыми хромосомными аномалиями, более чем с 50 различными пороками развития плода и генетическими синдромами, а также с внутриутробной гибелью плода. Превалирование хромосомных дефектов увеличивается экспоненциально с увеличением ТВП с 0,2% для тех, у кого ТВП находится между 5-м и 95-м перцентилями, до 65% при ТВП 6,5 мм и более [4—6].
ЧСС в норме увеличивается со 110 уд/мин в 5 нед беременности до 170 уд/мин в 10 нед, а затем постепенно снижается до 150 уд/мин к 14 нед беременности. При наличии хромосомных аномалий имеются определенные тенденции в изменении этого параметра [1]. Включение ЧСС в протокол комбинированного пренатального скрининга в I триместре беременности способствует диагностике трисомии 21-й и 18-й хромосомам и значительно увеличивает частоту выявления трисомии по 13-й хромосоме.
Расширение протокола осмотра с оценкой дополнительных ультразвуковых маркеров (оценка НК, кровотока в венозном протоке и на трикуспидальном клапане) улучшает чувствительность РПС за счет увеличения частоты обнаружения и уменьшения частоты ложно-положительных результатов. В работах многих авторов установлена взаимосвязь между патологией НК и наличием у плода ХА [1, 7—10].
Для ультразвуковой оценки состояния плода используют не только толщину ТВП, состояние НК, но и дополнительные ультразвуковые маркеры. Существуют врожденные пороки, которые являются маркерными для хромосомных заболеваний: наличие голопрозэнцефалии увеличивает риск обнаружения трисомии 13, атриовентрикулярного канала (АВК) — трисомии 21, диафрагмальная грыжа — трисомии 18, омфалоцеле и мегацистик увеличивают риск выявления трисомий хромосом 13-й и 18-й [1, 10].
Всего в Московской области за 5 лет, включенных в исследование, из 916 ХА, установленных пренатально в рамках РПС, было выявлено 433 (47%) случая трисомии по 21-й хромосоме, 166 (18%) случаев трисомии по 18-й хромосоме, 64 (7%) случая трисомии по 13-й хромосоме. Остальные 28% представлены другими генетическими хромосомными синдромами.
Трисомия 21 (синдром Дауна)
Суммарно у 433 плодов с пренатально установленной трисомией по 21-й хромосоме медиана ТВП составила 3,5 мм. Более 95-го перцентиля ТВП встречалась у 351 плода, что составило 81% (рис. 2, а). По данным литературы [1, 5, 6], значение ТВП более 95-го перцентиля встречается у 71% плодов с трисомией 21.

Медиана ЧСС при трисомии по 21-й хромосоме составила 161 уд/мин (см. рис. 2, б), что соответствует общепопуляционному значению и не подтверждает опубликованные данные литературы, согласно которым ЧСС плода превышает 95-й перцентиль примерно в 15% случаев [1].
У 429 плодов с трисомией по 21-й хромосоме в качестве дополнительного маркера ХА оценивалась НК (99%). Патология Н.К. была отмечена в 342 (79,7%) случаях. По усредненным данным мультицентровых исследований Фонда медицины плода, в 11—14 нед беременности НК была изменена у 60% плодов с трисомией 21 [1, 7—10, 12—15].
Всего при трисомии 21 нами было выявлено 288 различных ВПР и особенностей при оценке фенотипа плода. В 34 (7,8%) случаях зарегистрирована патология лимфатической системы с различной манифестацией: в 25 наблюдениях отмечено расширение яремных лимфатических протоков, в 9 — наличие множественных лимфангиом различной локализации. Кроме того, в 20 (4,6%) случаях отмечалась водянка плода. ВПР и особенности строения сердца и сосудов плода встречались у 43% плодов. Кроме диагностики АВК (14,7%), как крупного врожденного порока сердца (ВПС), влияющего на расчет риска по трисомии 21, у 25% патологических плодов (109 случаев) был диагностирован дефект межжелудочковой перегородки. Таким образом, патология лимфатической системы и дефекты межжелудочковой перегородки могут входить в перечень пренатальных маркеров трисомии по 21-й хромосоме.
Трисомия 18 (синдром Эдвардса)
У 166 плодов с трисомией по 18-й хромосоме медиана ТВП в среднем составила 4,0 мм (рис. 3, а), что выше, чем при трисомии 21 (3,5 мм). ТВП более 95-го перцентиля зарегистрирована у 118 (71%) плодов, что соответствует данным литературы (74%) [1, 5, 6].

Медиана ЧСС при трисомии 18 в нашем исследовании составила 160 уд/мин (см. рис. 3, б), что соответствует общепопуляционному значению и не подтверждает данные литературы о снижении ЧСС ниже 5-го пeрцентиля в 15% случаев трисомии по 18-й хромосоме [1].
НК как дополнительный эхо-маркер ХА НК оценивалась у 162 (97,6%) плодов с трисомией по 18-й хромосоме. Патология Н.К. встретилась у 125 (75%) из 162 плодов, и этот показатель выше, чем опубликованный в литературе [1, 7—10, 12—15], 50%.
Всего при трисомии по 18-й хромосоме было выявлено 318 ВПР и особенностей фенотипа плода. В 67% случаев встречались различные ВПС, в 38% случаев было обнаружено омфалоцеле, в 24% — ВПР и особенности строения лица: одно- и двусторонние расщелины лица, микрогнатия. В 27% случаев встречались ВПР и особенности строения верхних конечностей — лучевая косорукость и флексорное положение кистей. Данные факты позволяют относить ВПС, микрогнатию, расщелину лица, патологию кистей плода к маркерам ХА по трисомии 18.
Трисомия 13 (синдром Патау)
В 64 случаях трисомии по 13-й хромосоме медиана ТВП в среднем составила 3 мм (рис. 4, а), что ниже, чем при трисомии 21 (3,5 мм) и 18 (4 мм). Более 95-го перцентиля ТВП встречалась у 36 (56%) плодов. Полученный показатель ниже, чем по данным литературы (71%) [1, 5, 6].

Медиана ЧСС составила 179 уд/мин (см. рис. 4, б), что выше общепопуляционного значения и подтверждает литературные данные: превышение 95-го перцентиля в 85% случаев [1].
Как дополнительный маркер НК оценивалась у 61 (95,3%) плода с трисомией 13. Патология Н.К. встречалась в 35 (57%) случаях. По опубликованным данным [1, 7—10, 12—15], НК отсутствует у 40% плодов с трисомией по 13-й хромосоме.
Всего при трисомии 13 было выявлено 156 наблюдений ВПР и особенностей фенотипа плода. Обращала внимание высокая частота обнаружения в данной выборке патологии центральной нервной системы (ЦНС) — 39%. ВПР и особенности строения лица встречались у 42% всех пренатально выявленных трисомий 13, из них одно- и двусторонние расщелины лица составили 20 случаев из 27. Различные ВПС были отмечены у 64% плодов. В 40% случаев была диагностирована полидактилия. Таким образом, учитывая распространенность трисомии 13, можно рекомендовать использовать все эти маркеры для диагностики трисомии 13.
Таким образом, по результатам исследования, проведенного на материале Московской области, в России впервые установлены популяционные частоты ранее известных пренатальных эхо-маркеров при частых ХА, трисомии по 21, 18, 13-й хромосомам. Произведена оценка распространенности дополнительных ультразвуковых признаков данной патологии: ВПР и особенностей фенотипа плода. Использование полученных в исследовании результатов врачами ультразвуковой диагностики экспертного уровня в процессе выполнения ими мероприятий массового ультразвукового обследования беременных в сроках 11—14 нед позволит повысить эффективность раннего пренатального скрининга на частые хромосомные анеуплоидии у плода.
Выводы
1. В российской популяции (на примере региона «Московская область») при пренатально выявленной трисомии по 21-й хромосоме (синдром Дауна) медиана ТВП составила 3,5 мм, медиана ЧСС — 161 уд/мин, а патология носовой кости — в 342 (79,7%) из 433 выявленных случаев.
2. При трисомии по 18-й хромосоме (синдром Эдвардса) медиана ТВП составила 4 мм, ЧСС — 160 уд/мин, патология носовой кости встретилась у 125 (75%) плодов из 166 пренатально выявленных случаев.
3. В случаях трисомии по 13-й хромосоме (синдром Патау) медиана ТВП в среднем составила 3 мм, медиана ЧСС — 179 уд/мин, а патология носовой кости была выявлена в 35 (57%) случаях из 64.
4. В связи с высокой распространенностью в перечень дополнительных пренатальных ультразвуковых маркеров могут входить установление патологии лимфатической системы и дефектов межжелудочковой перегородки при трисомии по 21-й хромосоме; выявление ВПС, микрогнатии, расщелины лица, патологии положения кистей плода — при трисомии по 18-й хромосоме; ВПР ЦНС, ВПС, пороки развития и особенности лицевого черепа, полидактилия могут рассматриваться как дополнительные ультразвуковые признаки, пренатально повышающие прогнозирование при трисомии по 13-й хромосоме.
При поддержке гранта РГНФ № 15−06−10977/15