Лечение пяточной шпоры
Что же такое пяточные шпоры и откуда они берутся?
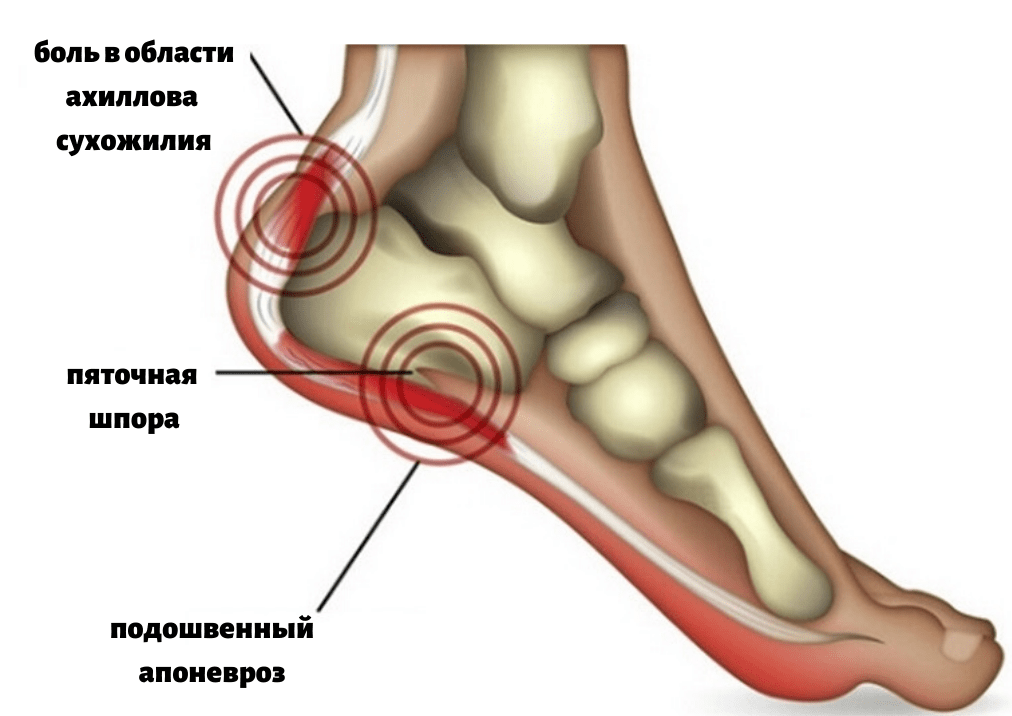
В результате различных процессов (избыточный вес, травма и др.) в данной области возникает хроническая травматизация сухожилия с образованием микронадрывов и постепенное развитие воспалительного процесса. Как компенсаторная реакция на травму и воспалительный процесс начинает образовываться костный вырост, он принимает форму шипа и, передавливая мягкие ткани подошвы стопы, вызывает характерные сильные боли в пяточной области. Самым значимым симптомом пяточной шпоры является сильная боль при ходьбе, особенно в самом начале ходьбы (так называемая, стартовая боль), при вставании со стула, с постели.
Основные причины образования пяточных шпор:
Проявления заболевания
Боли, возникающие при опоре на больную пятку, развиваются постепенно с ростом самой шпоры, характеризуются как жгучие или острые, с ощущением «гвоздя в пятке». Они могут локализоваться на внутренней поверхности больной пятки и переходить на всю стопу. При осмотре пяточной области нет никаких видимых изменений, редко отмечается отечность, болезненность определяется при надавливании на пятку. Интересно, что интенсивность боли не зависит от размера шпоры, что обусловлено, прежде всего, не наличием самой шпоры, а воспалительными изменениями в мягких тканях пятки. Диагноз пяточной шпоры подтверждается рентгенографией.
Основные принципы лечения пяточных шпор
1. Вначале необходимо выяснить причину развития воспалительного процесса в области подошвы и постараться максимально устранить ее. Т.е. выяснить, какой патологический процесс мог привести к избыточной травматизации фасции и возникновению воспаления. С этой же целью следует нормализовать вес, если он избыточный, дозировать физические нагрузки и ношение тяжестей, подобрать удобную, правильную обувь для занятий спортом и для повседневной носки. Снять и отложить в сторону неудобную обувь. На время экспресс-лечения следует ограничить нагрузку на ноги — сократить ходьбу и тем более бег или переноску тяжести насколько это возможно. Лучше носить удобные легкие кроссовки с хорошим супинатором.
2. Необходимо максимально возможное обеспечение физической разгрузки болезненной области, для чего рекомендуется подбор индивидуальных ортопедических стелек с выкладкой внутреннего и наружного продольного сводов, углублением и мягкой прокладкой под пяткой, а также временное ношение подпяточника с углублением или отверстием в центре. Как временную меру при лечении пяточной шпоры можно рекомендовать ношение обуви без задника;
3. Консервативное лечение направленно на ликвидацию воспалительного процесса и включает местное применение нестероидных противовоспалительных препаратов (гели и мази), обладающих противовоспалительным и рассасывающим эффектом. Но эти методы, как правило, приносят лишь только временный эффект, их обязательно нужно сочетать в комплексе с другими методами.
4. Наружное применение мазей при пяточной шпоре лучше сочетать с массажем стоп. Массаж при пяточной шпоре удобно делать самостоятельно.
5. В комплекс лечения пяточной шпоры включают теплые ванны с морской солью, содой. Ванночки необходимо делать перед применением мазей и массажа.
6. Определенные упражнения лечебной гимнастики с проведением массажа мышц стопы и голени — рекомендуются для улучшения кровоснабжения тканей стопы, с этой же целью можно проводить тепловые процедуры парафино- или озокеритотерапии.
7. В некоторых случаях (если развитие пяточной шпоры происходит на фоне артроза) в комплексной терапии рекомендуют прием хондропротекторов с анальгетическим и противовоспалительным эффектом, что останавливает прогрессивный воспалительный процесс, но эффект от внутреннего применения препаратов развивается только через 6 недель от начала лечения и сохраняется в течение 2–3 мес. после его отмены.
8. Методы медикаментозного лечения пяточной шпоры.
Официальная медицина на сегодняшний день разработала большое количество схем фармакологической терапии данного заболевания. Среди препаратов, применяемых для лечения пяточной шпоры: нестероидные противовоспалительные средства, гели, мази, кремы и пластыри для лечения пяточной шпоры местного применения, обладающие рассасывающим и противовоспалительным эффектом.
При малой эффективности консервативного лечения выполняются лекарственная блокада пяточной шпоры — обкалывание болезненного места шприцом с лекарственным веществом. Например, стойким эффектом обладает однократное местное введение дипроспана.
Препараты, применяемые с этой целью, оказывают выраженный местный противовоспалительный эффект, что быстро подавляет воспалительный процесс и снижает болевой синдром.
Данная процедура требует знаний и большого опыта, поэтому проводить ее может только квалифицированный специалист. Однако при частом использовании метода возможно разрушение связки или фасции.
9. К хирургическому лечению прибегают крайне редко, так как встречается много недостатков при данной методике. При проведении операции удаляют пяточную шпору. После чего конечность фиксируют гипсовой повязкой примерно на один месяц.
После снятия гипса назначают ортопедические стельки и проводят курсы восстановительного лечения. Помните, что в большинстве случаев пяточные шпоры вполне поддаются терапии и без операций.
10. Любой метод лечения необходимо сочетать с физиотерапевтическими воздействиями.
Ударно-волновая терапия пяточной шпоры
Является наиболее эффективным методом: терапия воздействует непосредственно на костные разрастания и способствует их уменьшению или даже рассасыванию. Ударно-волновая терапия — относительно новый метод лечения.
В нашей стране данная процедура начала практиковаться не очень давно, но первые результаты уже обнадеживают.
Имеющийся опыт позволяет утверждать, что при использовании данного метода лечения эффективность лечения пяточной шпоры очень высока. Метод основан на воздействии импульсов ударных волн определенной частоты. Эффект ударной волны разрыхляет отложения кальция в пяточной шпоре.
Это позволяет в дальнейшем вымывать разрыхленные отложения из организма с кровотоком. Пораженная связка избавляется таким образом от накопленных солей кальция.
Кроме того, при этом активизируются процессы регенерации тканей, уменьшаются отечность и воспалительные явления. С каждой проведенной процедурой болевой синдром становится все меньше и, как правило, значительно уменьшается или исчезает к концу лечения.
Пораженный участок во многом восстанавливает свою естественную структуру и возвращает себе способность переносить каждодневные нагрузки, не вызывая болезненных ощущений.
На начальных стадиях заболевания лечение требует небольшого количества процедур от 3 до 5 на курс, а при большой длительности процесса длительность лечения до 5-10 процедур на курс. Между сеансами обязателен перерыв 5-7 дней.
Продолжительность одного сеанса составляет 15-20 минут на одно поле. На кожу пятки наносят специальный гель, воздействие осуществляется с помощью излучателя.
Существуют противопоказаниями к лечению пяточной шпоры: нарушения свертываемости крови и тромбофлебит, злокачественные новообразования, беременность.
Нежелательно проведение процедур ударно-волновой терапии в течение месяца после введения в область пятки гормональных противовоспалительных препаратов.
Лучевая терапия (рентгенотерапия) пяточной шпоры
Использование рентгеновского излучения в лечении пяточной шпоры показывает весьма эффективные результаты. Метод заключается в том, что на область пятки направляются четко сфокусированные рентгеновские лучи, несущие пониженную дозу радиации.
Они вызывают блокирование нервных окончаний, и пациент перестает испытывать болевые ощущения.
Курс лечения чаще всего состоит из десяти сеансов, каждый из которых имеет продолжительность в 10 минут.
Рентгенотерапия в лечении пяточной шпоры обладает следующими преимуществами: полная безболезненность процедуры, высокая эффективность, минимум противопоказаний, воздействие излучения только на пяточную шпору, противоаллергическое и противовоспалительное действие, возможность амбулаторного лечения.
Противопоказанием к использованию данного метода является только беременность.
При применении рентгенотерапии сама шпора не исчезает, блокируются только болевые ощущения, исходящие от нее. Поэтому после проведения курса рентгенотерапии необходимо обязательной позаботиться о разгрузке стопы.
Лазерное лечение пяточной шпоры
В настоящее время низкоинтенсивная лазерная терапия — популярный и достаточно широко используемый метод лечения данного заболевания. Лазерная терапия воздействует на мягкие ткани, находящиеся вокруг шпоры.
Сфокусированное излучение вызывает увеличение кровообращения в области воспаления, что способствует уменьшению болей.
Среди пациентов бытует мнение о том, что лазерная терапия способна устранять саму пяточную шпору. Однако это является заблуждением. Проникая в ткани стопы, низкоинтенсивный лазерный луч на сам костный нарост не оказывает практически никакого действия.
Его эффект проявляется только на мягких тканях. А значит, после проведения курсов лазерной терапии также необходимо применять все методы, направленные на профилактику данного заболевания.
УВЧ-СВЧ-терапия
Этот метод заключается в применении переменного электромагнитного поля ультравысокой и сверхвысокой частоты. Влияние этих токов приводит к расширению капилляров в мягких тканях и к значительному усилению кровообращения. При этом уменьшается болевой синдром и воспаление.
Длительность одного сеанса составляет 10-15 минут. Для лечения пяточной шпоры требуется около 10-12 сеансов терапии.
Чаще врачи назначают пациентам переменное магнитное поле. Образуются слабые токи в крови и лимфе, которые влияют на метаболизм, а также на структуру воды и белков. Повышается сосудистая и кожная проницаемость, рассасываются отеки, уменьшается воспаление.
Данная методика позволяет достичь те же результаты, что и УВЧ-терапия.
Лечить шпоры на пятке можно и с помощью электрофореза или СМТ-ДДТ-фореза
Электрический ток повышает ионную активность в проводящих тканях, при этом увеличивается синтез многих биологически активных веществ. Лечебное действие обусловлено поступлением ионов лекарственных веществ (именно в ионной форме вещества наиболее активны), а также формированием кожного депо, из которого ионы постепенно поступают в ткани в последующие дни.
При электрофорезе используют специальные прокладки, пропитанные лекарством. Прокладки располагают между кожей пятки и пластинами электродов. Для лечения пяточной шпоры используют йодистый калий, гидрокортизон, новокаин и прочие препараты.
Эффективность таких методов физиолечения, как ультразвука и фонофореза (сочетанное применение ультразвука и лекарственного препарата) при пяточных шпорах составляет более 30%.
Основной эффект физиотерапии ультразвуком при лечении пяточной шпоры заключается в устранении воспалительного процесса, учитывая, что лучше всего ультразвук поглощается костной тканью.
При этом не следует бояться, что ультразвуковое лечение будет влиять на здоровую костную ткань пятки. Проведенные исследования низкочастотным ультразвуком показали, что разрушений костных тканей не вызывалось, но локальное применение ультразвуковых волн на область шпоры способствовало снижению содержания в ней кальция с замещением волокнистой соединительной тканью.
Также ультразвук оказывает рассасывающее и спазмолитическое действие, улучшая процессы локальной микроциркуляции.
Эффект от ультразвукового лечения усиливается сочетанным применением противовоспалительных мазевых препаратов. Озвучивание низкочастотным ультразвуком повышает проницаемость клеточных мембран, улучшает проницаемость и введение лекарственных веществ.
Наиболее часто применяют гидрокортизоновую мазь. Фонофорез способствует более глубокому проникновению лекарственного вещества в пораженную область, нежели применять мазь как самостоятельное средство лечения.
Метод фонофореза основан на свойстве ультразвука изменять проницаемость кожных покровов, в связи с чем лекарства, нанесенные на кожу, всасываются более активно.
Продолжительность самой процедуры — до 10 минут. На курс лечения может понадобится 5-10 процедур, с возможными повторными курсами.
Профилактика пяточной шпоры
Профилактические меры должны быть направлены, в первую очередь, на предупреждение преждевременного износа, старения и травм костно-суставного аппарата:
Данная страница не существует!
Услуги инфекционной клиники
Диагностика, профилактика и лечение
Фиброэластометрия и УЗ-диагностика молочных желез, щитовидной железы, мошонки, брюшной полости
Биохимия. Анализ крови: общий, клинический. Анализы на витамины, микроэлементы и электролиты. Анализ на ВИЧ-инфекцию, вирусные гепатиты, бактерии, грибки и паразиты
Максимально точное определение выраженности фиброза печени неинвазивным методом при помощи аппарата FibroScan 502 TOUCH
Гинеколог в H-Сlinic решает широчайший спектр задач в области женского здоровья. Это специалист, которому вы можете полностью доверять
Дерматовенерология в H-Сlinic — это самые современные и эффективные алгоритмы диагностики и лечения заболеваний, передающихся половым путем, грибковых и вирусных поражений, а также удаление доброкачественных невусов, бородавок, кондилом и папиллом
Возможности вакцинопрофилактики гораздо шире Национального календаря прививок. H-Clinic предлагает разработку плана вакцинации и современные высококачественные вакцины в наличии
Терапевт в H-Сlinic эффективно решает задачи по лечению заболеваний, которые зачастую могут становиться большой проблемой при наличии хронического инфекционного заболевания
Врач-кардиолог H-Сlinic проведет комплексную диагностику сердечно-сосудистой системы и при необходимости назначит эффективное терапию. Сердечно-сосудистые проблемы при инфекционных заболеваниях, требуют специфичных подходов, которые мы в состоянии обеспечить
Наша цель — новое качество вашей жизни. Мы используем современные диагностические алгоритмы и строго следуем наиболее эффективным протоколам лечения.
Общая терапия, Инфекционные заболевания, Гастроэнтерология, Дерматовенерология, Гинекология, Вакцинация, УЗИ и фиброэластометрия, Кардиология, Неврология
Биохимия, Общий/клинический анализ крови, Витамины и микроэлементы/электролиты крови, ВИЧ-инфекция, Вирусные гепатиты, Другие инфекции, бактерии, грибки и паразиты, Комплексы и пакеты анализов со скидкой
В наличии и под заказ качественные бюджетные решения и препараты лидеров рынка лечения инфекционных болезней. Аптека H-Clinic готова гибко реагировать на запросы наших клиентов. Мы поможем с оперативным поиском препаратов, которые обычно отсутствуют в сетях.
Нафталанотерапия что это такое
Выделяют схемы АРВТ первой, второй, третьей и т. д. линии и схемы резерва (спасения).
Также к схемам первого ряда (линии) относятся схемы, измененные вследствие развития побочных эффектов, нежелательных явлений. Таким образом можно сделать вывод, что комбинация противовирусных препаратов первой линии – это схема, которые не менялась по причине неэффективности.
Схема первой линии включает, как правило, 2 препарата нуклеозидной основы (например Тенофовир или Абакавир) и третий препарат из другой группы, с другим механизмом действия.
Этим они отличаются от схем лечения вич-инфекции, которые назначают особым категориям больных. Например, людям с когнитивными нарушениями, получающим лечение ХВГС, беременным, пациентам имеющие нарушения липидного профиля, сахарный диабет и другие.
Соответственно препараты третьей линии назначают при неэффективности схем второй.
Обычно они включают в себя препараты разных групп, подбор которых осуществляется индивидуально для каждого пациента, исходя из анализа теста на резистентность (мутаций вируса конкретного пациента), истории ранее проводимой терапии, межлекарственных взаимодействий, сопутствующих заболеваний.
Для оценки эффективности АРВТ главными показателями являются:
1. Исследование вирусной нагрузки (вирусологические критерии).
Поэтому своевременный лабораторный контроль поможет врачу правильно оценить эффективность.
2. Исследование уровня СД4 и других показателей иммунограммы (иммунологическая эффективность) – это критерии восстановления иммунной системы. Этот процесс происходит медленно и существенно зависит от степени иммунодефицита на момент начала лечения. У пациентов, начинающих лечение на фоне тяжелого иммунодефицита (CD4
Современная медикаментозная терапия ревматоидного артрита
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает 0,5–2% от общей численности населения в промышленно развитых странах [1, 2]. У больных ревматоидным артритом наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [3]. Трудно переоценить колоссальный ущерб, наносимый этим заболеванием обществу за счет ранней инвалидизации пациентов, которая при отсутствии своевременно начатой активной терапии может наступать в первые 5 лет от дебюта болезни.
Ревматоидный артрит — хроническое воспалительное заболевание неясной этиологии, для которого характерно поражение периферических синовиальных суставов и периартикулярных тканей, сопровождающееся аутоиммунными нарушениями и способное приводить к деструкции суставного хряща и кости, а также к системным воспалительным изменениям.
Патогенез заболевания весьма сложен и во многом недостаточно изучен. Несмотря на это, к настоящему времени хорошо известны некоторые ключевые моменты в развитии ревматоидного воспаления, которые определяют основные методы лечебного воздействия на него (рис. 1). Развитие хронического воспаления в данном случае связано с активацией и пролиферацией иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов), что сопровождается выделением клеточных медиаторов — цитокинов, факторов роста, молекул адгезии, а также синтезом аутоантител (например, антицитруллиновых антител) и формированием иммунных комплексов (ревматоидные факторы). Эти процессы ведут к формированию новых капиллярных сосудов (ангиогенез) и разрастанию соединительной ткани в синовиальной оболочке, к активации циклооксигеназы-2 (ЦОГ-2) с повышением синтеза простагландинов и развитием воспалительной реакции, к выделению протеолитических ферментов, активации остеокластов, а в результате — к деструкции нормальных тканей суставов и возникновению деформаций.
Лечение ревматоидного артрита
Исходя из патогенеза заболевания, становится очевидным, что эффективно воздействовать на развитие заболевания можно на двух уровнях:
Поскольку, помимо собственно воспаления, активация иммунной системы сопровождается многими другими патологическими процессами, воздействие на первом уровне является существенно более глубоким и эффективным, нежели на втором. Медикаментозная иммуносупрессия представляет собой основу лечения ревматоидного артрита. К иммуносупрессорам, применяющимся для лечения данного заболевания, относятся базисные противовоспалительные препараты (БПВП), биологические препараты и глюкокортикостероиды. На втором уровне действуют нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды.
В целом иммуносупрессивная терапия сопровождается более медленным развитием клинического эффекта (в широких рамках — от нескольких дней в случае биологической терапии до нескольких месяцев в случае применения некоторых БПВП), который в то же время бывает очень выраженным (вплоть до развития клинической ремиссии) и стойким, а также характеризуется торможением деструкции суставов.
Собственно противовоспалительная терапия (НПВП) может давать клинический эффект (обезболивание, уменьшение скованности) очень быстро — в течение 1–2 ч, однако при помощи такого лечения практически невозможно полностью купировать симптоматику при активном ревматоидном артрите и, по-видимому, оно совсем не влияет на развитие деструктивных процессов в тканях.
Глюкокортикостероиды обладают как иммуносупрессивным, так и непосредственным противовоспалительным эффектом, поэтому клиническое улучшение может развиваться быстро (в течение нескольких часов при внутривенном или внутрисуставном введении). Имеются данные о подавлении прогрессирования эрозивного процесса в суставах при длительной терапии низкими дозами глюкокортикостероидов и о положительном их влиянии на функциональный статус больного. В то же время из практики хорошо известно, что назначение только глюкокортикостероидов, без других иммуносупрессивных средств (БПВП), редко дает возможность достаточно эффективно контролировать течение болезни.
Немедикаментозные способы терапии ревматоидного артрита (физиотерапия, бальнеотерапия, диетотерапия, акупунктура и др.) представляют собой дополнительные методики, с помощью которых можно несколько улучшить самочувствие и функциональный статус пациента, но не купировать симптоматику и достоверно повлиять на деструкцию суставов.
Ортопедическое лечение, включающее ортезирование и хирургическую коррекцию деформаций суставов, а также реабилитационные мероприятия (лечебная физкультура и др.) имеют особое значение преимущественно на поздних стадиях заболевания для поддержания функциональной способности и улучшения качества жизни больного.
Основными целями лечения при РА являются [2, 6]:
Надо иметь в виду, что цели лечения могут существенно изменяться в зависимости от длительности болезни. На ранней стадии болезни, т. е. при длительности болезни 6–12 мес, достижение клинической ремиссии — вполне реальная задача, так же как и торможение развития эрозий в суставах. С помощью современных методов активной медикаментозной терапии удается добиться ремиссии у 40–50% пациентов [4, 5], показано также отсутствие появления новых эрозий по данным рентгенографии [7] и магнитно-резонансной томографии [8] у значительного количества больных при длительности наблюдения 1–2 года.
При длительно текущем ревматоидном артрите, особенно при недостаточно активной терапии в первые годы заболевания, достижение полной ремиссии теоретически тоже возможно, однако вероятность этого значительно ниже. То же самое можно сказать и о возможности остановить прогрессирование деструкции в суставах, уже существенно разрушенных за несколько лет болезни. Поэтому при далеко зашедшем ревматоидном артрите возрастает роль реабилитационных мероприятий, ортопедической хирургии. Кроме того, на поздних стадиях заболевания длительная поддерживающая базисная терапия может использоваться для вторичной профилактики осложнений болезни, таких как системные проявления (васкулит и др.), вторичный амилоидоз.
Базисная терапия ревматоидного артрита. БПВП (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) являются главным компонентом лечения ревматоидного артрита и при отсутствии противопоказаний должны быть назначены каждому пациенту с этим диагнозом [9]. Особенно важно максимально быстрое назначение БПВП (сразу после установления диагноза) на ранней стадии, когда имеется ограниченный период времени (несколько месяцев от появления симптоматики) для достижения наилучших отдаленных результатов — так называемое «терапевтическое окно» [10].
Классические БПВП обладают следующими свойствами.
БПВП существенно различаются между собой по механизму действия и особенностям применения. Основные параметры, характеризующие БПВП, представлены в таблице 1.
БПВП условно могут быть подразделены на препараты первого и второго ряда. Препараты первого ряда обладают наилучшим соотношением эффективности (достоверно подавляют как клиническую симптоматику, так и прогрессирование эрозивного процесса в суставах) и переносимости, в связи с чем назначаются большинству пациентов.
К БПВП первого ряда относятся следующие.
БПВП второго ряда применяются значительно реже в связи с меньшей клинической эффективностью и/или большей токсичностью. Они назначаются, как правило, при неэффективности или непереносимости БПВП первого ряда.
БПВП способны вызвать значительное улучшение (хороший клинический ответ) приблизительно у 60% пациентов. В связи с медленным развитием клинического эффекта назначение БПВП на сроки менее 6 мес не рекомендуется. Длительность лечения определяется индивидуально, типичная продолжительность «курса» лечения одним препаратом (в случае удовлетворительного ответа на терапию) составляет 2–3 года и более. Большинство клинических рекомендаций подразумевают неопределенно долгое применение поддерживающих дозировок БПВП для сохранения достигнутого улучшения.
При недостаточной эффективности монотерапии каким-либо базисным препаратом может быть избрана схема комбинированной базисной терапии, т. е. сочетания двух-трех БПВП. Наиболее хорошо зарекомендовали себя следующие сочетания:
В комбинированных схемах препараты обычно применяются в средних дозировках. В ряде клинических исследований было продемонстрировано превосходство комбинированной базисной терапии над монотерапией, однако более высокая эффективность комбинированных схем не считается строго доказанной. Комбинация БПВП ассоциирована с умеренным повышением частоты побочных эффектов.
Биологические препараты в лечении ревматоидного артрита. Термин биологические препараты (от англ. biologics) применяется по отношению к лекарственным средствам, производимым с использованием биотехнологий и осуществляющим целенаправленное («точечное») блокирование ключевых моментов воспаления с помощью антител или растворимых рецепторов к цитокинам, а также другим биологически активным молекулам. Таким образом, биологические препараты не имеют никакого отношения к «биологически активным пищевым добавкам». В связи с большим количеством «молекул-мишеней», воздействие на которые потенциально может подавлять иммунное воспаление, разработан целый ряд лекарственных средств из этой группы и еще несколько препаратов проходят клинические испытания.
К основным зарегистрированным в мире для лечения ревматоидного артрита биологическим препаратам относятся:
Для биологических препаратов характерны выраженный клинический эффект и достоверно доказанное торможение деструкции суставов. Эти признаки позволяют относить биологические препараты к группе БПВП. В то же время особенностью группы является быстрое (нередко в течение нескольких дней) развитие яркого улучшения, что объединяет биологическую терапию с методами интенсивной терапии. Характерная черта биологических средств — потенцирование эффекта в сочетании с БПВП, в первую очередь с метотрексатом. В связи с высокой эффективностью при ревматоидном артрите, в том числе у резистентных к обычной терапии пациентов, в настоящее время биологическая терапия выдвинулась на второе по значимости место (после БПВП) в лечении этого заболевания.
К отрицательным сторонам биологической терапии относятся:
Биологические методы терапии показаны, если лечение препаратами из группы БПВП (такими, как метотрексат) не является адекватным вследствие недостаточной эффективности или неудовлетворительной переносимости.
Одной из наиболее важных молекул-мишеней служит ФНО-a, который имеет множество провоспалительных биологических эффектов и способствуют персистенции воспалительного процесса в синовиальной оболочке, деструкции хряща и костной ткани за счет прямого действия на синовиальные фибробласты, хондроциты и остеокласты. Блокаторы ФНО-α являются наиболее широко применяемыми биологическими средствами в мире.
В России зарегистрирован препарат из этой группы инфликсимаб (ремикейд), представляющий собой химерное моноклональное антитело к ФНО-α. Препарат, как правило, назначается в сочетании с метотрексатом. У пациентов с недостаточной эффективностью терапии средними и высокими дозами метотрексата инфликсимаб существенно улучшает ответ на лечение и функциональные показатели, а также приводит к выраженному торможению прогрессирования сужения суставной щели и развития эрозивного процесса.
Показанием к назначению инфликсимаба в комбинации с метотрексатом является неэффективность одного или более БПВП, применявшихся в полной дозе (в первую очередь метотрексата), с сохранением высокой воспалительной активности (пять и более припухших суставов, скорость оседания эритроцитов (СОЭ) более 30 мм/ч, С-реактивный белок (СРБ) более 20 мг/л). При раннем ревматоидном артрите с высокой воспалительной активностью и быстрым нарастанием структурных нарушений в суставах комбинированная терапия метотрексатом и инфликсимабом может быть назначена сразу.
До назначения инфликсимаба требуется провести скрининговое обследование на туберкулез (рентгенография грудной клетки, туберкулиновая проба). Рекомендуемая схема применения: начальная доза 3 мг/кг массы тела больного в/в капельно, затем по 3 мг/кг массы тела через 2, 6 и 8 нед, далее по 3 мг/кг массы тела каждые 8 нед, при недостаточной эффективности доза может повышаться вплоть до 10 мг/кг массы тела. Длительность лечения определяется индивидуально, обычно не менее 1 года. После отмены инфликсимаба поддерживающая терапия метотрексатом продолжается. Следует иметь в виду, что повторное назначение инфликсимаба после окончания курса лечения этим препаратом ассоциировано с повышенной вероятностью реакций гиперчувствительности замедленного типа.
Вторым зарегистрированным в нашей стране препаратом для проведения биологической терапии является ритуксимаб (мабтера). Действие ритуксимаба направлено на подавление В-лимфоцитов, которые не только являются ключевыми клетками, отвечающими за синтез аутоантител, но и выполняют важные регуляторные функции на ранних стадиях иммунных реакций. Препарат обладает выраженной клинической эффективностью, в том числе у больных, недостаточно отвечающих на терапию инфликсимабом.
Для лечения ревматоидного артрита препарат применяется в дозе 2000 мг на курс (две инфузии по 1000 мг, каждая с промежутком в 2 нед). Ритуксимаб вводится внутривенно медленно, рекомендуется проведение инфузии в условиях стационара с возможностью точного контроля за скоростью введения. Для профилактики инфузионных реакций целесообразно предварительное введение метилпреднизолона 100 мг. При необходимости возможно проведение повторного курса инфузий ритуксимаба через 6–12 мес.
Согласно европейским клиническим рекомендациям, ритуксимаб целесообразно назначать в случаях неэффективности или невозможности проведения терапии инфликсимабом. Возможность применения ритуксимаба в качестве первого биологического препарата служит в настоящее время предметом исследований.
Глюкокортикостероиды. Глюкокортикостероиды обладают многогранным противовоспалительным действием, обусловленным блокадой синтеза провоспалительных цитокинов и простагландинов, а также торможением пролиферации за счет воздействия на генетический аппарат клеток. Глюкокортикостероиды оказывают быстрый и ярко выраженный дозозависимый эффект в отношении клинических и лабораторных проявлений воспаления. Применение глюкокортикостероидов чревато развитием нежелательных реакций, частота которых также повышается с увеличением дозы препарата (стероидный остеопороз, медикаментозный синдром Иценко–Кушинга, поражение слизистой ЖКТ). Эти препараты сами по себе в большинстве случаев не могут обеспечить полноценного контроля над течением ревматоидного артрита и должны назначаться вместе с БПВП.
Глюкокортикостероиды при данном заболевании применяются системно и локально. Для системного применения показан основной метод лечения — назначение низких доз внутрь (преднизолон — до 10 мг/сут, метилпреднизолон — до 8 мг/сут) на длительный период при высокой воспалительной активности, полиартикулярном поражении, недостаточной эффективности БПВП.
Средние и высокие дозы глюкокортикостероидов внутрь (15 мг/сут и более, обычно 30–40 мг/сут в пересчете на преднизолон), а также пульс-терапия глюкокортикостероидами — внутривенное введение высоких доз метилпреднизолона (250–1000 мг) или дексаметазона (40–120 мг) могут применяться для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.), а также некоторых особых форм болезни. Продолжительность лечения определяется временем, необходимым для купирования симптоматики, и составляет обычно 4–6 нед, после чего осуществляется постепенное ступенчатое снижение дозы с переходом на лечение низкими дозами глюкокортикостероидов.
Глюкокортикостероиды в средних и высоких дозах, пульс-терапия, по-видимому, не обладают самостоятельным влиянием на течение ревматоидного артрита и развитие эрозивного процесса в суставах.
Для локальной терапии применяются препараты в микрокристаллической форме, назначающиеся в виде внутрисуставных и периартикулярных инъекций: бетаметазон, триамсинолон, метилпреднизолон, гидрокортизон.
Глюкокортикостероиды для локального применения обладают ярко выраженным противовоспалительным действием, преимущественно в месте введения, а в ряде случаев — и системным действием. Рекомендуемые суточные дозы составляют: 7 мг — для бетаметазона, 40 мг — для триамсинолона и метилпреднизолона, 125 мг — для гидрокортизона. Эта доза (суммарно) может использоваться для внутрисуставного введения в один крупный (коленный) сустав, два сустава среднего размера (локтевые, голеностопные и др.), 4–5 мелких суставов (пястно-фаланговые и др.), либо для периартикулярного введения препарата в 3–4 точки.
Эффект после однократного введения обычно наступает на протяжении 1–3 дней и сохраняется в течение 2–4 нед при хорошей переносимости.
В связи с этим повторные инъекции глюкокортикостероидов в один сустав нецелесообразно назначать ранее чем через 3–4 недели. Проведение курса из нескольких внутрисуставных инъекций в один и тот же сустав не имеет терапевтического смысла и чревато осложнениями (локальный остеопороз, усиление деструкции хряща, остеонекроз, нагноение). В связи с повышенным риском развития остеонекроза внутрисуставное введение глюкокортикостероидов в тазобедренный сустав в целом не рекомендуется.
Глюкокортикостероиды для локального применения назначаются в качестве дополнительного метода купирования обострений ревматоидного артрита и не могут служить заменой системной терапии.
НПВП. Значение НПВП в лечении ревматоидного артрита за последние годы существенно снизилось в связи с появлением новых эффективных схем патогенетической терапии. Противовоспалительное действие НПВП достигается с помощью подавления активности ЦОГ, или избирательно ЦОГ-2, и тем самым снижается синтез простагландинов. Таким образом НПВП действуют на конечное звено ревматоидного воспаления.
Действие НПВП при ревматоидном артрите — уменьшение выраженности симптомов болезни (боль, скованность, припухлость суставов). НПВП обладают обезболивающим, противовоспалительным, жаропонижающим эффектом, но мало влияют на лабораторные показатели воспаления. В подавляющем большинстве случаев НПВП не способны как-либо заметно изменить течение заболевания. Их назначение в качестве единственного противоревматического средства при достоверном диагнозе ревматоидный артрит в настоящее время считается ошибкой. Тем не менее НПВП являются основным средством симптоматической терапии при данном заболевании и в большинстве случаев назначаются в сочетании с БПВП.
Наряду с лечебным эффектом, все НПВП, включая селективные (ингибиторы ЦОГ-2), способны вызывать эрозивно-язвенное поражение ЖКТ (в первую очередь верхних его отделов — «НПВП-гастропатия») с возможными осложнениями (кровотечения, перфорации и пр.), а также нефротоксические и другие нежелательные реакции.
Основные характерные черты, которые необходимо учитывать при назначении НПВП, следующие.
Существует индивидуальная чувствительность к различным НПВП как в отношении эффективности, так и переносимости лечения. Дозы НПВП при ревматоидном артрите соответствуют стандартным. Продолжительность лечения НПВП определяется индивидуально и зависит от потребности больного в симптоматической терапии. При хорошем ответе на терапию БПВП препарат из группы НПВП может быть отменен.
К наиболее часто применяющимся при ревматоидном артрите НПВП относятся:
Селективные НПВП, по эффективности достоверно не отличаясь от неселективных, реже вызывают НПВП-гастропатии и серьезные нежелательные реакции со стороны ЖКТ, хотя и не исключают развитие этих осложнений. Ряд клинических исследований продемонстрировал повышенную вероятность развития тяжелой сосудистой патологии (инфаркт миокарда, инсульт) у пациентов, получавших препараты из группы коксибов, в связи с чем возможность лечения целекоксибом должна обсуждаться с особой осторожностью у больных с ИБС и другими серьезными кардиоваскулярными патологиями.
Дополнительные медикаментозные методы лечения. В качестве симптоматического анальгетика (или дополнительного анальгетика при недостаточной эффективности НПВП) может использоваться парацетамол (ацетаминофен) в дозе 500–1500 мг/сут, который обладает относительно невысокой токсичностью. Для локальной симптоматической терапии используются НПВП в виде гелей и мазей, а также диметилсульфоксид в виде 30–50% водного раствора в форме аппликаций. При наличии остеопороза показано соответствующее лечение препаратами кальция, витамина Д3, бифосфонатами, кальцитонином.
Общие принципы ведения больных РА
Больному с установленным диагнозом ревматоидный артрит должен быть назначен препарат из группы БПВП, который при хорошем клиническом эффекте может применяться как единственный метод терапии [9]. Другие лечебные средства используются по мере необходимости.
Больной должен быть информирован о характере своего заболевания, течении, прогнозе, необходимости длительного сложного лечения, а также о возможных нежелательных реакциях и схеме контроля за лечением, неблагоприятных сочетаниях с другими препаратами (в частности, алкоголем), возможной активации очагов хронической инфекции на фоне лечения, целесообразности временной отмены иммуносупрессивных препаратов при возникновении острых инфекционных заболеваний, о необходимости контрацепции на фоне лечения.
Терапия ревматоидного артрита должна назначаться врачом-ревматологом и проводиться под его наблюдением. Лечение биологическими препаратами может проводиться только под контролем ревматолога, имеющего достаточные знания и опыт для его проведения. Терапия является длительной и подразумевает периодический контроль активности болезни и оценку ответа на терапию. Упрощенный алгоритм представлен на рисунке 2.
Мониторинг активности болезни и ответа на терапию включает оценку показателей суставного статуса (число болезненных и припухших суставов и др.), острофазовых показателей крови (СОЭ, СРБ), оценку боли и активности болезни по визуальной аналоговой шкале, оценку функциональной активности больного в повседневной деятельности с помощью русского варианта опросника состояния здоровья (HAQ). Существуют признанные международным сообществом ревматологов методики количественной оценки ответа на лечение с помощью рекомендованного Европейской лигой по борьбе с ревматизмом (EULAR) индекса DAS (Disease Activity Score) и критериев Американской коллегии ревматологов (ACR) [1]. Кроме того, должен осуществляться мониторинг безопасности проводимой пациенту терапии (в соответствии и формуляром и существующими клиническими рекомендациями). В связи с тем, что эрозивный процесс может развиваться даже при низкой воспалительной активности, помимо оценки активности болезни и ответа на терапию обязательно применяется рентгенография суставов. Прогрессирование деструктивных изменений в суставах оценивают путем стандартной рентгенографии кистей и стоп с использованием рентгенологической классификации стадий ревматоидного артрита, количественных методик по индексам Sharp и Larsen. С целью мониторинга состояния больного обследование рекомендуется проводить с определенной периодичностью (табл. 2).
Лечение резистентного к терапии РА
Резистентным к лечению целесообразно считать пациента с неэффективностью (отсутствием 20% улучшения по основным показателям) как минимум двух стандартных БПВП в достаточно высоких дозах (метотрексат — 15–20 мг/нед, сульфасалазин — 2000 мг/сут, лефлуномид — 20 мг/сут). Неэффективность может быть первичной и вторичной (возникающей после периода удовлетворительного ответа на терапию либо при повторном назначении препарата). Существуют следующие пути преодоления резистентности к терапии:
С точки зрения отдаленных результатов в отношении функциональных нарушений, качества жизни и ее продолжительности оптимальной стратегией терапии ревматоидного артрита является многолетнее лечение БПВП с планомерной сменой схемы их применения по мере необходимости [11].
Литература
Д. Е. Каратеев, доктор медицинских наук
Институт ревматологии РАМН, Москва