Мутация генов фолатного цикла что это такое при беременности
Среди важнейших задач современного акушерства все еще остается очень актуальным поиск возможных причин и диагностических маркеров невынашивания беременности. Огромная значимость проблемы невынашивания беременности заключается в высоком уровне частоты встречаемости внутриутробной гибели плода и/или аномалии развития и, к сожалению, отсутствия снижения данной патологии [1].
Важную и неоспоримую значимость имеет выявление носительства полиморфных и мутационных вариантов генов, а профилактика и своевременная коррекция патологических проявлений мутантных генов обеспечивает нормальное течение беременности. Кроме того при оценке рисков по данным зарубежных авторов огромное значение имеет не только анализ влияния отдельных аллелей полиморфных генов, но и необходимо детально подходить к изучению их комбинаций, так как именно комбинация в свою очередь формирует генетическую предрасположенность организма женщины к невынашиванию беременности [2].
Научная литература последних лет накопила опыт многочисленных исследований и данных клинических исследований, позволяющих выделить дефицит фолиевой кислоты, повышенный уровень гомоцистеина и полиморфизмы аллелей генов фолатного цикла, отдельной группой причин, которые потенцируют развитие разнообразной акушерской патологии. Именно поэтому остаются интересными научные исследования, посвященные выявлению носительства полиморфных вариантов генов, у женщин с неблагоприятным исходом беременности [3].
Мультифакторные заболевания отличаются тем, что одномоментно воздействие на организм происходит группой патологических и нормальных аллелей генов и вмешательство неблагоприятных условий окружающей среды, что и приводит к развитию различной патологии. Поэтому такие гены и были названы генами «предрасположенности». Однако до настоящего времени все еще изучение и анализ мультифакторных заболеваний с позиции рассмотрения влияния полиморфизма генов на возникающую патологию остается трудной задачей [4].
При этом в литературных данных последних лет акцент уделяется тому, что гены «предрасположенности», конечно же, определяют высокую вероятность развития различной акушерской патологии, но не всегда они передаются потомству [5].
Из этого следует, что исследования, посвященные изучению взаимосвязи различных функций организма с полиморфизмом аллелей различных генов, имеют огромное медико-социальное значение, а полученные авторами результаты лягут в основу прогнозирования различных клинических осложнений для каждого отдельно взятого полиморфизма генов [6].
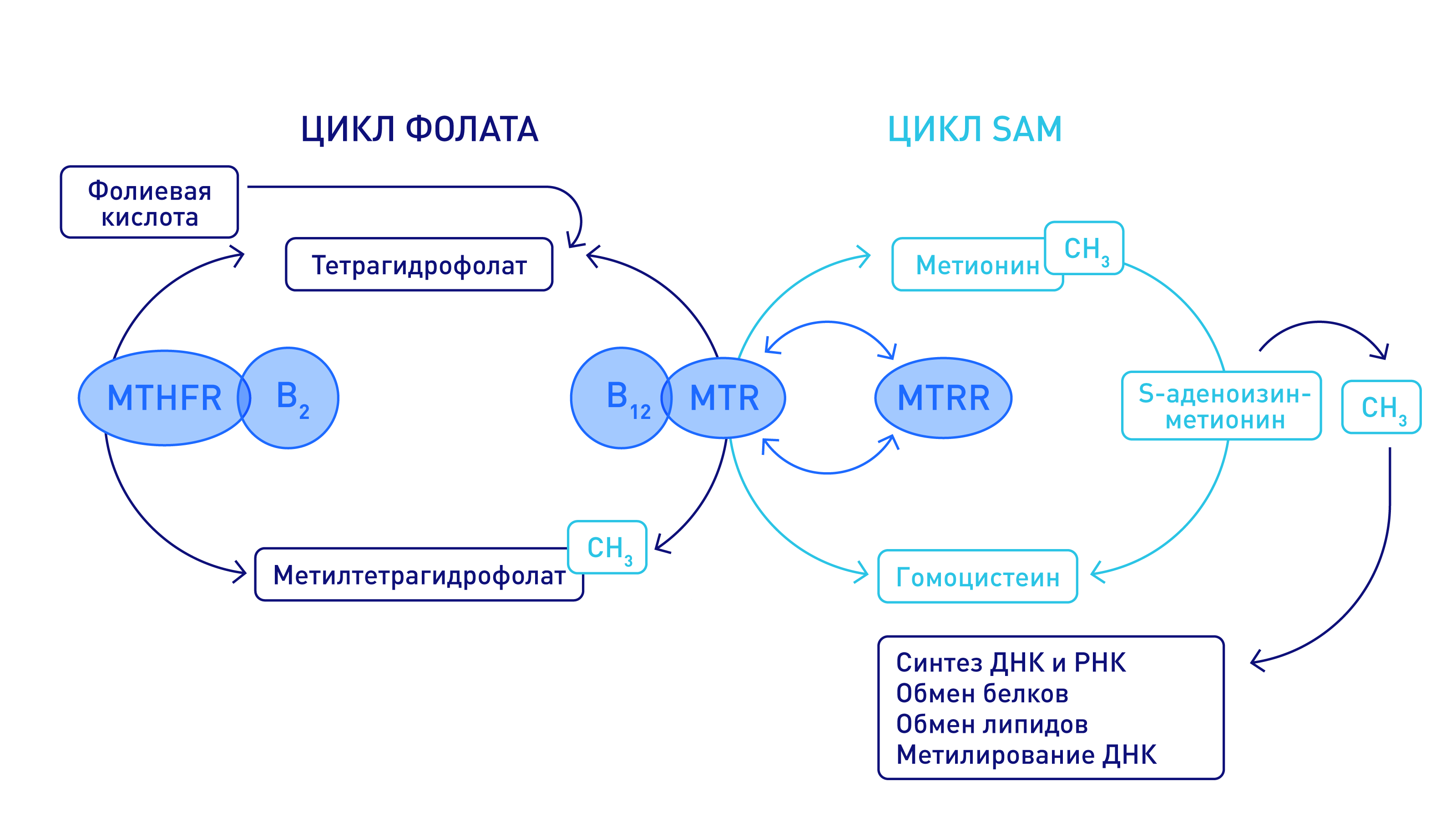
Фолатный цикл – это сложный каскадный процесс, в котором задействовано множество различных ферментов. Основные ферменты, обеспечивающие превращение фолиевой кислоты на различных этапах всего цикла – MTHFR, MTRR, MTR, литературные данные подчеркивают важную роль этих ферментов в поддержании нормального уровня гомоцистеина, а при снижении их активности происходит накопление и избыток гомоцистеина в организме [7].
Подчеркивая огромную роль и важность фолиевой кислоты в метаболизме нуклеиновых кислот, в процессах пролиферации и дифференциации быстро делящихся клеток эмбриона, следует отметить, что нарушения в фолатном цикле крайне опасны [8].
Поэтому исследования, посвященные ранней досимптоматической диагностике нарушений гестации, позволят разработать профилактически направленную терапию и не дать болезни проявиться. Особенно это актуально для женщин с генетической предрасположенностью [5].
Учитывая полную неизученность данного вопроса в Кыргызской Республике, изучение роли полиморфизма генов фолатного цикла у женщин с невынашиванием беременности в анамнезе с позиций предиктового акушерства представляет огромный научный интерес.
Цель исследования: изучить носительство различных полиморфизмов генов фолатного цикла у женщин с невынашиванием беременности.
Материалы и методы исследования
Проведено проспективное когортное исследование на базе Национального центра охраны материнства и детства (НЦОМиД) МЗ КР в 2015–2017 гг.
В исследование включены 127 беременных женщин, которые были разделены на 2 группы: 1-я группа (основная) – 74 женщины с невынашиванием беременности в анамнезе и 2-я группа (контрольная) – 53 условно здоровых женщин.
Средний возраст беременных женщин в основной группе составил 29,9 ± 2,5 на 100 обследованных, в группе контроля – 29,1 ± 2,5 соответственно, статистически значимой разницы в группах не выявлено, р > 0,005, т.е. группы сопоставимы.
В целях выявления генетической предрасположенности к невынашиванию беременности отобраны 4 полиморфных варианта генов метаболизма фоливой кислоты и витамина В12 – MTHFR, MTR и MTRR, ассоциированные с гипергомоцистеинемией и фолиево-дефицитными состояниями (табл. 1).
Гены фолатного цикла. Где миф, а где реальность?
Разбираемся, что такое фолатный цикл, зачем он нужен, какие в нем участвуют гены и почему о них можно не беспокоиться.
Фолатный цикл, или обмен витаминов В9 и В12, влияет на многие жизненно важные процессы, включая строительство ДНК и работу генов. Сбои в работе фолатного цикла связывают с целым рядом болезней: от инфаркта или инсульта до анемии и осложнений при беременности.
В этом сложном процессе участвует целый ряд ферментов, а также производные фолиевой кислоты или витамина В9. Гены, кодирующие эти ферменты, часто называют генами фолатного цикла. В них могут быть варианты, которые меняют активность и устойчивость ферментов. Анализ генов фолатного цикла может выявить эти варианты и указать на возможные проблемы. Однако связь между вариантами генов и развитием болезней до сих пор не доказана.
Содержание:
Эта статья носит исключительно образовательный и информационный характер и не может быть использована для диагностики или лечения, а также для замены профессиональных рекомендаций.
Зачем нужны гены фолатного цикла

Что можно узнать из генетического теста
Эти ферменты участвуют на разных этапах реакции восстановления фолатов, к которым относятся, например, витамины В9 и В12. Главная цель этой реакции — получить от фолатов как можно больше СН3 метильных групп и обезвредить гомоцистеин.
Это промежуточный продукт обмена фолатов и метионина — исходного материала для реакций метилирования или переноса метильной группы (СН3). Этот процесс очень важен для работы организма: метилирование ДНК регулирует работу генов, а фолатный цикл как бы расставляет «выключатели» в нужных местах генома.
За счет этого генетическая информация сохраняется и считывается лучше, а разные клетки организма синтезируют не все белки подряд, а только те, которые нужны им сейчас. Например, клетки слизистой оболочки желудка синтезируют пищеварительные ферменты. А вот у меланоцитов в коже геном тот же, но гены пищеварительных ферментов выключены и вместо них синтезируется меланин, который дает нам загар.
Основные функции трех генов фолатного цикла:
| Название гена | Название фермента | Функция |
|---|---|---|
| MTHFR | Метилентетрагидрофо-латредуктаза | Участвует в подготовке кофактора — активной формы фолиевой кислоты В9 для синтеза метионина из гомоцистеина |
| MTR | Метионин-синтаза | Участвует в реакции синтеза метионина из гомоцистеина с помощью В12 |
| MTRR | Метионин-синтаза-редуктаза | Поддерживает активность метионин-синтазы и обеспечивает непрерывную утилизацию гомоцистеина |
Откуда про эти гены столько мифов
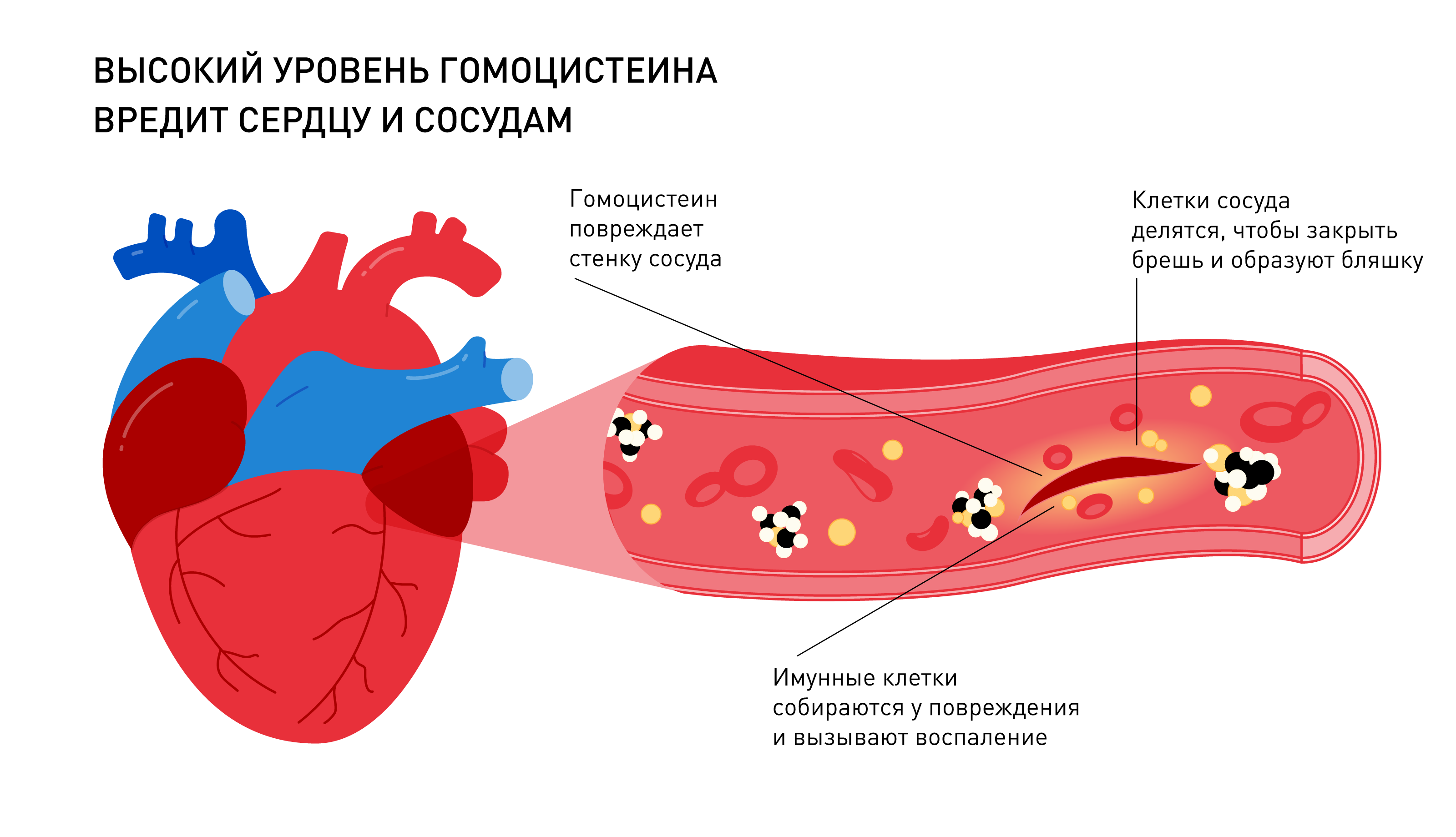
Из-за нарушений в работе фолатного цикла в организме может накапливаться гомоцистеин — производное метионина. В концентрации сильно выше лабораторных норм гомоцистеин повреждает сосуды и нейроны. Его высокое содержание в крови связывают со многими патологиями: ишемической болезнью сердца, инфарктом, атеросклерозом, болезнью Альцгеймера, анемией, тромбозом.

Как генетическое тестирование помогает при планировании семьи
Первые данные о влиянии гомоцистеина на здоровье появились в 1962 году, когда было описано редкое наследственное заболевание гомоцистинурия. Для этого состояния характерен высокий уровень гомоцистеина, который вызывает серьезную задержку в психическом развитии из-за неправильной работы гена СВS. Впервые повышение уровня гомоцистеина и развитие тромбоза в детстве было связано со сбоями в работе фермента MTHFR в 1991 году. А в 1995 были обнаружены варианты в гене MTHFR, которые влияют на активность фермента.
В итоге родилась теория о том, что варианты генов фолатного цикла могут приводить к высокому уровню гомоцистеина из-за нарушений в работе ферментов. Следовательно, наличие таких вариантов могло оказаться ценным маркером для диагностики и предотвращения различных заболеваний: от бесплодия до рака.
Сотни ученых искали взаимосвязь между патологиями и разными вариантами генов, и такая корреляция была найдена. Без достаточных доказательств клинического значения, на основании этой взаимосвязи анализ генов фолатного цикла стали предлагать пациентам.
Правда о генах фолатного цикла
Анализ генов фолатного цикла не входит в рекомендации большинства мировых генетических сообществ и клинических организаций. А если внимательно присмотреться к его научной базе, оказывается, что доказательств связи между вариантами этих генов и заболеваниями недостаточно.
Основная проблема в том, что полиморфизмы или варианты генов — далеко не единственная причина повышения уровня гомоцистеина в крови. Это справедливо только для редких случаев гомоцистинурии, а в остальном нельзя не учитывать диету, образ жизни и целый ряд других показателей обмена веществ.
Комплексных исследований, доказывающих связь болезней помимо гомоцистинурии с мутациями, пока нет. А опубликованные результаты не всегда согласуются друг с другом.
В 2018 году вышел большой критический обзор исследований, посвященных гену MTHFR. Авторы обзора пришли к выводу, что клинического значения мутаций генов фолатного цикла недостаточно, чтобы руководствоваться этим при ведении серьезных заболеваний. Сравнивая различные статьи по этой теме, ученые обнаружили методологические ошибки и нестыковки в данных.
Например, большинство исследований рассматривает небольшие выборки жителей Азии. При этом в других популяциях похожие связи не прослеживаются. Кроме того, публикаций с опровержением этого мифа может быть мало из-за академической предвзятости к негативным результатам исследований. Похожая ситуация и с другими двумя генами: MTRR и MTR.
Рекомендации
Профессиональные ассоциации генетиков и ключевые клинические организации в мире советуют обходиться без тестирования генов фолатного цикла при постановке диагноза и выборе лечения.
| Организация | Рекомендации | Документ |
|---|---|---|
| American Heart Association | Гомоцистеин не следует использовать в оценке риска сердечно-сосудистых заболеваний. | Greenland et al. (2010). |
| American Congress of Obstetricians and Gynecologists | Из-за недостаточной связи между C677T полиморфизмом в гене MTHFR и любыми осложнениями беременности, включая риск венозной тромбоэмболии, скрининг мутаций MTHFR не рекомендуется. | American Congress of Obstetricians and Gynecologists (2013). |
| American College of Medical Genetics | Генетический анализ MTHFR не следует включать в клиническую оценку риска тромбоза или рецидивирующей потери беременности. | Hickey et al. (2013). |
Анализ генов фолатного цикла не помогает вылечить или предотвратить сердечно-сосудистые заболевания, психические расстройства и осложнения при беременности.
С Генетическим тестом Атлас можно узнать, какие из ваших генов действительно влияют на предрасположенность к заболеваниям. Анализ вариантов в гене MTHFR или других генах “фолатного цикла” (MTR, MTRR) намеренно не включен в интерпретацию результатов генетического теста.
Мутация генов фолатного цикла что это такое при беременности
Комплексное генетическое исследование, которое представляет собой анализ шести генетических маркеров, связанных с риском хромосомных аномалий и изолированных пороков развития у плода (болезни Дауна, других трисомий, незаращения нервной трубки и др.), а также с предрасположенностью к повышенной свертываемости крови у матери.
Потеря беременности на ранних сроках часто вызвана генетическими нарушениями плода и дефектами развития плаценты вследствие ее тромботического повреждения.
Какой биоматериал можно использовать для исследования?
Буккальный (щечный) эпителий, венозную кровь.
Как правильно подготовиться к исследованию?
Подготовки не требуется.
Общая информация об исследовании
Одной из ведущих причин невынашивания беременности на ранних сроках является генетический фактор. Особое место занимает предрасположенность к тромбофилии и гипергомоцистеинемии. Данное генетическое исследование включает в себя две группы генетических маркеров: гены факторов свертывания крови и гены метаболизма фолиевой кислоты и витамина В12.
При неосложненном течении беременности в системе гемостаза происходят изменения: усиливаются общекоагуляционные свойства крови (количество факторов свертывания крови увеличивается в 1,5-2 раза) и снижается антикоагулянтный потенциал. Риск развития тромбофилического состояния повышается.
Микротромбозы при беременности – частая причина акушерской патологии (гестоза, плацентарной недостаточности, преждевременной отслойки нормально расположенной плаценты, привычной потери плода и др.).
Склонность к тромбообразованию несет угрозу в основном для плода: образующиеся сгустки крови нарушают кровообращение, и плод получает недостаточно питательных веществ. В результате может произойти прерывание беременности на раннем сроке, а также другие осложнения, связанные с повышенным свертыванием крови.
Наиболее частой причиной тромбофилии является мутация в гене фактора V свертывания крови, связанная с резистентностью к активированному протеину С, и мутация в гене протромбина (фактора II свертывания крови).
Мутации гена фактора свертываемости 5 (F5) среди причин синдрома потери плода отводят до 15 %. У женщин она в 8 раз повышает риск тромбозов в течение всей беременности и в 10 раз – риск преждевременной отслойки нормально расположенной плаценты.
Другой коагуляционный фактор (фактор II свертывания крови) – протромбин – один из главных компонентов свертывающей системы крови – в ходе его расщепления образуется тромбин. Данная реакция является первой стадией образования кровяных сгустков. Мутация в гене протромбина G20210A ассоциирована с риском тромбоэмболических осложнений во время беременности, который значительно возрастает при сопутствующей мутации фактора V.
Важно, что указанные риски сохраняются и в послеродовой период. Поэтому при принятии врачом решения о медикаментозной профилактике тромбоэмболических осложнений при наличии показаний ее следует применять не только на протяжении всей беременности, но и в послеродовом периоде.
Основными ферментами фолатного цикла, обеспечивающими превращение фолиевой кислоты на разных этапах цикла, являются MTHFR, MTRR, MTR. Известно, что снижение их активности – одна из важных причин накопления гомоцистеина в организме.
Повреждающее действие гомоцистеина на эндотелий сосудов и стимуляция тромбообразования могут приводить к таким осложнениям беременности, как преждевременная отслойка нормально расположенной плаценты, прерывание беременности, хроническая внутриутробная гипоксия плода и преэклампсия.
Дефицит ферментов, повышающий риск гипергомоцистеинемии и фолат-дефицитных состояний, возникает вследствие определенных мутаций в их генах.
При мутации в гене MTHFR развивается недостаток фермента метилентетрагидрофолатредуктазы (что нарушает метилирование ДНК), а гомоцистеин накапливается в избытке. Это состояние является наиболее частой генетической причиной повышенного уровня гомоцистеина.
При этом вероятность осложнений беременности повышается в сочетании с другими формами тромбофилии (мутация протромбина, фактора V Лейден и др.), поэтому их рекомендуется рассматривать в комплексе.
В расширенное комплексное исследование дополнительно к двум генетическим маркерам (MTHFR C677T и MTHFR A1298C), связанным с нарушением обмена фолатов, включены еще два – MTR A2756G и MTRR A66G, – которые кодируют ферменты, участвующие в метилировании, синтезе ДНК и белков и ответственны за превращение гомоцистеина в метионин.
В качестве кофактора в реакции превращения гомоцистеина в метионин принимает участие витамин В12 (кобаламин). Поэтому при сочетании патологических генотипов по данным генетическим маркерам и дефицита витамина В12 риск развития гипергомоцистеинемии и ее последствий возрастает.
Учитывая важную роль фолиевой кислоты в метаболизме нуклеиновых кислот, а следовательно, и в процессах пролиферации и дифференциации, нарушение фолатного цикла опасно для быстроделящихся клеток эмбриона.
Нехватка фолатов в пролиферирующих клетках ведет к разъединению нуклеотидов ДНК, способствует нарушению структуры ДНК и расхождения хромосом, повышению частоты хромосомных перестроек. Это повышает риск рождения детей с числовыми хромосомными аномалиями (например, с синдромом Дауна).
Гомоцистеин свободно переходит через плаценту и может оказывать тератогенное и фетотоксическое действие. Гипергомоцистеинемия является одной из причин дефектов развития нервной системы у плода, в частности анэнцефалии и незаращения костномозгового канала.
Изменение в гене MTHFR (генетический маркер C677T) связано не только с дефектами нервной трубки и с синдромом Дауна, но и с такими пороками развития плода, как расщелины губы и неба, пороки сердца.
Выявленные риски не свидетельствуют о генетических аномалиях у плода – они позволяют своевременно принять меры по недопущению последствий неблагоприятных генетических особенностей организма матери и обеспечить нормальное протекание беременности.
Витаминопрофилактика препаратами фолиевой кислоты и витаминами группы В, а также коррекция питания значительно снижает вероятность развития пороков нервной трубки у плода, а также нейтрализует избыточное количество гомоцистеина и, соответственно, его повреждающее действие.
Наследственная предрасположенность к любой акушерской патологии означает передачу потомству не самой патологии, а соответствующих аллелей генов, которые определяют вероятность развития этого заболевания.
Факторы риска развития тромбофилии и гипергомоцистеинемии:
Когда назначается исследование?
Что означают результаты?
Результатом генетического исследования являются генотипы, выявленные по каждому исследуемому генетическому маркеру, входящему в комплекс. На основании полученных генотипов составляется заключение о предрасположенности к раннему прерыванию беременности, при необходимости включающее в себя основные рекомендации по его профилактике.
Генетические маркеры
Генетический полиморфизм, ассоциированный с риском развития нарушений обмена гомоцистеина (фолатный цикл)
Фолиевая кислота – водорастворимый витамин B9, необходимый для роста и развития кровеносной и иммунной систем. Недостаток фолиевой кислоты может вызвать мегалобластную анемию у взрослых, а при беременности повышает риск развития дефектов нервной
трубки. Производные фолиевой кислоты называются фолатами. Животные и человек не синтезируют фолиевую кислоту, получая ее в основном вместе с пищей. Фолиевая кислота в больших количествах содержится в зеленых овощах с листьями, бобовых, в хлебе из муки грубого помола, дрожжах, печени. Во многих странах законодательство обязывает производителей мучных продуктов обогащать зерна фолиевой кислотой.
Группа соединений фолатов играет ведущую роль в широком спектре жизненно важных процессов:
Данные функции реализуются в процессе метаболизма фолатов, который составляет основу фолатного цикла.
Фолатный цикл – каскадный процесс, контролируемый ферментами, которые в качестве коферментов имеют производные фолиевой кислоты. Ключевым этапом в данном процессе является синтез метионина из гомоцистеина. Это достигается в процессе превращения фолатов: восстановления 5,10-метилентетрагидрофолата до 5-метилтетрагидрофолата, несущего метильную группу, которая необходима для превращения гомоцистеина в метионин. Восстановление фолатов происходит при участии фермента метилентетрагидрофолат-редуктазы (MTHFR). Метильная группа переносится на B12, который затем отдает ее гомоцистеину, образуя метионин с помощью фермента метионин-синтазы (MTR). Однако в некоторых случаях В12 может окисляться, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы (MTRR).
Нарушение фолатного цикла приводит к накоплению гомоцистеина в клетках и повышению общего уровня гомоцистеина в плазме крови. Главной формой фолата в плазме является 5-метилтетрагидрофолат, несущий на себе метильную группу, которая необходима для превращения гомоцистеина в метионин. Поскольку кобаламин (витамин B12) служит акцептором метильной группы 5-метилтетрагидрофолата, дефицит этого витамина приводит к «ловушке для фолата». Это тупиковый путь метаболизма, поскольку метилтетрагидрофолат не может восстанавливаться до тетрагидрофолата и возвращаться в фолатный пул.
Это приводит к истощению запаса метионина и выбросу в кровь избытка гомоцистеина, который
обладает атерогенным действием, гипертензивными свойствами, повышает гиперагрегацию тромбоцитов.
Кроме того, гомоцистеин свободно проходит через плаценту и оказывает тератогенное и фетотоксическое действие.
Нарушение метаболизма фолатов и повышение уровня гомоцистеина обусловливают повышенный
риск развития патологических процессов:
Нарушения фолатного цикла не оказывают изолированного влияния на возникновение венозных тромбозов при применении гормональной заместительной терапии и оральных контрацептивов, однако при наличии других тромбофилических полиморфизмов (особенно лейденской мутации и мутации гена протромбина: 20201 G>A) многократно усиливают их действие.
Причины нарушения фолатного цикла:
Анализ полиморфизмов в генах фолатного цикла позволяет определить предрасположенность
к указанным выше патологическим процессам и дает возможность своевременного принятия мер
посредством назначения корректирующей терапии.
П оказания к назначению профиля «Генетика метаболизма фолатов» :
Полиморфизм гена метионинсинтазы MTR(A2756G)
П оказания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, мегалобластная анемия, мутация MTRR.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(A1298C) (тератогенный фактор)
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности, дефект невральной трубки у плода в анамнезе.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена метилентетрагидрофолатредуктазы MTHFR(С677Т) (наследственная гипергомоцистеинемия)
Частота встречаемости гомозиготного носительства по данной мутации среди белого населения планеты составляет от 5 до 12 %. Гетерозиготная мутация С677Т наблюдается у 50% в популяции. Полиморфизм C677T связан, по крайней мере, с четырьмя группами многофакторных заболеваний: сердечно-сосудистыми заболеваниями (атеросклеротическое поражение сосудов, атеротромбоза и его осложнений), дефектами развития плода (дефект развития нервной трубки), колоректальной аденомой и раком молочной железы и яичника.
Показания к назначению: гипергомоцистеинемия, ИБС и инфаркт миокарда, атеросклероз и атеротромбоз, антифосфолипидный синдром, полипоз кишечника, колоректальная аденома и рак, мутации генов BRCA, цервикальная дисплазия, особенно в сочетании с папилломавирусной инфекцией.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена редуктазы метионинсинтазы MTRR(A66G) (тератогенный фактор)
Ген MTRR кодирует фермент метионинсинтазу редуктазу, участвующий в большом количестве биохимических реакций, связанных с переносом метильной группы. Одной из функций МСР является обратное превращение гомоцистеина в метионин. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин). Полиморфизм I22M A>G связан с аминокислотной заменой в молекуле фермента МСР. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска нарушений развития плода – дефектов невральной трубки. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма I22M A>G гена MTRR с полиморфизмом 677C-> T в гене MTHFR риск увеличивается. Полиморфизм I22M A->G гена MTRR также усиливает гипергомоцистеинемию, вызываемую полиморфизмом 677C-> T в гене MTHFR.
Показания к назначению: повторные эпизоды венозных тромбоэмболий в анамнезе, эпизоды тромбоэмболий во время беременности, в послеродовом периоде и во время приёма оральных контрацептивов, необъяснимая гибель плода во 2 или 3 триместрах беременности.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА