Выбор средств, влияющих на кашель, у детей с острыми инфекциями дыхательных путей
к.м.н., доцент Бовбель И.Э.
Назначение противокашлевых, отхаркивающих или муколитических средств является одним из основных направлений симптоматической терапии заболеваний респираторного тракта у детей и подростков. Широкий ассортимент лекарственных средств, влияющих на кашель, создает определенные трудности в выборе препарата для лечения.
Кашель (tussis) – сложный защитный рефлекс, направленный на выведение из дыхательных путей инородных веществ, поступающих с вдыхаемым воздухом и/или патологически измененного трахеобронхиального секрета. Раздражение нервных окончаний n.vagus, расположенных в дыхательных путях, и рецепторов плевры приводит к передаче нервных импульсов в кашлевой центр продолговатого мозга. Благодаря активизации кашлевого центра и при участии ретикулярной формации формируется ответная реакция – вдох, затем происходит синхронное сокращения мышц гортани, бронхов, грудной клетки, живота и диафрагмы при закрытой голосовой щели с последующим ее открытием и форсированным толчкообразным выдохом.
Инородные частицы и микроорганизмы, поступающие с вдыхаемым воздухом, осаждаются на слизистых респираторного тракта и в дальнейшем выводятся вместе со слизью. В физиологических условиях основным механизмом очищения трахеобронхиального дерева является мукоцилиарный клиренс и перистальтика мелких бронхов. Очищение дыхательных путей происходит благодаря скоординированной и содружественной деятельности реснитчатого эпителия трахеи и бронхов. В нормальных условиях кашель, в отличие от мукоцилиарного клиренса, не играет решающей роли в очищении дыхательных путей и имеет вспомогательное значение в процессах санации респираторного тракта.
Кашель и его характеристика
Основные причины кашля
У здоровых детей кашель отмечается крайне редко и может появляться только тогда, когда слизь во время сна скапливается в гортани. Возникновение кашля должно рассматриваться как проявление несостоятельности физиологических механизмов трахеобронхиального дерева.
Кашель является частым симптомом острых респираторных инфекций (ОРИ) тракта. При этом интенсивность и характер кашля варьируют от этиологического фактора, топики поражения респираторного тракта, периода заболевания, а также от индивидуальных особенностей организма.
При воспалительных заболеваниях верхних дыхательных путей (рините, синусите, аденоидите, гранулезном фарингите) кашель связан с раздражением кашлевых рецепторов придаточных пазух носа и гортани. Стекание слизистого или слизисто-гнойного отделяемого по задней стенке глотки, “подсушивание” слизистой оболочки глотки в связи с дыханием через рот приводят к появлению кашля, усиление которого происходит ночью и утром.
При ларингите кашель сухой, грубый (“лающий”), часто сочетается с осиплостью и реже с афонией, которые возникают в результате резкого отека голосовых связок и подслизистых пространств гортани. В начальном периоде острого трахеита и бронхита кашель обычно сухой и навязчивый, при трахеите может сопровождаться чувством давления или болями за грудиной. На второй неделе болезни кашель при этих заболеваниях, как правило, становится продуктивным, появляется тенденция к уменьшению его интенсивности и частоты. Кашель при пневмонии часто отрывистый, болезненный, при плеврите сопровождается локальной болезненностью. Продолжительность и интенсивность кашля во многом зависят от этиологии респираторного заболевания. Так, при микоплазменной и хламидийной инфекциях, несмотря на проведенную этиотропную терапию, кашель может сохраняться до 3-4 недель.
Длительно сохраняющийся кашель (более 3-х недель) требует исключения не только заболеваний инфекционно-воспалительного генеза, но и других состояний (инородное тело, аспирация и др.). Для диагностики причин кашля необходимо тщательно собрать анамнез, выяснить характер, интенсивность кашлевого синдрома.
Инородное тело в дыхательных путях проявляется внезапным развитием приступа кашля, нередко с цианозом и асфиксией. В дальнейшем приступы периодически возобновляются, кашель при этом частый, сухой, мучительный.
Кашель может возникать рефлекторно при заболеваниях сердца, пищевода, ЛОР-органов, в результате раздражения периферических рецепторов n.vagus. Хроническая аспирация пищи возникает нередко при трахео-пищеводном свище, гастро-эзофагельном рефлюксе, а также при органическом поражении ЦНС (бульбарные и псевдобульбарные нарушения). Характерным признаком этих патологических состояний является возникновение приступов сухого кашля во время или сразу после еды, нередко сопровождающихся цианозом.
Кашель является постоянным симптомом хронических неспецифических заболеваний легких, легочной формы муковисцидоза, врожденных пороков развития трахеи и бронхов (синдром Мунье-Куна, трахеобронхомаляции и бронхомаляции, синдром Вильямса-Кемпбела). Его интенсивность коррелирует с объемом поражения легочной ткани. Так, при поражении в пределах сегментов одной доли малопродуктивный кашель в период ремиссии бывает редким и непостоянным, отмечается обычно по утрам. В некоторых случаях при поражении 1-2-х легочных сегментов кашель появляется лишь при обострении воспалительного процесса. При распространенном процессе отмечается более постоянный кашель, иногда со значительным количеством мокроты.
В начальной стадии муковисцидоза малопродуктивный кашель непостоянен и возникает чаще в утреннее время. Однако со временем, при прогрессировании заболевания кашель становится постоянным, мучительным, приступообразным с трудно-отделяемой вязкой, густой, слизисто-гнойной мокротой.
При синдроме Мунье-Куна (трахеобронходилятации) в результате врожденной аномалии мышечной и эластичной ткани происходит расширение просвета трахеит и бронхов. Кашель при этом заболевании вибрирующий, постоянный, влажный с выделением большого количества слизисто-гнойной или гнойной мокроты. При трахеобронхомаляции и бронхомаляции – врожденной патологической мягкостью хрящевого каркаса стенок трахеи и крупных бронхов отмечаются (особенно при синдроме Вильямса-Кемпбела) симптомы тяжелого распространенного бронхита с постоянным влажным кашлем.
Наиболее частой и классической формой первичной цилиарной дискинезии, наследственного заболевания, является синдром Картагенера (обратное расположение внутренних органов, бронхоэктазы и синусит). Развитие воспалительного процесса связано с дисфункцией реснитчатого эпителия, выстилающего не только респираторный тракт, но также и средне и внутреннее ухо, эпендиму желудочков, фаллопиевы трубы. Бронхолегочные изменения при первичной цилиарной дискинезии сопровождаются постоянным кашлем с трудно-отделяемой слизистой или слизисто-гнойной мокротой.
Паразитарные заболевания легких у детей диагностируются редко. Легкие могут поражаться транзиторно при аскаридозе, эхинококкозе или служить местом окончательной локализации паразита (при парагонимозе). Кашель при этом влажный, мокрота слизистая, желтоватая, нередко с примесью крови.
Иммунодефицитные состояния у детей часто сопровождаются развитием хронических воспалительных процессов в бронхолегочной системе с постоянным кашлем, характеризующимся отхождением большого количества гнойной мокроты.
В ряде случаев кашель может быть связан с заболеваниями других органов и систем (центральной нервной системы, органов средостения и др.). Так, при патологическом возбуждении кашлевого центра в ЦНС развивается кашель центрального генеза. В ряде случаев кашель может отмечаться при невротических реакциях.
Роль кашля в санации дыхательных путей при воспалении респираторного тракта
Воздействие повреждающего инфекционного фактора (вирусы парагриппа, респираторно-синтициатльные, аденовирусы, внутриколеточно расположенные микроорганизмы и др.) на слизистые оболочки трахеи и бронхов вызывает острое воспаление, характеризующееся увеличением количества бокаловидных клеток, выделяющих слизистый секрет, при снижении санирующей и эвакуационной функций мерцательного эпителия. Установлено, что одновременно с гиперпродукцией слизи изменяется состав трахеобронхиального секрета – уменьшается удельный вес воды и повышается концентрация муцинов (нейтральных и кислых гликопротеинов), что ведет к увеличению вязкости мокроты.
Повышение вязкости секрета при воспалении респираторного тракта нарушает не только дренажную функцию бронхов, но также и местную защиту (снижается уровень секреторного IgA и других иммуноглобулинов, секретируемых плазматическими клетками слизистой оболочки дыхательных путей).
Таким образом, воспаление трахеи и бронхов приводит к нарушению мукоцилиарного клиренса, что не позволяет полноценно освобождать дыхательные пути от мокроты, и основным механизмом очищения дыхательных путей становится кашель.
В начале заболевания ОРИ кашель, как правило, сухой, непродуктивный или малопродуктивный, не приводящий к эффективному отхождению мокроты. Обычно к 3–4 дню кашель становится влажным, однако эвакуация бронхиального секрета нарушена вследствие повреждения мукоцилиарного эпителия.
Имеются особенности механизмов возникновения кашля при воспалении дыхательных путей у детей различного возраста. Так, в дошкольном возрасте непродуктивный кашель обусловлен повышением адгезивности бронхиального секрета, недостаточной активностью мерцательного эпителия бронхов и несостоятельностью сократительного аппарата бронхиол. Немалую роль играет недостаточность синтеза сурфактанта, особенно у недоношенных и детей первых месяцев жизни. Начиная с 5-6 летнего возраста, в механизмах возникновения кашля большое значение приобретает бронхоспазм и гиперреактивность бронхов.
Выбор терапии при кашле
Изучение механизмов возникновения непродуктивного кашля дерева при острых респираторных инфекциях важно для определения оптимального варианта терапии, направленной на разжижение слизи, стимуляцию выведения бронхиального секрета и регидратацию слизистой оболочки. Наоборот, при лечении продуктивного кашля с обильной жидкой мокротой основная задача заключается в изменении физико-химических свойств секрета, снижении его внутриклеточного образования. Такая терапия должна использоваться в ситуациях, когда кашель очень интенсивный, сопровождается рвотой и имеется риск развития аспирации (например, у недоношенных, у детей с тяжелой патологией центральной нервной системы, миопатией). Для правильного выбора средств, влияющих на кашель, необходимо:
Мукоактивная терапия
Мукоактивная терапия направлена на нормализацию функции дыхания. Это достигается санацией дыхательных путей с помощью мукоактивных препаратов. Выбор лекарственных средств должен осуществляться с учетом механизма их действия (таб. 1).
Классификация мукоактивных препаратов по механизму действия
Если кашляет малыш. Выбираем препараты для детей до 3-х лет
Поделиться:
Для лечения кашля используют разные группы лекарственных препаратов, но чаще всего используют муколитики и отхаркивающие средства.
Отхаркивающие средства – выводят мокроту из бронхов путём увеличения ее объема. Большинство этих препаратов содержат натуральные растительные компоненты, биологически активные вещества которых (в отличие от синтетических препаратов) естественным путем включаются в обменные процессы организма. К тому же они гораздо безопаснее, редко вызывают побочные эффекты и осложнения при лечении и зачастую разрешены к применению даже у маленьких детей.*
Растительные препараты для лечения кашля оказывают комплексное действие. Биологически активные вещества лекарственных трав препятствуют росту и размножению бактерий, обладают противовоспалительным действием, а также защищают дыхательные пути от раздражения, способствуя разжижению и отхождению мокроты. За счет этого происходит воздействие на все звенья патологического процесса.**
Именно такими лечебными свойствами обладает сироп Эвкабал®. В его состав входят экстракты чабреца (тимьяна) и подорожника. Содержание в лекарстве всего двух активных компонентов минимизирует риск аллергических реакций. Это выгодно отличает Эвкабал® от других многокомпонентных препаратов на растительной основе, при использовании которых бывает сложно понять, на какой именно ингредиент возникла аллергия. Сироп разрешен для применения у детей с 6 месяцев. Принимать его очень удобно: по 1 ч.л. дважды в сутки детям младшего возраста и всего один раз в сутки – детям с 6 мес. до 1 года.
Полный комплект для борьбы с кашлем
Важный момент: при использовании любых лекарственных средств (и химических, и растительных) всегда надо учитывать индивидуальную переносимость.
Главное в лечении кашля — комплексный подход, в любом случае, если вы заметили признаки длительного кашля у ребенка, не стоит затягивать с обращением к педиатру. Не забывайте о том, что любое остро возникшее заболевание может стать хроническим, если его не начать лечить своевременно, может беспокоить ребенка всю его жизнь. Необходимые обследования и своевременные рекомендации врача помогут вашему малышу вырасти здоровым и крепким!
* В.К. Котлуков, Т.В. Казакова и соавт. «Терапия кашля у детей при острых респираторных инфекциях с применением растительных экс-
трактов», // Медицинский совет №14-2015
** Е.М.Овсянникова, Н.А.Абрамова и соавт. «Лечение кашля у детей при ОРВИ», //Медицинский совет №9-2015
Муколитические препараты в терапии болезней органов дыхания у детей: современный взгляд на проблему
Болезни органов дыхания являются одной из наиболее важных проблем в педиатрии, занимая одно из первых мест в структуре детской заболеваемости. К числу основных факторов патогенеза воспалительных респираторных заболеваний относится нарушение механизма мукоцилиарного транспорта, что чаще всего связано с избыточным образованием и/или повышением вязкости бронхиального секрета. При этом перистальтические движения мелких бронхов и «мерцание» реснитчатого эпителия крупных бронхов и трахеи не в состоянии обеспечить адекватный дренаж бронхиального дерева. Реже, при пороках развития бронхолегочных структур или врожденной патологии реснитчатого эпителия, нормальная эвакуация бронхиальной слизи оказывается нарушенной изначально.
Следовательно, мукоцилиарный транспорт является важнейшим механизмом, обеспечивающим санацию дыхательных путей, одним из основных механизмов системы местной защиты и обеспечивает необходимый потенциал барьерной, иммунной и очистительной функции респираторного тракта. Очищение дыхательных путей от чужеродных частиц и микроорганизмов происходит благодаря оседанию их на слизистых оболочках и последующему выведению вместе с трахеобронхиальной слизью.
Воспаление органов дыхания, как правило, сопровождается компенсаторным увеличением слизеобразования. Изменяется и состав трахеобронхиального секрета: уменьшается содержание воды и повышается концентрация муцинов (нейтральных и кислых гликопротеинов), что приводит к увеличению вязкости мокроты. Отмечено, что чем выше вязкость слизи, тем ниже скорость ее продвижения по респираторному тракту. Увеличение вязкости бронхиального секрета способствует повышенной адгезии (прилипанию) патогенных микроорганизмов на слизистых респираторного тракта, что создает благоприятные условия для их размножения. Изменение состава слизи сопровождается и снижением бактерицидных свойств бронхиального секрета за счет уменьшения в нем концентрации секреторного иммуноглобулина А. В свою очередь, инфекционные агенты и их токсины оказывают неблагоприятное воздействие на слизистые дыхательных путей. Следовательно, нарушение дренажной функции бронхиального дерева может привести не только к вентиляционым нарушениям, но и снижению местной иммунологической защиты дыхательных путей с высоким риском развития затяжного течения воспалительного процесса и способствовать его хронизации [1,3,7].
Следует подчеркнуть, что у детей (особенно у детей раннего возраста) кашель чаще всего обусловлен повышенной вязкостью бронхиального секрета, нарушением «скольжения» мокроты по бронхиальному дереву, недостаточной активностью мерцательного эпителия. Поэтому основной целью терапии в подобных случаях является разжижение мокроты, снижение ее адгезивности и увеличение тем самым эффективности кашля.
Лекарственные препараты, улучшающие откашливание мокроты, можно разделить на несколько групп:
Средства, стимулирующие отхаркивание. Среди них выделяют рефлекторно действующие препараты и препараты резорбтивного действия. Рефлекторно действующие препараты при приеме внутрь оказывают умеренное раздражающее действие на рецепторы желудка, что возбуждает рвотный центр продолговатого мозга, рефлекторно усиливает секрецию слюнных желез и слизистых желез бронхов. К этой группе относятся препараты термопсиса, алтей, солодка, терпингидрат, эфирные масла и др. Действующим началом отхаркивающих средств растительного происхождения являются алкалоиды и сапонины, которые способствуют регидратации слизи за счет увеличения транссудации плазмы, усилению моторной функции бронхов и отхаркиванию за счет перистальтических сокращений бронхиальной проводимости, повышения активности мерцательного эпителия.
Ко второй подгруппе относят препараты резорбтивного действия: натрия и калия йодид, аммония хлорид, натрия гидрокарбонат и другие солевые препараты, которые, всасываясь в желудочно-кишечном тракте, выделяются слизистой бронхов и, увеличивая бронхиальную секрецию, разжижают мокроту и облегчают отхаркивание. Йодсодержащие препараты также стимулируют расщепление белков мокроты при наличии лейкоцитарных протеаз.
Средства, стимулирующие отхаркивание (преимущественно фитопрепараты) достаточно часто используются при лечении кашля у детей. Однако это не всегда оправдано. Во-первых, действие этих препаратов непродолжительно, необходимы частые приемы малых доз (каждые 2-3 часа). Во-вторых, повышение разовой дозы вызывает тошноту и, в ряде случаев, рвоту. В-третьих, лекарственные средства этой группы могут значительно увеличить объем бронхиального секрета, который маленькие дети не в состоянии самостоятельно откашлять, что приводит к значительному нарушению дренажной функции легких и реинфицированию.
Комбинированные препараты содержат два и более компонентов, некоторые из них включают противокашлевый препарат (стоптуссин, гексапневмин, лорейн), бронхолитик (солутан), жаропонижающие и/или антибактериальные средства (гексапневмин, лорейн). Эти препараты надо назначать только по строгим показаниям, нередко они противопоказаны детям раннего возраста. Кроме того, в некоторых комбинированных препаратах содержатся противоположные по своему действию медикаментозные средства (варианты порошка Звягинцевой) или субоптимальные дозы действующих веществ, что снижает их эффективность. Но, разумеется, имеются и вполне оправданные комбинации лекарственных средств.
Муколитические (или секретолитические) препараты в подавляющем большинстве случаев являются оптимальными при лечении болезней органов дыхания у детей. Муколитические препараты (бромгексин, амброксол, ацетилцистеин, карбоцистеин, месна, протеолитические ферменты и др.) воздействуют на гель-фазу бронхиального секрета и эффективно разжижают мокроту, не увеличивая существенно ее количество. Некоторые из препаратов этой группы имеют несколько лекарственных форм, обеспечивающих различные способы доставки лекарственного вещества (оральный, ингаляционный, эндобронхиальный и пр.), что чрезвычайно важно в комплексной терапии болезней органов дыхания у детей.
Выбор муколитической терапии определяется характером поражения респираторного тракта. Муколитики широко используются в педиатрии при лечении заболеваний нижних дыхательных путей, как острых (трахеиты, бронхиты, пневмонии), так и хронических (хронический бронхит, бронхиальная астма, врожденные и наследственные бронхолегочные заболевания, в том числе муковисцидоз). Назначение муколитиков показано и при болезнях ЛОР-органов, сопровождающихся выделением слизистого и слизисто-гнойного секрета (риниты, синуситы).
С другой стороны, существенное значение имеют возрастные особенности реагирования дыхательных путей на инфекционно-воспалительный или аллергический процесс. В частности, в неонатальном периоде высокая частота, затяжное и осложненное течение респираторной патологии обусловлены анатомо-физиологическими особенностями новорожденного. Одним из причинных факторов может явиться дефицит образования и выброса сурфактанта, в т.ч. качественный его дефицит. Кроме того, отсутствие кашлевого рефлекса у детей первых дней и недель жизни достаточно часто требует принудительного отсасывания слизи из верхних и нижних дыхательных путей, что может привести к травмированию и инфицированию слизистых. Особенностью физиологических реакций детей первых трех лет жизни является выраженная гиперпродукция и повышение вязкости слизи в сочетании с отеком слизистой бронхов, что вторично нарушает мукоцилиарный транспорт, вызывает обструкцию бронхов, способствует развитию инфекционного воспаления. Таким образом, при проведении комплексной терапии у детей с респираторной патологией необходимо учитывать возраст ребенка. Муколитики, безусловно, наиболее часто являются препаратами выбора у детей первых трех лет жизни.
В то же время механизм действия отдельных представителей этой группы различен, поэтому муколитики обладают разной эффективностью.
Протеолитические ферменты (трипсин, химотрипсин, РНК-аза) уменьшают как вязкость, так и эластичность мокроты, обладают противоотечным и противовоспалительным действием. Однако эти препараты практически не применяются в пульмонологии, т.к. могут спровоцировать бронхоспазм, кровохарканье, аллергические реакции. Исключение составляет рекомбинантная a-ДНК-аза, которую назначают больным с муковисцидозом.
Месна оказывает аналогичное ацетилцистеину действие, однако обладает большей эффективностью. Месна применяется исключительно для ингаляционного и интратрахеального введения.
Карбоцистеин не только обладает муколитическим эффектом, но и восстанавливает нормальную активность секреторных клеток. Имеются данные о повышении уровня секреторного IgA на фоне приема карбоцистеина. Препарат выпускается для приема внутрь (капсулы, сироп).
Амброксол относится к муколитическим препаратам нового поколения, является метаболитом бромгексина и дает более выраженный отхаркивающий эффект. В педиатрической практике в комплексной терапии органов дыхания предпочтительнее использовать препараты амброксола, имеющие несколько лекарственных форм: таблетки, сироп, растворы для ингаляций, для приема внутрь, для инъекций и эндобронхиального введения. Амброксол оказывает влияние на синтез бронхиального секрета, выделяемого клетками слизистой оболочки бронхов. Секрет разжижается путем расщепления кислых мукополисахаридов и дезоксирибонуклеиновых кислот, одновременно улучшается выделение секрета.
По данным Morgenroth, амброксол нормализует функции измененных серозных и мукозных желез слизистой бронхов, способствует уменьшению кист слизистой и активирует продукцию серозного компонента. Улучшение функции слизистых желез особенно важно у больных с хроническими заболеваниями легких, для которых характерны гипертрофия бронхиальных желез с образованием кист и уменьшением числа серозных клеток. Таким образом, амброксол способствует продукции качественно измененного секрета.
Амброксол не провоцирует бронхообструкцию. Более того, K.J. Weissman и соавт. [8] показали статистически достоверное улучшение показателей функции внешнего дыхания у больных с бронхообструкцией и уменьшение гипоксемии на фоне приема амброксола.
Данные литературы свидетельствуют о противовоспалительном и иммуномодулирующем действии амброксола. Препарат усиливает местный иммунитет, активируя тканевые макрофаги и повышая продукцию секреторного IgА. Амброксол оказывает подавляющее действие на продукцию мононуклеарными клетками медиаторов воспаления (интерлейкина 1 и фактора некроза опухоли) [4], а также усиливает естественную защиту легких, увеличивая макрофагальную активность. Предполагают, что ингибирование синтеза провоспалительных цитокинов может улучшить течение лейкоцит-обусловленного легочного повреждения. Доказано, что амброксол обладает противоотечным и противовоспалительным действием, эффективно способствует купированию обострения хронического бронхита и защищает против блеомицин-индуцированного легочного фиброза [6]. Stockley et al. сообщают, что амброксол ингибирует хемотаксис нейтрофилов in vitro.
Сочетание амброксола с антибиотиками, безусловно, имеет преимущество перед использованием одного антибиотика [7]. Амброксол способствует повышению концентрации антибиотика в альвеолах и слизистой оболочке бронхов, что улучшает течение заболевания при бактериальных инфекциях легких.
Применяют амброксол при острых и хронических болезнях органов дыхания, включая бронхиальную астму, бронхоэктатическую болезнь, респираторный дистресс-синдром у новорожденных. Можно использовать препарат у детей любого возраста, даже у недоношенных. Возможно применение у беременных женщин во II и III триместре беременности.
Для оценки клинической эффективности и переносимости препарата Амбробене у детей с болезнями органов дыхания нами проведено рандомизированное мультицентровое открытое сравнительное исследование. Работа осуществлялась в зимне-весенний период 2002 г. под руководством сотрудников кафедры детских болезней №1 РГМУ (зав. кафедрой проф. Г.А. Самсыгина) на трех клинических базах г. Москвы: ДКБ № 38 ФУ Медбиоэкстрем (гл. врач В.И. Голоденко), Морозовской ГДКБ (гл. врач проф. М.А. Корнюшин), родильного дома при ГКБ №15 (зам. гл. врача по акушерству и гинекологии проф. Г.М. Бурдули). Исследование проводилось в соответствии с требованиями Хельсинкской декларации (WMA, 1964) и «Декларации о политике в области обеспечения прав пациентов в Европе» (WHO/EURO, 1994).
Таблица 1. Распределение наблюдаемых больных.
| Характер патологического процесса | Амбробене | Бромгексин | Мукалтин | Не получали | Всего |
| Острые респираторные инфекции | 54 | 10 | 10 | — | 74 |
| Острая пневмония | 19 | — | — | — | 19 |
| Бронхиальная астма | 22 | 10 | 10 | — | 42 |
| Хронические заболевания легких | 20 | 10 | — | — | 0 |
| Пациенты после интубационного наркоза | 16 | 10 | 26 | ||
| Новорожденные с аспирационным синдромом и/или в/у пневмонией | 18 | 10 | 28 | ||
| Всего | 219 |
Детям с острой пневмонией (полисегментарной или долевой, неосложненной) Амбробене вводили по аналогичной схеме. Пациенты с острой плевропневмонией, а также дети первого года жизни получали препарат перорально в сочетании с ингаляциями. А у 3 пациентов с деструктивной пневмонией, осложненной гнойным плевритом, пневмотораксом, адекватный муколитический эффект был достигнут лишь при дополнительном парентеральном введении препарата.
Амбробене использовали у детей в возрасте от 1,5 до 15 лет с бронхиальной астмой. Дети поступали в приступном периоде в тяжелом (8 наблюдений) и среднетяжелом состоянии (14 наблюдений). С момента поступления и до купирования приступа лечение было интенсивным и комплексным: на фоне регидратационной терапии применяли бронхолитики, ингаляции b2-агонистов, кортикостероидов. Амбробене назначали с первых суток ингаляционно (2 раза в сутки) в сочетании с приемом препарата внутрь (2 раза в сутки). Длительность ингаляционного введения составила 5-7 дней, после появления продуктивного кашля с хорошо откашливающейся мокротой продолжали только прием препарата внутрь. В постприступном периоде при наличии бронхита, осложненного бактериальной инфекцией, назначение Амбробене, безусловно, способствовало разрешению болезни. По нашим наблюдениям, Амбробене не усиливает бронхоспазм. Однако у 2 детей раннего возраста (1,5 и 2 лет) на вторые сутки от начала терапии отмечалось значительное увеличение бронхореи, что потребовало отмены препарата.
В результате проведенного лечения у детей с хронической бронхолегочной патологией у половины пациентов кашель стал значительно реже на 7-10 день от начала комплексного лечения, у 9 детей перестали выслушиваться хрипы, у остальных количество хрипов уменьшилось. Бронхоскопически также была констатирована положительная динамика: у 11 детей гнойный компонент локального эндобронхита полностью купировался. Кроме того, проведение комплексных терапевтических мероприятий у 14 детей позволило ликвидировать обострение заболевания без антибактериального лечения. У больных с хроническими заболеваниями легких наилучший эффект был достигнут при приеме капсул ретард Амбробене внутрь в сочетании с лечебными бронхоскопиями, при которых препарат вводился и эндоброхиально. Проведенное нами сравнительное исследование Амбробене с бромгексином (внутрь в возрастных дозировках) показало низкую эффективность бромгексина у детей с хроническими заболеваниями легких.
Болезни органов дыхания являются одной из самых серьезных проблем неонатального периода. Мы применяли Амбробене у 18 доношенных новорожденных с весом 3000-3500 г. с аспирационным синдромом и/или внутриутробной пневмонией. Все дети родились с низкой оценкой по шкале Апгар (от 3 до 7 баллов в конце первой минуты жизни), всем проводилась интубация трахеи с целью санации трахеи и бронхов, 6 детей находились на ИВЛ. Степень дыхательной недостаточности оценивалась от 2 до 8 баллов по шкале Сильвермана. Амбробене применяли внутримышечно по 1 мл 2 раза в сутки от 7 до 14 дней. Группу сравнения составили новорожденные дети с аналогичными патологией и преморбидным фоном, не получающие муколитической терапии.
Было установлено, что включение Амбробене в комплексную терапию позволило улучшить оксигенацию при более низких концентрациях кислорода и давления на выдохе. Достоверно сократилась длительность использования оксигенации, нормализация газов крови была достигнута быстрее, чем в группе сравнения. В результате снизилось количество осложнений со стороны ЦНС. У детей, получавших Амбробене, в среднем по группе достоверно уменьшилось количество манипуляций на трахее, что привело к уменьшению частоты инфекционных бронхолегочных осложнений. Включение Амбробене в комплексную терапию новорожденных детей с аспирационным синдромом и/или внутриутробной пневмонией достоверно снижало продолжительность курса антибактериальной терапии. Побочных эффектов и нежелательных явлений при использовании Амбробене у новорожденных детей мы не наблюдали.
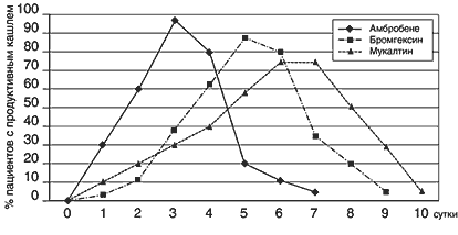
Таким образом, рандомизированное мультицентровое открытое сравнительное исследование показало, что у детей с острыми и хроническими заболеваниями дыхательных путей препарат Амбробене обладает высокой терапевтической эффективностью. Положительный результат лечения был подтвержден клиническими и лабораторными тестами, а также бронхоскопией, проведенной в динамике. При сравнительном исследовании установлено, что при применении Амбробене продуктивный кашель появляется быстрее, а курс лечения короче, чем при лечении бромгексином и мукалтином. Сочетание различных форм доставки препарата (ингаляционный, пероральный, инъекционный, эндобронхиальный) оправдано при многих болезнях органов дыхания. В лечении детей с тяжелыми формами хронической бронхолегочной патологии, при необходимости бронхоскопических санаций, пероральную форму Амбробене желательно сочетать с внутрибронхиальным его применением. У детей с бронхиальной астмой наилучший эффект отмечен при сочетании ингаляций Амбробене через небулайзер и приема препарата внутрь. Инъекционное введение Амбробене показано в комплексной терапии тяжелых осложненных пневмоний, при наличии заболеваний органов дыхания у новорожденных и после интубационного наркоза у часто болеющих респираторными инфекциями детей. Наш опыт применения Амбробене дает основание положительно оценить его значение в комплексном лечении детей с острой и хронической бронхолегочной патологией. Побочных явлений при использовании Амбробене выявлено не было. Препарат имеет удобную расфасовку, приятные органолептические качества и может применяться не только в стационаре, но и в домашних условиях.
В комплексной терапии болезней органов дыхания у детей выбор муколитических препаратов должен быть строго индивидуальным и учитывать механизм фармакологического действия лекарственного средства, характер патологического процесса, преморбидный фон и возраст ребенка.