Эффективность и безопасность Симбикорта 80/4,5 мкг, используемого в режиме гибкого дозирования у детей в возрасте от 6 до 12 лет, страдающих бронхиальной астмой
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
За последние годы накопилось много данных, свидетельствующих, что b2–агонисты длительного действия в сочетании со средними и низкими дозами ингаляционных глюкокортикостероидов (иГКС) более эффективны при бронхиальной астме (БА) средней тяжести и тяжелой, чем высокие дозы иГКС [1,2].
В педиатрической практике использование комбинированных препаратов, содержащих иГКС и b2–агонисты длительного действия, в качестве альтернативы иГКС в терапии астмы средней тяжести приводит к более быстрому достижению контроля над симптомами заболевания, достижению нормального качества жизни ребенка, устранению постнагрузочного бронхоспазма [3,4].
В настоящее время в России зарегистрированы два комбинированных препарата: Серетид (фармацевтическая компания Glaxo Smith Kline) и Симбикорт–турбухалер (фармацевтическая компания AstraZeneca).
Серетид выпускается в ингаляторе Мультидиск в дозах 50 мкг сальметерола на 100, 250 или 500 мкг флутиказона (50/100; 50/250; 50/500) и в форме аэрозоля.
Симбикорт содержит b2–агонист длительного действия – формотерол и иГКС – будесонид. Препарат выпускается в порошковом ингаляторе Турбухалер в двух дозировках: 160 мкг или 80 мкг будесонида на 4,5 мкг формотерола (160/4,5; 80/4,5). Формотерол отличается от сальметерола быстрым началом действия [5,6]. Эффект наступает через 1–3 мин. и продолжается до 10–12 часов.
При применении комбинированных препаратов встает вопрос о том, допустим ли дополнительный прием препарата при возникновении симптомов астмы или обострения заболевания, возможна ли гибкость дозирования комбинированных препаратов?
При применении Серетида для увеличения при необходимости дозы иГКС следует использовать отдельно дополнительный ингалятор, т.к. у сальметерола кривая «доза–ответ» при дозах свыше 50 мкг относительно плоская [7], т.е. увеличение дозы сальметерола не приводит к улучшению бронхопроходимости.
Применяя Симбикорт–турбухалер, можно варьировать дозу, используя от 1 до 4 ингаляций два раза в сутки. Общие суточные дозы будесонида и формотерола при 8 ингаляциях Симбикорта Турбухалера 160/4,5 в сутки не превышают максимальных суточных доз, разрешенных к применению у взрослых и детей старше 12 лет [3].
Гибкое дозирование при проведении поддерживающей терапии будесонидом/формотеролом позволяет значительно улучшить контроль астмы, уменьшить число обострений при снижении объема терапии по сравнению со значительно более высокими фиксированными дозами будесонида и формотерола [8]. Кроме того, использование будесонида/формотерола в режиме гибкого дозирования приводит к меньшим затратам на лечение, чем в режиме фиксированного дозирования [9].
В сравнительном рандомизированном двойном слепом с открытой фазой в параллельных группах исследовании эффективности и безопасности гибкого дозирования будесонида/формотерола в сравнении с фиксированными дозами будесонида/формотерола или сальметерола/флутиказона, включавшем 658 пациентов старше 12 лет, было показано, что будесонид/формотерол в режиме гибкого дозирования поддерживающей терапии хорошо переносится и обеспечивает более эффективный контроль БА, чем традиционная терапия фиксированными дозами будесонида/формотерола или сальметерола/флутиказона [10].
Целью настоящего исследования было изучение эффективности и безопасности Симбикорта 80/4,5 мкг в режиме гибкого дозирования у детей в возрасте от 6 до 12 лет, имеющих астму средней степени тяжести и тяжелую.
Работа проходила в четырех амбулаторных аллергоцентрах. Исследование проводили высококвалифицированные врачи–аллергологи со стажем более 15 лет, имеющие опыт в научно–исследовательской деятельности.
В исследовании приняли участие 35 детей в возрасте от 6 до 12 лет с верифицированным диагнозом БА и длительностью заболевания не менее 1 года. До включения в исследование дети могли получать кромоны либо иГКС в дозе не более 500 мкг/сут. по беклометазону и короткодействующие b2–агонисты и/или теофиллины по потребности.
Критериями включения в исследование являлись показатели ОФВ1 на момент скрининга не менее 60% от возрастной нормы и обратимости обструкции не менее 12% после применения сальбутамола.
Критериями исключения являлись:
• Известная или предполагаемая чувствительность к будесониду или лактозе.
• Любая клинически значимая патология, кроме БА, аллергического ринита и других аллергических заболеваний.
•Использование пролонгированных b2–агонистов и комбинированных препаратов менее чем за 1 месяц до включения в исследование.
• Использование системных ГКС в течение 3 месяцев, предшествующих включению в исследование.
Требования к сопутствующей терапии
• На протяжении всего исследования пациенты не должны получать никакой сопутствующей терапии для лечения БА, кроме короткодействующих b2–агонистов.
• Не разрешен прием антигистаминных препаратов, кроме однократного приема при обострении аллергического заболевания.
• Для лечения аллергического ринита разрешено применение только кромогликата натрия в виде дозированного спрея.
Дизайн исследования
Исследование включало два периода – вводный (2 недели) и лечебный (12 недель). В течение вводного периода дети могли получать базисную терапию кромонами или иГКС в дозе не более 500 мкг/сут. по беклометазону. Для снятия симптомов астмы допускался прием короткодействующих b2–агонистов.
В течение лечебного периода дети получали Симбикорт 80/4,5 мкг по 2 вдоха 2 раза в день в течение 1 месяца (стартовая терапия).
Затем пациенты переходили на прием Симбикорта 80/4,5 мкг по 1 вдоху 2 раза в день в течение 2–х месяцев (поддерживающая терапия). Применение режима гибкого дозирования Симбикорта в данном исследовании предусматривало: уменьшение дозы Симбикорта при переходе на поддерживающую терапию; увеличение дозы Симбикорта при ухудшении состояния пациента (рис. 1).
Ухудшение состояния определялось как два последовательных дня требующих использования короткодействующих b2–агонистов для облегчения симптомов БА более 2–х раз в день или наличие пробуждения из–за астмы, а также снижение показателя ПСВ ниже 80% от нормы.
Исследование предусматривало 7 визитов.
Визит 0 – скрининг
Визит 1 – через 2 недели. Рандомизация. Начало лечение Симбикортом 80/4,5 мкг.
Визит 2 – через 2 недели от начала лечения.
Визит 3 – через 4 недели от начала лечения. Снижение дозы Симбикорта 80/4,5 мкг – по 1 дозе 2 раза в день.
Визит 4 – через 2 недели от визита 3. При необходимости – коррекция дозы Симбикорта.
Визит 5 – через 2 недели от визита 4. При необходимости – коррекция дозы Симбикорта.
Визит 6 – через 4 недели от визита 5. Окончание исследования.
В течение всего исследования пациенты вели дневник наблюдения, в котором ежедневно утром (состояние за ночь) и вечером (состояние за день) отмечались симптомы астмы в баллах (0–4 балла), показатели ПСВ, потребность в короткодействующих b2–агонистах, изменение дозы Симбикорта.
Для оценки выраженности симптомов астмы использовали четырехбалльную шкалу (табл. 1).
На визитах 1, 3, 6 проводилось исследование функции внешнего дыхания (ФВД) исходно и через 15 минут после применения короткодействующего b2–агониста.
Все перечисленные показатели для оценки симптомов астмы, потребность в короткодействующих b2–агонистах и показатели функции внешнего дыхания рассчитывали как средние в группе за прошедший период.
Для статистического анализа полученных данных использовали критерий Стьюдента.
Результаты и обсуждение
В исследование было скринировано 40 пациентов, 35 из них были рандомизированы. 5 пациентов были исключены из исследования из–за несоответствия критериям включения по показателям ОФВ1 и/или по обратимости обструкции после пробы с b2–агонистом.
В течение лечебного периода под наблюдением находилось 35 детей в возрасте от 6 до 12 лет. У 33 детей астма была средней степени тяжести, у 2 детей – тяжелой. В течение вводного периода 18 детей получали иГКС и 17 детей кромоны (6 из них Интал, 11 детей – Тайлед). Сопутствующих аллергологических заболеваний не имели только 9 из 35 детей. 19 детей имели аллергический ринит; 4 – атопический дерматит и 3 – поллиноз.
В таблице 2 представлены клинико–функциональные показатели до и во время лечения Симбикортом.
На визите 1, до начала лечения Симбикортом, выраженность симптомов астмы оценена следующим образом: у 8 пациентов – 1 балл; у 26 – 2 балла; у 1–3 балла. При осмотре у всех пациентов фиксировался синдром бронхиальной обструкции. Во вводном периоде у всех пациентов проявления астмы требовали применения короткодействующих b2–агонистов. У 26 детей симптомы астмы возникали ночью, из них 9 детям требовались повторные ингаляции b2–агонистов. У 30 детей симптомы возникали днем, требовались повторные ингаляции b2–агонистов. У 15 из них потребность в b2–агонистах фиксировалась от 3 до 6 раз за день, у 5 детей – более 10 раз в сутки.
Средний балл ночных симптомов в группе за вводный период (В 1) составил 0,9; дневных симптомов – 1.0. Среднее число суток без симптомов астмы за неделю во вводном периоде составило 1,65 дня. Потребность в b2–агонистах за сутки – 1,98 доз. Показатели ФВД были существенно снижены. Показатель среднесуточной величины ПСВ в группе составил только 63,74% от нормы (желтая зона). Показатель суточной лабильности бронхов оказался достаточно высок и составил 20,21%. Показатель ОФВ1 в группе в день рандомизации составил только 81,8% от нормы. Прирост показателя ОФВ1 после пробы с b2–агонистом оказался значительным, что доказывает наличие бронхоспазма, и составил 17,6%.
Таким образом, все 35 пациентов до начала лечения Симбикортом имели нестабильное состояние и находились в периоде обострения астмы.
Уже через 2 недели лечения Симбикортом 80/4,5 мкг по 2 ингаляции 2 раза в день состояние пациентов значительно улучшилось. У 6 из 35 детей симптомы астмы не возникали; потребности в применении b2–агонистов ночью не испытывали 23 ребенка, днем – 18 детей.
Средний балл ночных и дневных симптомов БА снизился до 0,3 балла. Число суток без симптомов астмы за неделю увеличилось до 4,45 дней; потребность в b2–агонистах за сутки снизилась до 0,38 дозы. Показатель среднесуточной ПСВ увеличился до 82,27% (нижняя часть зеленой зоны), показатель суточной лабильности бронхов снизился до 1,89%.
Через 1 месяц от начала лечения (визит 3) Симбикортом (стартовая доза) симптомы астмы изчезли у 19 (54,3%) детей; b2–агонисты короткого действия не использовал 31 пациент. В ночные часы использовал b2–агонисты короткого действия один пациент; днем – 3 пациента. Существенная положительная динамика по всем показателям прослеживается в группе в целом по сравнению с визитом 1. Достоверно снизился средний балл ночных и дневных симптомов астмы и составил 0,1. Число суток без симптомов астмы также достоверно увеличилось и составило 6,1 за неделю. Потребность в b2–агонистах продолжала снижаться и составила 0,05 дозы в сутки.
Показатели ФВД продолжали улучшаться. Показатель средне–суточной ПСВ составил 85,88% от нормы. Проба с b2–агонистом на визите 3 была отрицательной у большинства пациентов. Процент прироста в среднем в группе составил – 5,8%. Улучшение всех оцениваемых показателей на визите 3 в сравнении с визитом 1 были статистически достоверным.
На визите 3 согласно протоколу доза Симбикорта 80/4,5 была снижена до 1 ингаляции 2 раза в день у 34 пациентов. Один пациент продолжил прием Симбикорта 80/4,5 в той же суточной дозе по 2 ингаляции 2 раза в день до визита 4, т.к. у него сохранялись симптомы астмы в ночные часы, но они не требовали использования короткодействующих b2–агонистов. На визите 4 доза Симбикорта у этого пациента была снижена.
Через 2 недели после уменьшения суточной дозы (визит 4) все пациенты были осмотрены. За прошедший период средние баллы ночных и дневных симптомов астмы, число суток без симптомов астмы не изменились. Показатели ПСВ и лабильности бронхов не ухудшились. Несколько увеличился показатель потребности в короткодействующих b2–агонистах за сутки до 1,66 против 0,05 (визит 3). На увеличение показателя потребности в b2–агонистах повлияло присоединение ОРВИ у одного из пациентов, который был на визите 4 переведен вновь на прием Симбикорта 80/4,5 по 2 дозы 2 раза в день.
Таким образом, уменьшение дозы Симбикорта при переходе на поддерживающую дозу позволило, с одной стороны, уменьшить объем фармакотерапии, а с другой стороны, сохранить достигнутую при стартовой терапии клинико–функциональную ремиссию.
К визиту 5 (лечение Симбикортом 80/4,5 по 1 дозе 2 раза в день в течение 4 недель) средние баллы ночных и дневных симптомов астмы, а также число суток без астмы сохранялись на достигнутом уровне к визиту 3, т.е. до снижения дозы Симбикорта. Потребность в b2–агонистах уменьшилась до 0,19 по сравнению 1,66 на визите 4. Показатели среднесуточной величины ПСВ и суточной лабильности бронхов находились в диапазоне нормы.
Таким образом, применение меньшей дозы Симбикорта позволило сохранить достигнутую клинико–функциональную ремиссию.
Однако двум пациентам в связи с наличием симптомов астмы была увеличена доза Симбикорта 80/4,5 до начальной, т.е. по 2 дозы 2 раза в день. Лечение в этой дозе было продолжено до конца исследования. Еще один пациент после визита 5, в связи с ухудшением состояния по астме, был госпитализирован и получал терапию системными ГКС. Он был исключен из исследования.
Таким образом, к концу лечебного периода (визит 6) под наблюдением находилось 34 пациента. 32 из них получали Симбикорт 80/4,5 по 1 дозе 2 раза в день и 2 – получали Симбикорт по 2 дозы 2 раза в день.
За период исследования 3 пациента перенесли ОРВИ. У одного из них была увеличена доза Симбикорта. У двух из них на фоне вирусной инфекции обострений БА не возникало, дополнительного применения короткодействующих b2–агонистов не потребовалось.
В течение последнего месяца лечения симптомы астмы не возникали у 28 из 34 детей. У 6 детей в течение последнего месяца терапии отмечались эпизодические кратковременные симптомы БА. У всех пациентов симптомы оценены в 1 балл. У 5 из них симптомы фиксировались в течение 4 суток (но не последовательно) за 28 дней. У 1 пациента симптомы отмечались 8 раз. Изредка использовали короткодействующие b2–агонисты только 4 пациента. Синдром бронхиальной обструкции при осмотре на визите 6 отсутствовал у всех пациентов.
Средние баллы ночных и дневных симптомов снизились более чем на 90% и составили 0,06 баллов против 0,9 (ночные) и 1,0 (дневные) балл до начала лечения. Число суток без симптомов астмы увеличилось на 74,5% и составило в среднем 6,48 дней за неделю против 1,65 дня до начала лечения. Потребность в короткодействующих b2–агонистах снизилась на 92,4% и составила 0,15 доз за сутки по сравнению с 1,98 дозы до начала лечения. Существенно улучшились показатели ФВД. Показатель среднесуточной величины ПСВ увеличился на 27,9% и составил 88,4% от нормы против 63,74% до лечения. Показатель суточной лабильности бронхов уменьшился на 90% и составил 2,01% против 20,21% до лечения. Средний показатель ОФВ1 в группе достиг 100%. Прирост показателя ОФВ1 после пробы с b2–агонистом уменьшился с 17,6% до лечения до 3,4% к концу лечения.
Таким образом, к концу 3–месячного курса лечения Симбикортом, используя гибкую систему дозирования, допускающую снижение или увеличение дозы препарата по мере необходимости, удалось добиться клинико–функциональной ремиссии, соответствующей критериям «хорошо контролируемой астмы» [11], при которой не требовалось дополнительного применения короткодействующих b2–агонистов, у большинства пациентов, завершивших исследование (30 из 34 – 88,2%).
Выводы
1. Назначение комбинированного препарата Симбикорт 80/4,5 по 2 дозы 2 раза в сутки в течение 1 месяца в качестве стартовой терапии приводит к достижению клинико–функциональной ремиссии у большинства пациентов (97,1%) с астмой тяжелой и средней тяжести.
2. Уменьшение в два раза дозы Симбикорта 80/4,5 при переходе на поддерживающую терапию позволяет сохранить достигнутую клинико–функциональную ремиссию у 88,5% пациентов.
3. Применение Симбикорта 80/4,5 в режиме гибкого дозирования позволяет достичь контроля астмы при меньшем объеме медикаментозной терапии.
4. Временное увеличение объема поддерживающей терапии при снижении контроля астмы дает положительный эффект.
5. Достижения лучшего контроля астмы с использованием минимально необходимого объема терапии возможно добиться в режиме гибкого дозирования поддерживающей терапии.
6. Симбикорт 80/4,5 в режиме гибкого дозирования хорошо переносится пациентами.
Новый препарат Сальмекорт в базисной терапии бронхиальной астмы
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Внастоящее время бронхиальная астма (БА) относится кчислу наиболее распространенных заболеваний. Основной задачей лечения БАявляется достижение контроля над заболеванием, который заключается втом, что упациентов отсутствуют симптомы болезни или они минимально выражены, нет ограничения повседневной деятельности, отсутствует (или минимальна) потребность впрепаратах неотложной помощи, частота обострений крайне низка [1–3]. Проявления заболевания устраняют спомощью адекватной ирациональной медикаментозной терапии. Фармакотерапия БАвключает 2 класса препаратов: быстродействующие, которые устраняют симптомы острой бронхоконстрикции, ибазисные— для длительного контроля заболевания, при регулярном применении улучшающие контроль над БАвцелом. При этом иногда базисные препараты принимают попотребности, аβ короткого действия— регулярно или профилактически [2, 4, 5]. Нодаже при очень хорошем контроле БАнесуществует гарантий полного отсутствия симптомов иобострений. Контакт саллергеном, пребывание внакуренном помещении идругие подобные ситуации могут вызвать затруднение дыхания, появление кашля ивнезапное развитие приступа удушья. Это может случиться влюбом месте ивлюбое время, азначит, необходимо иметь при себе средство для неотложной помощи и, конечно, уметь его применять.
Основными противовоспалительными препаратами для лечения БА являются ингаляционные глюкокортикостероиды (ИГКС). Контролируемые исследования, проведенные с учетом требований доказательной медицины, показали эффективность ИГКС в плане улучшения функции дыхания, уменьшения гиперреактивности дыхательных путей и выраженности симптомов, снижения частоты и тяжести обострений (уровень доказательности, А) [6–8].
В гг. в клиническую практику вошли селективные агонисты β, которые обладали преимущественным действием на гладкую мускулатуру бронхов и клинически незначимой активностью в отношении α- и β. Пациенты, регулярно принимавшие β короткого действия перед приемом ИГКС, демонстрировали большую клиническую эффективность терапии, чем принимавшие указанные препараты только по потребности. Это привело к созданию селективных длительно действующих β (ДДБА). В терапии БА используют ингаляционные сальметерол или формотерол, которые в комбинации с ИГКС являются основой базисной терапии БА. Включение их в схему лечения больных, у которых БА не удается полностью контролировать различными дозами ИГКС, позволяет достичь лучшего контроля над заболеванием, чем просто увеличение дозы ИГКС в 2 раза и более (уровень доказательности, А) [9–11]. ИГКС и ДДБА следует рассматривать как синергисты, что обусловлено их комплементарным воздействием на молекулярном и рецепторном уровнях [12–15]. Высокий противовоспалительный эффект совместного использования ИГКС и ДДБА является аргументом в пользу применения такого терапевтического подхода при БА, которая сопровождается воспалением слизистой бронхов, ее отеком, экссудацией плазмы (повышением сосудистой проницаемости), гипертрофией гладкомышечных клеток и десквамацией эпителия.
В 2005, 2008 и 2010 гг. Управление по контролю за продуктами и лекарствами США (FDA) провело дополнительную оценку безопасности ДДБА при БА. Из представленных данных следует, что повышенный риск отмечается в первую очередь у вполне определенной группы пациентов — темнокожих американцев, не получавших терапии ингаляционными гормональными препаратами до начала лечения ДДБА. Также отмечалось повышение риска тяжелых обострений в тех случаях, когда лечение этой группой препаратов было начато на фоне выраженного ухудшения или уже имевшегося обострения БА [16].
Пролонгированные β могут назначаться только в дополнение к ИГКС. Регулярное применение ДДБА для плановой терапии требует их обязательного сочетания с ИГКС. Врачам следует знать, что использование монотерапии β вызывает развитие феномена β, что может привести к тяжелым последствиям для пациентов вплоть до развития астматических состояний.
Комбинация флутиказона пропионата (ФП) и сальметерола ксинафоата (САЛ). Компоненты, входящие в состав этих препаратов, применяются достаточно давно: ФП — с 1993 г., САЛ — с 1990 г.
ФП — один из самых высокоактивных противовоспалительных препаратов на сегодняшний день. Препарат имеет низкую системную биодоступность (
1%), а абсолютная биодоступность составляет 10–30% в зависимости от типа ингалятора. ФП обладает высоким сродством к глюкокортикоидным рецепторам и имеет длительную связь с рецептором. Для предотвращения осиплости голоса и развития кандидоза при приеме ФП следует соблюдать те же правила, что и при приеме других ИГКС, полоскать рот и горло водой после ингаляции. В связи с высоким противовоспалительным действием ФП также показан больным с тяжелым течением БА и зависимостью от системных стероидов [17].
САЛ относится к ингаляционным ДДБА. Клинические исследования показали, что ДДБА оказывают стабилизирующее влияние на тучные клетки, ингибируют высвобождение ими гистамина, что приводит к уменьшению его системной и местной концентрации [18]. САЛ назначается только в качестве препарата для базисной терапии и не применяется по потребности, при обострении заболевания, астматическом состоянии, а также для купирования приступов затрудненного дыхания. Следует использовать только рекомендованные дозы, а для купирования симптомов использовать β короткого действия. Отметим, что САЛ имеет и ряд неожиданных свойств — в частности, он вызывает снижение патогенности Pseudomonas aeruginosa и обладает протективным эффектом в отношении Haemophilus influenzae в культурах эпителия респираторного тракта [19–21]. САЛ является высокобезопасным препаратом, что доказано многочисленными клиническими исследованиями.
Первым препаратом с фиксированной комбинацией был Серетид®, содержащий ИГКС ФП и САЛ и относящийся к ингаляционным β длительного действия.
Комбинированный препарат ФП и САЛ. В исследовании S. Kirby et al. было показано, что при использовании комбинации САЛ и ФП у здоровых людей не наблюдается системных фармакодинамических или фармакокинетических взаимодействий [22]. Исследование GOAL (Gaining Optimal Asthma control), результаты которого легли в основу стратегии контроля GINA (2006), демонстрируют преимущества комбинированной терапии ИГКС + ДДБА при среднетяжелой и тяжелой БА [23]. Результаты исследования GOAL имеют важное практическое значение, в нем сформулированы критерии эффективности лечения БА. По данным исследования GOAL, около 40% больных БА, получавших фиксированную комбинацию САЛ/ФП, достигли полного контроля над БА по истечении 12 мес. лечения. Не менее важно, что в группе, получавшей в качестве базисной терапии фиксированную комбинацию, пациентов, достигших полного контроля над БА, было достоверно больше, чем в случае монотерапии ФП. Благодаря исследованию GOAL был сделан важный вывод о том, что улучшить результаты лечения можно, выбрав наиболее эффективную базисную терапию.
Исследование, проведенное et al., продемонстрировало, что у пациентов с персистирующей БА стартовая терапия САЛ/ФП по сравнению с ФП обеспечивала в 1,65 раза более вероятное достижение хорошо контролируемой БА у пациентов с признаками плохого контроля БА до лечения и в 2,6 раза более вероятное достижение хорошо контролируемой БА у пациентов с признаками плохого контроля БА до лечения [24].
Оригинальные препараты и дженерики. Оригинальный препарат с фиксированной комбинацией ФП и САЛ Серетид® широко и с успехом применяется для лечения БА и ХОБЛ с помощью метиодозированного (МDI) и порошкового (Diskus) ингаляторов. Применение оригинальных препаратов возможно только при получении достоверно доказанных результатов клинических испытаний по изучению безопасности и эффективности препаратов. Так, на всех стадиях клинических исследований фиксируются все неблагоприятные реакции; это происходит и в течение ряда лет после вывода препаратов на рынок. Эти условия определяют цену оригинальных препаратов. Когда истекает срок действия патента оригинальных препаратов, наиболее успешные медикаменты начинают выпускать в виде дженериков — копий оригинального лекарства. Причем копия должна быть полной, на нее автоматически экстраполируются результаты клинических исследований оригинального препарата. Дженерики всегда дешевле оригинальных препаратов, что расширяет возможности терапии. Требования ВОЗ к дженерикам в отношении фармацевтической и терапевтической эквивалентности довольно жесткие — дженерик должен действовать точно так же, как оригинальный препарат, иметь такие же эффективность и безопасность.
В настоящее время на рынок выведен препарат Сальмекорт, в котором фиксированная комбинация активных компонентов — ФП и САЛ соответствует по дозировке оригинальному препарату, выпускаемому в MDI. В России было проведено открытое рандомизированное многоцентровое исследование по проверке гипотезы о не меньших эффективности и безопасности препарата Сальмекорт (25/250 мкг, в форме аэрозоля для ингаляций дозированного) по сравнению с препаратом Серетид® (25/250 мкг, в форме аэрозоля для ингаляций дозированного) при лечении пациентов с персистирующей БА и нуждающихся в комбинированной терапии высокими дозами ИГКС и β пролонгированного действия.
Задачи данного исследования:
1. Сравнительная оценка уровня контроля БА и его динамики в течение исследования.
2. Сравнительная оценка безопасности и переносимости препаратов Сальмекорт и Серетид®.
В исследовании принимали участие врачи из 5 ведущих медицинских учреждений России. Диагноз БА устанавливался врачом в соответствии с практикой лечебного учреждения. После подписания информированного согласия на участие в исследовании пациентам (113 человек) проводился скрининг, вводный период имел продолжительность в среднем 14 дней. За это время исследователь оценивал соответствие пациента критериям включения/невключения и стабильность заболевания. Затем 107 пациентов, соответствовавших критериям включения/невключения, были рандомизированы на 2 лечебные группы.
Пациентам группы (n=56) был назначен Сальмекорт по 2 ингаляции 2 р./сут, пациентам группы (n=51) — Серетид® по 2 ингаляции 2 р./сут. Первый прием препаратов проводился в центре под наблюдением медицинского персонала после выполнения спирометрии. Исследователь инструктировал пациентов, как правильно вводить препараты.
Пациенты принимали препараты ежедневно в течение 12 нед. У них систематически проводилась спирометрия. Пациенты должны были ежедневно вести дневник — утром и вечером записывать показатели пикфлоуметрии, а также наличие симптомов БА и потребность в бронходилататорах. В период приема исследуемых препаратов было предусмотрено 3 визита пациентов в центр с периодичностью 4 нед. После завершающего визита на день от начала лечения участие пациента в исследовании прекращалось, дальнейшая терапия осуществлялась лечащим врачом.
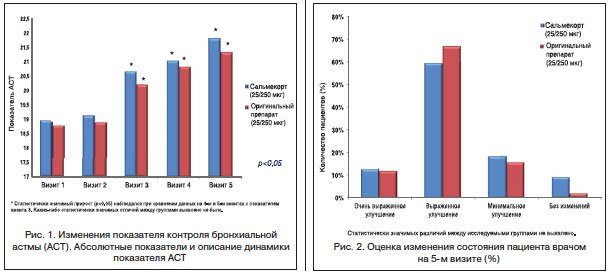
При проведении анализа эффективности было выявлено:
Анализ частоты возникновения нежелательных явлений, проведенный с использованием методики «bootstrap», не выявил статистически значимой разницы между группами терапии по данному параметру.
Ни в одном случае не было отмечено развития кандидозного поражения слизистых ротоглотки на фоне применения исследовавшихся препаратов.
Результаты исследования позволили сделать следующие выводы:
Следует помнить о том, что и Серетид®, и Сальмекорт не назначают для купирования симптомов БА. С этой целью предпочтительно назначать β короткого действия. При необходимости увеличения дозы ИГКС не следует превышать допустимые дозы САЛ. В этом случае следует назначить больному препарат с более высоким содержанием ФП.
Только для зарегистрированных пользователей