Можно ли заменить легкие у человека
Советы по трансплантации легких
1. Какие существуют основные типы трансплантации легких?
Пересадка одного легкого, пересадка обоих легких (билатеральная трансплантация) и трансплантация сердечно-легочного комплекса.
2. Какой человеческий орган был первым трансплантирован: сердце или легкие?
Хотя вначале сердечная трансплантология развивалась быстрее, и таким образом создается впечатление, что трансплантация сердца была осуществлена ранее трансплантации легких, однако на самом деле трансплантация легких предшествовала трансплантации сердца.
3. Кто произвел первую трансплантацию легких у человека? Когда?
Джеймс Ганди (James Handy) произвел первую трансплантацию легких в 1963 году. Однако прошло более 20 лет пока трансплантация легких стала рутинно осуществляться в клинической практике (за этот 20-летпий период только 1 пациент был выписан из стационара в удовлетворительном состоянии).
Это было обусловлено вторичным повреждением трансплантата вследствие неадекватной консервации органа, продолжительного периода ишемии, отсутствия надлежащей иммуносупрессии и технических сложностей.
4. Кто является кандидатом для трансплантации легких?
Больные при отсутствии альтернативных терапевтических или хирургических методов лечения с вероятностью смерти от легочного заболевания в течение 12-18 месяцев.
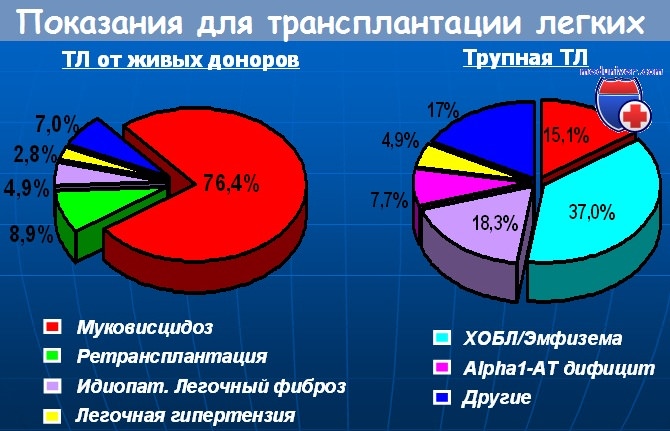
5. Каковы наиболее частые показания к трансплантации одного легкого?
• Эмфизема (40%)
• Идиопатический фиброз легких (20%)
• Недостаточность альфа-1 антигринсина (11%)
• Первичная легочная гипертензия и вторичная легочная гипертензия вследствие врожденного корригируемого заболевания сердца (10%)
6. Каковы наиболее частые показания к трансплантации обоих легких?
• Кистозный фиброз (35%)
• Эмфизема (20%)
• Недостаточность альфа-1 антитринсина (11%)
• Первичная легочная гипертензия и вторичная легочная гипертензия вследствие врожденного корригируемого заболевания сердца (20%)
• Идиопатический фиброз легких (8%)
7. Каковы наиболее частые показания к трансплантации сердечно-легочного комплекса?
Первичная легочная гипертензия (30%) и кистозный фиброз (16%) — примеры когда «плохие легкие разрушают хорошее сердце». И наоборот, при врожденных заболеваниях сердца (27%) «плохое сердце разрушает хорошие легкие».
8. Что к чему подшивается при трансплантации одного легкого? При трансплантации обоих легких?
При трансплантации одного легкого необходимо произвести следующие анастомозы, связывающие структуры реципиента с трансплантатом: бронхиальный, между легочными артериями и между легочными венами (предсердная манжетка). При трансплантации обоих легких осуществляются те же анастомозы, однако в этом случае чаще приходится прибегать к применению искусственного кровообращения. Во время имплантации второго легкого доминирование притока крови к ишемизированному легкому часто приводит к реперфузионному отеку легких и гипоксемии.
9. При каком заболевании трансплантация легких дает наилучшие результаты?
На самом деле отмечаются различия. У больных с эмфиземой и с недостаточность альфа-1 антитрипсииа отмечаются существенно лучшие результаты и достигается годовая выживаемость в 80%.
10. Почему из года в год уменьшается количество проводимых трансплантаций сердечно-легочного комплекса?
В 1990 году было осуществлено около 250 трансплантаций сердечно-легочного комплекса. В 1999 году их количество уменьшилось приблизительно до 150. Так как результаты трансплантаций одного и обоих легких улучшились, пет необходимости в проведении трансплантации сердечно-легочного комплекса у пациентов с изолированным заболеванием легких.
11. Какие осложнения встречаются наиболее часто после трансплантации легких?
• Нарушение хирургического заживление воздухоносных путей (в раннем периоде)
• Отторжение (в раннем периоде)
• Бактериальная и цитомегаловирусная инфекция (в периоде от нескольких недель до нескольких месяцев)
• Бронхолитическая облитерация (от нескольких месяцев до нескольких лет)
12. Что такое бронхолитическая облитерация?
Бронхолитическая облитерация — основная причина отдаленной смертности после трансплантации легких. При этом процессе в перепончатых и дыхательных бронхиолах определяются гистологические признаки субэпителиалнгого склерозирования, которое ведет к окклюзии просвета бронхиол. Клинически это проявляется диспноэ и обструкцией воздухоносных путей.
13. Как диагностируется отторжение трансплантированного легкого?
В отличие от сердца, диагностика отторжения трансплантированных легких неточна и основана на наличии комплекса признаков. Уменьшение насыщения кислородом, лихорадка, уменьшение толерантности к нагрузкам, рентгенологически определяемая инфильтрация говорят об отторжении. Последовательное сканирование легочного кровотока, демонстрирующее уменьшение перфузии помогает в диагностике отторжения после трансплантации одного легкого.
14. Опишите феномен химеризма в трансплантологии.
Химеризм проявляется распределением лейкоцитов между трансплантатом и реципиентом таким образом, что трансплантат становится генетическим объединением донора и реципиента. Химеризм увеличивает толерантность хозяина к трансплантату. Химеризм был впервые описан в 1969 году, когда у жешцин-реципиентов мужской печени было обнаружено (методом определения телец Барра) появление полностью женских клеток системы Капфера (Kupffer) (печеночные макрофаги).
В 1992 концепция распределения была клинически подтверждена, когда было обнаружено что лейкоциты из донорских почек располагаются в отдаленных лимфатических узлах.
15. Существуют ли тканевые макрофаги в сердце и легких?
Да, конечно. Тканевые миокардиальные макрофаги и тканевые альвеолярные макрофаги являются весьма активным клеточным компонентом сердца и легких.
16. Развивается ли химеризм в сердце и легких?
Да. Так как и в сердце, и в легких содержатся лейкоциты, участвующие в химеризме.
17. Чем интересен химеризм?
Природа пытается научить нас осуществлять трансплантацию без применения иммуносупрессии. Наша задача — понять, почему химеризм отмечается у некоторых реципиентов, а у других нет, т.е. обнаружить механизмы индукции химеризма, что бы получить возможность фармокологически индуцировать химеризм у всех реципиентов.
18. Перечислите основные типы растворов для консервации сердца и легких.
Раствор Евро-Колинс (Euro-Colins) и раствор Университета Висконсина для легких и кристаллоидной кардиоплегии и раствор Университета Висконсина для сердца.
19. Какой процент легочного кровотока поступает к трансплантированным легким после трансплантации одного легкого?
Обычно около половины (возможно почти весь) легочного кровотока проходит через слаборезистентную циркуляторную систему трансплантированных легких (в зависимости от пульмонарного сосудистого сопротивления контралатерального нативного легкого). При проведении предоперационного сканирования легочной перфузии и при равных прочих факторах следует сохранять легкое с наилучшей перфузией, а другое заменить.
20. Необходимо ли применение искусственного кровообращения при трансплантации легких?
Нет. Однако у больных с легочной гипертензией (первичной или вторичной) обычно применяют искусственное кровообращение до удаления легкого реципиента. Аппарат искусственного кровообращения всегда наготове.
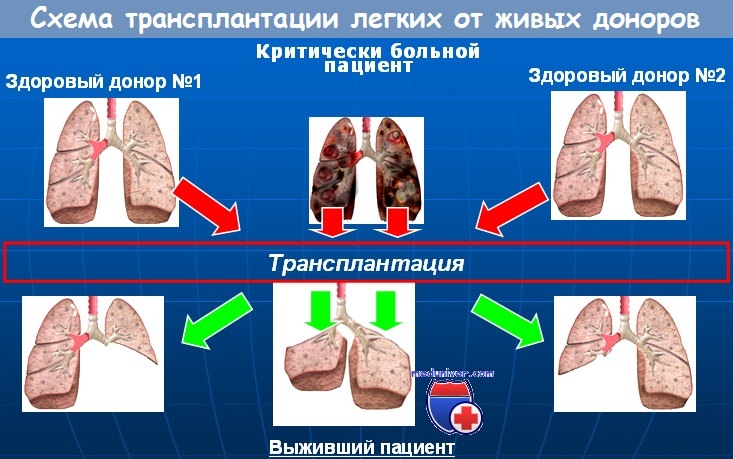
21. Возможна ли living-related (от живых доноров) трансплантация?
Да. Living-related трансплантация представляет собой новый подход с целью увеличения донорского фонда.
22. Что представляет собой объемо-редуцирующая хирургия легких? Насколько она важна для пациентов, ожидающих трансплантацию легких?
Объемо-редуцирующая хирургия легких предполагает консервативные методы лечения для больных: (1) не подлежащих трансплантации легкого или (2) ожидающих трансплантацию. При объемо-редуцирующей хирургии легких удаляются нефунционирующие и разрушенные сегменты легкого. Удаление нефункционирующих частей легких создает больше пространства для воздухообмена.
Таким образом лечат эмфизему, сглаженную диафрагму и диспноэ, связанное с курением (разрушение верхних долей) и недостаточностью альфа-1 антитрипсина (разрушение нижних долей).
23. Кто является наиболее подходящим кандидатом к объемо-редуцирующей хирургии легких?
Больные, не имеющие противопоказаний и у которых отсутствует или редуцирована перфузия приблизительно в 30-40% легких, с сохранением гомогенного распределения кровотока. Таким образом, качественное сканирование легочной перфузии обеспечивает существенной информацией в отборе пациентов.
24. Каковы противопоказания к объемо-редуцирующей хирургии легких?
• Легочная гипертензия (среднее давление в легочной артерии > 35 мм рт. сг. или систолическо > 45 мм рт. ст.)
• Тяжелая ишемическая болезнь сердца
• Торакотомия или плевродез в анамнезе
• Продолжительное течение бронхиальной астмы, бронхоэктазов или хронический бронхит с гнойной мокротой
• Выраженный кифосколиоз
25. В чем разница в составе между раствором Евро-Колинс и раствором Университета Висконсина?
Раствор Евро-Колинс — это раствор глюкозы с ионными компонентами, близкими по составу к межклеточной среде.
Раствор Университета Висконсина не содержит глюкозы, но содержит следующие компоненты, отсутствующие в растворе Евро-Колинс: гидрокси-этил-крахмал (предотвращает расширения интерстициального пространства), лактобионат и раффиноза (подавляют набухание клеток под воздействием гипотермии), глутатион и аллопуринол (уменьшают цитотоксическое действие свободных радикалов кислорода) и аденозин (субстрат для образования аденозинтрифосфата, вазодилятатор; активирует защитные механизмы прекондиции).
26. Сколько производится ежегодно трансплантаций легких? Увеличивается ли их количество или уменьшается?
Интересно, хотя первая трансплантация легких была произведена в 1963 году, до конца 80-х годов их количество было незначительным (в 1986 — 1 трансплантация легких; в 1989 — 132 трансплантации легких). Затем количество производимых трансплантаций резко возросло до 700 в год к 1994, а далее уменьшилось до 625 в год.
27. Отмечается ли разница в выживаемости при трансплантации одного легкого и двух легких?
Нет. Трехлетняя выживаемость составляет около 50% для каждой.
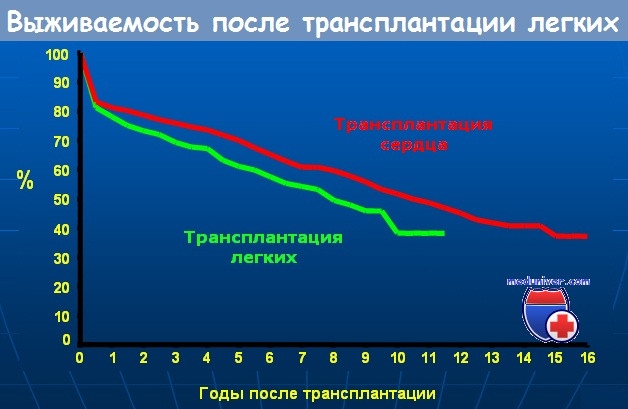
28. Какова одна-, двух- и трехлетняя выживаемость при трансплантации одного легкого?
Действительная выживаемость составляет соответственно 45%, 40% и 30%. В дальнейшем эти цифры закономерно уменьшаются.
Видео лекция по трансплантации легких в России и в мире
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Трансплантация легких
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Трансплантация одного или обоих легких используется с одинаковым успехом при большинстве заболеваний легких без вовлечения сердца; исключение составляют хронические диффузные инфекции (например, бронхоэктатическая болезнь), при которых предпочтительнее трансплантация обоих легких. Трансплантация комплекса сердце-легкие показана при синдроме Эйзенменгера и любых легочных заболеваниях с тяжелой необратимой желудочковой дисфункцией; corpulmonale (легочное сердце) не является показанием к подобной трансплантации, поскольку часто состояние рецидивирует после трансплантации легких. Трансплантация одного или двух легких проводится одинаково часто и по крайней мере в 8 раз чаще, чем трансплантация комплекса сердце-легкие.
Почти все легкие получают от доноров-трупов со смертью мозга и работающим сердцем. Реже, если органы донора-трупа не подходят, при трансплантации используется доля живого донора (обычно при трансплантации от родителей детям). Донором может быть человек моложе 65 лет, никогда не куривший, не имеющий активных заболеваний легких, что подтверждается оксигенацией (Pa 02/Fi 02 > 250-300 мм рт. ст.), растяжимостью легких (пиковое давление на вдохе 50 мм рт. ст.; давление в правом предсердии больше 10 мм рт. ст. и пиковое систолическое давление > 50 мм рт. ст. для пациентов с первичной легочной гипертензией; прогрессирование клинических, рентгенографических и физиологических симптомов заболевания.
Трансплантация легких до сих пор остается одним из наименее освоенных направлений современной трансплантологии. Успешное осуществление трансплантации легкого зависит от правильного подбора донора и реципиента, ранней диагностики кризов отторжения, эффективности иммуносупрессии, правильной противоинфекционной терапии в послеоперационном периоде.
Развитие терминальной стадии поражения легкого при деструкции легочной паренхимы или сосудистой сети является одной из ведущих причин инвалидизации и смертности взрослых больных. Для лечения терминальной стадии заболеваний легкого разработано несколько вариантов трансплантации, каждый из которых имеет определенные теоретические и практические преимущества. К ним относятся трансплантация легких, комплекса сердце-легкие. Выбор процедуры трансплантации легкого основан в значительной степени на последствиях оставления нативного легкого на месте. Например, однолегочная трансплантация легких не показана при наличии инфекции или тяжелой буллезной эмфиземы, которые присутствуют в контралатеральном легком. Перекрестная инфекция заразила бы здоровое пересаженное легкое, а выраженное буллезное поражение в нативном легком может приводить к большому несоответствию перфузии и вентиляции и смещению средостения. В таких случаях предпочтение отдается трансплантации обоих легких. Трансплантация одиночного легкого вполне выполнима без ИК и редко осложняется кровотечением. Другим преимуществом трансплантации одиночного легкого является то, что это выполняемый бронхиальный анастомоз заживает с существенно меньшим количеством осложнений по сравнению с единым трахеальным анастомозом при трансплантации блока двух легких.
При установлении диагноза хронической легочной гипертензии с правожелудочковой недостаточностью методом выбора является трансплантация комплекса сердце-легкие. Однако при сохраненных функциональных возможностях сердца оптимальной для больного с терминальной стадией заболеваний легкого может оказаться трансплантация изолированного легкого.
Анатомо-физиологические особенности дыхательной системы и патофизиологические изменения при терминальной стадии паренхиматозных заболеваний легких Терминальная стадия паренхиматозных заболеваний легкого по своей этиологии является рестриктивной, обструктивной или инфекционной. Рестриктивные заболевания легких характеризуются внутритканевым фиброзом с потерей эластичности и растяжимости легкого. По своей природе большинство фиброзных заболеваний являются идиопатическими (неясного происхождения), но они также могут быть вызваны ингаляционными повреждениями или иммунными процессами. Интерстициальные заболевания легких воздействуют на кровеносные сосуды с последующим проявлением легочной гипертензии. Болезни этой категории функционально проявляются снижением объемов легких и диффузионной способности при сохраненной скорости воздушного потока.
Наиболее частой причиной терминальной стадии обструктивных заболеваний легкого является эмфизема, вызываемая курением, однако есть и другие причины, включая астму и некоторые сравнительно редкие врожденные болезни. Среди них альфа1-антитрипсиновая недостаточность, связанная с выраженной буллезной эмфиземой. При обструктивных заболеваниях сопротивление дыхательных путей резко повышено, снижена скорость экспираторного потока и резко увеличен остаточный объем, нарушаются вентиляционно-перфузионные соотношения.
Инфекционную этиологию терминальной стадии заболеваний легкого имеют муковисцидоз и бронхоэктатическая болезнь. Муковисцидоз вызывает обтурацию периферических дыхательных путей слизью, хронический бронхит и бронхоэктазы. Кроме того, терминальная стадия легочных сосудистых заболеваний может быть следствием первичной легочной гипертензии, которая является относительно редким заболеванием неизвестной этиологии и проявляется повышением ЛСС вследствие мышечной гиперплазии ЛА и фиброза артериол маленького диаметра. Еще одной причиной деформации легочного артериального русла является ВПС с синдромом Eisenmenger и диффузными артериовенозными пороками развития.
Основными показаниями для трансплантации при терминальной стадии любой болезни легких являются прогрессивное ухудшение толерантности, повышение потребности в кислороде и задержка С02. Другими факторами, предопределяющими трансплантацию, являются возникновение необходимости постоянной инфузионнои поддержки и проявление физической и социальной несостоятельности.
Выполнение операции зависит от скорости нарастания функциональных нарушений и возможности ПЖ компенсировать прогрессирование легочной гипертензии. Учитывая ограниченность получения донорских органов, специальные противопоказания к трансплантации легкого включают выраженное истощение, нервно-мышечные заболевания или зависимость от ИВЛ (т.к. сила дыхательной мускулатуры чрезвычайно важна для успешного выздоровления); серьезную деформацию грудной клетки или заболевания плевры (усложнение хирургических процедур и послеоперационной вентиляции); прогрессирование правожелудочковой недостаточности или глюкокортикоидной зависимости (потому что заживлению анастомозированных дыхательных путей препятствуют стероиды).

Трансплантация легких: предоперационная подготовка
Исследование дооперационной функции легких и катетеризация правых отделов сердца, исследование вентиляционно-перфузионых соотношений и показатели газов артериальной крови весьма полезны для прогноза возможных трудностей, которые могут иметь место в течение и после индукции. Например, снижение скорости потока на выдохе и патологическая задержка воздуха в легких могут увеличивать гипоксемию и гиперкапнию и приводить к гемодинамической нестабильности во время масочной вентиляции и после интубации трахеи. Повышенное ДЛА может служить показателем необходимости применения ИК, потому что правожелудочковая недостаточность может развиться практически внезапно при начале однолегочной вентиляции или сшивании легочной артерии. Даже при отсутствии легочной гипертензии рекомендуется иметь аппарат для веновенозного обхода для этих случаев, поскольку газообмен настолько скомпрометирован. Очевидно, что мониторинг системного и легочного АД жизненно важен при трансплантации легкого, хотя выраженная одышка может обусловить значительные трудности катетеризации внутренней яремной вены до индукции.
Трансплантация одного легкого
Процедура трансплантации одного легкого включает пневмонэктомию и имплантацию нового легкого, а также мобилизацию сальника на сосудистой ножке для перемещения на бронхи. Если нативные легкие повреждены одинаково и нет признаков плеврального рубцевания, для трансплантации выбирается левое легкое по техническим причинам: правые легочные вены реципиента менее доступны, чем левые, левый бронх длиннее, к тому же левая половина грудной клетки легче адаптируется к донорскому легкому большего, чем у реципиента, размера. Большинство хирургов предпочитает, чтобы во время удаления донорское легкое было коллабировано, для этой цели используют блокираторы бронхов и двухпросветные эндобронхиальные трубки.
Для вводной анестезии используется методика быстрой интубации, предпочтение отдается ЛС, не имеющим кардиодепрессивного и гистаминогенного эффектов (например, этомидату, векурония бромиду). Использования динитрогена оксида избегают у больных с буллами или повышенным ЛСС, а также в случаях, когда для поддержания приемлемой сатурации артериальной крови необходимо использование 100% кислорода. Для поддержания анестезии успешно используются опиоиды в высоких дозах, мощные ИА в сочетании с длительно действующими миорелаксантами. С началом однолегочной вентиляции, как правило, возникают резкие нарушения газообмена и гемодинамики. Методы улучшения оксигенации в этих условиях включают использование ПДКВ в зависимом легком, СРАР или высокочастотную вентиляцию в независимом легком при сшивании легочной артерии. Если в этот момент резко возрастает ДЛА, может развиться правожелудочковая недостаточность.
Сосудорасширяющие и/или инотропные ЛС могут уменьшать нагрузку на правое сердце, при их неэффективности должна быть продолжена однолегочная вентиляция. Точно так же, если показатели гемодинамики или системная артериальная сатурация ухудшаются при пережатии легочной артерии перед пневмонэктомией, может возникнуть необходимость использования АИК.
После восстановления кровоснабжения донорского легкого заканчивается период ишемии, но до момента нормальной вентиляции трансплантата системное артериальное насыщение обычно снижено. На этой стадии может потребоваться процедура бронхоскопии, чтобы удалить из дыхательных путей секрет или кровь для восстановления наполнения трансплантата воздухом. Как только выполнен бронхиальный анастомоз, в грудную клетку перемещается сальник на неповрежденной сосудистой ножке, которым укутывается бронхиальный анастомоз. После закрытия грудной клетки эндобронхиальная трубка заменяется на стандартную эндотрахеальную.
Трансплантация обоих легких
Трансплантация обоих легких наиболее часто используется у больных с первичной легочной гипертензией или муковисцидозом. Операция трансплантации блока двух легких выполняется в положении лежа на спине, и, поскольку оба легких замещаются одновременно, использование АИК обязательно. Используется кардиоплегическая остановка сердца для выполнения анастомозов культи левого предсердия, содержащей все четыре легочных венозных отверстия. Дыхательные пути прерываются на уровне трахеи, поэтому используется стандартная эндотрахеальная трубка. Поскольку нарушено системное артериальное кровоснабжение трахеи, используется укутывание ее васкуляризированным сальником. Обширное ретрокардиальное рассечение часто приводит к денервации сердца; кроме того, затруднен контроль возникновения послеоперационного кровотечения. Двусторонняя последовательная трансплантация одиночным легким была введена для хирургического лечения того же контингента больных, которым показана трансплантация блока двух легких, но она устраняет необходимость проведения ИК и выполнения трахеального анастомоза. Относительным недостатком этой операции является то, что при последовательной имплантации время ишемии второго трансплантата легкого значительно удлиняется.
Процедура трансплантации легких
Холодный кристаллоидный консервирующий раствор, содержащий простагландины, вводится через легочные артерии в легкие. Донорские органы охлаждаются ледяным солевым раствором in situ или посредством легочно-сердечного шунта, затем удаляются. Назначается профилактический курс антибиотикотерапии.
Трансплантация одного легкого требует заднелатеральной торакотомии. Собственное легкое удаляется, формируются анастомозы с соответствующими культями бронхов, легочных артерий, легочных вен донорского легкого. Бронхиальный анастомоз для достижения адекватного заживления требует инвагинации (введения одного конца в другой) или обертывания сальником или перикардом. Достоинством является более простая техника операции, отсутствие необходимости применения аппарата искусственного кровообращения и системных антикоагулянтов (обычно), точного подбора размера и пригодность контралатерального легкого от того же донора для другого реципиента. Недостатки включают возможность несоответствия вентиляции/перфузии между собственным и трансплантированным легкими и возможность плохого заживления одиночного бронхиального анастомоза.
До реперфузии трансплантируемого легкого реципиентам часто назначают метилпреднизолон внутривенно. Обычный курс иммунносупрессивной терапии включает ингибиторы кальциневрина (циклоспорин илитакролимус), ингибиторы метаболизма пурина (азатиоприн или микофенолата мофетил) и метилпреднизолон. В течение первых двух недель после трансплантации профилактически назначают антитимоцитарный глобулин или ОКТЗ. Глюкокортикоиды могут быть отменены для нормального заживления бронхиального анастомоза; они заменяются более высокими дозами других лекарств (например, циклоспорин, азатиоприн). Иммуносупрессивная терапия продолжается неограниченно долго.
Отторжение развивается у большинства пациентов, несмотря на иммуносупрессивную терапию. Симптомы и объективные признаки похожи при гиперострой, острой и хронической формах и включают лихорадку, диспноэ, кашель, снижение Sa02, появление интерстициальных инфильтратов на рентгенограмме, снижение ОФВ более чем на 10-15 %. Гиперострое отторжение необходимо отличать от ранней дисфункции трансплантата, причиной которой является ишемическое поражение в течение процедуры трансплантации. Диагноз подтверждается бронхоскопической трансбронхиальной биопсией, при которой обнаруживается периваскулярная лимфоцитарная инфильтрация мелких сосудов. Обычно эффективно внутривенное введение глюкокортикоидов. Лечение рецидивирующих или резистентных случаев проводится по-разному и включает высокие дозы глюкокортикоидов, циклоспорин аэрозольно, антитимоцитарный глобулин иОКТЗ.
Хроническое отторжение (через год и более) встречается менее чем у 50 % пациентов; оно принимает форму облитерирующего бронхиолита или не так часто, атеросклероза. Острое отторжение может увеличить риск возникновения хронического. У пациентов с облитерирующим бронхиолитом отмечается кашель, диспноэ, снижение ОФВ с физикальными или рентгенографическими признаками процесса в дыхательных путях или без них. При дифференциальной диагностике необходимо исключить пневмонию. Диагноз ставится на основании данных бронхоскопии и биопсии. Никакое лечение не является особенно эффективным, но может быть рекомендовано назначение глюкокортикоидов, антитимоцитарного глобулина, ОКТЗ, циклоспорина ингаляционно и ретрансплантации.
Наиболее частыми хирургическими осложнениями являются плохое заживление трахеального или бронхиального анастомозов. Менее чем у 20 % реципиентов одного легкого развивается бронхиальный стеноз, который приводит к одышке и обструкции дыхательных путей; его можно лечить путем дилатации и установки стен-та. Среди других хирургических осложнений выделяют охриплость голоса и паралич диафрагмы, которые являются следствием поражения возвратного гортанного или диафрагмального нервов; нарушение моторики ЖКТ из-за поражения торакального отдела блуждающего нерва; пневмоторакс. У некоторых пациентов развиваются наджелудочковые аритмии, возможно, вследствие изменения проводимости при наложении швов между легочной веной и предсердием.
Какой прогноз имеет трансплантация легких?
Оценка состояния пациента после трансплантации легких
Послеоперационное лечение больных после изолированного трансплантата легкого включает интенсивную респираторную поддержку и дифференциальную диагностику между отторжением и инфекцией легкого, для чего используются трансбронхиальные биопсии, выполняемые с помощью гибкого бронхоскопа. Ранняя дыхательная недостаточность может возникать вследствие консервации или реперфузионных повреждений и характеризуется наличием выраженного артериоальвеолярного градиента по кислороду, снижением эластичности легочной ткани (низким легочным комплайенсом) и наличием паренхиматозных инфильтратов, несмотря на низкое сердечное давление наполнения. В этих случаях обычно используется ИВЛ с ПДКВ, но, учитывая особенности анастомозирования вновь восстановленных дыхательных путей, ингаляционное давление поддерживается на минимальных значениях. Fi02 также поддерживается на самых низких значениях, позволяющих получить достаточную сатурацию крови.
Кровотечение является осложнением, которое наиболее часто происходит после трансплантации двух легких единым блоком, особенно у больных с плевральным поражением или синдромом Eisenmenger с обширными средостенными сосудистыми коллатералями. Диафрагмальный, блуждающий и возвратный ларингеальный нервы подвергаются большой опасности в ходе трансплантации легкого, и их повреждение усложняет процесс прекращения ИВЛ и восстановления адекватного самостоятельного дыхания. Первичное заживление обычно имеет место для большинства бронхиальных анастомозов; весьма редко бронхиальные фистулы приводят к стенозам, которые могут успешно лечиться с помощью силиконовых стентов и дилатаций. Несостоятельность трахеальных анастомозов, напротив, часто приводят к фатальным медиастинитам. После выполнения трансплантации комплекса сердце-легкие описано развитие облитерирующего бронхиолита, характеризующегося деструкцией малых дыхательных бронхиол.