Покрытие золотом в домашних условиях: методы золочения
Научившись выполнять золочение в домашних условиях, что не так сложно, как может показаться на первый взгляд, вы сможете вернуть вторую жизнь любимым украшениям из меди и серебра. Изделия, изготовленные из золота, уже на протяжении многих лет пользуются огромной популярностью как у женщин, так и у мужчин. Чтобы обладать такими изделиями без серьезных затрат на их приобретение, достаточно овладеть технологией золочения.
Покрыть позолотой можно как цветные сплавы, так и сталь или чугун
На изделия из каких металлов можно наносить слой позолоты
Наиболее распространенным процессом является золочение серебра, но золотое покрытие можно наносить и на поверхность других металлов. Так, позолота может быть нанесена на изделия из меди, латуни и цинка, а также из железа и стали и др.
На вопрос о том, как позолотить металл в домашних условиях, однозначного ответа не существует. Все зависит от того, изделия из какого металла необходимо подвергнуть такой обработке. На выбор технологии золочения, осуществляемого в домашних условиях, влияет также результат, которого необходимо добиться.
С помощью золочения можно придать обычным вещам совершенно другой вид
Для золочения металла могут использоваться разные методы, наиболее распространенными из которых являются:
Каждый из таких методов золочения, выполняемого в домашних условиях, требует использования определенных химических реактивов, инструментов и оборудования.
Приготовление и использование хлорного золота
Чтобы покрыть слоем позолоты металл, часто используют раствор, называемый хлорным золотом. Для приготовления такого раствора золото растворяют в «царской водке», представляющей собой смесь соляной и азотной кислот. Соляную и азотную кислоты берут в пропорции 3 : 1. Золото помещают в этот состав, а затем выпаривают жидкость. Выполнять процедуру выпаривания жидкости из такого раствора следует очень аккуратно, чтобы не получить ожоги кожных покровов и дыхательных путей. Сухое вещество, оставшееся после выпаривания, как раз и является хлорным золотом.
При выпаривании нужно отделить открытый огонь от емкости с раствором, например, сделав прослойку из асбестовой крошки, насыпанной в отдельную посудину
Перед тем как применять хлорное золото для позолоты, его необходимо смешать с раствором цианистого калия и отмученным мелом, в результате чего должна получиться кашицеобразная масса. Такой кашицей, используя кисточку, покрывают изделие, после чего его выдерживают некоторое время, а затем тщательно промывают и полируют.
Для золочения стали хлорное золото смешивают с эфиром. Покрытое таким составом изделие оставляют на некоторое время, пока эфир полностью не испарится, а затем обработанную поверхность просто натирают тканью для придания золотого блеска.
Используя хлорное золото, предварительно смешанное с эфиром, на металлический предмет можно наносить различные надписи и узоры. Для того чтобы провести такую процедуру, в полученный раствор окунают гусиное перо и выполняют требуемые надписи и узоры, которые после испарения эфира и полировки будут сверкать золотым блеском.
Большие поверхности покрывают позолотой с помощью мягкой кисти
Как уже говорилось выше, золотое напыление часто наносят на серебро, для чего также может использоваться хлорное золото. Чтобы выполнить химическое золочение изделий из данного металла, необходимо приготовить смесь, включающую в себя следующие компоненты:
Химическое золочение, которому необходимо подвергнуть серебро, можно также выполнять с использованием смеси из:
Саму процедуру напыления слоя золота на поверхность металла при использовании химических растворов выполняют в следующей последовательности.
Применение цинкового контакта
Чтобы получить более толстый позолоченный слой, используют цинковый контакт. Таким методом можно, например, покрыть слоем золота серебро. Для золочения готовят состав из таких компонентов, как:
Потребуется некоторое время на растворение всех компонентов состава
Изделия, изготовленные из меди и латуни, покрываются под золото в растворе следующего состава:
Предметы, на поверхность которых необходимо нанести слой позолоты, тщательно очищаются от грязи и жира, затем их помещают в предварительно нагретый состав для золочения. Уже находящиеся там изделия соединяют с цинковой палочкой, которая и выступает в качестве контакта.
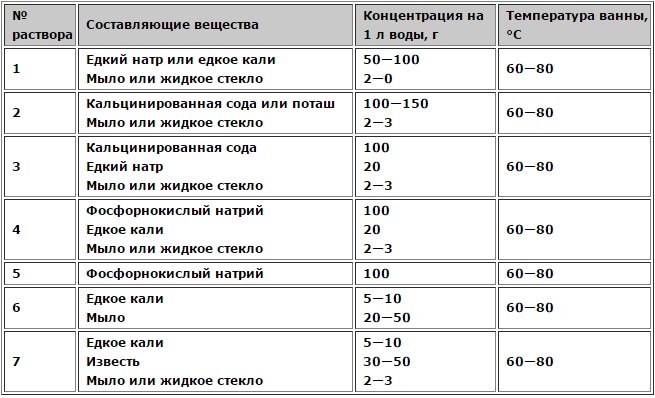
Составы обезжиривающих растворов
Чтобы позолота, нанесенная на поверхность изделий из стали, цинка и олова, была качественной и отличалась хорошей адгезией, перед золочением их необходимо подвергнуть процедуре омеднения.
Гальванический метод нанесения позолоты
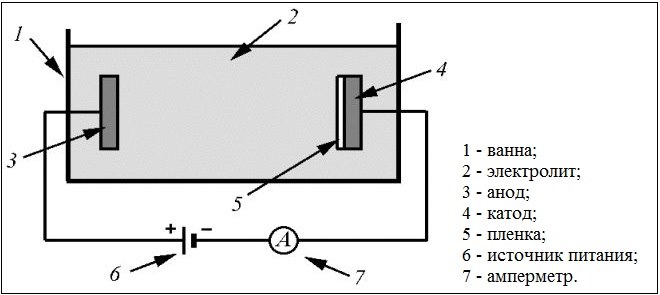
Наиболее прочный и качественный слой позолоты позволяет получить гальваническое покрытие золотом, выполняемое в специальных электролитических растворах. Такая технология золочения очень напоминает цинкование, так как для ее реализации используются гальваника и аналогичные электрохимические процессы.
Схема гальванической ванны
В зависимости от химического состава раствора, в котором выполняется гальванизация, сформированная позолота может иметь красноватый или светло-желтый оттенок. В основном золочение изделий из металла по данной технологии выполняют в растворах двух типов.
Электролиты для золочения первого типа готовят в следующей последовательности.
Чтобы позолотить серебро или любой другой металл таким методом, приготовленный состав доводят до температуры 50–62° и используют для протекания процесса платиновый анод. После истощения такого электролита для золочения в него добавляют хлорное золото.
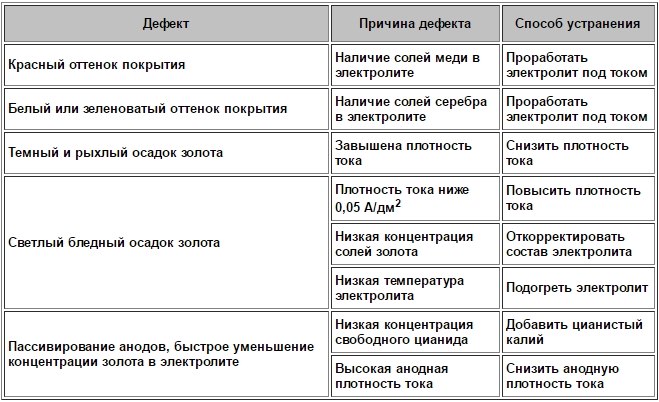
Дефекты при использовании электролитов золочения и способы их устранения
Второй тип электролита для золочения носит название «золотая ванна Зельми». В таком растворе золотят серебро, сталь, изделия из олова, меди, латуни, христофлевого металла. Приготовление этого электролита для золочения происходит в несколько этапов.
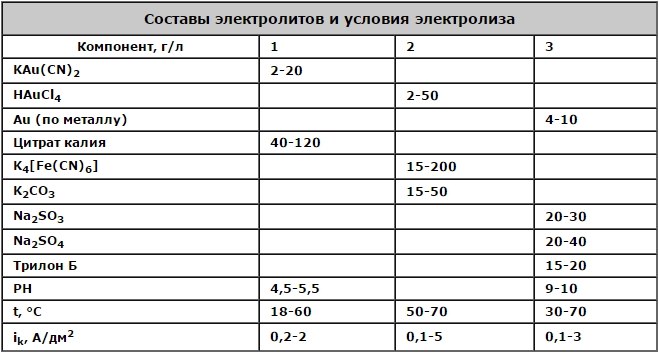
Менее токсичными считаются условно бесцианидные электролиты золочения, характеристики которых приведены в таблице
Обработку в таком электролите для золочения проводят на протяжении 15–16 часов, используя для этого элемент Даниэля и слабые токи. В результате на поверхности металлического изделия формируется эффектная матовая позолота.
Задаваясь вопросами о том, что такое золочение и как его выполнить, следует учитывать, что для его осуществления используются различные методики, только часть из которых описана выше. Выбирая из таких технологий оптимальную, надо принимать во внимание целый ряд факторов, а также ориентироваться на желаемый результат.
Различные способы нанесения позолоты в домашних условиях
Золочение в домашних условиях осуществляют двумя способами: электролитическим (гальваническим) и химическим. Для покрытия изделий позолотой требуются реактивы, которых не найти в свободной продаже: цианид калия, азотная и соляная кислоты. Также необходимо специальное оборудование: электролитические ванны и источник постоянного тока. Процесс золочения достаточно трудоемкий, требует сноровки, аккуратности и некоторого опыта.
Химический способ
А) Химическое золочение — процесс нанесения хлорида золота на металл, из которого сделано изделие. Хлорное золото готовится так: металл нужно расковать в фольгу и измельчить на мелкие кусочки, погрузить их в смесь азотной и соляной кислот (в так называемую царскую водку). Необходимо взять 30 г концентрированной соляной и 10 г концентрированной азотной кислот. На 1 г золота должно приходиться 10 мл раствора.
Нанесение позолоты в домашних условиях
Растворение должно происходить в фарфоровой посуде, процесс может длиться от нескольких часов до 2-3 суток. Когда металл полностью растворится, необходимо выпарить смесь в водяной бане при 70-80 градусах до появления вязкой золотистой жидкости. При выпаривании раствор помешивают стеклянной палочкой.
Чтобы приготовить смесь для золочения, потребуются:
Перед нанесением позолоты поверхность предмета необходимо обезжирить 10-20% едким натрием или кипячением в растворе соды. Далее промывают изделие в 25% растворе соляной кислоты, т. е. протравливают. После обезжиривания необходимо промыть предмет в воде.
Далее погружают изделие для позолочения в приготовленную смесь из горячей воды, поташа, хлорида натрия и хлорного золота. Предмета касаются цинковой палочкой, через некоторое время он становится позолоченным. После этого его извлекают и промывают, вытирают насухо и полируют при помощи шерстяной ткани.
Б) Помимо метода химического золочения используют метод натирания при помощи пасты. При таком способе нанесения позолоты слой покрытия тоньше. В состав пасты для натирания входит желтая кровяная соль (гексацианоферрат [II] калия), винный камень, порошок из мела, хлорное золото. Для изготовления 100 г пасты берут 55 г мела, 5 г кремортартара, 30 г желтого гексацианоферрата калия и 10 г хлорида золота, ингредиенты перемешивают. Полученную пасту разбавляют водой до образования кашицы. Этой смесью натирают обезжиренное изделие при помощи шерстяной ткани.
В) Существует третий метод покрытия. Для этого 10 г золота растворяют в смеси азотной и соляной кислоты, воды — всех компонентов взять по 25 г. Добавляют в этот состав 300 г поташа (карбоната калия). Готовят котел, в котором кипятится вода (2 л), вливают в нее эту смесь. Кипячение продолжается 2 часа.
Украшения, нуждающиеся в позолочении, прокаливают и протравливают сначала серной кислотой, потом азотной. Затем изделие обматывают проволокой из латуни (сплав цинка и меди), и погружают на мгновение в смесь азотной, серной и соляной кислот. Потом предметы ополаскивают, далее поочередно загружают их в ртуть, а потом в воду. Через полминуты их окунают в приготовленную жидкость, моют, высушивают в горячих опилках.
Изделие с позолотой
Чтобы покрыть позолотой изделия из стали и железа, необходимо растворить сироп хлорида золота в эфире. Полученным составом, нанесенным на тряпочку, покрывают и натирают поверхность предмета из стали или железа. Затем эфир испаряется, а золото остается.
Если необходимо не просто покрыть позолотой изделие, а сделать на нем узор, то в смеси эфира с хлорным золотом смачивают перо и проводят им по предмету.
Желательно до позолочения предметов из железа, стали, олова, цинка покрывать поверхность медью, так как на нее лучше ложится позолота.
2) Цинковые предметы.
Покрытие цинковых изделий осуществляется при помощи натирания их пастой. Готовится она из 60 г цианида калия, 20 г хлорного золота и 100 г воды — эти ингредиенты смешиваются. В данный раствор добавляют 5 г кремортартрата и 100 г порошка карбоната кальция (мела). Полученный состав наносят при помощи щеточки или кисти.
Для покрытия серебряных украшений есть два варианта раствора, в которые погружают предметы:
Во время погружения изделия необходимо прикоснуться к нему цинковой палочкой и оно начнет покрываться золотом. После этого предмет извлекается из раствора, промывается и вытирается, полируется шерстяной тряпкой.
Хлорид золота (2 г) и цианид калия (32 г) растворяют в 0,5 л воды. В других полутора литрах воды тем временем растворяют едкий калий (6 г) и фосфорно-натриевую соль (10 г). Смешивают оба раствора и кипятят.
Гальваника
Существует два способа:
Способы позолоты в домашних условиях трудоемки и не всегда доступны. Предпочтителен метод химического золочения или натирания.
Цинкование меди в золотой цвет.
поэтому кто будет пользоваться таким способом цинкования, используйте его исключительно для декоративных предметов.
Получилась медь, покрытая латунью.
тут был парень с историей как ему продали медное колечко под видом золотого. признавайся, твоих рук дело?
никто не подскажет как получить серебристый цвет меди без нагрева..
В каком магазине ты нашел цинковые гвозди?
Метод отлично работает, и не только с медью.
Вулкан Бёттгера. Эксперимент. (запись №6)
Окислителем является хром ( VI ), который в результате реакции превращается в хром ( III ). В результате этого образуется зеленый оксид хрома.
(NH4)2Cr2O7 = N2 + 4H2O + Cr2 O 3
Ученый решил провести опыты по способности вещества взрываться от удара и загораться от лучины. При ударе кристаллы дихромата аммония превратились в порошок.
После чего ученый поднес к горке порошка горящую лучину. Возгорания не произошло, но вокруг лучинки начали подпрыгивать раскаленные частицы вещества, а горка начала увеличиваться.
Также изменился ее цвет, он стал зеленым.
Металлы, стоящие в ряду левее водорода, вытесняют водород при взаимодействии с водными растворами кислот-неокислителей; наиболее активные металлы (до алюминия включительно) и при взаимодействии с водой.
Дихромат аммония до термической реакции (фото из интернета, не мое)
Хлорируем Mo, W, Al, Ga, As, Sb
Продолжаем серию видео, в котором смотрим на то, как на практике происходит взаимодействие хлора с разными химическими элементами. На бумаге-то оно всё хорошо. А вот на практике важны условия протекания процессов.
P.S.: в прошлых видео сжигали в хлоре галогены, щелочные металлы, золото, ртуть, уран, кремний, германий, олово, железо, медь.
P.S.2: в следующий раз будем поджигать воду во фторе.
Фараоновы змеи. Эксперимент (запись №5)
Для опыта необходимы:
1) Глюконат кальция
4) Негорючая поверхность
Во время нагревания глюконата кальция, происходит реакция с выделением углерода, углекислого газа, оксида кальция и воды.
С12H22CaO14 + O2 = 10C + 2CO2 ↑ + СaO + 11H2O
Из-за выделения газа и происходит «рост».
«Фараоновы змеи» довольно хрупкие, достигают в длину около 15 см.
Вот что происходит с таблетками глюконата кальция при нагревании
ГЕКСАХЛОРМОЛИБДАТ КАЛИЯ
В этом видео покажу технологию синтеза этого страшного вещества.
Надо ли вам об этом знать? – Вряд ли.
Что может быть интересно? – различные нюансы работы.
Чем занимается химик-инженер [2]
Во тьме ночной, при свете дня
Гружу сырье в реактор я
Катализатор коль забыл
Но все же вспомнил: тот внутри
И можно сгрызть печенья три
Серная кислота. Способы получения и химические свойства
Получаем натрий из ВОДНОГО раствора
Как всем известно (ну тем, кто учил химию) получить щелочные металлы из водных растворов невозможно. По крайней мере так учат в школе. Речь идёт об электролитическом методе.
При этом в продолжении темы рассказывают об электролизе расплавов щелочей, из которых всё же можно выделить щелочные металлы в виде металлов.
В видео ниже вы увидите, как буквально на коленке можно организовать процесс электролиза расплава щелочей и получить металлический натрий. (готовьте салфетки, чтобы подтирать кровь из глаз)
А также продемонстрирован лайфхак, как получить щелочные металлы их ВОДНЫХ растворов их солей.
Карманное пособие по анодированию. )))
Химический Брендинг на грани
Новый Брендинг на грани — политическая партия химиков)
P.S.: Сегодняшний пост должен был быть приурочен ко Дню химика (30.05), но там вмешался День защиты детей. В общем, лучше поздно, чем никогда – химики, с прошедшим!)
Также я создал отдельные сообщества для Брендинга на грани. Там будут появляться как новые выпуски, так и выходившие ранее и полюбившиеся вам)
Электроны. Свойства. Опыты
Наконец смог собрать всевозможные газоразрядные трубки, чтобы поэкспериментировать с ними и продемонстрировать валам, какие же опыты ставили большее 100 лет назад такие ученые, как Уильям Крукс, Вильгельм Конрад Рентген и другие.
В этом видео поиграем с электронами ( будем толкать их магнитным полем), сделаем рентген нокии 3310 и ещё всякое по мелочи.
P.s.: дизайнер обложек занят, сдаёт ЕГЭ, поэтому пока слепил то, что получилось.
Изотопы водорода
Попытка пошутить о работе v.3
Пять красивых опытов, которые вы можете провести дома вместе с детьми
Детей с раннего возраста нужно приучать к науке. Лучше всего для этого подойдут опыты — наглядные, интересные и приводящие к неожиданным для детей результатам. Мы подобрали пять научных и красивых экспериментов, которые можно провести в домашних условиях.
Зачастую родителям кажется, что научить детей чему-то, связанному с наукой, — просто сизифов труд. Конечно, можно предоставить эту нелегкую задачу интернету — вам на помощь придут Google и «Яндекс». Но рано или поздно придется разбивать сложные темы на уроки, которые ребенок сможет усвоить. Так что… Может, лучше оставить выполнение этой задачи профессионалам?
Как бы то ни было, вовсе необязательно, чтобы белый лабораторный халат — вдруг он у вас есть — пылился в шкафу. Вместе со своими детьми вы можете провести множество увлекательных и простых экспериментов, которые помогут им понять некоторые основные принципы научного мира.
Эксперимент № 1. Электромотор
Как помочь ребенку — или даже себе — понять силу магнитов? Попробуйте сделать электромотор! Для этого эксперимента вам понадобятся всего лишь одна пальчиковая батарейка (АА), магнит и немного медной проволоки.
Для начала прикрепите магнит к отрицательному полюсу батарейки — так, чтобы она могла твердо стоять на нем. Затем согните медную проволоку, чтобы получилось что-то в форме бабочки (можно и в форме сердца — главное, чтобы по двум сторонам от батарейки были примерно одинаковые «лопасти»). Также можно сделать небольшую вмятину на положительном полюсе батарейки, чтобы конструкция из проволоки держалась устойчивее. Наденьте конструкцию на батарейку так, чтобы свободные концы проволоки слегка касались магнита: у вас получится униполярный мотор или самоподдерживающийся двигатель, использующий противоположные магнитные поля.
Эксперимент № 2. Шагающаявода
Вода — удивительная субстанция, и вы в очередной раз сможете убедиться в этом, а заодно и удивить детей, в ходе этого эксперимента. Для него понадобятся восемь пластиковых стаканчиков (можно больше или меньше), вода, пищевой краситель разных цветов и бумажные полотенца (или салфетки).
Расположите стаканы в ряд, налейте немного воды в каждый второй, а затем добавьте в каждый краситель разного цвета. После сделайте несколько полосок из бумажных полотенец и поместите каждую из них в стаканы — одним концом в стакан с водой, другим — в пустой. В итоге вода постепенно переместится в пустые стаканчики, а в качестве бонуса вы получите интересную художественную инсталляцию.
Эксперимент № 3. Фейерверки в стакане
Вам потребуются вода, две столовые ложки растительного масла и пищевой краситель. Все это поможет узнать о весе разных жидкостей, а в процессе устроить «фейерверки».
Для начала добавьте немного красителя в масло, затем перелейте эту смесь в чашу с водой. Более легкое масло будет плавать поверх воды, а более тяжелый краситель начнет постепенно выбираться из своей маслянистой «темницы», при этом рисуя в воде занимательные узоры — своего рода фейерверки.
Эксперимент № 4. Один стакан, семь слоев
Еще один способ показать детям, что не все жидкости одинаковы. Вам понадобятся мед, кукурузный сироп, средство для мытья посуды, вода, растительное масло, медицинский спирт, масло для лампады и высокий сосуд (желательно не очень широкий).
Аккуратно налейте каждый из ингредиентов в сосуд в порядке, указанном выше. Так каждая из жидкостей займет свой слой, и они не перемешаются.
Тумбага
Перед вами женское нагрудное украшение южноамериканской доколумбовой культуры Кимбая, датированное 300–1600 гг. н. э. Оно выполнено из специфического сплава золота и меди под названием тумбага.
Тумбага (испанские конкистадоры заимствовали это название из малайского языка, tembaga означает «медь» или «латунь») — собирательное название для сплавов, состоящих главным образом из меди и золота. Тумбага широко применялась в доколумбовых цивилизациях Южной и Центральной Америки (где сплавы сходного состава назывались гуанин; см. Guanín). Из нее изготавливали церемониальные предметы, украшения, статуэтки.
По химическому составу тумбага представлена смесью золота и меди с переменным количеством серебра или других примесей. Вариации состава в различных изделиях весьма значительны — от 97% золота до 97% меди (скорее всего, состав зависел от доступности источников этих металлов в том или ином регионе). У сплава, содержащего 44% меди, температура плавления составляет 910°C, что ниже, чем у золота (1064°C) и меди (1084°C) по отдельности. Итоговый сплав, будучи тверже меди, сохраняет пластичность, и его легко обрабатывать.
Сложные изделия из тумбаги изготавливали методом литья по выплавляемым моделям. Сплав заливали в подготовленные формы, и изделие после остывания подвергали дальнейшей обработке методом золочения с истощением (см. Depletion gilding). В отличие от обычных методов золочения, когда золото наносится на поверхность изделия, метод золочения с истощением основан на удалении более активных металлов с поверхности изделия — чтобы увеличить долю золота в поверхностном слое. Изделие подвергали действию различных кислот (например, щавелевой кислоты) и нагревали, удаляя с поверхности медь. Получался тонкий поверхностный слой почти чистого золота. Считается, что эта технология была известна в Перу уже в 400 году до н. э и повсеместно использовалась по крайней мере за 1000 лет до прибытия конкистадоров.
В результате такой обработки изделие выглядело как выполненное из золота, хотя под золотой поверхностью был сплав меди и золота. Так, образцы золота, которые были отправлены Христофором Колумбом в Испанию, состояли из золота чуть больше, чем на половину. Но в полной мере испанцы столкнулись с тумбагой во время завоеваний Эрнана Кортеса, когда в руки конкистадоров попало огромное количество золотых изделий ацтеков.
Испанцы и их союзники плавят добычу. Руки и ноги на переднем плане обозначают, как надевались украшения. Рисунок из Флорентийского кодекса (глава 17) — произведения XVI века по истории ацтеков, написанного испанским монахом Бернардино де Саагуном
Но когда они подвергли изделия переплавке, выяснилось, что в них велика доля меди. Часть таких переплавленных в слитки изделий была обнаружена в 1993 году на корабле, затонувшем около 1528 года у берегов Большого Багамы. Широкий разброс в составе слитков говорит о том, что они были изготовлены в кустарных условиях, из крайне неоднородного материала, что вполне ожидаемо в условиях сразу после завоевания.
Один из слитков, найденных на затонувшем корабле близ Большого Багамы. На слитке видна печать, подтверждающая право собственности короля Испании Карла V Габсбурга. Фото с аукциона Daniel Frank Sedwick
Современник завоеваний Кортеса, историк Гонсало Фернандес де Овьедо писал, что индейцы знают, как позолотить изделия, изготовленные из меди и низкопробного золота, и применяют для этого сок определенного растения (скорее всего из рода кислица). Этот метод способен удалить медь, но не удаляет другие металлы, такие как серебро. Поэтому существовали другие методы золочения с истощением. Один из них заключался в нагревании предмета из тумбаги в смеси из квасцов, поваренной соли и кирпичной пыли. Смесь реагировала с поверхностью сплава с образованием хлоридов серебра и меди, которые поглощались кирпичной пылью. После охлаждения и промывки поверхность полировалась. Другой метод заключался в выдерживании изделия в течение 10 дней в растворе квасцов, поваренной соли и сульфата железа при комнатной температуре (аналог предыдущего способа, но без прогрева). Затем изделие промывалось в солевом растворе и нагревалось для получения более однородного поверхностного слоя.
Еще одно известное изделие, выполненное из тумбаги, — фигурка, изображающая плот муисков. Согласно легенде, новый правитель индейцев покрывал свое тело смолой или глиной, и помощники обсыпали его золотым песком. Затем новый правитель в сопровождении слуг на плоту выплывал на середину озера Гуатавита (расположено в Колумбии) и кидал в воду золотые дары. После этого он вплавь добирался до берега, в результате чего с правителя смывалась «золотая кожа». Испанцы были так поражены этим ритуалом, что многократно преувеличили его, передавая из уст в уста, и со временем человек превратился в город, затем — в королевство и, наконец, в империю Эльдорадо (по-испански el hombre dorado — «золотой человек»).
Фигура, изображающая церемонию вступления на трон нового правителя муисков. Размеры плота: 19,5 см на 10,1 см, высота самой большой фигурки (скорее всего, вождя) — 10,2 см. Изделие хранится в Музее золота в Боготе, столице Колумбии. Фото с сайта en.wikipedia.org
Если верить легенде, то количество золота на дне озера Гуатавита должно быть поистине огромным. Было несколько попыток осушить озеро (последняя — в начале XX века), но все они закончились неудачей, так как обнаруженного золота не хватало на покрытие расходов. В 1965 году колумбийское правительство объявило озеро охраняемой территорией, любые попытки искать в нем золото или тем более его осушить теперь незаконны.
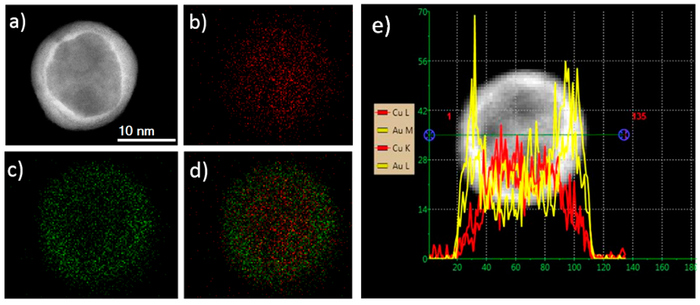
Сплавы на основе золота не потеряли своего значения и по сей день. Они нашли применение не только в ювелирном деле, но и как катализаторы в нанотехнологиях. Интересно, что наиболее стабильная форма наночастиц из золота и меди удивительным образом напоминает тумбагу: краевая часть обогащена золотом, а центральная часть содержит больше меди.
a) изображение наночастицы из золота и меди, полученное с помощью электронного микроскопа; b) распределение меди в частице; с) распределение золота в частице; d) совмещенные изображения; e) EDX-спектр элементов, из которых состоит частица. Изображение из статьи G. Guisbiers et al., 2014. Gold–Copper Nano-Alloy, «Tumbaga», in the Era of Nano: Phase Diagram and Segregation