Содержание
Дерматология в России
Зарегистрируйтесь!
Если Вы врач, то после регистрации на сайте Вы получите доступ к специальной информации.
Если Вы уже зарегистрированы, введите имя и пароль (форма в верхнем правом углу или здесь).
Опыт комбинированного лечения острого простого герпеса
ОПЫТ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ ОСТРОГО ПРОСТОГО ГЕРПЕСА – ПРОТИВОВИРУСНАЯ НАРУЖНАЯ ТЕРАПИЯ И КОРОТКОВОЛНОВОЕ УЛЬТРАФИОЛЕТОВОЕ ИЗЛУЧЕНИЕ. ПРАКТИЧЕСКОЕ НАБЛЮДЕНИЕ
Медицинский центр «Демос», Санкт-Петербург
При воздействии на организм человека электромагнитное поле оптического диапазона в большей степени оказывает свое влияние на его кожный покров. Ответные фотобиологические реакции возникают вследствие поглощения электромагнитной энергии теми тканями, на которые направлен источник излучения. Степень поглощения энергии определяется энергией световых квантов и возрастает с увеличением длины волны используемого излучения.
Ответная реакция биологических тканей проявляется в диапазоне от чисто теплового эффекта до разрушения тех структур, которые облучались. Например, коротковолновое ультрафиолетовое (КУФ) излучение длиной волны 180-280 нм вызывает ионизацию и разрушение ковалентных связей молекул в зоне непосредственного действия данного физического фактора. Это свойство широко применяется в лечебной физиотерапевтической практике.
КУФ-излучение с патогенетической точки зрения при воздействии на кожу и слизистые обладает бактерицидным и микоцидным, а также иммуностимулирующим и катаболическим лечебными эффектами. Благодаря этому одними из показаний для его применения в дерматологической практике являются:
-острые и подострые воспалительные заболевания кожи, в т.ч. инфекционной этиологии;
. раны с опасностью присоединения анаэробной инфекции;
Абсолютным противопоказанием является повышенная чувствительность кожи конкретного пациента к ультрафиолетовому излучению. С осторожностью КУФ-облучение назначается пациентам, принимающим лекарственные препараты, обладающие фотосенсибилизирующим действием.
Одним из заболеваний, часто встречающихся в практике врача-дерматолога, является острый простой герпес. Процесс носит инфекционный характер и проявляется типичным стадийным течением – продрома, стадия клинических проявлений различной степени выраженности, реконвалесценция, ремиссия (носительство).
Нами было пролечено 15 человек с диагнозом «острый простой герпес, экстрагенитальная форма» легкой степени тяжести; на стадии продромы – 4 человека и на стадии начальных клинических проявлений – 11 человек. Противовирусная терапия пероральными препаратами не проводилась.
Лечебная процедура проводилась следующим образом:
— обработка очага поражения (накожно) кожным антисептиком «Октенисепт»;
-местно КУФ-облучение очага поражения 1-1,5 биодозы (на нашем излучателе 1 биодоза составила 3 минуты), расстояние до излучателя 5 см, ежедневно, N 3-5;
-нанесение 5 % противовирусной мази «Ацикловир» или цинк-салициловой пасты в зависимости от стадии вирусного процесса.
В результате проводимого лечения у всех пациентов отмечалось укорочение сроков заболевания до 5-7 дней с полной регрессией клинических проявлений. У 13 человек после однократной процедуры уменьшались болевой синдром, отечность и дискомфортные ощущения в области очага поражения.
Таким образом, учитывая опыт данного практического наблюдения лечения острого простого герпеса комбинированием наружной терапии и лечебной физиотерапевтической методики, можно говорить об успешном их применении в повседневной практике врача-дерматолога с целью быстрого прерывания уже начавшегося инфекционного процесса.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
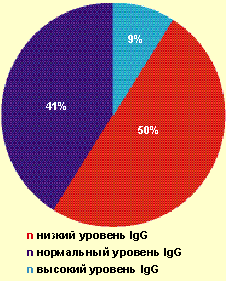 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
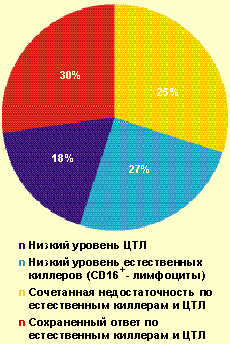 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Применение УФО при простом герпесе или пузырьковом лишае
Простой герпес (herpes simplex) является частой патологией, возникающей при острых респираторных и других простудных заболеваниях, при стрессовых ситуациях, иммунодефицитных состояниях и в других случаях.
Заболевание вызывается вирусом простого герпеса (ВПГ-1 или ВПГ-2) и склонно к рецидивированию. Оно проявляется возникновением небольших пузырьков, наполненных прозрачным, а затем мутным экссудатом, которые через несколько дней ссыхаются и превращаются в желтовато-серую корку. Последняя отпадает или вскрывается, вызывая кровоточивость или образуя эрозию.
Характерна локализация простого герпеса – участки кожи с высыпаниями располагаются около естественных отверстий: углы рта и красная кайма губ, крылья носа, половые органы, полость рта и др. Высыпание пузырьков вызывает гиперемию и отек окружающих тканей, покалывание, жжение и боль и может осложняться вторичной инфекцией.
Общее состояние пациента удовлетворительное, однако заболевание ослабляет процессы иммунитета, вызывает ряд неудобств, неприятных ощущений и является косметическим дефектом, особенно при его локализации в области лица.
В комплексном лечении одним из основных методов терапии является УФ-облучение, проводимое прежде всего на очаги пузырьковых высыпаний. Применяют УФ-облучатели интегрального спектра («ОРК-21М», «ОКН-11М и др.) или портативные ДУФ-облучатели («ОУН-1»).
Очаги пузырьковых высыпаний облучают дозой 2–3 биодозы при использовании УФ-облучателей интегрального спектра и 3–4 биодозы при использовании ДУФ-облучателей, повторное облучение назначают соответственно через день или на следующий день после первого.
Каждый очаг высыпаний облучают 3–4 раза с увеличением дозы на 1 биодозу при каждом последующем воздействии, после чего можно дополнительно облучать очаг (очаги) поражения КУФ-облучателем («БОД-9», «БОП-4») 3–4 раза 2–3 биодозами для оказания бактериостатического действия. Воздействия на очаги высыпаний целесообразно сочетать с УФ-облучением интегрального спектра рефлекторно-сегментарных зон.
При пузырьковом лишае в области лица облучению (1–2 биодозы) подвергают шейно-грудной отдел позвоночника, включая паравертебральные зоны; при поражении половых органов – пояснично-крестцовую область (2–3 биодозы). Облучение каждого поля осуществляют 3–4 раза с увеличением интенсивности воздействия на 1 биодозу.
Методики ультрафиолетовой терапии
В чем заключается ультрафиолетовая терапия?
Механизм действия УФ-лучей основан на способности некоторых атомов и молекул избирательно поглощать энергию света. В результате этого молекулы тканей переходят в возбужденное состояние, что запускает фотохимические процессы в чувствительных к УФ-лучам молекулах белка, ДНК и РНК.
Фотолиз белков эпидермальных клеток приводит к высвобождению биологически активных веществ (гистамина, ацетилхолина, простагландинов), которые при поступлении в кровоток вызывают расширение сосудов, миграцию лейкоцитов. Не меньшее значение имеют рефлекторные реакции, вызванные активацией многочисленных рецепторов продуктами фотолиза и биологически активными веществами, а также гуморальное воздействие на нервную, эндокринную, иммунную и другие системы организма. Естественно, что УФ-излучение вызывает ответные реакции со стороны организма человека, которые и составляют основу физиологического и лечебного действия УФ-лучей.
Одним из основных компонентов этого лечебного действия являются эффекты, связанные с формированием ультрафиолетовой (или фотохимической) эритемы. Максимальным эритемообразующим свойством обладает СУФ-излучение с длиной волны 297 нм.
УФ-эритема оказывает противовоспалительное, десенсибилизирующее, трофико-регенераторное, а также обезболивающее действие. Антирахитическое действие УФ-лучей заключается в том, что под влиянием этого излучения в облученной коже образуется витамин Д. Поэтому УФО является специфической лечебно-профилактической процедурой у детей, страдающих рахитом.
Влияние ультрафиолетового облучения на организм человека
Широко используется бактерицидное действие УФО. Различают прямое и непрямое бактерицидное действие УФ-лучей. В результате прямого действия происходит коагуляция и денатурация белков микроорганизмов на поверхности раны, слизистой оболочке, что приводит к гибели бактериальной клетки. Непрямое действие УФ-излучения связано с изменением иммунобиологической реактивности организма под влиянием УФ-лучей.
УФ-лучи активно влияют на липидный, белковый и углеводный обмен. Под влиянием их субэритемных доз в коже из производных холестерина синтезируется витамин Д3, контролирующий фосфорно-кальциевый обмен. Они снижают содержание атерогенного холестерина крови у больных атеросклерозом.
Благодаря своему многообразному действию, УФО (наряду с УВЧ-терапией и ультразвуковой терапией) нашло широкое применение для профилактики и лечения широкого спектра заболеваний.
Определение биодозы
Дозируют УФ-излучение биологическим методом Горбачева-Дакфельда. Метод является простым и базируется на свойстве УФ-лучей вызывать при облучении кожи эритему. Единицей измерения в этом методе является одна биодоза. За одну биодозу принимают минимальное время облучения данного больного с определенного расстояния определенным источником УФ-лучей, которое необходимо для получения слабой, однако четко очерченной эритемы. Время измеряют в секундах или минутах.
Результат биодозометрии проверяется через 24 часа. Одной биодозой будет считаться наиболее слабая гиперемия кожи. С изменением расстояния от излучаемой поверхности для получения той же биодозы время облучения изменяется обратно пропорционально квадрату расстояния. Например, если время для получения одной биодозы с расстояния 20 см равняется 2 мин., то с расстояния 40 см потребуется 8 мин. Время облучения можно выбирать дискретно от 30 сек. до 60 сек., а расстояние от тела (его кожи) до излучателя от 10 см до 50 см. Все зависит от типа кожи, но выбирать эти параметры нужно так, чтобы получить наглядную картину эритем кожи.
Реакция кожи на ультрафиолет
Чувствительность кожи к УФ-лучам зависит от многих причин, среди которых наиболее важны локализация воздействия, цвет кожи, время года, возраст и исходное состояние пациента. Существенную роль играют и заболевания, которыми страдает человек. При фотодерматозах, экземе, подагре, заболеваниях печени, гипертиреозе и др. чувствительность кожи к УФ-лучам повышена, при другой патологии (пролежни, отморожения, трофические раны, газовая гангрена, рожистое воспаление, заболевания периферических нервов и спинного мозга ниже уровня поражения) чувствительность кожи к УФО, наоборот, снижена.
Показания к УФ-облучению
Общее ультрафиолетовое облучение применяется для:
Местное УФО имеет более широкий круг показаний и применяется:
Назначаются общие УФО с учетом индивидуальных особенностей и чувствительности кожи к УФ-облучению по основной или ускоренной схеме. Для нормализации иммунного статуса при хронических вялотекущих воспалительных процессах, а также для профилактики ОРВИ проводят безэритемное общее УФО длинными и средними волнами с расстояния 50-100 см.
Облучают последовательно переднюю, заднюю и боковые поверхности тела. Во время всех процедур на глаза надевают защитные очки. УФ-облучение по методике PUVА-терапии (или фотохимиотерапия) проводят следующим образом. Больным с псориазом или парапсориатическими заболеваниями дают в соответствующей дозе внутрь или наносят наружно препараты фурокумаринового ряда (пувален, псорален, бероксан и др.). Препараты принимают только в день процедуры 1 раз за 2 часа до облучения после еды, запивая молоком. Индивидуальную фоточувствительность пациента определяют обычным способом биодозиметром, но также через 2 часа после приема препарата. Начинают процедуру с минимальных субэритемных доз.
Средневолновое ультрафиолетовое облучение показано при острых и подострых воспалительных заболеваниях внутренних органов, последствиях травм костно-мышечной системы, заболеваниях периферической нервной системы вертеброгенной этиологии с выраженным болевым синдромом, рахите, вторичных анемиях, нарушениях обмена веществ, рожистом воспалении. (Аппаратура: ОУФд-01, ОУФв-02 «Солнышко»).
Коротковолновое ультрафиолетовое облучение используется при острых и подострых заболеваниях кожи, носоглотки, внутреннего уха, для лечения ран с опасностью присоединения анаэробной инфекции, туберкулеза кожи. (Аппаратура: ОУФб-04 «Солнышко»).
Противопоказаниями для местных и общих УФ-облучений являются злокачественные новообразования, системные заболевания соединительной ткани, активная форма туберкулеза легких, гипертиреоз, лихорадочные состояния, склонность к кровотечению, недостаточность кровообращения II и III степеней, артериальная гипертензия III степени, выраженный атеросклероз, заболевания почек и печени с недостаточностью их функции, кахексия, малярия, повышенная чувствительность к УФ-лучам, фотодерматозы, инфаркт миокарда (первые 2-3 недели), острое нарушение мозгового кровообращения.
Некоторые частные методики ультрафиолетовой терапии
Вульвит.
Бартолинит.
Кольпит.
В лечении и реабилитации больных с различными болезнями большое место занимают лечебные физические факторы, как природные, так и получаемые искусственно.
Лечебные физические факторы оказывают гомеостатическое влияние на различные органы и системы, способствуют повышению сопротивляемости организма к неблагоприятным воздействиям, усиливают его защитно-приспособительные механизмы, обладают выраженным саногенным действием, повышают эффективность других терапевтических средств и ослабляют побочные эффекты лекарств. Их применение доступно, высокоэффективно и экономически выгодно.
Очень важно понять, что ультрафиолетовая физиотерапия является одним из важнейших компонентов всего комплекса физических методов лечения и реабилитации больных. Достоинство лечебных физических факторов в полной мере реализуется при их правильном применении и комбинировании с другими лечебно-профилактическими и реабилитационными мероприятиями.
