Цефтриаксона натриевая соль : инструкция по применению
Описание
Состав
Каждый флакон содержит: активное вещество – цефтриаксон (в виде цефтриаксона натриевой соли) – 500 мг или 1000 мг.
Фармакотерапевтическая группа
Антибактериальные средства для системного применения. Цефалоспорины третьего поколения.
Фармакологическое действие
Бактерицидная активность цефтриаксона обусловлена подавлением синтеза клеточных мембран микроорганизмов. Цефтриаксон ацетилирует мембраносвязанные транспептидазы, нарушая перекрестную сшивку пептидогликанов, необходимую для обеспечения прочности и ригидности клеточной мембраны бактерий.
Цефтриаксон активен in vitro в отношении большинства грамотрицательных и грамположительных микроорганизмов. Цефтриаксон характеризуется высокой устойчивостью к большинству бета-лактамаз (как пенициллиназ, так и цефалоспориназ) грамположительных и грамотрицательных бактерий.
Распространенность приобретенной устойчивости может изменяться географически и со временем для отдельных видов, поэтому при лечении тяжелых инфекций необходимо учитывать местную информацию о резистентности возбудителей к цефтриаксону.
Обычно чувствительные виды
Грамположительные аэробы: Staphylococcus aureus а (метициллин-чувствительные штаммы), Staphylococci коагулазоотрицательные а (метициллин-чувствительные штаммы), Streptococcus pyogenes (группа A), Streptococcus agalactiae (группа В), Streptococcus pneumoniae, Streptococci группы Viridans.
Грамотрицательные аэробы: Borrelia burgdorferi, Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Neisseria meningitidis, Proteus mirabilis, Providencia spp., Treponema pallidum.
Виды, которые могут приобретать устойчивость
Анаэробы: Bacteroides spp., Fusobacterium spp., Peptostreptococcus spp., Clostridium perfringens.
Грамположительные аэробы: Enterococcus spp., Listeria monocytogenes.
Грамотрицательные аэробы: Acinetobacter baumannii, Pseudomonas aeruginosa, Stenotrophomonas maltophilia.
Анаэробы: Clostridium difficile.
Другие: Chlamydia spp., Chlamydophila spp., Mycoplasma spp., Legionella spp., Ureaplasma urealyticum.
a все метициллин-устойчивые стафилококки устойчивы к цефтриаксону.
b уровень резистентности >50% по меньшей мере в одном регионе.
c штаммы, продуцирующие расширенный спектр бета-лактамаз, всегда резистентны.
Показания к применению
– острый средний отит;
– осложненные инфекции мочевыводящих путей, включая пиелонефрит;
– инфекции костей и суставов;
– осложненные инфекции кожи и мягких тканей;
Цефтриаксона натриевая соль может применяться для:
– лечения обострения хронической обструктивной болезни легких у взрослых;
– лечения диссеминированного Лайм-боррелиоза (в ранних (II стадия) и поздних (III стадия) периодах болезни) у взрослых и детей, включая новорожденных с 15-дневного возраста;
– предоперационнной профилактики хирургических инфекций;
– лечения пациентов с нейтропенией и лихорадкой, которая предположительно связана с бактериальной инфекцией;
– лечения пациентов с бактериемией, вызванной или предположительно вызванной какой-либо из вышеперечисленных инфекций.
Цефтриаксона натриевая соль должна назначаться совместно с другими антибактериальными средствами, когда возможный диапазон этиологических факторов не соответствует спектру его действия.
Следует учитывать официальные руководства по надлежащему использованию антибактериальных средств.
Способ применения и дозы
Доза зависит от типа, локализации и тяжести инфекции, чувствительности возбудителя, от возраста пациента и состояния функций его печени и почек.
Дозы, указанные в таблицах, приведенных ниже, являются рекомендованными дозами для применения при этих показаниях. В особенно тяжелых случаях следует рассматривать целесообразность назначения самых высоких доз из указанных диапазонов.
Взрослые и дети старше 12 лет (масса тела ≥50 кг)
| Доза* | Кратность применения** | Показания |
| 1-2 г | 1 раз в сутки | Негоспитальная пневмония. Обострение хронической обструктивной болезни легких. Интраабдоминальные инфекции. Осложненные инфекции мочевыводящих путей (в том числе пиелонефрит). |
| 2 г | 1 раз в сутки | Госпитальная пневмония. Осложненные инфекции кожи и мягких тканей. Инфекции костей и суставов. |
| 2-4 г | 1 раз в сутки | Пациентам с нейтропенией и лихорадкой, вызванной бактериальной инфекцией. Бактериальный эндокардит. Бактериальный менингит. |
*При установленной бактериемии рассматриваются наиболее высокие дозы из приведенного диапазона.
**При назначении препарата в дозе более чем 2 г в сутки рассматривается возможность применения препарата 2 раза в день.
Показания для взрослых и детей старше 12 лет (масса тела ≥50 кг), которые требуют специального режима введения препарата:
Острый средний отит
Как правило, достаточно однократного внутримышечного введения препарата в дозе 1-2 г. Ограниченные данные свидетельствуют о том, что в тяжелых случаях или при отсутствии эффекта от предшествующей терапии может быть эффективно внутримышечное введение цефтриаксона в дозе 1-2 г в сутки в течение 3 дней.
Предоперационная профилактика хирургических инфекций
Однократное введение перед операцией в дозе 2 г.
Однократное внутримышечное введение в дозе 500 мг.
Рекомендованные дозы 0,5 г или 1 г один раз в день увеличивают до 2 г один раз в день при нейросифилисе, продолжительность лечения – 10-14 дней. Рекомендации по дозировке при сифилисе, в том числе при нейросифилисе, основаны на ограниченных данных. Необходимо принимать во внимание национальные и местные руководства.
Диссеминированный Лайм-боррелиоз (ранняя (II) и поздняя (III) стадия)
Применять в дозе 2 г один раз в сутки в течение 14-21 дня. Рекомендуемая продолжительность лечения варьирует. Необходимо принимать во внимание национальные и местные руководства.
Для детей с массой тела 50 кг и более дозы соответствуют дозам взрослых пациентов.
Новорожденные, младенцы и дети от 15 дней до 12 лет (масса тела
Побочное действие
Частота развития побочных эффектов приведена в следующей градации: очень часто (≥1/10); часто (≥1/100,
Противопоказания
• гиперчувствительность к цефтриаксону, другим цефалоспоринам или к любому из вспомогательных веществ;
• тяжелые реакции гиперчувствительности (например, анафилактические реакции) на любой другой тип бета-лактамных антибактериальных препаратов (пенициллины, монобактамы, карбапенемы) в анамнезе;
• недоношенные новорожденные до возраста 41 недели (гестационный возраст + хронологический возраст)*;
• доношенные новорожденные (до 28 дней жизни):
– при наличии гипербилирубинемии, желтухи, гипоальбуминемии или ацидоза, состояний, при которых возможно нарушение связывания билирубина*;
– если им требуется (или может потребоваться) внутривенное введение кальция или содержащих кальций растворов из-за риска образования преципитатов кальциевой соли цефтриаксона.
*Исследования in vitro показали, что цефтриаксон может вытеснить билирубин из его связи с сывороточным альбумином, что увеличивает риск билирубиновой энцефалопатии у этих пациентов.
Лидокаин нельзя использовать в качестве растворителя ни для одного из способов введения!
Передозировка
Симптомы: тошнота, рвота, диарея.
Гемодиализ и перитонеальный диализ не снижают сывороточную концентрацию цефтриаксона. Специфический антидот отсутствует.
Лечение: симптоматическая терапия.
Меры предосторожности
Реакции гиперчувствительности: как и по поводу других бета-лактамных антибактериальных средств, поступали сообщения о серьезных и внезапных смертельных реакциях гиперчувствительности на цефтриаксон. В случае развития тяжелых реакций гиперчувствительности лечение цефтриаксоном следует немедленно прекратить и начать проведение адекватных лечебных мероприятий. Перед началом лечения следует установить, имеются ли у пациента в анамнезе тяжелые реакции гиперчувствительности на цефтриаксон, на другие цефалоспорины или на другие бета-лактамы. С осторожностью следует применять цефтриаксон пациентам с нетяжелыми реакциями гиперчувствительности на другие бета-лактамные препараты в анамнезе. Были зарегистрированы сообщения о тяжелых кожных побочных реакциях (синдром Стивенса-Джонсона или токсический эпидермальный некролиз), однако частота развития этих реакций неизвестна.
Взаимодействие с кальцийсодержащими растворами: были описаны случаи отложения нерастворимых солей цефтриаксона кальция в тканях легких и почках у недоношенных и доношенных новорожденных в возрасте менее 1 месяца, имевшие летальный исход. По крайней мере, в одном из этих случаев цефтриаксон и кальций вводили в разное время и по разным системам для внутривенного введения. В имеющихся научных данных нет сообщений о подтвержденных случаях образования внутрисосудистых осадков у пациентов, кроме новорожденных, получавших цефтриаксон и кальцийсодержащие растворы или любые другие содержащие кальций лекарственные средства. Исследования in vitro показали, что новорожденные имеют повышенный риск образования осадков цефтриаксона кальция по сравнению с пациентами других возрастных групп.
Для пациентов любого возраста не следует использовать в качестве растворителей при разведении цефтриаксона для внутривенного введения кальцийсодержащие растворы (например, раствор Рингера и раствор Хартмана) или вводить одновременно с цефтриаксоном другие кальцийсодержащие растворы, даже при использовании разных венозных доступов и разных инфузионных систем. Тем не менее, пациентам старше 28-дневного возраста цефтриаксон и кальцийсодержащие растворы можно вводить последовательно один за другим, если инфузионные системы имеют разные венозные доступы, или если инфузионные системы меняются или тщательно промываются между инфузиями с физиологическим солевым раствором, чтобы избежать образования осадка.
У пациентов, требующих длительной инфузии кальцийсодержащего парентерального питания, лечащим врачом должен быть рассмотрен вариант использования альтернативных антибактериальных средств, для которых вероятность выпадения осадка отсутствует. Если нет возможности отказа от использования цефтриаксона у пациента, требующего непрерывного питания, растворы парентерального питания и цефтриаксона можно вводить одновременно, но с помощью различных внутривенных систем в различные венозные доступы. Другой вариант: введение раствора парентерального питания приостановить на время введения цефтриаксона и тщательно промыть инфузионную систему между введениями двух растворов.
Применение у детей: безопасность и эффективность цефтриаксона у детей установлена для доз, описанных в разделе «Способ применения и дозы». Исследования показали, что цефтриаксон, как и некоторые другие цефалоспорины, может вытеснять билирубин из связи с сывороточным альбумином. Применение цефтриаксона противопоказано у недоношенных и доношенных новорожденных из группы риска по развитию билирубиновой энцефалопатии.
Иммунологически опосредованная гемолитическая анемия: наблюдались случаи развития иммунологически опосредованной гемолитической анемии у пациентов на фоне лечения цефалоспоринами, включая цефтриаксон. Описаны тяжелые случаи гемолитической анемии у взрослых пациентов и детей, включая случаи с летальным исходом. Если у пациента на фоне лечения цефтриаксоном развивается анемия, следует оценить вероятность ее развития на фоне приема цефалоспоринового антибиотика и прекратить его введение до установления этиологии анемии.
Длительная терапия: при длительном лечении следует регулярно контролировать полный анализ крови.
Колит/Избыточный рост нечувствительных микроорганизмов: имеются сообщения об ассоциированном с антибактериальным средством колите и псевдомембранозном колите в случае применения почти всех антибактериальных средств, включая цефтриаксон. Тяжесть колита может варьировать от легкой степени до опасной для жизни. Поэтому важно учитывать этот диагноз у пациентов, у которых наблюдается диарея во время или после лечения цефтриаксоном. Следует рассмотреть вопрос о прекращении терапии цефтриаксоном и назначении специфического лечения Clostridium difficile. В данном случае не следует применять лекарственные средства, которые подавляют перистальтику. Как и в случае применения других антибактериальных средств на фоне лечения цефтриаксоном могут отмечаться суперинфекции, вызванные нечувствительными микроорганизмами.
Тяжелые нарушения функций печени и почек: при тяжелой почечной и печеночной недостаточности рекомендуется проводить клинический мониторинг безопасности и эффективности.
Влияние на лабораторные тесты: при лечении цефтриаксоном могут отмечаться ложноположительные результаты пробы Кумбса, пробы на галактоземию, определение глюкозы в моче (при определении глюкозы в моче неферментативным методом). Определение глюкозы в моче во время применения цефтриаксона должно проводиться ферментативно.
Натрий: один флакон Цефтриаксона натриевой соли 500 мг содержит около 1,8 ммоль натрия. Один флакон Цефтриаксона натриевой соли 1000 мг содержит около 3,6 ммоль натрия. Это необходимо принимать во внимание у пациентов, находящихся на диете с низким содержанием натрия.
Антибактериальный спектр действия: цефтриаксон имеет ограниченный спектр антибактериального действия и может быть непригодным в качестве единственного препарата для лечения некоторых видов инфекций, за исключением случаев, когда возбудитель уже подтвержден. При полимикробных инфекциях, когда предполагаемые возбудители включают микроорганизмы, устойчивые к цефтриаксону, необходимо рассмотреть возможность приема дополнительных антибиотиков.
Билиарный литиаз: если при ультразвуковом исследовании (эхографии) наблюдаются затемнения, следует оценить вероятность выпадения в осадок соли цефтриаксона кальция. Затемнения, ошибочно принимаемые за камни в желчном пузыре, обнаруживаются на эхограммах желчного пузыря чаще при применении доз цефтриаксона 1000 мг в сутки и более. Особую осторожность следует соблюдать при применении цефтриаксона в педиатрической практике. Такой преципитат исчезает после прекращения терапии цефтриаксоном. Преципитаты цефтриаксона кальция редко ассоциируются с симптомами. В симптоматических случаях рекомендуется проводить консервативное лечение и рассмотреть целесообразность отмены терапии цефтриаксоном на основании специальной оценки соотношения пользы и риска.
Билиарный стаз: у пациентов, получавших цефтриаксон, были зарегистрированы случаи панкреатита, возможно, вызванного непроходимостью желчных путей. У большинства пациентов присутствовали факторы риска билиарного стаза и билиарного сладжа, например, предшествующая основная терапия, тяжелое заболевание и полное парентеральное питание. Не следует исключать триггерный фактор или кофактор образования желчных преципитатов вследствие применения цефтриаксона.
Нефролитиаз: были зарегистрированы случаи обратимого нефролитиаза, который исчезал после отмены цефтриаксона. В симптоматических случаях необходимо ультразвуковое исследование (эхография). Решение о применении цефтриаксона у пациентов с нефролитиазом или гиперкальциемией в анамнезе должно приниматься врачом на основании специальной оценки пользы и риска.
Применение во время беременности и в период лактации
Беременность: цефтриаксон проникает через плацентарный барьер. Данные об использовании цефтриаксона беременными женщинами ограничены. В исследованиях на животных цефтриаксон не оказывал прямого или косвенного неблагоприятного воздействия на развитие эмбриона/плода, на перинатальное и послеродовое развитие. Исходя из этого применение цефтриаксона во время беременности возможно, если ожидаемая польза превышает потенциальный риск, особенно в первом триместре беременности.
Грудное вскармливание: цефтриаксон выделяется в грудное молоко в низких концентрациях и в терапевтических дозах никакого эффекта на грудного ребенка не ожидается. Тем не менее, нельзя исключать возможный риск развития диареи и грибковой инфекции слизистых оболочек. Следует принимать во внимание возможность сенсибилизации. Следует либо прекратить грудное вскармливание, либо прекратить/воздержаться от терапии цефтриаксоном, учитывая преимущество грудного вскармливания для ребенка и пользу терапии для женщины.
Фертильность: исследования не показали никаких признаков неблагоприятного воздействия на фертильность мужчин и женщин.
Влияние на способность к управлению автотранспортом и другими потенциально опасными механизмами
Во время лечения цефтриаксоном могут возникать нежелательные эффекты (например, головокружение), которые могут влиять на способность управлять транспортом и другими механизмами (см. раздел «Побочное действие»). Пациентам следует проявлять осторожность при управлении транспортными средствами или другими механизмами.
Взаимодействие с другими лекарственными средствами
Кальцийсодержащие лекарственные средства: для приготовления растворов цефтриаксона для внутривенного введения из порошка, содержащегося во флаконах, или для дальнейшего разведения приготовленного раствора, нельзя использовать кальцийсодержащие растворители, такие как раствор Рингера или раствор Хартмана из-за возможности образования осадка. Также теоретически возможно образование осадка вследствие взаимодействия цефтриаксона и кальция при смешивании цефтриаксона с кальцийсодержащими инфузионными растворами в одном венозном доступе. Цефтриаксон не следует вводить одновременно с кальцийсодержащими внутривенными растворами, в том числе в виде непрерывных инфузий кальцийсодержащих растворов, таких как растворы парентерального питания через Y-соединения.
Допускается введение цефтриаксона и кальцийсодержащих растворов пациентам, за исключением новорожденных, последовательно один за другим при условии, что инфузионная система тщательно промывается физиологическим раствором между введениями во избежание выпадения осадка. Исследования in vitro с использованием плазмы взрослых и пуповинной крови новорожденных показали, что новорожденные имеют повышенный риск выпадения осадка вследствие взаимодействия цефтриаксона с кальцием.
Пероральные антикоагулянты: одновременное применение цефтриаксона с пероральными антикоагулянтами (лекарственные средства группы антивитаминов К) может усилить их эффект и увеличить риск кровотечений.
Рекомендуется частый контроль международного нормализованного отношения (МНО) и соответствующий подбор дозы лекарственных средств группы антивитаминов К, как во время, так и после окончания терапии цефтриаксоном.
Аминогликозиды: имеются противоречивые данные о возможном повышении нефротоксичности аминогликозидов при их одновременном применении с цефалоспоринами. В таких случаях необходим строгий клинический мониторинг уровней аминогликозидов (и функции почек).
Хлорамфеникол: в исследовании in vitro наблюдался антагонизм между хлорамфениколом и цефтриаксоном.
Не поступало сообщений о взаимодействии между цефтриаксоном и пероральными кальцийсодержащими лекарственными средствами, а также о взаимодействии между цефтриаксоном при его внутримышечном введении и кальцийсодержащими лекарственными средствами при их внутривенном или пероральном введении. Одновременное применение пробенецида не уменьшает элиминацию цефтриаксона.
Сильнодействующие диуретики: при одновременном применении больших доз цефтриаксона и сильнодействующих диуретиков (например, фуросемида) нарушений функции почек не наблюдалось.
Согласно литературным данным, цефтриаксон фармацевтически несовместим с амсакрином, ванкомицином, флуконазолом и аминогликозидами.
Условия хранения
В защищенном от влаги и света месте при температуре не выше 25° С.
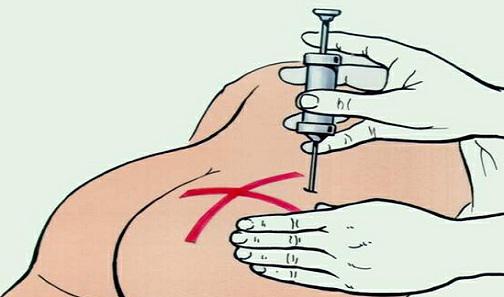
Техника правильного выполнения внутримышечных инъекций
Внутримышечная инъекция – это простой и популярный метод введения медикаментов в организм человека. Однако при неаккуратном проведении этой процедуры могут возникнуть осложнения, избежать которых можно, если владеть правильной техникой ее выполнения.
Знание алгоритма процедуры внутримышечных инъекций нужно не только врачам. В жизни каждого человека может произойти ситуация, когда необходимо проколоть курс уколов самостоятельно. Прежде, чем отрабатывать внутримышечные инъекции на практике, нужно тщательно изучить теорию, касающуюся этой манипуляции. Соблюдение всех норм позволит избежать осложнений.
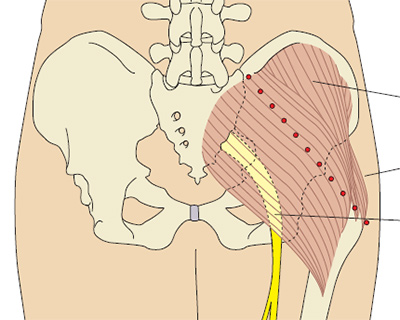
Места для инъекций
Наилучшие места для внутримышечных уколов – это верхняя часть ягодицы, широкая мышца бедра и дельтовидная мышца плеча. При выполнении инъекции в ягодицу ее нужно зрительно разделить на 4 квадранта. Укол делается в верхний наружный квадрант – это самый безопасный участок без крупных нервов и сосудов. В случае бедра так же на 4 квадранта делят его переднюю поверхность. Колют во внешний наружный квадрант.
Правильное место для укола в плечо можно найти так: мысленно разделить руку от локтевого до плечевого сустава на 3 одинаковых участка. Центр средней области будет наиболее подходящим местом. Однако сделать укол в плечо без чьей-либо помощи сложнее, чем в бедро или ягодицу.
Этапы проведения уколов
Процедура внутримышечных инъекций делится на следующие этапы:
Возможные осложнения
Некорректное выполнение внутримышечного укола может спровоцировать появление различных осложнений: от незначительных до болезненных. Поэтому лучше ознакомиться с возможными из них еще до того, как они появятся:
Если от постинъекционного осложнения не удается избавиться самостоятельно, обязательно покажитесь медицинскому работнику.
Желаем, чтобы необходимые уколы проходили для вас всегда легко и безболезненно.
Безопасная техника инъекций
Safe injection techniques
Article 498. Workman B (1999) Safe injection techniques. Nursing Standard. 13, 39,
В данной статье Barbara Workman описывает правильную методику внутрикожных, подкожных и внутримышечных инъекций.
Цели и предполагаемые результаты обучения
Поскольку знания о процедурах ежедневной сестринской практики медсестер растут, разумно пересмотреть некоторые рутинные процедуры.
В данной публикации приведен обзор принципов проведения внутрикожных, подкожных и внутримышечных инъекций. Показано, как правильно выбрать анатомическую область инъекции, предусмотреть возможность непереносимости лекарственных препаратов, а также особые потребности пациента, которые могут повлиять на выбор места выполнения инъекции. Освещены аспекты подготовки пациента и кожи, а также особенности оснащения, и способы уменьшения дискомфорта у пациента во время выполнения процедуры.
Основная цель статьи — побудить медицинскую сестру критически пересмотреть собственную технику выполнения инъекций, исходя из принципов медицины, основанной на доказательствах, и обеспечить пациенту эффективную и безопасную помощь.
После прочтения данной статьи медсестра должна знать и уметь следующее:
Введение
Проведение инъекций — это рутинная, и пожалуй, самая частая работа медсестры, и хорошая техника инъекций может сделать эту манипуляцию относительно безболезненной для пациента. Однако, техническое мастерство без понимания манипуляции подвергает пациента ненужному риску осложнений. Изначально выполнение инъекций было врачебной манипуляцией, но, с изобретением пенициллина в сороковые годы, обязанности медсестры значительно расширились (Beyea and Nicholl 1995). В настоящее время большинство медсестер выполняют эту манипуляцию автоматически. Поскольку сейчас сестринская практика становится основанной на доказательствах, то вполне логично пересмотреть эту фундаментальную процедуру с позиций доказательной медицины.
Лекарственные препараты вводят парентерально потому, что обычно они так всасываются быстрее, чем из желудочно-кишечного тракта, или же, как инсулин, разрушаются под действием пищеварительных ферментов. Некоторые препараты, как например, медокси-прогестерона ацетат или флуфеназин, высвобождаются в течение длительного времени, и требуется такой путь введения, который бы обеспечил постоянное всасывание препарата.
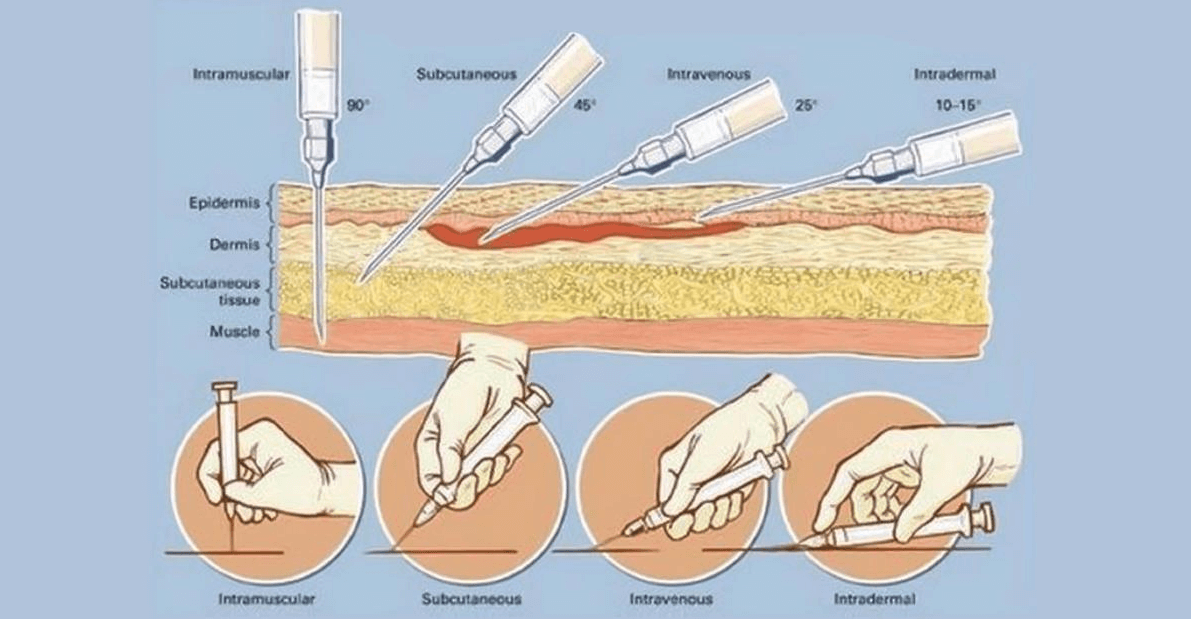
Существуют четыре главных характеристики инъекции: место введения, путь введения, техника инъекции и оснащение.
Внутрикожный путь введения
Внутрикожный путь введения предназначен для обеспечения скорее местного, а не системного действия препаратов, и, как правило, применяется в основном для диагностических целей, например аллерготестов и туберкулиновых проб, или для введения местных анестетиков.
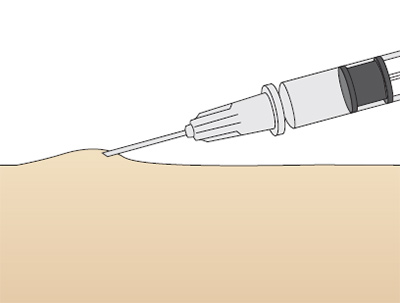
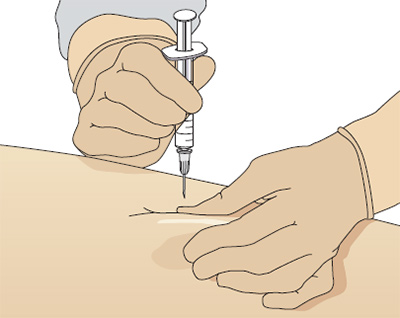
Для выполнения внутрикожной инъекции иглу калибра 25G срезом кверху вводят в кожу под углом исключительно под эпидермис и вводят до 0.5 мл раствора, до появления на поверхности кожи так называемой «лимонной корочки» (Рис. 1). Такой путь введения применяется для выполнения аллерготестов, и место инъекции должно быть обязательно отмечено, чтобы отследить аллергическую реакцию через определенный промежуток времени.
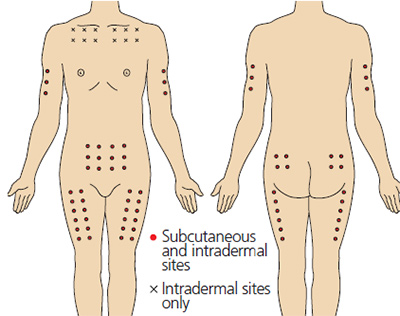
Места для выполнения внутрикожных инъекций аналогичны таковым для выполнения подкожных инъекций (Рис. 2), но также их можно выполнять на внутренней стороне предплечья и под ключицами (Springhouse Corporation 1993).
При проведении аллергопроб очень важно обеспечить наличие противошокового набора в ближайшем доступе, если у пациента будет реакция гиперчувствительности или анафилактический шок (Campbell 1995).
Рис. 1. «Лимонная корочка», которая образуется при внутрикожной инъекции.
ВАЖНО (1):
Вспомните симптомы и признаки анафилактических реакций.
Что вы будете делать при анафилактическом шоке?
Какие препараты, которые вы применяете, могут спровоцировать аллергическую реакцию?
Подкожный путь введения
Подкожный путь введения препаратов используется, когда необходимо медленное равномерное всасывание медикамента в кровь, при этом препарата вводят под кожу. Этот путь введения идеален для таких лекарственных препаратов, как инсулин, который требует медленного равномерного высвобождения, он относительно безболезненный и подходит для частых инъекций (Springhouse Corporation 1993).
На Рис. 2 представлены места, пригодные для выполнения подкожных инъекций.
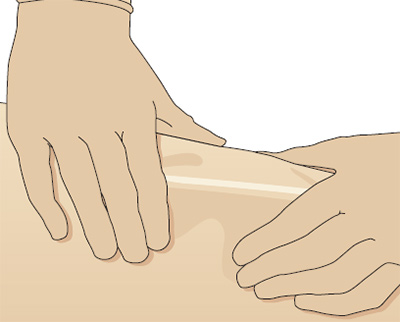
Традиционно, подкожные инъекции проводятся путем вкола иглы под углом 45 градусов в складку кожи (Thow и Home 1990). Однако с введением в практику более коротких инсулиновых игл (длиной 5, 6 или 8 мм), инъекции инсулина сейчас рекомендуется выполнять со вколом иглы под углом 90 градусов (Burden 1994). Следует обязательно брать кожу в складку, для того, чтобы отделить жировую ткань от подлежащих мышц, особенно у худых пациентов (Рис. 3). Некоторые исследования с применением компьютерной томографии для отслеживания направления движения инъекционной иглы, показали, что иногда при подкожном введении препарат непреднамеренно оказывается в мышце, особенно при инъекциях в переднюю брюшную стенку у худых пациентов (Peragallo-Dittko 1997).
Инсулин, введенный внутримышечно, всасывается намного быстрее, и это может привести к нестабильной гликемии, и возможно, даже к гипогликемии. Гипогликемические эпизоды могут отмечаться и в том случае, если меняется анатомическая область проведения инъекции, так как инсулин из разных участков всасывается с разной скоростью (Peragallo-Dittko 1997).
По этой причине должна проводиться постоянная смена мест введения инсулина, например, в течение нескольких месяцев используется область плеча или живота, затем место введения меняется (Burden 1994). Когда госпитализируется пациент с диабетом, надо посмотреть, нет ли в местах введения инсулина признаков воспаления, отека, покраснения или липоатрофий, и обязательно отметить это в медицинской документации.
Проводить аспирацию содержимого иглы при подкожном введении в настоящее время признано нецелесообразным. Peragallo-Dittko (1997) сообщает о том, что прокол кровеносных сосудов перед подкожной инъекцией встречается очень редко.
Информацию о необходимости аспирации не содержат и обучающие материалы для пациентов с диабетом. Также было отмечено, что аспирация перед введением гепарина повышает риск образования гематомы (Springhouse Corporation 1993).
Внутримышечный путь введения
При внутримышечном введении лекарственный препарат оказывается в хорошо перфузируемой мышце, что обеспечивает его быстрое системное воздействие, и всасывание достаточно больших доз, от 1 мл из дельтовидной мышцы до 5 мл в других мышцах у взрослых (для детей эти значения следует делить пополам). Выбор места для инъекции должен быть основан на общем состоянии пациента, его возрасте и объеме раствора лекарственного препарата, который нужно ввести.
Предполагаемое место инъекции следует осмотреть на предмет признаков воспаления, отека и инфекции, следует избегать введения препарата в участки повреждений кожи. Аналогичным образом через часа после манипуляции место проведения инъекции следует осмотреть, чтобы убедиться, что нет никаких нежелательных явлений. Если инъекции часто повторяются, то надо отмечать места введения, чтобы менять их.
Это снижает дискомфорт у пациента и уменьшает вероятность развития осложнений, например, атрофии мышц или стерильных абсцессов вследствие плохого всасывания препаратов (Springhouse Corporation 1993).
ВАЖНО (2):
При госпитализации пациентов с диабетом должна вестись специальная медицинская документация.
Как вы отмечаете места ротации инъекций?
Как вы мониторируете пригодность места инъекции?
Обсудите это со своими коллегами.
Рис. 2. Анатомические области для внутрикожных и подкожных инъекций. Красные точки — места подкожных и внутрикожных инъекций, черные крестики — места выполнения только внутрикожных инъекций.
Рис. 3. Захват складки кожи при выполнении подкожной инъекции.
У пожилых и истощенных людей мышечная масса меньше, чем у молодых, более активных людей, поэтому перед выполнением внутримышечной инъекции надо оценить, достаточна ли для этого мышечная масса. Если у пациента мало мышц, то можно взять мышцу в складку до того, как проводить инъекцию (Рис. 4).
Рис. 4. Как взять мышцу в складку у истощенных или пожилых пациентов.
Существует пять анатомических областей, пригодных для выполнения внутримышечных инъекций.
На Рис. 5(a-d) подробно показано, как определить анатомические ориентиры всех этих областей. Вот эти анатомические области:
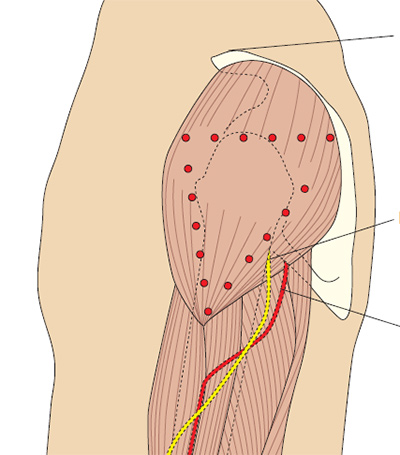
Рис. 5a. Определение положения дельтовидной мышцы.
Самая плотная часть мышцы определяется так: от акромиального отростка проводится линия до точки на плече на уровне подмышки. Игла вводится примерно на 2.5 см ниже акромиального отростка на глубину 90º.
Следует избегать лучевого нерва и плечевой артерии (Springhouse Corporation 1993).
Можно попросить пациента положить кисть на бедро (как это делают модели во время показов), что облегчает поиск мышцы.
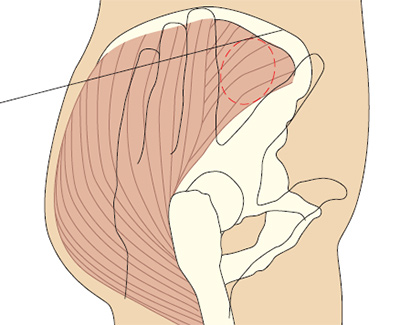
Для определения большой ягодичной мышцы: пациент может лежать на боку со слегка согнутыми коленями, или направив большие пальцы ног вовнутрь. Если ноги слегка согнуты, то мышцы более расслаблены и инъекция менее болезненная (Covington и Trattler 1997).
Рис. 5b. Определение наружного верхнего квадранта ягодицы.
Проведите воображаемую горизонтальную линию от места начала межъягодичной щели до большого вертела бедра. Затем нарисуйте другую воображаемую линию вертикально в середине предыдущей, и вверху латерально будет верхний наружный квадрант ягодицы (Campbell 1995). Мышца, которая в нем лежит — это большая ягодичная мышца. При ошибке во время выполнения инъекции можно повредить верхнюю ягодичную артерию и седалищный нерв. Типичный объем жидкости для введения в этой области составляет
Рис. 5c. Определение переднее-ягодичной области.
Положите ладонь правой руки на большой вертел левого бедра пациента (и наоборот). Указательным пальцем нащупайте верхний передний гребень подвздошной кости и отодвиньте средний палец, чтобы образовалась буква V (Beyea и Nicholl 1995). Если у вас маленькие руки, то это получается сделать не всегда, поэтому просто сдвиньте руку в сторону гребня (Covington и Trattler 1997).
Иглу вводят в среднюю ягодичную мышцу в середине буквы V под углом 90º. Типичный объем раствора препарата для введения в этой области составляет
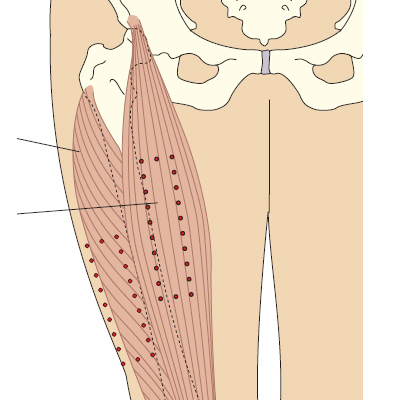
Рис. 5d. Определение латеральной головки четырехглавой мышцы бедра и прямой мышцы бедра.
У взрослых латеральную головку четырехглавой мышцы бедра можно определить на ладонь ниже и латеральнее большого вертела, и на ладонь выше колена, в средней трети четырехглавой мышцы бедра. Прямая мышца бедра находится в средней трети передней поверхности бедра. У детей и пожилых, или у истощенных взрослых, иногда эту мышцу приходится брать в складку, чтобы обеспечить достаточную глубину введения препарата (Springhouse Corporation 1993). Ого раствора препарата составляет для младенцев —
Прямая мышца бедра — это часть передней четырехглавой мышцы бедра, это место редко используется для инъекций медсестрами, но нередко используется при самостоятельном введении лекарственных препаратов, или у младенцев (Springhouse Corporation 1993).
ВАЖНО (3):
Научитесь определять анатомические ориентиры для каждой из этих пяти областей для внутримышечных инъекций.
Если вы привыкли вводить препараты только в верхне-наружный квадрант ягодицы, то научитесь использовать новые области и регулярно совершенствует свою практику.
Методика
От угла введения иглы зависит боль от инъекции. Иглу при внутримышечной инъекции следует вводить под углом 90° и убедиться, что игла достигла мышцы — это позволяет уменьшить боль от инъекции. Исследование Katsma и Smith (1997) выявило, что не все медсестры вводят иглу под углом 90°, считая, что именно такая методика делает инъекцию более болезненной, так как игла быстро проходит сквозь ткани. Растягивание кожи уменьшает вероятность повреждений от иглы и улучшает точность введения препарата.
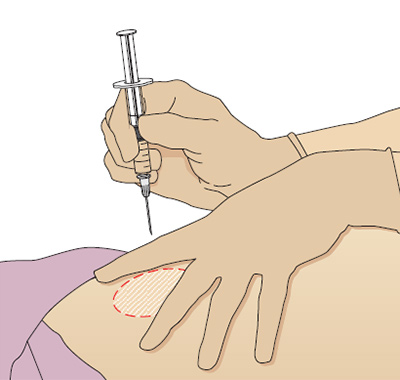
Чтобы правильно ввести иглу, положите кисть нерабочей руки и натяните кожу над местом вкола указательным и средним пальцем, а запястье рабочей руки положите на большой палец нерабочей. Держите шприц между подушечками большого и указательного пальцев, именно так удается ввести иглу точно и под нужным углом (Рис. 6).
Рис. 6. Методика выполнения внутримышечной инъекции, угол вкола иглы 90º, переднее-ягодичная область.
В Великобритании проводилось мало исследований на эту тему, поэтому у медсестер могут быть совершенно разные навыки и технологии выполнения инъекций (MacGabhann 1998). Традиционная методика выполнения внутримышечных инъекций заключалась в растяжении кожи над местом ее прокола, чтобы снизить чувствительность нервных окончаний (Stilwell 1992) и быстрый укол иглой под углом в 90° к коже.
Однако в обзоре литературы, подготовленном Beyea и Nicholls’ (1995) указано, что использование Z-методики дает меньший дискофморт и сниженное количество осложнений по сравнению с традиционной методикой.
Z—методика
Эта методика изначальна была предложена для введения лекарственных препаратов, которые окрашивают кожу или являются сильными раздражителями. Сейчас она рекомендуется для внутримышечного введения любых медикаментов (Beyea и Nicholl 1995), так как считается, что ее применение уменьшает болезненность, и вероятность вытекания препарата (Keen 1986).
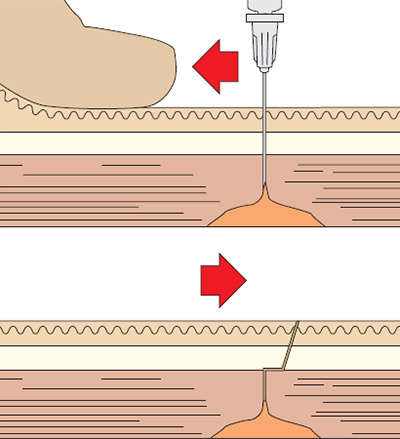
В этом случае кожу на месте инъекции оттягивают вниз или в сторону (Рис. 7). Это сдвигает кожу и подкожную клетчатку примерно на Очень важно помнить, что при этом направление иглы меняется и можно не попасть в нужное место.
Поэтому, после определения места инъекции, нужно выяснить, какая мышца находится под поверхностными тканями, а не какие кожные ориентиры вы видите. После введения препарата подождите 10 секунд до удаления иглы, чтобы препарат всосался в мышцу. После удаления иглы, отпустите кожу. Ткани над местом инъекции закроют депозит раствора лекарственного средства и предотвратят его утечку. Считается, что если конечность после инъекции будет двигаться, то всасывание препарата ускорится, так как в месте инъекции увеличится кровоток (Beyea и Nicholl 1995).
Рис. 7. Z-методика.
Методика воздушного пузырька
Эта методика была очень популярна в США. Исторически она была разработана во времена использования стеклянных шприцев, в которых требовалось использовать пузырек воздуха для того, чтобы убедиться, что доза препарата правильная. Сейчас «мертвое пространство» в шприце не считается необходимым, так как пластиковые шприцы откалиброваны более точно, чем стеклянные и эта методика больше не рекомендуется производителями (Beyea and Nicholl 1995).
Недавно в Великобритании были проведены два исследования на муляжах (масляный раствор с медленным высвобождением препарата) (MacGabhann 1998, Quartermaine и Taylor 1995), в которых сравнивалась Z-методика и методика воздушного пузырька, предназначеная для предупреждения утечки раствора после инъекции.
Quartermaine и Taylor (1995) предположили, что методика воздушного пузырька более эффективна для предупреждения утечки по сравнению с Z-методикой, но результаты MacGabhann (1998) не позволили сделать каких-то определенных выводов.
Существуют вопросы, связанные с точностью дозировки при использовании данной методики, так как доза препарата в данном случае может существенно повышаться (Chaplin et al 1985). Требуются дальнейшие исследования данной методики, так как для Великобритании она считается относительно новой. Однако, если она используется, медицинская сестра должна убедиться, что она вводит пациенту правильную дозу препарата, и что методика используется строго в соответствии с рекомендациями.
Методика аспирации
Хотя в настоящее время методика аспирации не рекомендована для контроля при проведении подкожных инъекций, ее следует использовать при внутримышечных инъекциях. Если игла по ошибке попала в кровеносный сосуд, то препарат можно непреднамеренно ввести внутривенно, что иногда приводит к эмболии вследствие специфических химических свойств лекарств. При внутримышечном введении препарата, в течение нескольких секунд следует проводить аспирацию содержимого иглы, особенно если используются тонкие длинные иглы (Torrance 1989a). Если в шприце видно кровь, то его вынимают, и готовят свежий препарат для инъекции в другом месте. Если крови нет, то препарат можно вводить, со скоростью примерно 1 мл за 10 секунд, это кажется немного медленным, но позволяет мышечным волокнам раздвинуться для правильного распределения раствора. Перед тем, как удалять шприц, надо подождать еще 10 секунд, а потом убрать шприц и прижать место введения салфеткой со спиртом.
Массировать место инъекции не нужно, так как в этом случае может возникнуть утечка препарата из места введения и раздражение кожи (Beyea и Nicholl 1995).
Обработка кожи
Хотя известно, что очистка кожи салфеткой со спиртом до проведения парентеральных манипуляций снижает число бактерий, на практике имеются противоречия. Протирание кожи для подкожного введения инсулина предрасполагает к уплотнению кожи под действием алкоголя.
Ранее проведенные исследования позволяют предположить, что такое протирание не является необходимым, и что отсутствие подготовки кожи не приводит к инфекционным осложнениям (Dann 1969, Koivisto и Felig 1978).
Некоторые специалисты сейчас считают, что если пациент соблюдает чистоту, а медсестра четко выполняет все стандарты гигиены и асептику во время выполнения процедуры, то дезинфекция кожи при выполнении внутримышечной инъекции не является необходимой. Если практикуется дезинфекция кожи, то кожу нужно протирать не менее 30 секунд, потом давать ей высохнуть в течение еще 30 секунд, в противном случае вся процедура неэффективна (Simmonds 1983). Вдобавок, выполнение инъекции до высыхания кожи, не только увеличивается ее болезненность, но и в толщу тканей могут попасть еще живые бактерии с кожи (Springhouse Corporation 1993).
ВАЖНО (4):
Какие рекомендации по обработке кожи перед инъекциями существуют в вашем учреждении?
Уточните, какие рекомендации есть по проведению инъекций инсулина.
Соответствуют ли эти рекомендации данным исследований, приведенным в статье?
Как вы будете поступать?
ВАЖНО (5):
Представьте себе, что вы наблюдаете за студентом, который собирается выполнить свою первую инъекцию. Какие подсказки или советы вы будете использовать в этом случае, чтобы обучающийся правильно развивал навыки выполнения инъекций?
Оборудование
Иглы для внутримышечных инъекций должны быть такой длины, чтобы они достигли мышцы, и при этом не менее четверти иглы должны оставаться над кожей. Чаще всего для внутримышечных инъекций используются иглы калибра 21G (зеленые) или 23 (синие), длиной от 3 до 5 см. Если у пациента много жировой ткани, то для выполнения внутримышечных инъекций требуются более длинные иглы, чтобы они достигли мышцы. Cockshott et al (1982) обнаружили, что толщина подкожно-жировой клетчатки у женщин в ягодичной области может быть на 2.5 см больше, чем у мужчин, поэтому стандартная инъекционная игла 21 G длиной 5 см достигает большой ягодичной мышцы только у 5% женщин и 15% мужчин!
Beyea и Nicholl (1995) рекомендовали смену иглы при выполнении внутримышечной инъекции после набора препарата из ампулы или флакона, чтобы быть уверенными в том, что игла чистая, сухая и острая.
Если иглой уже прокалывали резиновую крышку флакона, то она тупится, и в этом случае инъекция будет более болезненной, так как кожу приходится прокалывать с большим усилием.
Размер шприца определяется объемом вводимого раствора. Для внутримышечного введения растворов в объеме менее 1 мл, применяются только шприцы малого объема, чтобы точно отмерить нужную дозу препарата (Beyea и Nicholl 1995). Для введения растворов объемом 5 мл и более, лучше разделить раствор на 2 шприца и вводить в разные участки (Springhouse Corporation 1993). Обратите внимание на наконечники шприцов — они имеют разное предназначение.
Перчатки и вспомогательные материалы
В некоторых учреждениях правила требуют использования перчаток и фартуков во время выполнения инъекций. Следует помнить, что перчатки защищают медицинскую сестру от выделений пациента, от развития лекарственной аллергии, но они не обеспечивают защиты от повреждений от игл.
Некоторые медицинские сестры жалуются, что в перчатках им работать неудобно, особенно если изначально они учились выполнять ту или иную манипуляцию без них. Если медицинская сестра работает без перчаток, то нужно проявлять осторожность, и следить за тем, чтобы на руки ничего не попало — ни лекарств, ни крови пациентов. Даже чистые иглы надо сразу же утилизировать, их ни в коем случае нельзя повторно закрывать колпачками, иглы сбрасывают только в специальные контейнеры. Помните, что иглы могут упасть из лотков для инъекций на кровать пациенту, что может привести к травмам как у пациентов, так и у персонала.
Для защиты спецодежды от брызгов крови или растворов для инъекций можно использовать чистые одноразовые фартуки, также это полезно в тех случаях, когда необходим особый санэпидрежим (для профилактики переноса микроорганизмов от одного больного к другому). Нужно аккуратно снимать фартук после процедуры, чтобы попавшие на него загрязнения не вступали в контакт с кожей.
ВАЖНО (6):
Составьте список из всех способов, которые помогают уменьшить болезненность инъекций. Сравните с Таблицей 1.
Как вы сможете использовать больше способов уменьшения болезненности инъекций в вашей практике?
Таблица 1. Двенадцать шагов к тому, чтобы сделать инъекции менее болезненными
| 1 | Подготовьте пациента, объясните ему сущность процедуры, так, чтобы он понял, что будет происходить, и четко выполнял все ваши инструкции |
| 2 | Поменяйте иглу после того, как вы набрали препарат из флакона или ампулы, и убедитесь, что она острая, чистая и достаточной длины |
| 3 | У взрослых и детей старше семи месяцев местом выбора для инъекций является передне-ягодичная область |
| 4 | Расположите пациента так, чтобы одна нога была слегка согнута — это уменьшает болезненность при инъекции |
| 5 | Если вы используете салфетки со спиртом, убедитесь, что до выполнения инъекции кожа полностью высохла. |
| 6 | Можно использовать лед или замораживающий спрей, чтобы обезболить кожу, особенно это важно для маленьких детей и пациентов, которые страдают фобией уколов. |
| 7 | Используйте Z-методику (Beyea и Nicholl 1995) |
| 8 | Меняйте стороны выполнения инъекций и отмечайте это в медицинской документации |
| 9 | Прокалывайте кожу аккуратно, под углом, близким к 90 градусам, чтобы предотвратить болезненность и смещение тканей |
| 10 | Аккуратно и медленно введите раствор, со скоростью 1 мл за 10 секунд, чтобы она распределилась в мышце |
| 11 | Перед тем, как убирать иглу, подождите 10 секунд, и вытаскивайте иглу под тем же углом, что и вводили |
| 12 | Не массируйте место инъекции после ее завершения, просто прижмите участок укола марлевой салфеткой |
Уменьшение боли
Пациенты очень часто боятся выполнения инъекций, поскольку предполагают, что это больно. Боль обычно возникает вследствие раздражения болевых рецепторов кожи, или рецепторов давления в мышце.
Torrance (1989b) привел список факторов, которые могут вызывать боль:
В Таблице 1 перечислены способы уменьшения болезненности от введения препарата.
У пациентов может быть сильная боязнь уколов и игл, страх, беспокойство — все это значительно усиливает болезненность при инъекциях (Pollilio и Kiley 1997). Хорошая техника выполнения процедуры, адекватное информирование пациента и спокойная, уверенная медсестра — лучший путь к уменьшению болезненности манипуляции и уменьшению реакции больного. Можно также использовать методики модификации поведения, особенно в случае, когда пациенту предстоят длительные курсы лечения, а иногда приходится применять безыгольные системы (Pollilio и Kiley 1997).
Предполагается, что обезболивание кожи льдом или охлаждающими спреями до укола позволяет уменьшить боль (Springhouse Corporation 1993), хотя в настоящее время нет доказательств эффективности этой методики, полученных в исследованиях.
Медицинские сестры должны понимать, что пациенты могут даже переживать синкопальные состояния или обмороки после обычных инъекций, даже если в остальном они вполне здоровы. Нужно выяснить, было ли такое ранее, и желательно, чтобы рядом была кушетка, на которую больной может прилечь — это уменьшает риск травм. Чаще всего такие обмороки случаются у подростков и молодых мужчин.
ВАЖНО (7):
Оцените возможность возникновения осложнений, которые мы обсуждали.
Запишите, что вы можете сделать, чтобы их предотвратить.
Осложнения
Осложнения, которые развиваются в результате инфицирования, могут быть предупреждены строгим соблюдением мер асептики и тщательным мытьем рук. Стерильные абсцессы могут возникать в результате частых инъекций или плохого местного кровотока. Если место инъекции отечное или эта область тела парализована, то препарат будет плохо всасываться, и такие участки не стоит использовать для инъекций (Springhouse Corporation 1993).
Тщательный выбор места инъекции позволит избежать повреждения нерва, случайно внутривенной инъекции и последующей эмболии компонентами препарата (Beyea и Nicholl 1995). Систематическая смена места инъекции предупреждает такие осложнения, как инъекционная миопатия и липогипертрофия (Burden 1994). Подходящая длина иглы и использование для инъекций передне-ягодичной области позволяет ввести лекарственный препарат точно в мышцу, а не в подкожно-жировую клетчатку. Применение Z-методики уменьшает боль и окрашивание кожи, характерное для применения некоторых лекарственных препаратов (Beyea и Nicholl 1995).
Профессиональная ответственность
Если препарат введен парентерально, то «вернуть» его уже никак нельзя. Поэтому всегда надо проверять дозу, правильность назначения, и уточнять у пациента его фамилию, чтобы не перепутать назначения. Итак: нужное лекарство нужному пациенту, в нужной дозе, в нужное время, и нужным способом — это позволит избежать медицинских ошибок. Все препараты надо готовить исключительно по инструкции производителя, все медсестры должны знать, как действуют эти препараты, противопоказания к их применению и побочные действия. Медицинская сестра должна оценить, а можно ли вообще применять препарат у данного пациента в данное время (UKCC 1992).
Выводы
Безопасное выполнение инъекций — одна из основных функций медицинской сестры, оно требует знания анатомии и физиологии, фармакологии, психологии, навыков общения, и практического опыта.
Существуют исследования, которые доказывают эффективность методик выполнения инъекций для предупреждения осложнений, но до сих пор есть «белые пятна», которые нуждаются в дополнительных исследованиях. В данной статье акцент сделан на доказанных в исследованиях методиках, чтобы медицинские сестры могли включать данные процедуры в свою ежедневную практику.
Список литературы
Beyea SC, Nicholl LH (1995) Administration of medications via the intramuscular route: an integrative review of the literature and research-based protocol for the procedure. Applied Nursing Research. 5, 1, (1994) A practical guide to insulin injections. Nursing Standard. 8, 29, (1995) Injections. Professional Nurse. 10, 7, G et al (1985) How safe is the air bubble technique for IM injections? Not very say these experts. Nursing. 15, 9, 59.
Cockshott WP et al (1982) Intramuscular or intralipomatous injections. New England Journal of Medicine. 307, 6, TP, Trattler MR (1997) Learn how to zero in on the safest site for an intramuscular injection. Nursing. January, (1969) Routine skin preparation before injection. An unnecessary procedure. Lancet. ii, D, Smith G (1997) Analysis of needle path during intramuscular injection. Nursing Research. 46, 5, (1986) Comparison of Intramuscular injection techniques to reduce site Koivisto VA, Felig P (1978) Is skin preparation necessary before insulin injection? Lancet. i, (1998) A comparison of two injection techniques. Nursing Standard. 12, 37, V (1997) Rethinking subcutaneous injection technique. American Journal of Nursing. 97, 5, AM, Kiley J (1997) Does a needless injection system reduce anxiety in children receiving intramuscular injections? Pediatric Nursing. 23, 1, S, Taylor R (1995) A Comparative study of depot injection techniques. Nursing Times. 91, 30, (1983) CDC guidelines for the prevention and control of nosocomial infections: guidelines for prevention of intravascular infections. American Journal of Infection Control. 11, 5, Corporation (1993) Medication Administration and IV Therapy Manual. Second edition. Pennsylvania, Springhouse Corporation.
Stilwell B (1992) Skills Update. London, MacMillan Magazines.
Thow J, Home P (1990) Insulin injectiontechnique. British Medical Journal. 301, 7, July (1989a) Intramuscular injection Part 2. Surgical Nurse. 2, 6, (1989b) Intramuscular injection Part 1. Surgical Nurse. 2, 5, Kingdom Central Council for Nursing, Midwifery and Health Visiting (1992) Standards for Administration of Medicine. London, UKCC.