Можно ли капать пенициллин в нос
Пенициллины представляют собой группу антибиотиков, в основе структуры которых лежит бета-лактамное кольцо. Соединяясь с пенициллинсвязывающими белками клеточной мембраны бактерий, они приводят к их осмотическому лизису и гибели.
а) Естественные пенициллинны. К естественным пенициллинам относится пенициллин V для перорального приема и ряд препаратов для парентерального введения (например, бензатин-пенициллин G, водная/кристаллическая формы, прокаин-пенициллин).
Клиническое применение. Естественные пенициллины активны в отношении Streptococcus pyogenes (β-гемолитического группы А), большинства штаммов Streptococcus pneumoniae, Treponema pallidum, Actinomyces и некоторых анаэробов полости рта. Естественные пенициллины инактивируются под действием бета-лактамаз многих грам-негативных бактерий и анаэробов полости рта, также их разрушает пенициллиназа золотистого стафилококка. Другим механизмом развития устойчивости является трансформация пенициллинсвязывающих белков, он встречается у некоторых штаммов стафилококка и пневмококка.
б) Пенициллины, устойчивые к действию пенициллиназ. Клиническое применение. Активны в отношении золотистого стафилококка, за исключением штаммов, резистентных к метициллину (MRSA). Сохраняют активность в отношении большинства штаммов стрептококков и пневмококков. Нафциллин метаболизируется печенью, поэтому он может использоваться у больных с заболеваниями почек.
Из пероральных препаратов данной группы наибольшая концентрация в плазме крови наблюдается при приеме диклоксациллина.
в) Аминопенициллины. К данному классу относятся ампициллин и амоксициллин.
Клиническое применение. Активны в отношении некоторых грамотрицательных организмов, Proteus, Haemophilus influenzae и Escherichia coli. Разрушаются под действием бета-лактамаз, неэффективны в отношении золотистого стафиллокока.
г) Пенициллины широкого спектра действия. Группа включает в себя амоксициллин/клавулонат натрия (аугментин, Reddis), ампициллин/сульбактам (уназин, Pfizer), пиперациллин/тазобактам (зосин, Pfizer), тикарциллин/клавулонат натрия (тиментин, GlaxoSmithKline).
Клиническое применение. Это комбинированные препараты, в состав которых входит пенициллин и ингибитор бета-лактамаз. Они эффективны в отношении Н. influenzae, М. catarrhalis, анаэробов и некоторых стафилококков (но не MRSA). Тиментин и зосин также могут использоваться при синегнойной инфекции. Тикарциллин и пиперациллин без ингибиторов бета-лактамаз не активны в отношении грамположительной флоры.
д) Побочные эффекты антибиотиков пенициллинов. После приема пенициллинов сыпь возникает примерно у 5% пациентов, но при повторном приеме она повторяется лишь у половины из них. Анафилактические реакции возникают у 0,05% пациентов, они являются противопоказанием к дальнейшему использованию пенициллинов. Другими возможными побочными эффектами являются интерстициальный нефрит, анемия и лейкопения. При длительном (более двух недель) приеме высоких доз требуется контроль показателей креатинина и клеточного состава крови.
Аугментин часто вызывает нежелательные побочные эффекты со стороны желудочно-кишечного тракта. У больных с инфекционным мононуклеозом прием амоксициллина приводит к появлению розеолезной сыпи у 65-90% пациентов; в данном случае ее нельзя считать проявлением истинной аллергии. Пероральные пенициллины, за исключением амоксициллина, разрушаются кислотой желудочного сока, поэтому их необходимо принимать натощак. Пациентам с серьезной аллергической реакцией на пенициллины в анамнезе перед их приемом должны проводиться кожные пробы и десенсибилизация.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Острый гайморит: как не довести болезнь до серьезных осложнений?
На сегодняшний день практически каждый человек слышал о таком заболевании, как острый гайморит. Самое главное, что важно знать, это что такое гайморит и как не «запустить» болезнь. Итак, острый гайморит — это острое воспаление гайморовых пазух. Гайморовы пазухи — это две полости (или по-научному «синусы»), располагающиеся в толще верхней челюсти, поэтому есть и другое название заболевания: «верхнечелюстной синусит».
Причины острого гайморита
Для того, чтобы разобраться в том, как развивается острый гайморит, надо понимать, что происходит в полости носа и пазухе при возникновении болезни. В полости носа находится слизистая оболочка, которая распространяется в полость пазухи. В свою очередь, пазуха как бы «открывается» в нос при помощи отверстия или соустья. Когда в носу начинается воспаление, то возникает активный рост бактерий, которые через соустье попадают в пазуху. А из-за выраженного отёка слизистой носа соустье закрывается, и бактерии, попавшие в пазуху, начинают расти в ней, вызывая воспаление. Так же частой причиной развития гайморита могут стать и больные зубы. Дело в том, что часть зубов верхней челюсти опускаются корнями в полость пазухи. Когда в зубе имеется воспалительный процесс, то он распространяется на слизистую оболочку пазухи. Гораздо реже гайморит может развиться из-за снижения иммунитета, особенно при длительных хронических заболеваниях.
Таким образом, причинами, вызывающими острый гайморит являются:
Симптомы острого гайморита
Диагностика острого гайморита
Зачастую, в диагностике острого гайморита сложностей не возникает. Для этого пациента должен осмотреть врач-оториноларинголог. Диагноз ставится на основании жалоб и анамнеза болезни, данных осмотра, рентгенологического исследования (в последнее время чаще используется компьютерная томография околоносовых пазух), общего анализа крови, мазка из полости носа или пазухи на микрофлору и чувствительности к антибиотикам.
При осмотре (метод носит название «передняя риноскопия») выявляется покрасневшая и отечная слизистая полости носа с гнойным или слизисто-гнойным отделяемым. Так же врач оценивает и состояние перегородки носа (бывает такое, что она искривлена, что может значительно ухудшить процесс лечения). Далее проводится постукивание (или «перкуссия») передних стенок верхнечелюстных пазух, при выраженном воспалении пациент почувствует боль.
Рентгенологическое исследование или компьютерная томография позволяет точно установить диагноз и оценить состояние пазух, что позволит назначить правильное лечение.
В общем анализе крови обычно бывает повышение лейкоцитов, СОЭ, палочкоядерных нейтрофилов.
Мазок покажет, какой микроб вызвал это воспаление, а определение чувствительности — подобрать правильный препарат.
Лечение острого гайморита
Острый гайморит лечится антибиотиками. При первом посещении врача назначается антибиотик широкого спектра действия. А когда будет готов результат мазка, то антибиотик может быть заменён, за исключением, если микроб уже чувствителен к препарату. Для того, чтобы убрать отёк в носу, пациенту назначаются сосудосуживающие капли в нос на срок от 5 до 7 дней. Так же назначаются антигистаминные (противоаллергические) препараты. Хороший эффект дают растительные муколитические препараты, они способствуют разжижению и лучшему отхождению содержимого пазух.
Промывание полости носа и пазух солевыми растворами позволяет убрать содержимое из носа. Промывание может проводиться в домашних условиях специальными устройствами, купленными в аптеке, или в лечебных учреждениях при помощи аспиратора и насадки.
Самой распространённой процедурой для лечения гайморита является пункция верхнечелюстной пазухи. Пункция (или в простонародии «прокол») позволяет быстро убрать гной из пазухи и значительно ускорить выздоровление.
Если пациент во время обратится к врачу и начнёт лечение, то процесс выздоровления наступит значительно раньше, и можно избежать многих осложнений, связанных с острым гайморитом.
Опыт применения комбинированных препаратов при лечении ринитов и синуситов у детей
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых и особенно хронических воспалительных заболеваний носа и околоносовых пазух является нарушение механизма мукоцилиарного транспорта. Это чаще всего связано с отеком слизистой оболочки, избыточным образованием и повышением вязкости носового секрета, что влечет за собой расстройство дренажной, дыхательной, секреторной и обонятельной функций. Наиболее распространенный метод лечения синуситов — пероральное или внутримышечное назначение антибиотиков. Так как поступление антибиотика из кровяного русла в очаг воспаления ограничено, лечение синуситов должно носить комплексный характер.
В первую очередь это должно касаться улучшения вентиляции, а также дренажа околоносовых пазух и носоглотки.
До настоящего времени врачи-оториноларингологи не всегда практикуют назначение включенных в схему терапии больных синуситами адекватных мукорегулирующих препаратов, которые, разжижая густой вязкий секрет и улучшая мукоцилиарный клиренс, способствуют удалению секрета из пазух. Среди препаратов, воздействующих на мукоцилиарную активность, ранее использовались средства, стимулирующие разжижение ринобронхиального секрета, или так называемые муколитики, которые изменяют вязкость секрета, воздействуя на его физико-химические свойства. Речь идет о ферментах (трипсине, химотрипсине и т. д.), которые из-за наличия побочных эффектов в настоящее время не применяются.
Муколитическим действием обладают также препараты, снижающие поверхностное натяжение, т. е. воздействующие на гель-фазу отделяемого и разжижающие как мокроту, так и носоглоточный секрет. К этой группе относится флуимуцил (N-ацетилцистеин), действие которого связано со способностью свободной сульфгидрильной группы N-ацетилцистеина расщеплять межмолекулярные дисульфидные связи агрегатов гликопротеинов слизи, оказывая сильное разжижающее действие и уменьшая вязкость в отношении любого вида секрета: гнойного, слизисто-гнойного, слизистого. Особенность флуимуцила состоит в том, что помимо прямого муколитического действия N-ацетилцистеин обладает мощными антиоксидантными свойствами и способен обеспечить защиту органов дыхания от цитотоксического воздействия метаболитов воспаления, факторов окружающей среды, табачного дыма.
В группе муколитиков большой интерес представляют комбинированные препараты, а именно ринофлуимуцил, в состав которого кроме N-ацетилцистеина, разжижающего секрет, входит симпатомиметик — туаминогептана сульфат, обладающий мягким сосудосуживающим действием и не вызывающий излишней сухости слизистой оболочки. После разрыва дисульфидных мостиков слизь и мокрота теряют вязкость, начинают впитывать в себя воду и мягко удаляются при сморкании, чихании, кашле. Показаниями к применению ринофлуимуцила являются:
Оценка эффективности препарата производилась в группе из 55 пациентов в возрасте от 6 до 14 лет; ринофлуимуцил впрыскивали по одной дозе в каждую половину носа 3-4 раза в день, курс составил 6-7 дней. Состояние детей оценивали по их субъективным ощущениям до и после применения препарата, а также объективным критериям (уменьшение гиперемии и застойных явлений в слизистой оболочке, улучшение носового дыхания, уменьшение слизи, изменение ее реологических свойств).
Уже после 6-8 ингаляций ринофлуимуцила была отмечена положительная динамика.
Результат применения препарата оценивался следующим образом: 70% больных — отлично; 20% — хорошо; 10% — удовлетворительно.
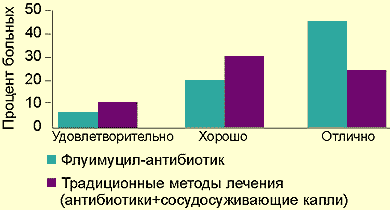 |
| Рисунок. Сравнительные результаты лечения флуимуцилом-антибиотиком ИТ и традиционными методами |
Побочных явлений от применения препарата не отмечено. Достоинство ринофлуимуцила в том, что он воздействует на поверхность слизистой оболочки и, разжижая слизь, уменьшает ее вязкость и способствует продуктивному физиологическому акту очищения полости носа.
Следующий препарат, на который следует обратить внимание, — это флуимуцил-антибиотик ИТ, соединяющий в одной лекарственной форме два компонента: N-ацетилцистеин и тиамфеникола глицинат (тиамфеникол — препарат из группы хлорамфениколов). Спектр антимикробной активности препарата представлен в табл. 1 (Клиническая фармакология антибактериальных препаратов/Под ред. Ю. Б. Белоусова, 1988).
Препарат обладает сочетанным антибактериальным и муколитическим действием и рекомендуется для лечения заболеваний органов дыхания, вызванных бактериальной инфекцией и сопровождающихся образованием густого вязкого секрета. Антимикробная активность тиамфеникола обусловлена его вмешательством в синтез бактериальных белков. Последние исследования показали, что сочетание тиамфеникола и N-ацетилцистеина позволяет препарату сохранять неконъюгированную форму и достигать очага воспаления в концентрациях, достаточных для создания бактерицидного эффекта. Препарат проявляет муколитическую активность в отношении любого вида секрета — слизистого, слизисто-гнойного, гнойного. Флуимуцил-антибиотик ИТ облегчает отделение мокроты и носовой слизи. Препарат эффективен при введении в околоносовые пазухи.
Мы располагаем данными лечения препаратом флуимуцил-антибиотик ИТ у 37 детей, из них у 17 был диагностирован острый гайморит, у 10 — обострение хронического гайморита и у 10 — обострение хронического гнойного гаймороэтмоидита. Контрольная группа пациентов лечилась традиционным методом без применения флуимуцила-антибиотика. Сравнительные данные представлены на рисунке.
Препарат использовался для промывания околоносовых пазух после пункций или после оперативного вмешательства, в том числе после эндоназального вскрытия клеток решетчатого лабиринта. Хорошие результаты были получены уже после 2-3 промываний: улучшилось носовое дыхание, сократился отек слизистой оболочки полости носа, уменьшилось количество секрета, исчез его гнойный характер. Показания и способы применения препарата представлены в табл. 2.
Эффективность флуимуцила-антибиотика ИТ определяется не только антибактериальным воздействием, но и способностью обеспечивать быстрое и полное удаление экссудата, что в свою очередь усиливает антибактериальный эффект.
Литература
Обратите внимание!
Флуимуцил-антибиотик ИТ обладает следующими фармакологическими и терапевтическими свойствами:
Ингибиторозащищенные пенициллины в лечении острого бактериального риносинусита
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Инфекции верхних дыхательных путей (ВДП) – это воспалительный процесс респираторного тракта от слизистой оболочки полости носа до трахеобронхиального дерева. Причиной большинства инфекций ВДП являются вирусы. Поэтому лечение с использованием антибактериальных препаратов при этом достаточно ограниченно, а их назначение нецелесообразно. Назначение антибиотиков при необходимости должно в каждом конкретном случае быть строго индивидуальным, при этом прежде всего должно быть оценено соотношение риска и пользы для пациента.
Острый риносинусит (ОРС) – достаточно часто встречающееся осложнение острой респираторной вирусной инфекции (ОРВИ). ОРС – воспаление слизистой оболочки носа и как минимум одной из околоносовых пазух (ОНП). Это состояние входит в десятку наиболее часто встречающихся в амбулаторной практике врача-интерниста заболеваний. Исследования с использованием компьютерной томографии показали, что при ОРВИ у 87% больных развивается риносинусит, который следует расценивать как вирусный. В 1–2% случаев вирусная инфекция осложняется развитием бактериального ОРС (ОБРС) [4, 7, 20].
ОБРС – достаточно распространенное заболевание с постоянной тенденцией к росту числа заболевших. Например, в США за последние годы по поводу ОРС было приблизительно 25 млн обращений за медицинской помощью в год [24]. В России данная проблема осложняется еще и тем, что из года в год все большему количеству больных требуется стационарное лечение. Причем удельный вес больных, госпитализированных по поводу заболеваний ОНП, ежегодно увеличивается на 1,5–2% [5, 13].
Классификация ОБРС основана на длительности, повторяемости и тяжести симптомов. Наиболее удачной, по нашему мнению, является классификация, предложенная специальной комиссией Американской академии отоларингологов (American Academy of Otolaryngology Head and Neck Surgery) (табл. 1).
По тяжести течения выделяют:
1. Легкое: заложенность носа, слизистые или слизисто-гнойные выделения из носа и/или в ротоглотку, повышение температуры тела до 37,5°С, головная боль, слабость, гипосмия; на рентгенограмме околоносовых синусов – толщина слизистой оболочки менее 6 мм.
2. Среднетяжелое: заложенность носа, гнойные выделения из носа и/или в ротоглотку, температура тела выше 37,5°С, боль и болезненность при пальпации в проекции синуса, головная боль, гипосмия, недомогание, могут быть иррадиирущие боли в зубы, уши; на рентгенограмме ОНП синусов утолщение слизистой оболочки более 6 мм, полное затемнение или уровень жидкости в 1-м или 2-х синусах.
3. Тяжелое: заложенность носа, часто обильные гнойные выделения из носа и/или в ротоглотку (но может быть полное их отсутствие), температура тела выше 38°С, сильная болезненность при пальпации в проекции синуса, головная боль, аносмия, выраженная слабость; на рентгенограмме ОНП синусов полное затемнение или уровень жидкости более чем в 2-х синусах. Анализ крови: лейкоцитоз, сдвиг формулы влево, увеличение СОЭ. Наличие орбитальных, внутричерепных осложнений или подозрение на них. Серьезным осложнением является тромбоз кавернозного синуса, летальность при котором достигает 30% и не зависит от адекватности антибактериальной терапии [22].
Если говорить об этиологии, то спектр возбудителей острого вирусного риносинусита практически не отличается от возбудителей ОРВИ (риновирус, аденовирус, РС-вирус, парагрипп и др.). Что касается микробного пейзажа, то самыми распространенными возбудителями ОБРС являются Streptococcus pneumoniae и Haemophilus influenzae [4, 12, 25]. В патогенезе ОБРС большая роль отводится повреждению мерцательного эпителия ОНП вследствие цитотоксического действия вирусов, что, как правило, приводит к нарушению функционирования ресничек эпителиальных клеток вследствие десквамации поверхностных слоев слизистой оболочки полости носа. Вследствие этих патологических изменений угнетается мукоцилиарный клиренс, что в свою очередь создает благоприятные условия для вторичного бактериального инфицирования с образованием гнойного экссудата [25].
Основные цели лечения ОРС:
С этих позиций ключевым методом лечения ОБРС считается антибиотикотерапия. Но хорошо известно, что около 2/3 пациентов с ОБРС выздоравливают и без лечения антибиотиками [18]. Очень важно перед началом лечения провести дифференциальную диагностику ОБРС от ОРС вирусной этиологии. Это определит необходимость антибиотикотерапии, а также целесообразность назначения антибиотиков узкого спектра действия.
Антибиотикотерапия показана пациентам с продолжительностью заболевания более 7 дней и при наличии 2-х или более клинических критериев ОБРС (гнойные выделения из носовых ходов, боль в области зубов верхней челюсти или лицевая боль, особенно односторонняя; односторонняя болезненность при пальпации в проекции верхнечелюстной пазухи или ухудшение симптомов после начального улучшения) или с тяжелым течением заболевания [3, 11, 16, 18, 23].
Прежде чем перейти к протоколам лечения, хотелось бы остановиться на основных механизмах действия антибактериальных препаратов первой линии – препаратов пенициллинового ряда [1, 2, 4, 12]. Трудно переоценить роль пенициллина для лечения инфекционных заболеваний. История пенициллина началась еще в XIX в., когда итальянский врач Б. Гозио обнаружил первый в мире антибиотик. Скорее всего, это был пенициллин, который, однако, не получил практического применения и был забыт. В 1928 г. английский бактериолог А. Флеминг совершенно случайно пришел к выводу, что обычная плесень синтезирует вещество, уничтожающее бактерии, и назвал выделенное вещество пенициллином. Но открытие ученого не вызвало интереса у врачей. Только в 1938 г. ученые Оксфордского университета Г. Флори и Э. Чейн выделили чистую форму пенициллина. В период Второй мировой войны началось производство этого антибиотика в больших масштабах. А в 1945 г. Флеминг, Флори и Чейн получили Нобелевскую премию за свое открытие. В Советском Союзе выпуск пенициллина был также налажен во время Великой Отечественной войны. В 1944 г. первые его партии поступили в госпитали и на фронт. Пенициллин стал незаменимым лекарством и спас жизни многим людям.
Пенициллины – первые природные антибиотики. Они относятся к группе β-лактамов наравне с цефалоспоринами, карбапенемами и монобактамами. Данный класс антибиотиков занимает ведущее место в лечении большинства инфекций. В настоящее время данная группа включает более 10 антибиотиков, которые в зависимости от источников получения, особенностей строения и антимикробной активности подразделяются на несколько подгрупп: природные, полусинтетические, среди которых выделяют антистафилококковые (оксациллин), расширенного спектра действия (аминопенициллины), антисинегнойные (карбоксипенициллины, уреидопенициллины), ингибиторозащищенные, комбинированные (ампициллин + оксациллин).
Общими свойствами всех препаратов данной группы являются бактерицидное действие, низкая токсичность, преимущественное выведение через почки, широкий диапазон дозировок, наличие перекрестной аллергии между пенициллинами, цефалоспоринами и карбапенемами. β-лактамы нарушают синтез пептидогликана – основного компонента клеточной стенки бактерии, оказывая таким образом бактерицидный эффект.
Бензилпенициллин – первый природный антибиотик. Несмотря на применение в течение более чем 60 лет, он продолжает оставаться значимым препаратом. Природные пенициллины активны в отношении грамположительных бактерий: Staphylococcus, Bacillus, Enterоcoccus, Listeria, Erysipelothrix, Corynebacterium spp. Из грамотрицательных бактерий к природным пенициллинам чувствительны Neisseria, Pasteurella multocida, Haemophilus ducreyi. Большинство анаэробов и спирохеты также чувствительны к природным пенициллинам. Исключение составляют бактероиды, в т. ч. Bacteroides fragilis. У стафилококков все чаще встречается природная резистентность, связанная с продукцией β-лактамаз и пенициллиносвязывающего белка, поэтому для лечения стафилококковой инфекции данные препараты не используются.
Достоинствами природных пенициллинов являются бактерицидная активность в отношении ряда клинически значимых антибиотиков, небольшая токсичность и низкая стоимость. Но помимо приобретенной резистентности стафилококков, пневмококков, гонококков, бактероидов отмечается высокая аллергенность, в т. ч. перекрестная, со всеми пенициллинами. В настоящее время природные пенициллины используются для эмпирической терапии инфекций. Данные препараты применяются для лечения тонзиллофарингита и сифилиса ЛОР-органов, рожистого воспаления, скарлатины и ревматизма.
Для преодоления резистентности микроорганизмов, связанной с продукцией β-лактамаз, были разработаны ингибиторы этих ферментов: клавулановая кислота, сульбактам и тазобактам, которые участвуют в создании ингибиторозащищенных аминопенициллинов. Антимикробный спектр данных препаратов расширен для таких грамотрицательных бактерий, как Klebsiella, Proteus vulgaris, бактероидов, а также микрофлоры с приобретенной устойчивостью, а именно с β-гемолитическими стафилококками, гонококками, Moraxella catarrhalis, гемофильной палочкой. Таким образом, в результате сочетания пенициллинов с ингибиторами β–лактамаз восстанавливается природная активность пенициллинов против данных микроорганизмов.
Аминопенициллины относятся к группе пенициллинов с расширенным спектром активности и включают в себя ампициллин и амоксициллин. Аминопенициллины, а также их ингибиторозащищенные производные являются препаратами выбора для лечения бактериальной инфекции ЛОР-органов (острого риносинусита, острого тонзиллофарингита), а также обострений хронических инфекций (хронического трахеобронхита, ларингита, обострений хронического риносинусита, среднего отита). Препараты данной группы назначаются при легких и неосложненных инфекциях, ингибиторозащищенные производные – при тяжелых формах инфекции, а также при высокой распространенности β-лактамазопродуцирующих микроорганизмов.
К сожалению, микроорганизмы постепенно приобретают способность преодолевать защиту, заложенную в структуру антимикробного препарата при его создании. Причем это достигается не только путем формирования новых механизмов устойчивости, но и за счет продукции новых типов β-лактамаз. Этот процесс прогрессирует: если в 1900 г. было описано 14 типов β-лактамаз, то сейчас их число превосходит 300. Ярким примером последствия такой агрессии является практически полная беззащитность цефалоспоринов III поколения перед мутантами β-лактамаз широкого спектра грамотрицательных бактерий. С этой точки зрения, более предсказуемым представляется защитное действие ингибиторов β-лактамаз, удлиняющих «клиническую жизнь» целого ряда полезных, но исходно незащищенных антибиотиков.
Интересно, что ингибиторы β-лактамаз потенцируют действие пенициллинов не только за счет блокады энзимов, но и за счет антиинокуляционного эффекта, усиления бактерицидных свойств полиморфноядерных нейтрофилов, а также своеобразного «пост-β-лактамазотормозного» эффекта. Последний отличается от известного постантибиотического действия антибиотиков и сохраняется в отношении некоторых микроорганизмов, например Haemophilus Influenzae, до 5 ч и более [1, 2, 15, 17].
Тем не менее аминозащищенные пенициллины успешно применяются в ЛОР-практике и являются препаратами первой линии при лечении инфекции ВДП. Для оптимизации фармакотерапии необходимы не только точный выбор препарата, но и правильные его применение, доза, способ введения, что во многом определяет комплаентность пациента.
Хорошо себя зарекомендовал в лечении синуситов антибиотик из группы пенициллинов – Флемоклав Солютаб в форме диспергируемых таблеток, который относится к числу новых лекарственных форм антибактериальных препаратов. Достоинствами данной формы являются благоприятные фармакокинетические свойства, что подразумевает высокую биодоступность, а также равномерное нарастание концентрации действующего вещества в крови. Следует подчеркнуть, что данная форма в наименьшей степени вызывает диспепсические явления из-за высокой степени абсорбции и ограниченного влияния на микрофлору кишечника. А возможность применения формы в виде раствора позволяет использовать его у детей, в т. ч. новорожденных, пациентов с затруднением глотания.
В России зарегистрировано несколько антибиотиков, выпускаемых в форме диспергируемых таблеток Солютаб: амоксициллин (Флемоксин Солютаб), амоксициллин/клавуланат (Флемоклав Солютаб), доксициклина моногидрат (Юнидокс Солютаб), джозамицин (Вильпрофен Солютаб, цефиксим (Супракс Солютаб). Амоксициллин в форме диспергируемых таблеток Солютаб обладает большей биодоступностью, достигая концентрации в крови, близкой к концентрации при применении парентеральных форм. Вследствие низких остаточных концентраций в кишечнике гораздо реже возникают такие неприятные побочные эффекты, как диспепсия, диарея, которые достаточно часто встречаются при применении пенициллинов. Форма диспергируемых таблеток амоксициллина/клавуланата обладает всеми вышеперечисленными достоинствами, а также создает стабильные плазменные концентрации клавулановой кислоты, что обеспечивает прогнозируемое терапевтическое действие, снижает риск нежелательных лекарственных реакций [15, 17].
Что касается лечебных протоколов, то при легком течении синусита может назначаться амоксициллин внутрь по 0, 5–1 г 3 р./сут; при среднетяжелом либо при обострении хронического синусита в качестве стартовой антибиотикотерапии следует назначать Флемоклав Солютаб (амоксициллин/клавуланат) внутрь по 0, 625 г 3 р./сут или 1,0 г 2 р./сут, т. к. этот антибиотик активен в случае пенициллинрезистентных пневмококков и продуцирующих β-лактамазы штаммов гемофильной палочки. Хорошо зарекомендовал себя препарат цефалоспоринового ряда цефиксим (в дозе 400 мг 1 р./сут).
По данным ряда авторов, в большинстве случаев амоксициллин является адекватным средством терапии риносинусита, но при неэффективности ранее проводимой терапии, патологии фронтального, сфеноидального синуса, а также у детей требуется применение ингибиторозащищенных пенициллинов [18, 21, 23].
Помимо амоксицилина и цефалоспорина в лечении ОБРС могут быть использованы современные макролиды, такие как джозамицин (внутрь 1,0 г 2 р./сут), азитромицин (внутрь по 500 мг 1 р./сут, 3 дня), кларитромицин (внутрь 0,25–0,5 г 2 р./сут или 0,5 г 1 р./сут), рокситромицин (внутрь по 0,15 г 2 р./сут или 0,3 г 1 р./сут, 10–12 дней). По клинической эффективности макролиды мало уступают антибиотикам первого ряда. Джозамицин – это 16-членный макролид, который характеризуется активностью в отношении штаммов грамположительных микроорганизмов, устойчивых к 14- и 15-членным макролидам (азитромицину, кларитромицину, эритромицину, рокситромицину). Макролиды могут быть препаратами выбора либо при непереносимости аминопенициллинов и цефалоспоринов, либо при наличии данных о хроническом течении процесса в ОНП (полипозно-гнойном и др.). В этом случае назначение на первом этапе рационально вследствие особенностей микрофлоры при хроническим процессе, а также благоприятном влиянии макролидов на полипозную ткань [ 8, 10, 11, 15, 18, 21].
В случае неэффективности первого курса антибиотикотерапии в настоящее время применяются фторхинолоны: левофлоксацин (0,5 г 1 р./сут 5–10 дней), моксифлоксацин (0, 4 г 1 р./сут, 5–10 дней), спарфлоксацин (0,4 г 1 р./сут 5–10 дней). Именно на «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин) в последнее время возлагаются большие надежды в лечении синуситов, вызванных пенициллиноустойчивыми пневмококками. Активность этих препаратов распространяется и на пенициллиноустойчивые штаммы Streptococcus pneumoniae, β-лактамазопродуцирующие штаммы Haemophilus influenzae, Moraxella catarrhalis, а также на атипичные и анаэробные микроорганизмы.
Критерием рациональности назначенной антибиотикотерапии является оценка состояния больного через 72 ч после начала лечения. Положительная динамика состояния пациента предполагает продолжение стартовой антибиотикотерапии. При отсутствии такой динамики через 72 ч следует сменить антибиотик. В лечении синуситов в большинстве случаев приоритет остается за монотерапией. Назначение 2-х и более антибиотиков оправданно при тяжелом течении синусита или наличии либо формировании осложнений [5, 14].
Продолжительность лечения зависит от выбранного препарата и степени тяжести синусита. Курс лечения может составлять от 7 до 14 дней. Важно полностью купировать воспалительный процесс в ОНП, поэтому, имея целью полную эрадикацию возбудителя, следует ориентироваться на срок лечения в 7–10 дней. Значительную роль в патогенезе ОБРС играют отек слизистой оболочки полости носа и обструкция соустий естественных отверстий ОНП, поэтому большое значение имеют сосудосуживающие препараты: ксилометазолин, оксиметазолин, фенилэфрин и др. Топические глюкокортикостероиды сравнительно недавно вошли в арсенал лекарственных средств для лечения ОРС. Их применение способствует уменьшению секреции желез слизистой оболочки и тканевого отека и, как следствие, улучшению носового дыхания (мометазона фуроат спрей для носа по100 мкг 2 р./сут) [7, 12].
В заключение отметим, что любой протокол лечения может меняться по мере накопления знаний о терапии синуситов, а тактика – пересматриваться и дополняться. Спектр применяемых в лечении синуситов антибактериальных препаратов представлен весьма широко, и поэтому сложно однозначно сказать, когда оправданно применение аминопенициллинов, а когда следует выбрать их ингибиторозащищeнные формы, цефалоспорины или фторхинолоны. Ингибиторозащищeнные формы пенициллинов удачно зарекомендовали себя при лечении ОБРС, а форма диспергируемых таблеток Солютаб наряду с высокой эффективностью характеризуется хорошей переносимостью пациентами. Данный антибактериальный препарат (Флемоклав Солютаб) может быть рекомендован для лечения ОБРС в качестве препарата первого ряда.
Только для зарегистрированных пользователей