Нескучный урок физики в 7-м классе по теме: «Диффузия»
Разделы: Физика
Тип урока: комбинированный.
Ход урока.
1. Оргмомент
2. Повторение
(На столе листы с текстом физического диктанта (1-2 вариант). Школьники записывают под соответствующим номером «да», если они считают это утверждение верным, или «нет», если считают его неверным)
3. Основной материал.
Урок начинаю с распыления освежителя; в случае, если ученик почувствовал запах, он должен встать. Таким образом, постепенно, через пару минут, встанут все учащиеся класса. Они безошибочно определят, что за освежитель был распылен.
У меня на столе в высокий стакан налиты две жидкости: снизу голубой раствор медного купороса, сверху – вода; между ними резкая граница. Если купорос и вода способны самопроизвольно смешаться, то граница между ними должна исчезнуть. Предлагаю ученикам следить за этой границей между жидкостями.
В это время демонстрирую диффузию газов на следующем опыте: к внутренним стенкам высокого цилиндрического сосуда прикрепляю смоченные фенолфталеином полоски белой бумаги. Цилиндр закрываю сверху картоном с прикрепленным к нему кусочком ваты, смоченной нашатырным спиртом. Газ аммиак диффундирует вниз. Если аммиак и воздух перемешиваются, то рано или поздно полоски бумаги окрасятся в ярко-малиновый цвет.
Предлагаю также следить за их цветом.
Хорошо очищенные и плотно прижатые друг к другу пластины из золота и свинца диффундируют на глубину 1мм за 5 лет.
Демонстрация диффузии кристаллов йода на стекле под слоем парафина.
(парафин около кристалликов йода окрасился в коричневый цвет)
Учитель: Итак, что же произошло за это время в первых двух экспериментах?
Учащиеся: Граница между жидкостями не изменилась, а листочки окрасились, т.е. аммиак и воздух перемешались в сосуде.
Учитель: Однако смотрите, что получилось в стакане, куда аккуратно налили купорос и воду неделю назад.
Учащиеся: Граница размыта, купорос и вода перемешались.
Учитель: Сформулируйте ответ, вытекающий из наблюдений и опытов.
Учащиеся: Если привести в соприкосновение твердые тела, жидкости или газы из разных веществ, то они сами собой смешиваются.
Учитель: Мы познакомились с новым явлением, в физике оно известно под названием ДИФФУЗИЯ.
(Работа с учебником, запись определения в тетрадь.)
Явление, при котором происходит самопроизвольное взаимное проникновение молекул одного вещества между молекулами другого, называют диффузией
(В итоге, в тетради обучающихся и на доске создается опорный конспект. Смотри приложение №1.)
(Достаточно эффектно видно, как проникают крупинки пшена в промежутки между горошинами)
После проведенного эксперимента и беседы с учащимися подчеркиваю, что явление диффузии происходит без вмешательства извне, за счет движения самих молекул, т.е. может быть объяснено только тем, что молекулы беспрерывно и беспорядочно движутся и сталкиваются.
Учитель: Как будет вести себя маленькая частичка нерастворимого вещества в жидкости, если окружающие ее молекулы жидкости непрерывно и беспорядочно движутся?
Учащиеся: Молекулы, окружающие частицу, движутся в разных направлениях, часть из них ударяются о частицу. Поскольку частица маленькая, она может двигаться под действием этих ударов. Т.к. молекулы движутся беспорядочно, то число ударов с разных сторон в один и тот же момент различно, и частица будет двигаться то в одну, то в другую сторону, беспорядочно.
(демонстрация с помощью прибора «Модель броуновского движения»)
Явление беспорядочного движения взвешенных нерастворимых частиц вещества в жидкости или газе называют броуновским движением.
Откуда такое название, вы узнаете дома из учебника. Пронаблюдать броуновское движение можно под микроскопом, на перемене это каждый сможет сделать.
Различие в скорости протекания диффузии твердых тел, жидкостей и газов объясняют ученики.
4. Закрепление.
5. Итоги урока
Чем отличаются молекулы воды и молекулы льда?
Понятие молекулы ( и производные от него представления о молекулярном строении вещества, структуры собственно молекулы) позволяет понимать свойства веществ создающих мир. Современные, как и ранние, физико-химические исследования опираются и базируются на грандиозном открытие об атомно-молекулярном строении вещества. Молекула – единая «деталь» всех веществ, существование которой предположил ещё Демокрит. Потому именно её структура и взаимосвязь с другими молекулами (образуя определенное строение и состав) и определяет/объясняет все различия между веществами, их видом и свойствами.
Сама молекула, будучи не самой мельчайшей составной частью вещества (коей является атом) имеет определенную структуру, свойства. Определяется структура молекулы числом вхожих в неё определенных атомов и характером связи (ковалентной) между ними. Состав этот неизменен, даже если вещество преобразуется в другое состояние(как примеру, происходит с водой – об этом пойдет речь дальше).
Характеристики воды, её состояния
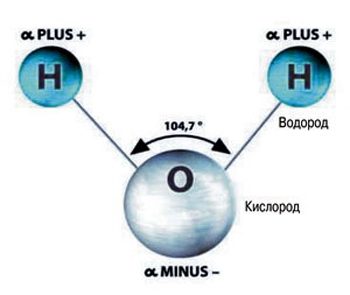
Состав такого вещества, как вода (равно как и её химическая формула) знаком каждому. Каждую её молекулу составляют три атома: атом кислорода, обозначающийся буквой «О», и атомы водорода – латинская «Н», в количестве 2-х. Форма молекулы воды не симметрична (схожа с равнобедренным треугольником).
Вода, как вещество, составляющие её молекулы, реагирует на внешнюю «обстановку», показатели окружающей среды — температуру, давление. Зависимо от последних вода способна изменять состояние, которых три:
Помимо данных различий, естественно, разнятся и способы «перехода» вещества из одного состояния (жидкого) в другие. Эти переходы и трансформируют вещество, и провоцируют передачу энергии (выделение/поглощение). Среди них есть процессы прямые – преобразование жидкой воды в пар (испарение), в лед (замерзание) и обратные – в жидкость из пара (конденсация), из льда (таяние). Также и состояния воды — парообразное и лед — могут трансформироваться друг в друга: возгонка – лед в пар, сублимация – обратный процесс.
Специфичность льда как состояния воды
Широко известно, что лед замерзает ( трансформируется из воды) при пересечении температурой в сторону уменьшения границы в ноль градусов. Хотя, в этом всем понятном явлении, есть свои нюансы. К примеру, состояние льда неоднозначно, различны его виды, модификации. Отличаются они первоочередно условиями, при которых возникают – температурой, давлением. Таких модификаций насчитывается аж пятнадцать.
Лед в разных своих видах имеет различное молекулярное строение (молекулы же неотличимы от молекул воды). Природный и естественный лед, в научной терминологии обозначающийся как лед Ih — вещество с кристаллической структурой. То есть, каждая молекула с четырьмя окружающими её «соседками» (расстояние между всеми равное) создают геометрическую фигуру тетраэдр. Другие фазы льда обладают более сложной структурой, к примеру высокоупорядоченная структура тригонального, кубического или моноклинного льда.
Основные отличия льда от воды на молекулярном уровне
Первое и напрямую не относящееся к молекулярному строению воды и льда различие между ними – показатель плотности вещества. Кристаллическая структура, присущая льду, образовываясь, способствует одновременному уменьшению плотности (с показателя почти в 1000 кг/м³ до 916,7 кг/м³). А это стимулирует увеличение объема на 10%. 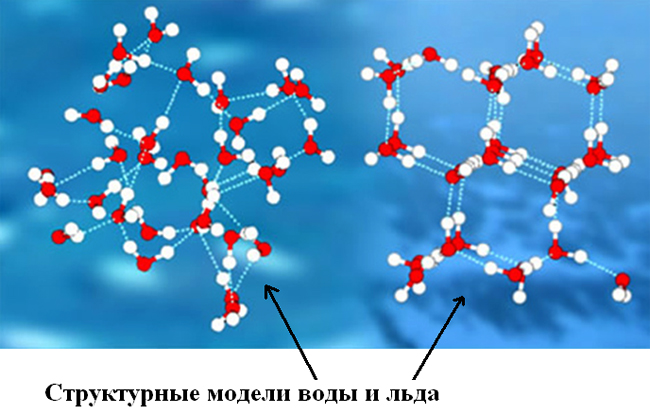
Основное же отличие в молекулярном строении этих агрегатных состояний воды (жидкого и твердого) в количестве, виде и силе водородных связей между молекулами. Во льду же (твердом состоянии) ими объединены пять молекул, а собственно связи водородные прочнее.
Отличает вещество воды в разных её состояниях (агрегатных) не только структура расположения молекул (молекулярное строение), но и движение их, сила взаимосвязи/притяжения между ними. Молекулы воды в жидком состоянии достаточно слабо притягиваются, обеспечивая текучесть воды. В твердом же льду наиболее сильно притяжение молекул, потому и мала их двигательная активность (она обеспечивает постоянство формы льда).
Урок №7 «Движение молекул»
Выбранный для просмотра документ Ур.№7 Движение молекул.docx
Образовательная : раскрыть важнейшее положение молекулярно-кинетической теории: молекулы вещества находятся в непрерывном движении ;
Развивающая : развитие познавательных интересов к предмету, внимания, мышления, памяти, расширять кругозор;
Воспитательная : воспитание аккуратности, дисциплинированности.
Мультимедийное оборудование, презентации «Движение молекул», «Диффузия», учебник.
Тип урока: Комбинированный
Сообщение темы и целей урока;
Знакомство с новым материалом;
Домашнее задание пояснения к нему.
Организационный момент. Приветствие учащихся. Проверка готовности к уроку.
Проверка домашней работы (слайд 2)
Измерение диаметра волоса, толщины учебника.
(слайд 3) Какой ученый первым утверждал, что в природе есть неделимая наименьшая частица, которую он назвал атомом? (Демокрит)
(слайд 4) Какой из приведённых ниже опытов подтверждает гипотезу о том, что вещества состоят из отдельных частиц, между которыми есть промежутки?
а) растворение сахара в воде б) притяжение булавок к магниту
в) падение тел на землю г) расширение тела при нагревании
(слайд 5) Одинаковы ли молекулы воды, налитой в стакан; капельки росы; водяного пара, образовавшегося над кипящей в кастрюле водой; кусочка пищевого льда? (молекулы всех указанных веществ одинаковы)
(слайд 6) Как объяснить расширение тел при их нагревании? (увеличиваются промежутки между молекулами)
(слайд 7) Как называется способ измерения размеров малых лет? (способ рядов)
Вещество состоит из мельчайших частиц, едва различимых невооруженным глазом. (Нет)
Объем газа при нагревании увеличивается, т. к. каждая молекула становится больше по размеру. ( Нет )
Пленка масла, растекаясь по поверхности воды, может занять любую площадь. ( Нет )
Молекулы воды точно такие же, как и молекулы льда. ( Да )
Атомы состоят из молекул. ( Нет )
Объем тела при нагревании уменьшается. ( Нет )
Объем жидкости при охлаждении уменьшается, т. к. промежутки между молекулами становятся меньше. ( Да )
Молекулы водяного пара отличаются от молекул воды. ( Нет )
При сжатии газа уменьшается размер молекул. ( Нет )
Газом из двухлитрового сосуда можно заполнить четырехлитровый сосуд. ( Да )
Самопроверка (слайд 11)
(слайд 12) В чем заключается первое положение о строении вещества? ( Все вещества состоят из мельчайших частиц – молекул и атомов, между которыми есть промежутки)
(слайд 13) Сегодня мы поговорим о том, как ведут себя молекулы. Представим ситуации. Капнем каплю пахучего вещества на стол. Например, одеколона. Что мы через некоторое время почувствуем? (Запах одеколона)
(слайд 14) О чем говорит факт распространения запаха веществ, если учесть, что все вещества состоят из молекул? (Молекулы могут двигаться)
Сообщение темы и целей урока.
На основании всего вышесказанного назовите тему урока: (Движение молекул) (слайд 15)
(слайд 16) Назовите цели урока:
Узнать: Что такое диффузия?
Понять: Как происходит диффузия.
Выяснить: Как скорость диффузии зависит от температуры.
Знакомство с новым материалом.
Движение молекул нельзя обнаружить ни в лупу, ни в микроскоп. Двигаясь в воздухе, молекулы духов сталкиваются с молекулами газов, которые входят в состав воздуха. При этом они постоянно меняют направление движения и, беспорядочно перемещаясь, разлетаются по комнате. Поэтому, двигаясь очень быстро, молекулы духов доносят запах до разных концов комнаты довольно медленно .
Растворение марганцовки в воде (демонстрация).
Проделаем опыт, который подтверждает гипотезу о непрерывном движении молекул. В сосуд с водой бросим несколько кристалликов марганцовки. Они опустятся на дно сосуда, и вокруг них образуется небольшое облачко окрашенной воды. Оставим сосуд в покое на некоторое время. Будем наблюдать, как постепенно происходит окрашивание воды в сосуде.
Опыт с воздухом и парами брома.
Аналогичное явление можно наблюдать на другом опыте. Если удалить разделяющую перегородку между сосудами, в нижнем из которых находятся пары брома, а в верхнем – воздух, то спустя определенное время они полностью перемешаются между собой.
Наблюдаемое явление объясняется тем, что молекулы воздуха и брома, расположенные возле границы разделов газов меняются местами. Далее, двигаясь непрерывно и беспорядочно, молекулы газов распространяются по всему объему. Газ в сосуде становится однородным.
Явление, при котором происходит взаимное проникновение молекул одного вещества между молекулами другого, называется диффузией (стр. 28)
Диффузия золота и свинца.
Итак, причиной диффузии является непрерывное и беспорядочное движение частиц вещества. Так как все молекулы движутся, то диффузия может происходить и в газах, и в жидкостях, и в твердых телах. Диффузию в газах и жидкостях мы с вами рассмотрели. О диффузии в твердых телах прочитайте в учебнике на стр. 28
Зависимость скорости диффузии от температуры вещества (демонстрация).
Проведем еще один опыт. Нальем в один стакан холодную воду, а в другой – теплую и опустим сахар (рафинад) в каждый стакан.
Что мы наблюдаем? (в стакане с горячей водой сахар растаял, а в холодной – нет)
Какой вывод можно сделать? (процесс диффузии ускоряется с повышением температуры).
А почему диффузия ускоряется? (потому что с повышением температуры увеличивается скорость движения молекул)
Итак, явление диффузии протекает по-разному при разной температуре: чем выше температура вещества, тем быстрее происходит диффузия.
Презентация «Движение молекул» (слайд 17, 18)
В каких веществах диффузия протекает быстрее всего? (в газах)
В каком стакане вода быстрее окрасится в цвет краски? (где выше температура)
Явление диффузии экспериментально доказывает, что молекулы … (движутся)
Что мешает молекулам духов мгновенно распространяться по комнате? (столкновение с молекулами воздуха)
Домашнее задание и пояснение к нему. § 9, 10, задание 1, 2 стр. 29, ответить на вопросы после параграфов.
Выбранный для просмотра документ Ур.№7 Движение молекул.pptx
Структура и свойства воды и льда
Карельский Государственный Педагогический университет
Структура и свойства воды и льда
Вступление
Пожалуй, на Земле нет более распространенного и в то же время более загадочного вещества, чем вода в жидкой и твердой фазах. Действительно, достаточно
вспомнить, что все живое вышло из воды и состоит из нее более чем на 50%, что 71% поверхности Земли покрыт водой и льдом, а значительная часть северных территорий суши представляет собой вечную мерзлоту.
Несмотря на многовековую историю изучения, простейший химический состав и исключительную важность для жизни на Земле, природа воды и льда таит в себе много
загадок из-за сложной динамической протонной и молекулярной структуры.
Основы современного понимания физикохимии воды заложили около 200 лет назад Генри Кавендиш и Антуан Лавуазье, обнаружившие, что вода – это не простой химический элемент, как считали средневековые алхимики, а соединение кислорода и водорода в определенном отношении. Собственно и название свое водород (hydrogene) – рождающий воду – получил только после этого открытия, и вода приобрела современное химическое обозначение H2O.
Водородная связь (Н-связь) – особый тип взаимодействия между реакционно-способными группами, при этом одна из групп содержит атом водорода, склонный к такому взаимодействию. В отличие от обычных химических связей, Н-связь появляется не в результате целенаправленного синтеза, а возникает в подходящих условиях сама и проявляется в виде межмолекулярных или внутримолекулярных взаимодействий.
Само понятие и термин «водородная связь» ввели В. Латимер и Р. Родебуш в 1920, для того, чтобы объяснить высокие температуры кипения воды, спиртов и др. соединений. Они выявили закономерность. Из этой закономерности следовало, что вода должна кипеть на 200° С ниже, чем наблюдаемое истинное значение.
Молекула воды

Для объяснения природы воды необходимо принять во внимание электронную структуру ее молекул. Как известно, на верхней оболочке у атома кислорода находятся четыре электрона, а у водорода имеется всего лишь один электрон. В образовании каждой ковалентной связи O–H участвуют по одному электрону от атомов кислорода и водорода. Два оставшихся у кислорода электрона получили название неподеленной пары, так как в изолированной молекуле воды они остаются свободными, не участвуя в образовании связей внутри молекулы H2O. Но при сближении с другими молекулами именно эти неподеленные электроны и играют решающую роль в образовании молекулярной структуры воды.

 Лед
Лед
С точки зрения обычного человека, лед более или менее одинаков независимо от того, где он образовывается: в атмосфере в виде градинок, на краях крыш в виде сосулек или в водоемах в виде пластин. С точки зрения физики имеется множество разновидностей льда, отличающихся своей молекулярной и мезоскопической структурой. Во льду, существующем при нормальном давлении, каждая молекула H2O окружена четырьмя другими, то есть координационное число структуры равно четырем (так называемый лед Ih ) Фрагмент структуры льда Ih. Молекулы воды, соединяющие их стержни – водородные связи (вся структура состоит из шестичленных колец); Характерной особенностью структуры льда является то, что в ней молекулы упакованы рыхло.
Соответствующая кристаллическая решетка (а) – гексагональная – не является плотноупакованной, поэтому плотность обычного льда (≈0,9 г/см ) ниже плотности воды (≈1 г/см ). Фиксированные положения в структуре льда занимают только атомы кислорода. Два атома водорода могут занимать различные положения на четырех связях молекулы H2O с другими соседями. Ввиду гексагональности решетки кристаллики, растущие в свободном состоянии (например, снежинки), имеют шестигранную форму.

Гексагональная фаза далеко не единственная форма существования льда. Точное число других кристаллических фаз – полиморфных форм льда – до сих пор неизвестно. Они образуются при высоких давлениях и низких температурах (рис. ). Одни исследователи считают точно установленным наличие 12 таких фаз, в то время как другие насчитывают их до 14. Количество различных фаз льда продолжают открывать и по сегодняшний день.
Римскими цифрами обозначены области существования стабильных фаз. Лед IV – метастабильная фаза, располагающаяся на диаграмме внутри области V.
Аномалии воды
Аномалия плотности


В последнее время много внимания уделяется изучению свойств переохлажденной воды, то есть остающейся в жидком состоянии ниже точки замерзания 0°С. (Переохладить воду можно либо в тонких капиллярах, либо – еще лучше – в виде эмульсии: маленьких капелек в неполярной среде – “масле”). Что же происходит с аномалией плотности при переохлаждении воды? Она ведет себя странно (см. рис.). С одной стороны, плотность воды сильно уменьшается по мере переохлаждения, но, с другой стороны, она приближается к плотности льда при понижении температуры (то есть вторая аномалия ослабевает). Чем ниже температура, тем ажурнее становится сетка, обусловливая уменьшение плотности при понижении температуры ниже 4°С.
 Аномалия сжимаемости
Аномалия сжимаемости

Аномалия теплоёмкости
Величина теплоемкости, как известно, показывает, сколько нужно затратить тепла, чтобы поднять температуру вещества на один градус. Для подавляющего числа веществ теплоемкость жидкости после плавления кристалла увеличивается незначительно – никак не более 10%. Другое дело – вода. При плавлении льда теплоемкость скачет от 9 до 18 кал/моль* град, то есть в два раза! Такого огромного скачка теплоемкости при 
Во льду энергия, подводимая для нагревания, тратится в основном на увеличение тепловой скорости молекул. Скачок теплоемкости после плавления означает, что чтобы деформировать сетку при изменении температуры, перестроить ее структуру, нужно затратить энергию; это и объясняет аномальный вклад в теплоемкость. Как видно на рис. сетка водородных связей в воде существует на всем интервале существования жидкости: с ростом температуры водородные связи не разрываются, а постепенно изменяют свою конфигурацию.
В переохлажденной воде рост теплоемкости также связан с изменением конфигурации водородных связей.
Свойства льда
Текучесть льда

Влияние скорости деформации на механические свойства монокристаллического льда хорошо иллюстрирует след. рис. Видно, что при увеличении скорости деформирования механические напряжения σ, необходимые для пластического течения, быстро нарастают и на зависимости относительной деформации Е от σ появляется гигантский зуб текучести.

Электрические свойства льда
Не менее замечательны и электрические свойства льда. Величина проводимости и ее экспоненциально быстрое возрастание с повышением температуры резко отличают лед от металлических проводников и ставят его в один ряд с полупроводниками. Обычно лед бывает очень чист химически, даже если растет из грязной воды или раствора (вспомните чистые прозрачные льдинки в грязной луже). Это обусловлено низкой растворимостью примесей в структуре льда. В результате при замерзании примеси оттесняются на фронте кристаллизации в жидкость и не входят в структуру льда. Поэтому рассчитывать на большую примесную проводимость во льду не приходится. Но в нем нет и свободных электронов, как в металлах. Лишь в 50-е годы XX века было установлено, что носителями заряда во льду являются неупорядоченные протоны, то есть лед является протонным полупроводником.

 Дефекты
Дефекты
а – пара ионных дефектов H3O+ и OH-; б – пара ориентационных дефектов Бьеррума
Рост кристаллов льда

Память воды
защитил диссертацию, посвященную памяти воды. До сих пор считалось, что вода не может образовывать долгоживущих структур. Однако его расчеты показали, что вода представляет собой иерархию правильных объемных структур, в основе которых лежит кристаллоподобный «квант воды», состоящий из 57 ее молекул. Эта структура энергетически выгодна и разрушается с освобождением свободных молекул воды лишь при высоких концентрациях спиртов и подобных им растворителей. «Кванты воды» могут взаимодействовать друг с другом за счет свободных водородных связей, что приводит к появлению структур второго порядка в виде шестигранников. Они состоят из 912 молекул воды, которые практически не способны к взаимодействию за счет образования водородных связей.

Кристаллы воды после «прослушивания» музыкальных произведений.
«Пасторали» Бетховена «Прощальной Песни» Шопена тяжелого металлического рока
Вывод
Вода, лед и их взаимные фазовые превращения еще таят в себе множество загадок. Их разгадывание представляет собой не только очень интересную физическую проблему, но и чрезвычайно важно для жизни на Земле, так как имеет прямое отношение к здоровью и благополучию человека. Возможно, они дают один из самых ярких примеров роли электронной и молекулярной структуры в формировании физических свойств при простейшем и хорошо известном химическом составе вещества.
Литература:
ВОДА И ЛЕД – ЗНАЕМ ЛИ МЫ О НИХ ДОСТАТОЧНО?
//Соросовский образовательный журнал, том 6, №9 2000 с.66-72
ЗАГАДКИ ВОДЫ. // Соросовский образовательный журнал, №5 1996, с. 41-48



 Лед
Лед Аномалия сжимаемости
Аномалия сжимаемости
 Дефекты
Дефекты

