Что происходит с организмом при избытке мочевой ксилоты
Наверное, вы много раз слышали о гиперурикемии — избыток мочевой кислоты в крови. Но знаете ли вы, о чем конкретно идет речь? Почему возникает такое состояние? И как это угрожает здоровью?
Повышенный уровень мочевой кислоты: причины, симптомы и лечение
Мочевая кислота — это вещество, которое наше тело производит в результате собственного метаболизма. Хотя ее небольшая часть образуется в процессе разложения пурина, типа белка, присутствующего в пище, которую мы потребляем. Чем больше белков мы получаем, тем больше мочевой кислоты вырабатывает организм. Обычно мочевая кислота не вызывает никаких проблем со здоровьем, если она функционально выводится почками. Проблема возникает, когда ее уровень повышается. То есть, когда организм вырабатывает слишком много МК или не выводит ее должным образом.
В таком случае, образуются твердые кристаллы, которые оседают на суставах, вызывая сильную боль.
Основные причины повышенного содержания МК:
Кроме этого, существует несколько факторов риска, которые повышают вероятность заболевания:
Высокое содержание МК может и не вызвать симптомов. Хотя одним из основных последствий этой проблемы является появление подагры, из-за накопления кристаллов кислоты они откладываются в суставах.
Другие симптомы:
Лечение направлено на доведение мочевой кислоты до нормального уровня. Оно основано на диете: минимизации или исключении продуктов с высоким содержанием пурина и потреблении большого количества воды с низким содержанием минералов. Чтобы облегчить боль, вызванную воспалением суставов, можно принимать ибупрофен или противовоспалительные средства, не содержащие стероидов. Врачи часто назначают препараты, которые блокируют всасывание уратов.
Что касается профилактики подагры, то тут применяются ингибиторы ксантиноксидазы. Хотя их не рекомендуется использовать только при возникновении боли в суставах, поскольку состояние может ухудшиться. Очень важно соблюдать диету, чтобы снизить уровень МК.
Вот некоторые из продуктов, на которые нужно обратить внимание:
• Артишок • Лук • Сельдерей • Тыква • Морковь • Хлопья • Яблоки • Клубника • Цитрусовые • Черника • Курица • Яйца • Вода с низкой минерализацией
А это продукты, которые под запретом:
Чтобы избежать повышения уровня МК, нужно следовать некоторым советам:
Эта статья несет информационный характер. Не занимайтесь самолечением и любые советы обсуждайте с врачом.
Мочевая кислота в крови
Другие названия: пурин-2,6,8-трион, продукт метаболизма пуриновых оснований, тригидроксипурин, 2,6,8-триоксипурин, гетероциклический уреид мочевины, Uric acid, UA
Код услуги для заказа 1059 (Мочевая кислота) в медицинской лаборатории Синэво.
Общая информация:
Мочевая кислота — продукт обмена пуринов, входящих в состав нуклеиновых кислот (РНК и ДНК). Пурины появляются в основном после естественной гибели клеток. Наряду с этим, мочевая кислота образовывается при переваривании продуктов (телятина, субпродукты, рыба) и жидкостей (чай, кофе, какао) с высоким содержание пуринов. Поэтому концентрация мочевой кислоты у здоровых людей может несколько увеличиваться при употреблении большого количества такой пищи.
70 % мочевой кислоты транспортируется кровью от печени к почкам, где фильтруется и выделяется с мочой, оставшиеся 30% удаляется через желудочно-кишечный тракт.
Повышенное содержание мочевой кислоты (гиперурикемия) лежит в основе развития ряда заболеваний. Так, при концентрации мочевой кислоты выше нормы образуются кристаллы (ураты), которые накапливаются и откладываются в различных органах. Постоянно повышенный уровень мочевой кислоты может привести к подагре – воспалению суставов. Кроме того, вследствие высокого уровня мочевой кислоты формируются камни в мочевыделительной системе.
Увеличение концентрации мочевой кислоты в крови может быть вызвано врождённой склонностью организма к чрезмерному производству мочевой кислоты или недостаточным её выведением в связи со сниженной функцией почек при их поражении. При массовой гибели клеток, например, при лечении опухолей, уровень мочевой кислоты также возрастает.
Анализ на уровень мочевой кислоты в крови чаще всего используется при диагностике подагры и мочекаменной болезни.
Важно! Повышенное содержание мочевой кислоты в крови не является полным основанием для постановки диагноза «подагра«.
Во время беременности увеличение содержания мочевой кислоты является тревожным знаком возможного развития преэклампсии и эклампсии.
Высокий уровень мочевой кислоты в крови не всегда соответствует выраженным симптомам, у 10 % взрослых гиперурикемия протекает бессимптомно. Людям с наследственной предрасположенностью к подагре, образованию камней или поражению почек следует проводить профилактику этих заболеваний, несмотря на отсутствие симптомов.
Некоторые исследования показывают, что чрезмерное количество мочевой кислоты повышает риск заболеваний сердца. Считается, что это играет роль в течении сахарного диабета, в ухудшении липидного обмена, повышении артериального давления и увеличивает вероятность инсульта и эклампсии. Но непосредственными следствиями гиперурикемии являются 2 состояния: подагра и мочекаменная болезнь.
Показания к назначению:
Метод: ферментативный колориметрический метод с уриказой
Анализатор: Cobas 6000
Единицы измерения: мкмоль/л
Материал для исследования: сыворотка венозной крови
Подготовка:
Интерпретация результатов:
Результат лабораторных исследований не является достаточным основанием для постановки диагноза диагнозом. Интерпретация результатов и постановка диагноза осуществляется только лечащим врачом.
Референтные значения:
Дети: Хейль В., Коберштейн Р., Цавта Б. «Референтные пределы у взрослых и детей» (Roche Diagnostics):
Ревматологическое обследование
Скидки для друзей из социальных сетей!
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
В этом месяце жителям районов Савеловский, Беговой, Аэропорт, Хорошевский» предоставляется скидка 5% на ВСЕ мед.
Гуляев Сергей Викторович
Врач-ревматолог, терапевт, нефролог
Кандидат медицинских наук
«Men’s Health», медицинский блог (август 2016г.)
Если ваши суставы опухают и болят по ночам, врач-ревматолог предложит вам проверить ревматологический профиль. Это обследование поможет поставить точный диагноз, проследить динамику заболевания и назначить правильное лечение.
При подозрении на ревматическую болезнь используют следующие исследования:
Анализ крови на уровень мочевой кислоты
Мочевая кислота – это окончательный продукт распада пуринов. Ежедневно человек получает пурины вместе с продуктами питания, преимущественно с мясными продуктами. Затем с помощью определенных ферментов, пурины перерабатываются с образованием мочевой кислоты.
В нормальных физиологических количествах мочевая кислота нужна организму, она связывает свободные радикалы и защищает здоровые клетки от окисления. Кроме того, она так же, как и кофеин, стимулирует клетки головного мозга. Однако повышенное содержание мочевой кислоты имеет вредные последствия, в частности может приводить к подагре и некоторым другим заболеваниям.
Исследование уровня мочевой кислоты дает возможность диагностировать нарушение обмена мочевой кислоты и связанные с этим заболевания.
Когда нужно провести обследование:
Уровень мочевой кислоты
Уровень мочевой кислоты определяют в крови и в моче.
Мочевая кислота в крови называется урекемия, в моче – урикозурия. Повышенное содержание мочевой кислоты – гиперурикемия, пониженный уровень мочевой кислоты – гипоурикемия. Патологическое значение имеет только гиперурикемия и гиперурикозурия.
Концентрация мочевой кислоты в крови зависит от следующих факторов:
В обычном состоянии наш организм поддерживает уровень мочевой кислоты в норме. Увеличение ее концентрации так или иначе связано с обменными нарушениями.
Нормы содержания мочевой кислоты в крови
У мужчин и женщин может наблюдаться различная концентрация мочевой кислоты в крови. Норма может зависеть не только от пола, но и возраста человека:
Если превышение нормы происходит в течение длительного времени, то кристаллы соли мочевой кислоты (ураты) откладываются в суставах и тканях, вызывая различные болезни.
Гиперурикемия имеет свои признаки, но может протекать и бессимптомно.
Причины повышения содержания мочевой кислоты:
Как снизить концентрацию мочевой кислоты
Те, кто болен подагрой, знают, сколько неприятностей может доставить повышенная концентрация мочевой кислоты. Лечение этого недуга должно быть комплексным и обязательно включать прием препаратов, снижающих концентрацию мочевой кислоты в крови (ингибиторы ксантиноксидазы). Рекомендуется употребление большего количества жидкости и снижение потребления продуктов богатых пуринами.
Важно также постепенно избавиться от лишнего веса, поскольку ожирение обычно ассоциируется с повышением мочевой кислоты. Диета должна быть составлена так, чтобы количество продуктов, богатых пуринами было ограничено (красное мясо, печень, морепродукты, бобовые). Очень важно отказаться от алкоголя. Необходимо ограничить употребление винограда, томатов, репы, редьки, баклажанов, щавеля – они повышают уровень мочевой кислоты в крови. Зато арбуз, наоборот, выводит мочевую кислоту из организма. Полезно употреблять продукты, ощелачивающие мочу (лимон, щелочные минеральные воды).
Антинуклеарные антитела (АНА)
С помощью АНА теста можно определить наличие в крови антинуклеарных антител (антител к ядерным антигенам).
АНА – это группа специфических аутоантител, которые производит иммунная система нашего организма в случае аутоиммунных нарушений. Антитела оказывают повреждающее действие на клетки организма. При этом человек испытывает различные болезненные симптомы, например боль в мышцах и суставах, общую слабость и др.
Обнаружение в сыворотке крови антител принадлежащих к группе АНА (например, антител к двуспиральной ДНК) помогает выявить аутоимунное заболевание, контролировать течение болезни и эффективность его лечения.
Исследование крови на АЦЦП
Анализ крови на С-реактивный белок
Исследование крови на АЦЦП
Когда необходим анализ крови на антинуклеарные антитела
Выявление антинуклеарных антител может быть признаком следующих аутоиммунных заболеваний:
Как выполняется тест на антинуклеарные антитела
Кровь на антинуклеарные антитела берется из вены на локтевом сгибе, натощак. Перед исследованием можно не придерживаться никакой диеты.
В некоторых случаях, для того чтобы дифференцировать различные аутоиммунные заболевания, могут потребоваться дополнительные уточняющие тесты на аутоантитела из группы антинуклеарных антител, так называемый иммуноблот АНА.
Что обозначают данные теста
У здорового человека с нормальным иммунитетом антинуклеарных антител в крови быть не должно или их уровень не должен превышать установленные референсные значения.
Нормальное значение АНА подразумевает титр антител, не превышающий значение 1: 160. Ниже этого значения анализ считается отрицательным.
Положительный анализ на антинуклеарные антитела (1:320 и более) указывает на повышение антинуклеарных антител, и наличие у человека заболевания аутоиммунной природы.
В настоящее время для выявления антинуклеарных антитела используются две методики: непрямую реакцию иммунофлюоресценции с использованием так называемой клеточной линии Нер2 и иммуноферментный анализ. Оба теста дополняют друг друга, в связи с чем их рекомендуют выполнять одновременно.
Можно выделить следующие виды антинуклеарных тел АНА в реакции непрямой иммунофлюоресненции:
При положительном анализе на антинуклеарные антитела необходимо провести иммуноблот антинуклеарных антител для уточнения типа аутоиммунного заболевания и постановки диагноза.
Ревматоидный фактор
Исследование крови на ревматоидный фактор направлено на выявление специфических антител класса IgM к антителам класса IgG.
Лабораторный тест на ревматоидный фактор является скрининговым исследованием, направленным на выявление аутоиммунных нарушений. Главная задача исследования на ревматоидный фактор – выявление ревматоидного артрита, болезни и синдрома Шегрена и ряда других аутоиммунных болезней.
Анализ на ревматоидный фактор может потребоваться при следующих симптомах:
Мочевина повышена в крови: причины, что значит и о чем говорит
Если при анализе крови у пациента обнаруживается повышенный уровень мочевины (мочевой кислоты), диагностируют гиперурикемию. Это состояние может быть обусловлено физиологическими или патологическими факторами. Чтобы установить, какая причина спровоцировала рост мочевины, проводят комплексную диагностику. В случае необходимости, назначается медикаментозная терапия или разрабатываются мероприятия по коррекции образа жизни.
Что такое мочевина?
Мочевина представляет собой органическое соединение, содержащее в составе азот. Синтезируется в печеночной железе. Принадлежит к шлакам (азотистым метаболитам). Является продуктом обмена пуринов (азотсодержащих соединений), преимущественно поступающих в организм с пищей и требующихся клеткам для осуществления метаболизма.
Впервые мочевая кислота была обнаружена в составе урины и формирующихся в ней камней. Именно поэтому она получила такое название.
Умеренное количество мочевины приносит определенную пользу — способствует защите кровеносных сосудов, нормальной работе нервной системы, предупреждению неврологических и раковых заболеваний. Избытки этого вещества активно выводятся вместе с мочой.
Патологические причины гиперурикемии
Чаще всего повышенная концентрация мочевины у мужчин и женщин обусловлена нарушениями, возникающими со стороны почек. Такое явление развивается на фоне почечной азотемии, при которой мочевая кислота недостаточно выделяется с мочой. Также ее может спровоцировать сбой, происходящий в гемодинамике почек.
Высокий уровень мочевины выступает симптомом разнообразных инфекционных заболеваний — вирусной или бактериальной пневмонии, тяжелых форм гриппа, брюшного тифа, холеры, дизентерии, желтушного лептоспироза. Повышенная концентрация мочевой кислоты также наблюдается у пациентов со следующими патологиями:
Нарушению подвержены люди с различной степенью ожирения, включая начальную стадию, непроходимостью кишечника, обширными ожогами, синдромом Дауна. Гиперурикемия способна возникнуть в результате кровотечений в верхних отделах ЖКТ, спровоцированных язвенной болезнью желудка или 12-перстной кишки. Часто она наблюдается при отравлении свинцом (свинцовой нефропатии).
Физиологические факторы роста мочевины
Среди подобных факторов значатся:
Другие физиологические причины, приводящие к развитию гиперурикемии – существенное обезвоживание, соблюдение некоторых видов диет.
Если мочевая кислота возрастает на фоне перечисленных факторов, потребность в медикаментозном лечении часто отсутствует. Для нормализации такого показателя достаточно внести необходимые коррективы в повседневный уклад.
Если концентрация мочевины возрастает незначительно и обусловлена физиологическими явлениями, негативные симптомы могут отсутствовать. Иногда они проявляются незначительно и полностью исчезают после коррекции рациона, отказа от вредных привычек, отсутствии неумеренных нагрузок.
Значительное возрастание уровня мочевой кислоты провоцирует неприятную симптоматику, которая проявляется:
Возникновение подобных состояний требует обязательного обращения к специалисту для проведения тщательного медицинского обследования и назначения результативного лечебного курса.
Поставить пациенту определенный диагноз на основании одного только повышения мочевины невозможно. Чтобы выяснить причину, по которой возникла проблема, и разработать эффективные меры по ее устранению, требуется расширенная диагностика.
Обследование и лечение
Первым и основным специалистом, к которому стоит обратиться, является терапевт. Пациентам с высоким показателем мочевины в крови назначается комплексная диагностика. Обследование включает в себя осмотр суставов, изучение анамнеза, выявление имеющихся хронических патологий, уточнение разновидностей принимаемых препаратов.
Также предусмотрены другие процедуры:
При незначительном повышении уровня мочевины медикаменты чаще всего не назначаются. В подобных случаях показаны:
В остальных случаях пациентам могут потребоваться такие виды лекарственных препаратов как глюкокортикостероиды, НПВС, колхициновые алкалоиды, урикодепрессоры, ощелачивающие средства, селективные ингибиторы ксантиноксидазы.
Предупредить развитие гиперурикемии позволяют сбалансированный режим питания, снижение объема животной пищи, трезвый образ жизни, умеренные физические нагрузки. При наличии хронических заболеваний и почечных патологий следует регулярно проходить медицинские осмотры, сдавать все назначенные специалистами анализы.
Диагностика и лечение подагрического артрита
Подагра — хроническое прогрессирующее заболевание, связанное с нарушением пуринового обмена, которое характеризуется повышением мочевой кислоты в крови и отложением в тканях опорно-двигательного аппарата и внутренних органах натриевой соли мочевой кислот
Подагра — хроническое прогрессирующее заболевание, связанное с нарушением пуринового обмена, которое характеризуется повышением мочевой кислоты в крови и отложением в тканях опорно-двигательного аппарата и внутренних органах натриевой соли мочевой кислоты (уратов) с развитием рецидивирующего острого артрита и образованием подагрических узелков (тофусов).
Подагра относится к «старым» болезням и известна со времен глубокой древности. Термин «подагра» происходит от греческих слов pus, что означает стопа, и agra — захват. Таким образом, уже в названии заболевания подчеркивается одно из кардинальных проявлений подагрического артрита. Подагра рассматривается не только как недуг, при котором патологический процесс локализуется в опорно-двигательном аппарате, но и как системное заболевание, характеризующееся поражением жизненно важных органов, и прежде всего почек. Распространенность подагры в различных регионах варьирует в широких пределах и во многом связана с особенностями питания населения, составляя в среднем 0,1%. В США этот показатель равен 0,84% (возможно, эта цифра завышена).
Подагрой болеют преимущественно мужчины (отношение мужчины/женщины составляет 9:1). У мужчин и в норме наблюдается более высокий уровень мочевой кислоты. У женщин репродуктивного возраста повышенное содержание эстрогенов способствует увеличению почечного клиренса уратов. В постменопаузальном периоде уровень мочевой кислоты у них такой же, как и у мужчин соответствующего возраста. Поэтому, если пик заболеваемости у мужчин падает на возраст 35–50 лет, то у женщин — на 55–70 лет. Однако подагра может развиваться и в более молодом возрасте и отмечается даже у детей.
Как известно, мочевая кислота является конечным продуктом расщепления пуринов и выделяется из организма почками. У здоровых лиц за 24 ч выделяется с мочой 400–600 мг мочевой кислоты. Для понимания патогенеза подагры следует остановиться на клиренсе мочевой кислоты. Он характеризует объем крови, способный очиститься в почках от мочевой кислоты за 1 мин. В норме этот показатель равен 9 мл/мин. Источником образования мочевой кислоты в организме являются пуриновые соединения, которые поступают с пищей или образуются в организме в процессе обмена нуклеотидов. В плазме крови мочевая кислота находится в виде свободного урата натрия. В норме верхняя граница этого показателя для мужчин составляет 0,42 ммоль/л (7 мг%) и для женщин — 0,36 ммоль/л (6 мг%). Содержание мочевой кислоты выше этих цифр расценивается как гиперурикемия и рассматривается в качестве фактора высокого риска развития подагры. Так, по данным Фремингемского исследования, развитие подагрического артрита наблюдается у 17% мужчин и женщин с урикемией 7,0–7,9 мг%, у 25% — с 8–8,9 мг% и у 90% — при уровне мочевой кислоты выше 9,0 мг%.
При наличии стойкого повышения мочевой кислоты в сыворотке крови выше для данного индивидуума уровня она начинает откладываться в тканях в виде свободного урата натрия, который в мочевых путях переходит в мочевую кислоту.
Выделяются следующие клинические варианты подагры:
Гиперурикемия может длительное время протекать без каких-либо субъективных и объективных симптомов и лишь случайно диагностироваться при обследовании больного. Однако она не столь безобидна, как это может показаться на первый взгляд, и нередко ассоциируется с нарушениями жирового и углеводного обмена, а также, что еще более серьезно, приводит к уратной нефропатии. Следует отметить условность дефиниции «асимтоматическая подагра». Для ее выявления необходимо повторно исследовать уровень мочевой кислоты, особенно у «подагрической личности», т. е. у мужчин молодого возраста с пристрастием к алкоголю, ожирением и артериальной гипертонией. В некоторых случаях период асимптоматической (химической) гиперурикемии длится несколько лет и только после этого происходит клиническая презентация подагры. Следует иметь в виду, что гиперурикемии обычно предшествует гиперурикозурия. Поэтому у больных с мочекислым диатезом нужно повторно исследовать уровень мочевой кислоты не только в крови, но и в моче с целью своевременного выявления подагры.
Содержание мочевой кислоты в крови может повышаться под влиянием различных факторов, как внутренних, так и внешних. Эти факторы способствуют либо увеличению образования эндогенных пуринов, либо замедлению их выделения почками. С этих позиций выделяют два типа гиперурикемии — метаболический и почечный. Метаболический тип характеризуется повышением синтеза эндогенных пуринов при наличии высокой урикозурии и нормальном клиренсе мочевой кислоты. Напротив, при почечном типе наблюдается низкий клиренс мочевой кислоты и, следовательно, нарушение выделения мочевой кислоты почками. Представленные типы гиперурикемии имеют первостепенное значение в выборе противоподагрических модифицирующих болезнь препаратов, используемых в терапии этого заболевания.
Причины повышенного биосинтеза пуринов
Нозологические формы и клинические синдромы:
Лекарства, диета и хронические интоксикации:
Причины замедления выведения мочевой кислоты почками
Нозологические формы и клинические синдромы:
Лекарства и хронические интоксикации:
Выделяют также первичную и вторичную подагру. При первичной подагре какое-либо фоновое заболевание, предшествующее ее развитию, отсутствует. В основе такой подагры лежит семейно-генетическая аномалия пуринового обмена, детерминированная несколькими генами, или так называемый «конституциональный диспуризм». Исследования уратного гомеостаза показали аутосомно-доминантный тип наследования таких аномалий. В частности, это наблюдается при врожденных нарушениях в содержании энзимов, занимающих ключевое положение в метаболизме пуринов. Так, при снижении активности гипоксантин-гуанин-фосфорибозилтрансферазы происходит увеличение ресинтеза пуринов из нуклеотидов, что способствует развитию синдрома Леша-Найхана. Этот синдром встречается только у детей и у лиц молодого возраста и обычно заканчивается уратной нефропатией с летальным исходом. При высоком содержании фосфорибозилпирофосфата также наблюдается метаболический тип гиперурикемии, так как этот фермент участвует в синтезе предшественников мочевой кислоты. Что касается вторичной подагры, то она является одним из синдромов другого заболевания, «второй болезнью», развивающейся при многих патологических процессах и чаще всего при хронической почечной недостаточности.
Большое значение в распознавании подагры, особенно ее ранней стадии, имеет клиническая картина острого подагрического артрита. Она хорошо известна, однако частота диагностических ошибок в первый год заболевания достигает 90%, а через 5–7 лет правильный диагноз ставится только в половине случаев. Поздняя диагностика связана с недооценкой классических ранних признаков заболевания, а также с многообразием дебюта и течения подагры. Ее диагностика строится на особенностях клинической картины заболевания, повышенного содержания мочевой кислоты в крови и обнаружения кристаллов урата натрия в тканях. На практике широко применяются следующие так называемые Римские диагностические критерии подагры:
Диагноз подагры считается достоверным при наличии любых двух из четырех критериев.
Менее распространены диагностические критерии подагры, предложенные Американской коллегией ревматологов (АСК) в 1977 г., которые скорее характеризуют острый воспалительный артрит или его рецидивирующие атаки, нежели подагру в целом. Согласно этим критериям, достоверный диагноз ставится при наличии 6 из 12 признаков:
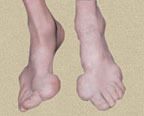
В первые 3–4 года подагра протекает по типу рецидивирующего острого воспалительного моноартрита с полным обратным развитием и восстановлением функции суставов, при этом межприступный период продолжается от нескольких месяцев до 1–2 лет. В дальнейшем этот период укорачивается, в процесс вовлекаются все новые и новые суставы и воспалительные явления локализуются не только в суставах стоп, но распространяются на суставы верхних конечностей, что обычно совпадает с образованием тофусов. Тофусы представляют собой депозиты кристаллов мочевой кислоты. Они появляются в среднем спустя 6 лет после первого приступа подагры, но иногда и через 2–3 года. Ураты чаще всего откладываются на поверхности суставного хряща, в синовиальной оболочке, синовиальных влагалищах, сухожилиях, а также в субкортикальной области эпифизов костей. Наиболее часто они располагаются на ушных раковинах и на задней поверхности локтевых суставов. Тофусы подразделяются на единичные и множественные, а также классифицируются в соответствии с их размерами, при этом к мелким относят тофусы до 1 см в диаметре, к средним — от 1 до 2,5 см и к крупным — более 2,5 см. Подагрические узлы с локализацией в опорно-двигательном аппарате являются основным элементом формирования хронического подагрического артрита. Тофусы могут располагаться в почках и других висцеральных органах.
Хроническое течение подагры не ограничивается только вовлеченностью суставов и формированием тофусов, но и характеризуется поражением внутренних органов. Подагрическая нефропатия является наиболее важным с прогностической точки зрения проявлением подагры и самой распространенной причиной летальных исходов при этом заболевании. Среди отдельных вариантов подагрической нефропатии выделяют острую мочекислую блокаду канальцев почек, мочекислый нефролитиаз, обусловленный отложением солей мочевой кислоты в чашечках и лоханках почек, хроническую уратную нефропатию и диффузный гломерулонефрит. Острая мочекислая блокада канальцев почек происходит, например, при распаде опухоли вследствие массивной медикаментозной или рентгенотерапии. Хроническая уратная нефропатия связана с отложением уратов в интерстиции почек, а развитие диффузного гломерулонефрита — с иммунными нарушениями у лиц с дисрегуляцией пуринового обмена. Такой гломерулонефрит по своей иммуноморфологии чаще всего является мезангиопролиферативным и при нем выявляют депозиты IgG и комплемента. Следует иметь в виду, что подагра часто ассоциируется с такими патологическими состояниями, как артериальная гипертония, ожирение, гиперлипидемия, жировая дистрофия печени, атеросклероз, нарушения мозгового кровообращения, алкогольная зависимость.
Течение подагры характеризуется разнообразием темпов развития болезни. Возможно относительно доброкачественное течение с редкими приступами, небольшой гиперурикемией и урикозурией и длительным сохранением функциональной недостаточности опорно-двигательного аппарата. В других случаях, напротив, с самого начала заболевания наблюдаются частые атаки острого артрита с сильными болями или непрерывные атаки с множественным поражением суставов на протяжении нескольких недель или месяцев (подагрический статус). Рефрактерное к проводимой терапии течение подагры приводит к быстрому развитию функциональной недостаточности суставов и почек.
В основе выделения вариантов течения подагры лежат: количество приступов артрита в течение года, число пораженных суставов, выраженность костно-хрящевой деструкции, наличие тофусов, патология почек и ее характер.
Варианты течения подагры
Легкое: приступы артрита 1–2 раза в год и захватывают не более 2 суставов, нет поражения почек и деструкции суставов, тофусы отсутствуют или они единичные и не превышают 1 см в диаметре.
Средней тяжести: 3–5 приступов в год, поражение 2–4 суставов, умеренно выраженная костно-суставная деструкция, множественные мелкие тофусы, поражение почек ограничено почечно-каменной болезнью.
Тяжелое: частота приступов более 5 в год, множественное поражение суставов, множественные тофусы крупных размеров, выраженная нефропатия.
Основными задачами терапии подагрического артрита являются:
Купирование острого подагрического артрита проводится противовоспалительными средствами. Для этих целей используются: колхицин — колхицин, колхикум-дисперт; нестероидные противовоспалительные препараты (НПВП) — вольтарен, дикловит, диклоран, целебрекс, мовалис); кортикостероиды — полькортолон, преднизолон, метилпреднизолон; или комбинация НПВП и кортикостероидов — амбене. Как колхицин, так и НПВП способствуют обратному развитию острого артрита в течение нескольких часов, в то время как у не прошедших лечение больных он может длиться несколько недель. До недавнего времени полагали, что лучшим препаратом для купирования приступа острого артрита при подагре является колхицин. Ярко выраженный и быстрый (в течение 48 ч) эффект колхицина рассматривался как один из диагностических признаков этого заболевания. Колхицин способен предупредить дальнейшее развитие острого приступа подагры при его назначении в первые 30–60 мин атаки. Его лечебное действие обусловлено угнетением фагоцитарной активности нейтрофилов. При остром приступе подагры мононатриевые соли уратов, фагоцитированные нейтрофилами, приводят вследствие мембранолитического их действия к гибели этих клеток и высвобождению лизосомальных ферментов, которые отвечают за развитие острого воспаления.
Из НПВП предпочтение отдают индометацину (индотард, метиндол) и диклофенаку (вольтарен, диклоран, диклофен). Эти препараты назначают в дозе 200–250 мг/сут, причем в первые часы приступа применяют большую часть суточной дозы. Проведенные контролированные исследования не выявили более высокой эффективности традиционных НПВП по сравнению с селективными ингибиторами ЦОГ-2 (нимесил, нимулид, целебрекс), например целекоксибами (коксиб, целебрекс). Однако окончательное суждение о сравнительной эффективности этих препаратов можно вынести только в ходе дальнейших исследований. Суточная доза колхицина составляет 4–6 мг/сут, причем 2/3 этой дозы больной принимает до 12 ч дня в первый день приступа. Обычно разовая доза составляет 0,6 мг и ее принимают каждый час до явного снижения подагрического воспаления. После значительного уменьшения воспаления дозу колхицина начинают снижать по 0,6 мг 2 раза в день, вплоть до полной отмены. Нередко у больных не удается наращивать суточную дозу до оптимальной из-за появления побочных реакций. Основными побочными эффектами колхицина являются тошнота, рвота, понос, возможны также геморрагический гастроэнтерит, лейкопения, нейропатия. При подагрическом статусе, характеризующемся непрерывными атаками острого артрита, рефрактерными к терапии НПВП, возможно внутривенное введение колхицина.
Противоподагрическая терапия (базисная, модифицирующая болезнь) направлена на профилактику рецидивов острого артрита, снижение содержания мочевой кислоты в крови, предупреждение дальнейшего формирования тофусов и их обратное развитие. Все противоподагрические препараты делятся на две большие группы: урикодепрессоры (урикостатики) и урикозурики. Урикодепрессоры тормозят синтез мочевой кислоты путем ингибирования фермента ксантиноксидазы, превращающего гипоксантин в ксантин, а ксантин в мочевую кислоту. Урикозурики повышают экскрецию мочевой кислоты, подавляя обратную реабсорбцию уратов почечными канальцами.
К препаратам первой группы относится аллопуринол (аллопуринол, аллопуринол-эгис, аллупол, пуринол, ремид, тиопуринол, милурит), который занимает лидирующее положение среди дру-гих противоподагрических средств. Показанием к применению аллопуринола являются метаболическая подагра, высокая гиперурикемия, частые острые атаки артрита, мочекислая болезнь, генетически обусловленный дефицит гипоксантин-гуанин-фосфорибозилтрансферазы. Применение аллопуринола возможно и у больных с подагрической нефропатией с начальными проявлениями хронической почечной недостаточности и небольшой азотемии. Начальная доза аллопуринола составляет 300 мг/сут. В случае неэффективности такой дозы ее увеличивают до 400–600 мг/сут, а при достижении клинического эффекта постепенно снижают. Поддерживающая доза определяется уровнем гиперурикемии и обычно составляет 100–300 мг/сут.
Аллопуринол способствует исчезновению атак острого артрита или их заметному ослаблению, обратному развитию тофусов и отчетливому их размягчению, снижению уровня мочевой кислоты до субнормальных цифр, нормализации показателей мочевого синдрома, урежению почечных колик и выделительной функции почек. У некоторых больных он поначалу вызывает повышение уровня мочевой кислоты и обострение подагрического артрита, поэтому на первом этапе терапии его комбинируют с противовоспалительными препаратами, в частности с низкими дозами колхицина или НПВП. По этой причине его не следует принимать при остром подагрическом артрите. При лечении аллопуринолом нередко развиваются побочные реакции, которые проявляются желудочно-кишечной токсичностью, аллергическими реакциями (кожная сыпь, эозинофилия), гепатотоксичностью с повышением сывороточных аминотрансфераз.
Урикозурические препараты, представляющие собой слабые органические кислоты, имеют меньшее значение в терапии подагры, чем урикостатики. Их не следует назначать при высоком содержании мочевой кислоты в крови, а также при нефропатии даже с начальными проявлениями почечной недостаточности. Из урикозурических препаратов сульфинпиразон и пробенецид особенно широко используются в США. Сульфинпиразон (сульфинпиразон, апо-сульфинпиразон, антуран) назначают по 200–400 мг/сут в два приема. Его, как и другие урикозурические средства, принимают с большим количеством жидкости, которую для профилактики нефролитиаза следует ощелачивать. Побочные реакции встречаются относительно часто и проявляются желудочной и кишечной диспепсией, лейкопенией, аллергическими реакциями. Противопоказанием к назначению сульфинпиразона является язвенная болезнь желудка и, конечно, подагрическая нефропатия.
Пробенецид (бенемид) является производным бензойной кислоты. Препарат назначается по 1,5–2,0 г/сут. Бензойная кислота содержится в клюкве, а также в ягодах и листьях брусники. Поэтому отвары и морсы из ягод и листьев этих растений показаны больным подагрой и в большей степени больным с подагрической нефропатией, тем более что помимо бензойной кислоты они содержат гиппуровую кислоту, обладающую урикосептическими свойствами. Урикозурическая активность присуща блокатору рецептора ангиотензина II и фенофибрату (грофибрат, нофибал). Наиболее эффективны производные бензбромарона, которые обладают не только урикозурическими свойствами, но и урикодепрессорными. Они используются в качестве монотерапии или в сочетании с аллопуринолом. Таким комбинированным препаратом является алломарон. Алломарон содержит 20 мг бензбромарона и 100 мг аллопуринола, его обычно принимают по 1 таблетке 2 раза в день.
Составной частью комплексной терапии подагры являются ощелачивающие препараты и ощелачивающие растворы, которые способны снизить риск развития нефропатии и, в частности, мочекаменной болезни. К этим препаратам относятся магурлит, блемарен и уралит. Их применение должно регулярно контролироваться показателем рН мочи. Помимо этих средств, можно принимать питьевую соду 2–4 г в день или щелочные минеральные воды.
При выраженных симптомах артрита необходимо также проводить местное лечение (долобене, финалгон, диклоран плюс, долгит крем, немулид гель, бишофит-гель).
Диете при подагре придают наибольшее значение по сравнению с другими ревматическими болезнями. Она предусматривает снижение общего калоража пищи, тем более что при подагре обычно наблюдается повышенная масса тела. Необходимо уменьшить поступление в организм экзогенных пуринов и животных жиров. Жиры снижают экскрецию мочевой кислоты почками. Крайне осторожно следует подходить к употреблению любых алкогольных напитков, включая пиво и красное вино. Исключают из пищевого рациона печенку, почки, жирные сорта мяса, мясные бульоны, копчености, горох, бобы, чечевицу, шпинат, цветную капусту, шпроты, сельдь. Следует ограничить потребление мяса до 2–3 раз в неделю, при этом лучше употреблять его в отварном виде.
Сочетание строгой диеты с длительным применением противоподагрических препаратов, а также активное воздействие на заболевания, которые повышают содержание мочевой кислоты в крови, способны существенно замедлить темпы прогрессирования костно-хрящевой деструкции, предупредить дальнейшее формирование тофусов и сохранить функциональное состояние опорно-двигательного аппарата и почек.
В. В. Бадокин, доктор медицинских наук, профессор
РМАПО, Москва