Пресс-центр
Роль магнитно-резонансной томографии в оценке местной распространенности рака прямой кишки
Балясникова С.С., Сураева Ю.Э., Долгушин Б.И., Барсуков Ю.А, Мамедли З.З., Полыновский А.В., Кузьмичев Д.В.
ФГБУ «РОНЦ им.Н.Н. Блохина», РАМН, г. Москва (директор – академик РАМН и РАН, профессор М.И. Давыдов
ВВЕДЕНИЕ
Совершенствование хирургической техники и современные данные о результатах лечения рака прямой кишки (MERCURY Study Group) диктуют необходимость персонализированного подхода в назначении неоадьювантной химиолучевой терапии с учетом критериев риска рецидивирования рака в зависимости от местного распространения опухоли. В связи с этим, роль специалистов лучевой диагностики в планировании предстоящего лечения и оценки его эффективности стала критически значимой. Информация, получаемая при интерпретации изображений (с высоким разрешением) органов малого таза, дает детализированное представление о местной распространенности опухолевого процесса, что позволяет более грамотно определять тактику лечения больных и улучшать, тем самым, отдаленные результаты.
Магнитно-резонансная томография (МРТ) на сегодня является методом выбора для оценки местной распространённости рака прямой кишки 4. Обладая высоким мягкотканным контрастом, МРТ дает возможность визуализировать эндофитное и экстрамуральное распространение опухоли, в частности, определять нарушение зональной структуры кишечной стенки, распространение опухоли в мезоректальную клетчатку и вовлечение в опухолевой процесс мезоректальной фасции, а также органов малого таза, костных и мышечных структур; изменения в лимфатических узлах (ЛУ), расположенных как экстрафасциально так и в параректальной клетчатке.
Было доказано, что использование контрастных препаратов, как внутривенных, так и трансректальных, не улучшает диагностическую точность 9. Введение внутривенных МР-контрастных препаратов не дает клинически значимой дополнительной информации. Для опухолей прямой кишки характерно интенсивное накопление контрастного препарата (за исключением муцинозных опухолей – где кистозный компонент преобладает над солидным). Однако, столь же интенсивное накопление контрастного препарата может наблюдаться в отечной окружающей клетчатке при развитии десмопластической реакции (состояния, при котором отмечается разрастание соединительной ткани без элементов опухолевого роста) и неправильная интерпретация результатов в этом случае, будет приводит к завышению стадии экстрамуральной распространенности [4, 11-13]. По данным работ ряда авторов, динамическое МР-контрастирование может быть использовано в качестве метода, позволяющего оценить эффективность предстоящего неоадъювантного лечения. Получаемые в ходе этого вида исследования данные (такие показатели, как степень и интенсивность накопления контрастного препарата) отображают ангиогенез опухоли, ключевой фактор опухолевого роста и диссеминации, и дают возможность рассчитывать эффективность использования препаратов ингибиторов ангиогенеза в будущем [14].
В начале своей работы некоторым больным (у которых отсутствовали противопоказания) мы выполняли исследования с трансректальным введением ультразвукового геля. Следует отметить, что растяжение кишечной стенки при введении геля трансректально позволяло легко определять внутрипростветное распространение опухоли, но не увеличило точность оценки внутристеночной или трансмуральной глубины инвазии. Наоборот, перерастяжение кишечной стенки приводило к сокращению истинного пространства мезоректальной клетчатки и не позволяло определять фактическое расстояние от латерального края опухоли до мезоректальной фасции 14.
В исследовании MERCURY было доказано, что на Т2-изображениях можно визуализировать глубину инвазии мезоректальной клетчатки с точностью до 0,5 мм [15]. Но, несмотря на столь высокие показатели, стандартные режимы МРТ имеют свои диагностические ограничения в определении изменений лимфатических узлов, оценке эффективности проводимой терапии и диагностике локорегионарных рецидивов 17. В литературе существует ряд работ, оправдывающих использование диффузионно-взвешенного режима с целью улучшения диагностических возможностей МРТ в оценке местной распространенности рака прямой кишки и его рецидивов.
Давно известный в нейрорадиологии, но сравнительно недавно применяемый в онкодиагностике метод диффузионно-взвешенной МРТ (ДВ-МРТ) позволяет быстро и более точно проводить первичное стадирование опухолей и оценивать эффективность предоперационного лечения [11, 15-17].
Методика ДВ-МРТ основана на оценке степени подвижности молекул воды в исследуемых тканях. Неопластический процесс приводит к увеличению количества клеток и соответствующему уменьшению межклеточных пространств, что отображается на ДВ-изображениях с высоким b-value, в виде зон гиперинтенсивного сигнала в участках самой опухоли и пораженных Л/У. С физической точки зрения в диффузионно-взвешенном режиме изображения получают, благодаря применению двух равных по силе и длительности диффузионных градиентов, используемых перед (дефазирующий градиент) и после (рефазирующий градиент) 180 ° радиочастотного импульса в последовательности spin-echo T2. Таким образом, если молекулы воды в той или иной мере статичны, то действие на них дефазирующего градиента будет минимизировано за счет применения рефазирующего градиента, и такие молекулы будут иметь яркий сигнал на изображениях. И наоборот, если молекулы воды подвижны, то на них не сможет подействовать рефазирующий градиент, направленный в ту же точку пространства, что и дефазирующий и, следовательно, такие молекулы не будут в фазе, и это приведет к снижению сигнала на Т2-изображениях.
В-фактор (b value) отображает силу, продолжительность и время между используемыми диффузионными градиентами. В большинстве онкологических протоколов используются 2 и более b-факторов, один низкий b-value, равный 0 с/мм2, один – средний, порядка 50/100 с/мм2, и один или несколько высоких b-value 500/800/1000 с/мм2, в зависимости от зоны исследования. В процессе постобработки “сырых” данных возможно получение карт истинного коэффициента диффузии (ИКД (ADC) карт), на которых могут быть посчитаны значения ADC (apparent diffusion coefficient).
С целью определения роли магнитно-резонансной томографии в оценке местной распространенности рака прямой кишки были изучены результаты МР исследований, проведенных 110 пациентам (60 мужчин, 50 женщин), получавшим лечение в хирургическом отделении колопроктологии ФГБУ РОНЦ им Н.Н. Блохина, с 2011 по 2014 гг. Восемнадцать больных (19,8%) не получали неоадъюватной терапии, а только хирургическое лечение, и поэтому МР исследование им было проведено один раз с целью__местного стадирования опухоли. Остальным 92 больным (80,2%) исследование проводилось дважды: с целью первичного стадирования опухоли и повторно, для оценки эффективности проводимого лечения.
Рисунок 1. T2 cor. Красными линиями обозначено поле исследования и угол наклона сагиттальных срезов
Результаты тотальной мезоректумэктомии с применением водоструйной диссекции при раке прямой кишки: взгляд хирурга и патоморфолога
Сидоров Д.В., Франк Г.А., Майновская О.А., Ложкин М.В., Гришин Н.А., Петров Л.О., Троицкий А.А.
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва, Россия
В работе приведен собственный, первый в России опыт применения водоструйного диссектора ERBEJET2 ® в ходе выполнения оперативных вмешательств по поводу рака прямой кишки.
Методика водоструйной диссекции на этапе мобилизации препарата применена нами у 5 больных раком прямой кишки. Средний возраст больных составил 58,3±14,2 лет (47-78). В исследованной группе было 2 мужчин и 3 женщины. У всех больных оперативные вмешательства выполняли по поводу аденогенного рака прямой кишки, морфологически верифицированного на предоперационном этапе. Удаленные препараты исследованы морфологически. Для оценки качества хирургического лечения были использованы критерии, разработанные в исследованиях Ph. Quirke. При микроскопическом исследовании циркулярного края резекции, помимо определения хирургического клиренса, оценивали выраженность и глубину повреждения ткани мезоректума. Для сравнения были выбраны две контрольные группы по 5 больных, у которых мобилизацию прямой кишки производили с применением монополярного коагулятора и гармонического скальпеля. Исследованные группы были сопоставимы по гендерному составу, возрасту, локализации и распространенности опухоли. Все оперативные вмешательства выполняла одна бригада хирургов.
Средняя продолжительность операции составила 143±39,1 мин. (от 105 до 190). Объем кровопотери оценен как минимальный во всех 5 наблюдениях. Интраоперационных осложнений не зафиксировано. Течение послеоперационного периода гладкое у всех больных. Дизурические нарушения отсутствовали. Средняя продолжительность послеоперационного пребывания пациентов в стационаре – 9 дней (7-11).
При морфологическом исследовании качество мезоректумэктомии было оценено как хорошее (Grade 3) у всех 5 пациентов. Среднее количество исследованных лимфоузлов составило 24,2±6,4. Метастатическое поражение лимфатических узлов мезоректальной клетчатки выявлено у трех больных. В двух контрольных группах качество мезоректумэктомии также было оценено как хорошее (Grade 3) у всех 10 пациентов. В группе больных, у которых мобилизацию прямой кишки выполняли с применением водоструйной диссекции, повреждения тканей (фасции и клетчатки) практически не отмечалось. Наибольшее повреждение ткани (в виде термического воздействия, вплоть до очагов коагуляционного некроза) по латеральному краю резекции отмечали при использовании монополярного коагулятора. Глубина термического повреждения ткани по латеральному краю в этой группе составила от 1,7 до 3,0 мм. Латеральное повреждение тканей при мобилизации прямой кишки при помощи гармонического скальпеля было менее выражено, чем при использовании монополярного коагулятора. Ткани удаленного препарата практически не имели признаков термического воздействия, и изменения проявлялись преимущественно в деформации тканевых структур. Максимальная глубина повреждения ткани по латеральному краю резекции в данной группе составляла от 1,0 до 1,5 мм.
Водоструйные диссекторы могут занять свое место в списке оборудования, используемого при выполнении оперативных вмешательств по поводу рака прямой кишки и внести свой вклад в улучшение онкологических и функциональных результатов хирургического лечения данной группы больных.
Ключевые слова: рак прямой кишки, тотальная мезоректумэктомия, водоструйная диссекция.
Хирургический метод остается основным в лечении больных раком прямой кишки (РПК). Радикально выполненное оперативное вмешательство позволяет рассчитывать как на достижение локального контроля, так и на хорошие онкологические результаты данной категории больных в целом. Пионерская работа, посвященная технике и отдаленным результатам тотальной мезоректумэктомии (ТМЭ), опубликованная R.J. Heald в 1986 г. [7], положила начало новой эпохе в онкопроктологии. До внедрения в практику рутинного выполнения ТМЭ частота развития местных рецидивов после радикальных операций по поводу РПК, по данным разных авторов, достигала 20-38% [6, 16]. В настоящее время ТМЭ является общепризнанным «золотым стандартом» хирургического лечения рака прямой кишки и позволяет достичь 5-летнего локального контроля у 90-97% больных [1, 10, 12].
Методика ТМЭ подразумевает мобилизацию прямой кишки острым путем под контролем зрения в пределах мезоректальной фасции, с сохранением элементов вегетативной нервной системы таза. Для выполнения такой мобилизации хирурги во всем мире традиционно используют ножницы, коагулятор, в последние годы – гармонический скальпель.
Несмотря на публикации, посвященные возможностям применения водоструйной диссекции на этапе ТМЭ при выполнении внутрибрюшных резекций по поводу РПК [9, 22], данная методика к настоящему моменту не получила широкого распространения в онкопроктологии. Так, в доступной отечественной литературе упоминания об использовании водоструйного диссектора в хирургии РПК отсутствуют, а общее число таких публикаций в зарубежной печати не превышает десятка.
В работе мы приводим собственный, первый в России опыт применения водоструйного диссектора ERBEJET2 ® в ходе выполнения оперативных вмешательств по поводу РПК.
Материалы и методы
Методика водоструйной диссекции на этапе мобилизации препарата применена нами у 5 больных РПК. Средний возраст больных составил 58,3±14,2 лет (47-78). В исследованной группе было 2 мужчин и 3 женщины. У всех больных оперативные вмешательства выполняли по поводу аденогенного РПК, морфологически верифицированного на предоперационном этапе. Объем предоперационного обследования, помимо клинических и лабораторных методов, включал УЗИ (в т.ч. – трансректальное и трансвагинальное) и МРТ органов малого таза. Опухоли локализовались в среднеампулярном (у 3 пациентов) и нижнеампулярном (2 больных) отделах прямой кишки. Расстояние от нижнего полюса опухоли до края ануса варьировало от 4 до 9 см. Латеральное распространение опухоли по результатам предоперационного обследования расценено как Т2 (инвазия мышечной оболочки стенки кишки без выхода в мезоректальную клетчатку) у трех больных, T3 (выход опухоли за пределы стенки кишки) – у двух пациентов. Данных за поражение лимфатических узлов мезоректальной клетчатки и других регионарных зон не было получено ни у одного пациента. Противопоказаниями к проведению предоперационной химиолучевой терапии у больных с опухолевой инвазией мезоректальной клетчатки в одном наблюдении были эпизоды активных кровотечений из опухоли, во втором – наличие синхронных билобарных метастатических очагов в печени.
Использование водоструйного диссектора начинали на этапе мобилизации ректосигмоидного отдела. Строго под контролем зрения мобилизовали заднюю и боковые стенки прямой кишки, при этом выделяли и аккуратно отделяли правый и левый гипогастральные нервы от мезоректума. Благодаря водоструйной диссекции в корректном слое («holy plane») внутритазовая фасция оставалась интактной, покрывая пресакральные сосуды ниже промонториума, внутренние подвздошные сосуды и грушевидные мышцы таза. Возникающее в ходе диссекции капиллярное кровотечение, как правило, не требовало остановки коагуляцией и купировалось самостоятельно. Диссекция продолжалась до тазового дна. Пересечение более плотных соединительнотканных структур производили гармоническим скальпелем или коагулятором.
Далее производили водоструйную диссекцию (при необходимости – с дополнительной обработкой гармоническим скальпелем) в области боковых связок прямой кишки. В большинстве случаев дистальные ветви средних прямокишечных артерий, проходящие в «боковых связках» прямой кишки от внутритазовой фасции к мезоректуму, имеют незначительный диаметр и легко поддаются коагуляции.
После пересечения «боковых связок» продолжали мобилизацию прямой кишки по задней и боковым поверхностям до уровня париетальной тазовой фасции и фасции Вальдейера, идущей от леваторов и покрывающей дистальную часть прямой кишки и аноректальный переход. Пересечение прямой кишки производили при помощи аппарата Countur. После этого приступали к формированию аппаратного колоректального или колоанального анастомоза с формированием превентивной трансверзостомы. Для формирования анастомозов использовали циркулярные сшивающие аппараты.
Удаленные препараты подвергали морфологическому исследованию. Макроскопическое исследование препарата включало оценку сохранности собственной фасции прямой кишки, степени выраженности клетчатки по передней, задней и боковым поверхностям кишки. Для оценки качества хирургического лечения были использованы критерии, разработанные в исследованиях Ph. Quirke [17]. Кроме этого, при микроскопическом исследовании циркулярного края резекции, помимо определения хирургического клиренса, оценивали выраженность и глубину повреждения ткани мезоректума. Для сравнения были выбраны две контрольные группы по 5 больных, у которых мобилизацию прямой кишки производили с применением монополярного коагулятора и гармонического скальпеля. Исследованные группы были сопоставимы по гендерному составу, возрасту, локализации и распространенности опухоли. Предоперационную лучевую терапию не проводили ни одному из 15 пациентов. Все оперативные вмешательства выполняла одна бригада хирургов.
Всем больным выполнены нервосберегающие низкие передние резекции прямой кишки с парааортальной лимфаденэктомией. Одной пациентке дополнительно произведена билатеральная обтураторная лимфаденэктомия. Средняя продолжительность операции составила 143±39,1 мин. (от 105 до 190). Объем кровопотери оценен как минимальный у всех 5 больных. Интраоперационных осложнений не зафиксировано. Течение послеоперационного периода гладкое у всех больных. Дизурических нарушений не было. Самостоятельное мочеиспускание восстановилось на 1-е сутки (после удаления мочевого катетера) у всех 5 пациентов. Средняя продолжительность послеоперационного пребывания пациентов в стационаре – 9 дней (7-11).
При морфологическом исследовании качество мезоректумэктомии было оценено как хорошее (Grade 3) у всех 5 пациентов. Инвазия опухоли в мезоректальную клетчатку рТ3 выявлена у трех больных; опухоль в пределах стенки кишки рT2 – у двух пациентов (у одного больного имела место некоторая недооценка распространенности опухоли по данным предоперационного обследования). Статус CRM расценен как негативный в 4 наблюдениях. В одном случае выявлен опухолевый депозит в мезоректальной клетчатке на расстоянии менее 1 мм от циркулярного края резекции (CRM+). Среднее количество исследованных лимфатических узлов составило 24,2±6,4. Метастатическое поражение лимфатических узлов мезоректальной клетчатки выявлено у трех больных.
В двух контрольных группах качество мезоректумэктомии также было оценено как хорошее (Grade3) у всех 10 пациентов. У двух зафиксирован положительный статус циркулярного края резекции (опухолевый депозит и метастатический лимфатический узел на расстоянии менее 1 мм от CRM).
При исследовании глубины повреждения тканей по латеральному краю удаленного препарата получены следующие данные.
В группе больных, у которых мобилизацию прямой кишки выполняли с применением водоструйной диссекции, повреждения тканей (фасции и клетчатки) практически не отмечалось (рис. 1, 2).
Рис. 1. Макропрепарат. На поверхности мезоректума (вид сзади) при его мобилизации с использованием водоструйного диссектора определяется небольшое разволокнение собственной фасции кишки без ее повреждения.
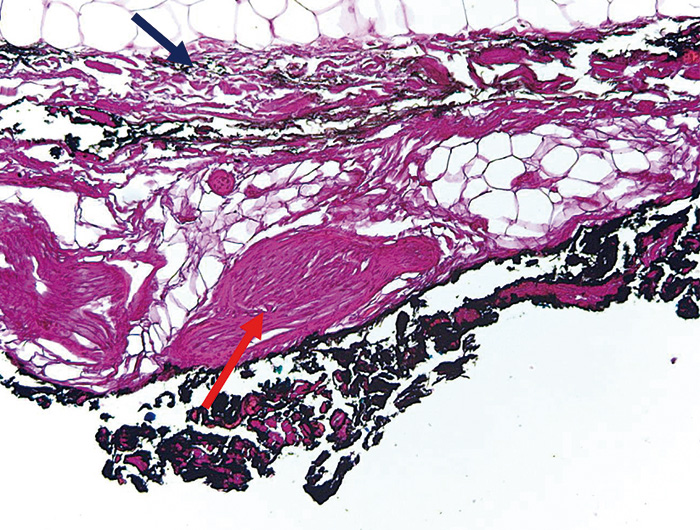
Рис. 2. Микропрепарат. Мобилизация прямой кишки с использованием водоструйного диссектора. Небольшое разволокнение собственной фасции (окрашена черной краской) без ее деформации (синяя стрелка) и полное сохранение субфасциальных структур – нервных стволов (красные стрелки). Окраска гематоксилином и эозином. Увеличение ×100.
Наибольшее повреждение ткани (в виде термического воздействия, вплоть до очагов коагуляционного некроза) по латеральному краю резекции отмечали при использовании монополярного коагулятора. Причем в большей степени деформации подвергались мезоректальная фасция, элементы боковых связок и резецированные экстрафасциальные структуры (сосуды и нервы). Глубина термического повреждения ткани по латеральному краю в группе больных, оперированных с применением монополярного коагулятора, составила от 1,7 до 3,0 мм (рис. 3, 4).
Рис. 3. Макропрепарат. Поверхность мезоректума (вид сзади) при его мобилизации с использованием монополярного коагулятора: определяются крупные участки термовоздействия (стрелки).
Рис. 4. Микропрепарат. Мобилизация прямой кишки с использованием монополярного коагулятора: широкая зона термического воздействия по латеральному краю резекции (окрашен черной краской) с выраженной деформацией фасции и экстрафасциальных структур – нервных стволов (стрелки). Окраска гематоксилином и эозином. Увеличение ×50.
Латеральное повреждение тканей при мобилизации прямой кишки при помощи гармонического скальпеля менее выражено, чем при использовании монополярного коагулятора. Ткани удаленного препарата практически не имели признаков термического воздействия, и изменения проявлялись преимущественно в деформации тканевых структур. Максимальная глубина повреждения ткани по латеральному краю резекции в данной группе составляла от 1,0 мм до 1,5 мм (рис. 5, 6).
Рис. 5. Макропрепарат. Поверхность мезоректума (вид сзади) при его мобилизации с использованием гармонического скальпеля. Определяются небольшие участки воздействия на уровне боковых связок кишки (стрелка).
Рис. 6. Микропрепарат. Мобилизация прямой кишки с использованием гармонического скальпеля. Умеренно выраженная деформация по латеральному краю резекции (окрашен черной краской) с разволокнением собственной фасции (синяя стрелка) и значительной деформацией экстрафасциальных структур – нервных стволов (красная стрелка). Окраска гематоксилином и эозином. Увеличение ×100.
Принцип водоструйной диссекции долгое время применяли в областях, далеких от медицины (в стекольной промышленности, для обработки металлических изделий и т.п.). Первые упоминания о возможности клинического применения тонкой струи воды под высоким давлением для резекции паренхиматозных органов относятся к началу 90-х годов прошлого века [2]. Несмотря на тот факт, что данная методика является относительно новой, она уже нашла достаточно широкое применение в различных областях хирургии. Основной областью применения водоструйных диссекторов в настоящий момент следует признать хирургическую гепатологию [18, 19, 23]. При этом в мировой литературе имеются многочисленные публикации о применении данной методики в хирургии печени, почек, предстательной железы и в нейрохирургии [3, 22]. В качестве основных преимуществ метода упоминается деликатность разделения тканей, сохранение целостности сосудистых и других трубчатых структур, минимальная травматизация окружающих тканей, отсутствие термического повреждения [18, 23].
Последняя из перечисленных особенностей методики водоструйной диссекции (отсутствие возникновения так называемого «латерального термического повреждения» тканей) обусловливает потенциальные преимущества метода именно при выполнении тотальной мезоректумэктомии. В последние годы многие авторы большое внимание уделяют возможности сохранения элементов вегетативной нервной системы таза (см. выше) при выполнении оперативных вмешательств по поводу РПК [5, 11, 14]. Улучшение функциональных результатов и повышение качества жизни больных при выполнении так называемых «нервосберегающих» передних резекций прямой кишки убедительно показано в большом числе исследований и связано, прежде всего, со снижением частоты урологических расстройств и нарушений сексуальной функции (эректильная дисфункция у мужчин, сухость влагалища и диспареуния у женщин) [4, 13, 20].
С другой стороны, в литературе имеются данные (в т.ч. и экспериментальные) о возможности латерального термического повреждения вегетативных нервов при мобилизации прямой кишки с применением коагулятора и в меньшей степени – гармонического скальпеля [8, 21]. Особенно высок риск травматизации тазовых нервов при работе в «критических точках», в т.ч. у латеральной стенки прямой кишки и на уровне промонториума [15]. В связи с этим существуют даже предложения об отказе от применения в этих зонах каких-либо генераторов и возврате к использованию «острой» диссекции ножницами.
Как показали результаты нашего исследования, глубина латерального повреждения тканей при использовании водоструйного диссектора минимальна, что связано с техническими особенностями метода – диссекция тонкой струей воды комнатной температуры. Аналогичный показатель в группе больных, оперированных с применением монополярного коагулятора и гармонического скальпеля, достигает 1,5 мм и 3,0 мм соответственно. Это обусловливает возможность повреждения элементов вегетативной нервной системы таза даже при точном соблюдении плоскости мобилизации препарата. Такое повреждение, в свою очередь, может существенно ухудшить функциональные результаты операций по поводу РПК за счет денервации соответствующих тазовых структур (мочевого пузыря, предстательной железы, шейки матки и влагалища).
Нам представляется, что применение водоструйного диссектора на этапе мобилизации прямой кишки в зонах максимального риска повреждения нервных структур (уровень промонториума, боковые поверхности мезоректальной клетчатки) позволяет свести к минимуму риск латерального термического повреждения тазовых нервов и избежать связанных с этим осложнений. При этом для мобилизации препарата в зонах, удаленных от описанных нервных структур, вполне возможно применение традиционных методик и генераторов (моно- или биполярная коагуляция, гармонический скальпель). Такое комбинированное применение различных методов разделения тканей позволяет рассчитывать на выполнение действительно «нервосберегающих» резекций прямой кишки без существенного увеличения продолжительности операции.
Таким образом, наш первый опыт применения водоструйного диссектора в ходе тотальной мезоректомэктомии свидетельствует о безопасности и эффективности данной методики. Отсутствие эффекта латерального термического повреждения тканей (в первую очередь – элементов вегетативной нервной системы таза) позволяет использовать данный метод диссекции в «критических точках» мезоректумэктомии без риска повреждения названных структур. Совместное применение водоструйного диссектора и других генераторов позволяет рассчитывать на минимальную травматизацию тазового сплетения и, как результат, лучшие функциональные результаты лечения больных.
Водоструйные диссекторы, с нашей точки зрения, могут занять свое место в длинном списке оборудования, используемого при выполнении оперативных вмешательств по поводу РПК, внести свой вклад в улучшение онкологических и функциональных результатов хирургического лечения данной группы больных.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.