Метаболизм костной ткани что это такое
Физиология паратгормона настолько сильно связана с витамином D и метаболизмом костной ткани, что рассматривать эти вопросы по отдельности, не потеряв их сути, невозможно. Графически взаимоотношения представлена на рисунке ниже. Паратгормон в первую очередь регулирует содержание ионов кальция в межклеточном пространстве. Витамин D контролирует всасывание кальция из пищи, а также косвенно отвечает за минерализацию костной ткани, которая содержит в себе 99% всего кальция организма.
«Можно ли считать кость органом?» Да! Поскольку костная ткань проявляется очень высокую метаболическую активность, а также содержит большие запасы кальция, она напрямую включена в процессы регуляции содержания кальция в межклеточном пространстве и плазме крови. Нормальная концентрация кальция в межклеточном пространстве необходима для выполнения множества клеточных функций, среди которых передача сигнала между клетками, секреция гормонов, нормальная работа мышц и нервов, поэтому необходимо строгое ее сохранение в определенных пределах.
Гипокальциемия ведет к нервно-мышечной гипервозбудимости; умеренное снижение уровня кальция проявляется гиперестезиями с положительными симптомами Хвостека и Труссо; тяжелая гипокальциемия ведет к развитию тетании, судорог и смерти. Гиперкальциемия проявляется летаргией, слабостью, комой и, наконец, смертью. Около 50% внеклеточного кальция находится в ионизированной форме, но точное соотношение зависит от pH. Содержание кальция внутри клеток на порядки меньше, чем вне ее, но некоторые органеллы, например, митохондрии, содержат в себе повышенные концентрации кальция. Колебания уровня внеклеточного ионизированного кальция обычно не превышают ± 10%.
а) Физиология обмена паратгормона. Паратгормон (паратиреоидный гормон, ПТГ, РТН) по химическому строению является 84-аминокислотным полипептидом; было выяснено, что за биологическую активность гормона ответственны первые 34 аминокислотных остатка паратгормона, именно они используются в клинической практике, например, в лечении остеопороза. Определение последовательности классического рецептора ПТГ показало его связь с G-белком и наличие семи трансмембранных сегментов, проявляющих одинаковое сродство как с паратгормоном, так и с ПТГ-родственным пептидом (ПТГ-рП).
Но ПТГ-рП не обладает таким же активирующим действием на 1-гидроксилазы почек, как сам ПТГ.
Наибольшее количество рецепторов к ПТГ находится в костной ткани и в почках, хотя в других органах они также присутствуют в меньших количествах. Недавно был обнаружен новый подвид ПТГ-рецептора, который связывается с карбоксильным остатком паратгормона. Ранее считалось, что данные рецепторы находятся в неактивном состоянии. Этот недавно обнаруженный рецептор не связывается с ПТГ-рП. Неизвестно, играет ли он какую-либо роль в метаболизме костной ткани или имеет какие-либо другие функции.
Клетки паращитовидных желез также экспрессируют рецепторы, чувствительные к кальцию. И они являются рецепторами, связанными с G-белками, и имеют в своем составе семь трансмембранных доменов. Данные рецепторы могут соединяться с различными катионами, но физиологически подходящими для них являются только двухвалентные катионы кальция и магния. Снижение уровня ионизированного кальция ведет к повышению секреции ПТГ, повышение уровня ионизированного кальция ведет к снижению секреции ПТГ.
Таким образом, и концентрация ионизированного кальция, и концентрация ПТГ в плазме крови колеблются лишь в узких пределах. Были описаны различные мутации данных рецепторов, некоторые из них приводят к повышению их активности, другие — к понижению. Данные мутации являются ключом к пониманию семейной гипокальциурической гиперкальциемии и некоторых гипокальциемических синдромов, например, семейного гипопаратиреоидизма.
Паратгормон (ПТГ) повышает резорбцию кальция в почках, усиливает резорбцию костной ткани, повышает активность D1-гидроксилазы почек. Эти механизмы помогают восстановить уровень кальция в плазме крови.
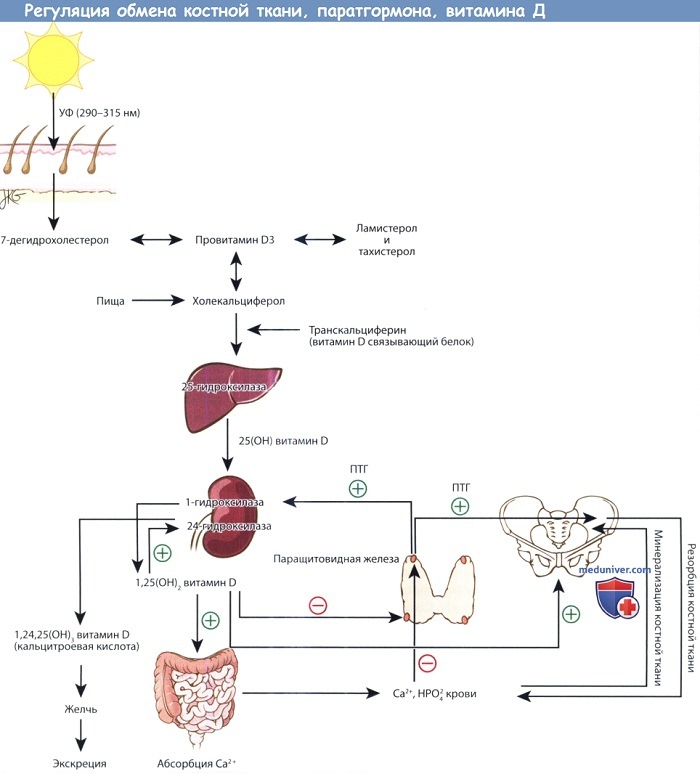
Предшественники витамина D синтезируются в коже под действием ультрафиолета. Превращение 25-ОН витамина D, депонированной формы витамина, в активную форму,
т.е. 1,25-(ОН)2 витамин D, регулируется паратгормоном. 1,25-(ОН)2 витамин D повышает всасывание кальция в желудочно-кишечном тракте.
Кальций и фосфор плазмы крови регулируют содержание паратгормона крови, а также участвуют в минерализации новообразованного костного матрикса.
При повышении уровня паратгормона усиливается резорбция костной ткани, поскольку это необходимо для поддержания необходимого уровня кальция в плазме,
а также стимулируется синтез 1,25-(ОН)2 витамина D почками.
б) Физиология обмена витамина Д. Синтез провитамина D (холекальциферола) происходит в коже из 7-дегидрохолестерола в результате фотокатализа под действием ультрафиолетовых лучей с длиной волны 290-315 нм. Ультрафиолетовые лучи именно с такой длиной волны могут преодолеть атмосферу, поэтому у жителей возвышенностей синтез провитамина D подвержен сезонным колебаниям. Синтез предшественников провитамина D тоже зависит от воздействия солнечных лучей, поэтому избыточное пребывание на солнце не приводит к гипервитаминозу.
Возможности получения витамина D с пищей очень ограничены, лишь крайне малое число продуктов содержит в себе витамин D. Молоко и молочные продукты, производимые в США и Европе, дополнительно обогащаются витамином D. Одна их порция содержит около 100 ME витамина. К сожалению, необогащенные молочные продукты и человеческое грудное молоко содержат крайне малое количество витамина. В желтке яйца содержится около 20 ME витамина D, в белке витамина D нет. Рыба является источником, богатым витамином D.
Витамин D представляет из себя провитамин, активной формой которого является 1-25-(ОН)2 витамин D (кальцитриол). В норме кальцитриол продуцируется почками из витамина D, кальцидиола, в результате реакции 1-гидроксилирования. Активность 1-гидроксилазы почек контролируется ПТГ, поэтому уровень 1-25-(ОН)2 витамина D напрямую коррелирует с уровнем ПТГ. Высокий уровень ПТГ, как правило при гипокальциемии, стимулирует образование 1-25-(ОН)2 витамина D. В результате происходит повышение абсорбции кальция в кишечнике и нормализация его уровня в плазме крови.
При определенных патологических состояниях некоторые другие ткани также могут проявлять 1-гидроксилазную активность, иногда независимо от действия ПТГ.

в) Метаболизм минеральных веществ в костной ткани. Мы часто воспринимаем кости лишь как опорные структуры, но на самом деле костная ткань играет важную роль в метаболизме, выступая в качестве депо кальция, фосфатов и карбонатов, также она участвует в поддержании кислотно-щелочного равновесия. Матриксом кости является частично минерализованная ткань и специфические костные клетки. Костную систему человека разделяют на осевой скелет, к которому относят череп, позвоночный столб, грудину, ребра и таз, и на скелет конечностей, от их проксимальных отделов до кончиков пальцев.
Также костная ткань подразделяется на губчатую (трабекулярную), которая обладает высокой метаболической активностью, и кортикальную, которая имеет большую плотность и меньшую метаболическую активность. Изменения в кортикальной костной ткани наступают при тяжелых или длительно текущих заболеваниях. В осевом скелете преобладает содержание трабекулярной кости, в скелете конечностей — кортикальной.
К костным клеткам относят остеобласты, остеокласты и остеоциты. Остеобласты происходит из мезенхимальных стволовых клеток, они образуют соединительнотканный матрикс кости, который затем минерализуется, формируя новую костную ткань. Большинство остеобластов подвергаются апоптозу, но часть из них остается включенной в костный матрикс и превращается в остеоциты, а другая часть остается на поверхности кости, формируя надкостницу.
Трансформируясь в остеоциты, эти клетки образуют длинные отростки, которыми они создают щелевой контакт с соседними клетками и с клетками надкостницы. Остеоциты воспринимают механическое давление, оказываемое на кость, и играют важную роль в моделировании костной ткани. Остеокласты представляют собой крупные многоядерные клетки, происходящие из одноядерных макрофагов. Процесс дифференцировки клеток в остеокласты происходит под контролем ядер-ного фактора кВ (каппа-Б, RANKL), продуцирующего в ходе апоптоза остеобластов, и под контролем колониестимулирующего фактора макрофагов.
Остеокласты участвуют в резорбции костной ткани, разрушая минеральный компонент и коллагеновый матрикс костной ткани посредством протеолиза.
В норме костная ткань постоянно разрушается остеокластами и одновременно заново синтезируется остеобластами. Этот процесс получил название ремоделирования костной ткани. В здоровом организме процессы разрушения и синтеза костной ткани находятся в равновесии. Ремоделирование костной ткани крайне важно для поддержания структурной целостности (прочности) скелета, т. к. с ее помощью постоянно восстанавливаются микропереломы костей, возникающие от каждодневных физических нагрузок.
г) Кальций-чувствительные рецепторы. Как уже упоминалось выше, паращитовидные клетки экспрессируют кальций-чувствительные рецепторы. Первоначально данные рецепторы были выделены из паращитовидных клеток крупного рогатого скота, затем их наличие было подтверждено и у человека. Кроме паращитовидных желез, где они и были впервые обнаружены, данные рецепторы экспрессируются в почках, костях, желудке, легких, головном мозге и других тканях.
Как мутации, так и приобретенные дисфункции данных рецепторов могут стать причиной появления различных заболеваний, связанных как с повышением, так и с понижением кальция крови. Более подробно эти заболевания будут рассмотрены ниже.
Учебное видео расшифровки биохимического анализа крови
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Современные подходы к диагностике и лечению остеопороза
Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболи
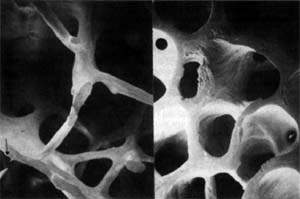 |
| Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. |
Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболизма.
Остеопороз — это системное заболевание скелета, характеризующееся снижением костной массы и нарушением микроархитектоники костной ткани, ведущими к повышенной хрупкости костей с последующим увеличением риска их переломов (рис. 1). Помимо наиболее распространенного постменопаузального остеопороза, в настоящее время в цивилизованных странах в связи с растущей продолжительностью жизни все чаще встречается сенильный остеопороз, а также вторичный остеопороз, обусловленный различными заболеваниями (эндокринная патология, ревматические болезни, заболевания желудочно-кишечного тракта и пр.) или связанный с длительным приемом некоторых лекарственных препаратов, например кортикостероидов.
В настоящее время для диагностики остеопороза используются преимущественно неинвазивные методы, которые легковыполнимы, безопасны и могут повторяться неоднократно у одного и того же больного. К таким методам относятся рентгенографическое исследование, костная денситометрия и исследование биохимических маркеров костного метаболизма. Каждый из этих методов занимает свою нишу в диагностике заболе-вания.
С целью ранней диагностики остеопороза применяются различные технологии, объединенные под общим названием «костная денситометрия», с ее помощью можно определить минимальную плотность костной ткани (МПК), являющуюся главным критерием прочности кости. В настоящее время выделяют четыре типа и два подтипа технологий для измерения МПК:
В данном перечне отсутствует фотонная денситометрия — предшественница рентгеновской денситометрии, в последнее время используемая весьма редко.
 |
| Рисунок 2 |
Системы DXA являются наиболее изученными и широко применяются в клинической практике (рис. 2). DXA позволяет измерять МПК в центральных отделах скелета: в поясничном отделе позвоночника и в проксимальном отделе бедренной кости. В этих участках происходят наиболее тяжелые переломы. Кроме того, многие из этих приборов снабжены программой «все тело», позволяющей определить содержание минералов во всем скелете, а также исследовать мягкие ткани — мышечную и жировую. В новых модификациях приборов DXA имеется возможность латерального сканирования и морфометрического измерения позвонков,что значительно повышает информативность этого метода. Метод DXA также адаптирован для оценки состояния МПК в области периферических участков скелета, в частности в области предплечья и пяточной кости (рис. 3).
Радиографическая абсорбциометрия используется редко, поскольку требует специально оборудованного центра, где при помощи микроденситометра производится сканирование рентгеновских снимков фаланг и определяется их оптическая плотность.
 |
| Рисунок 3 |
Для определения МПК позвоночника можно использовать и QCT, которая является единственным методом, представляющим результаты исследования в трехмерном измерении. Возможность проведения измерений в поперечном сечении, заложенная в QCT, позволяет выделить этот метод среди других, так как он дает возможность дифференцированно оценивать МПК в трабекулярной и кортикальной костной ткани, фиксируя истинные значения МПК в г/см3 [1]. В отличие от DXA при QCT нет искажений МПК, связанных с тучностью пациента, а также вызванных сопутствующей патологией, например спондилоартритом и остеофитами, обызвествлением стенки аорты или участками остеосклероза, развивающимися в результате дегенеративных заболеваний или переломов позвонков. Но большие дозы облучения при QCT, а также высокая стоимость обследования ограничивают широкое применение этой технологии в диагностике остеопороза, использование ее оправданно лишь в ситуациях, требующих дифференциальной диагностики (рис. 4).
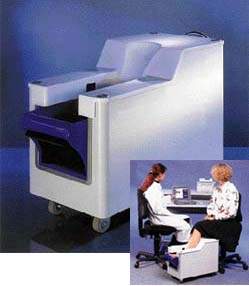 |
| Рисунок 4 |
В последние годы активно развивается ультразвуковая сонография, которая, в отличие от рентгеновской денситометрии, позволяет обследовать другие характеристики костной ткани: SOS — скорость распространения ультразвука в кости и BUA — широковолновое рассеивание (затухание) ультразвуковой волны в исследуемом участке скелета. Эти параметры, по данным многих исследователей, отражают степень эластичности и прочности костной ткани и достаточно высоко коррелируют с МПК позвоночника и шейки бедра [2]. В настоящее время многие специалисты высказывают мнение о том, что с помощью ультразвуковой денситометрии можно предсказывать риск переломов, тем самым обосновывая ее значение как метода для скрининга. Вопрос о возможности применения этих приборов в диагностике остеопороза и оценке эффективности терапии продолжает дискутироваться.
Рентгенография довольно активно используется для диагностики остеопороза и его осложнений. Однако ее нельзя отнести к методам ранней диагностики, поскольку рентгенологические признаки остеопороза появляются тогда, когда 20 — 30% костной массы уже потеряно [3]. Наиболее сложно оценить выраженность остеопороза в позвоночнике, поскольку ни один из его рентгенологических признаков не является специфичным. Часто рентгенография позволяет выявить остеопороз лишь на поздней стадии, когда уже имеются остеопоретические переломы. Для объективной оценки степени снижения минерализации костей разработаны так называемые полуколичественные методы. В основе их лежит вычисление вертебральных, феморальных и метакарпальных индексов. Но они также не могут претендовать на достаточную точность и чувствительность при выявлении ранней стадии заболевания (остеопении), хотя успешно применяются при эпидемиологических исследованиях распространенности остеопороза в популяции [4, 5]. Таким образом, основной функцией ренгенографического метода в диагностике остеопороза является обнаружение переломов, динамическое наблюдение за появлением новых переломов и дифференциальная диагностика остеопоретических переломов от других типов деформаций позвоночника.
С помощью методов «костной денситометрии» можно судить об основных параметрах прочности костной ткани, однако эти методы не дают никакой информации об уровне костного метаболизма. Уровень формирования и резорбции костной ткани может быть оценен несколькими способами: путем измерения ферментной активности костных клеток (остеобластов и остеокластов) или определения продуктов деградации костного матрикса, которые высвобождаются в циркуляцию в процессе костного обмена (табл. 1).
Таблица 1. Биохимические маркеры костного метаболизма
маркеры
мочи
Представленные в таблице костные маркеры являются предикторами потери костной массы, переломов костей скелета и используются для мониторинга антиостеопоретической терапии. По этим биохимическим показателям можно судить об эффективности терапии, об адекватности дозы препарата и о его переносимости. Особенно полезны костные маркеры для оценки эффективности терапии в сравнительно короткие промежутки времени, когда денситометрическое исследование еще не информативно (полагают, что повторные денситометрические исследования надо выполнять не чаще одного раза в год). Уровень маркеров костного метаболизма изучался в основном у женщин постменопаузального периода. Оказалось, что уровень почти всех маркеров, за исключением IPCP, повышен и коррелирует со снижением МПК [6]. Полагают, что сочетание денситометрии и исследования биохимических маркеров костного метаболизма позволит получить более полную информацию о риске развития постменопаузального остеопороза. По мнению P. Delmas (1996) увеличение скорости костной резорбции (по оценке уровней биохимических маркеров) существенно повышает риск развития переломов независимо от исходной костной массы пациентов [7]. Это связано с тем, что хрупкость кости при остеопорозе зависит не только от МПК, но и от нарушения микроархитектоники костной ткани, выраженность которой можно оценить с помощью биохимических маркеров костной резорбции. Это предположение подтверждается данными P. Garnero et al. (1996), полученными в рамках исследования EPIDOS [6]. Доказано, что увеличение уровня СТх или свободного диоксипиридинолина на 1SD от нормы ассоциировалось с 1,3- и 1,4-кратным увеличением риска переломов шейки бедра (рис. 5).
 |
| Рисунок 5. Комбинированная оценка МПК и скрытой костной резорбции для определения риска перелома шейки бедра у пожилых. МПК определялась по критериям ВОЗ с учетом показателей ниже 2,5 SD от нормальных показателей МПК у молодых здоровых женщин (Ts core |
При этом снижение МПК шейки бедра и увеличение маркеров костной резорбции, независимо друг от друга, связаны с высоким риском переломов шейки бедра. Для оценки эффективности проводимой терапии рекомендуется исследовать биохимические маркеры через каждые три месяца после начала лечения. При исследовании биохимических маркеров необходимо принимать во внимание факторы, влияющие на воспроизводимость результатов: диета, условия хранения материала, биологические факторы (циркадные и сезонные колебания, менструальный цикл, возраст, пол, наличие сопутствующих заболеваний и т. д.).
Многолетний опыт изучения остеопороза за рубежом показывает, что ни один из существующих в настоящее время лекарственных препаратов не может надежно восстановить количество и качество кости, поэтому основной мерой в борьбе с этим заболеванием является профилактика. Профилактику остеопороза надо начинать рано и уделять особое внимание средовым факторам, влияющим на достижение пика костной массы, который наступает примерно к тридцати годам. В числе этих факторов — питание и физическая активность, адекватное поступление в организм витамина D и инсоляция. К наиболее важным периодам относятся период роста кости (юношество), беременность, лактация и перименопауза. Пик костной массы может быть значительно улучшен за счет включения в рацион продуктов с повышенным содержанием кальция (прежде всего молочные и рыбные продукты). Суточное потребление кальция должно составлять в среднем 1000 — 1500 мг, предпочтительно с пищей. Регулярные физические упражнения с весовой нагрузкой в период роста кости приводят к увеличению пика костной массы. У взрослых после достижения пика костной массы адекватное потребление кальция, постоянная физическая нагрузка и наличие регулярного менструального цикла также способствует сохранению костной массы. Профилактику остеопороза среди взрослого населения нужно проводить в «группах риска».
Проблема лечения остеопороза за рубежом изучается давно, причем особенно активно в последнее десятилетие, что связано с введением денситометрии. Однако до настоящего времени не разработаны общепринятые терапевтические программы и режимы лечения этого заболевания, что, по-видимому объясняется его многофакторной природой и сложным патогенезом. Основная цель лечебных мероприятий — сбалансирование процессов костного метаболизма и сохранение или улучшение качества жизни пациента. Для этого необходимо добиться замедления или прекращения потери костной массы; уменьшить болевой синдром в позвоночнике и периферических костях; улучшить функциональное состояние больного и предотвратить возможные падения; восстановить трудоспособность и психоэмоциональное состояние. Наряду с этиопатогенетической терапией препаратами, направленными на нормализацию процессов ремоделирования костной ткани и на сохранение минерального гомеостаза, применяется и симптоматическая терапия, включающая в себя диету с повышенным содержанием солей кальция и фосфора, нестероидные противовоспалительные средства, анальгетики, миорелаксанты, которые позволяют уменьшить болевой синдром, мышечное напряжение и тем самым расширить двигательную активность пациента и ускорить начало реабилитационных мероприятий.
Реабилитация подразумевает лечебную физкультуру, ношение корсетов, плавание, курсы легкого массажа.
Все препараты для лечения остеопороза можно разделить на три группы:
В этиопатогенетической терапии остеопороза предпочтение отдается группе препаратов, подавляющих резорбцию костной ткани, вследствие их более высокой эффективности и сравнительно небольшого побочного действия.
В целом терапия остеопороза должна быть комплексной и проводить ее следует длительно в виде непрерывного или курсового лечения. Поскольку в настоящее время нет идеального препарата для лечения остеопороза, перспективна комбинированная терапия, в которой сочетаются препараты с различным механизмом действия, что позволяет потенцировать их антиостеопоретическое действие, снизить частоту и выраженность побочных эффектов.
| Профилактика остеопороза заключается в сбалансированном питании, физической активности, и адекватном поступлении в организм витамина D |
При комбинированной терапии лекарственные средства назначают одновременно или последовательно. Их выбор осуществляется индивидуально для каждого больного в зависимости от формы остеопороза, скорости костного обмена, тяжести клинического течения, сопутствующих заболеваний. Основным критерием эффективности любого антиостеопоретического средства является снижение частоты переломов, однако в каждом конкретном случае надо ориентироваться в первую очередь на показатели МПК по данным костной денситометрии и на биохимические маркеры костного обмена. Увеличение МПК более чем на 1% и нормализация биохимических показателей, если они были изменены, свидетельствуют об эффективности проводимой терапии. Учитываться должна и положительная динамика клинической картины: уменьшение болевого синдрома, повышение функциональной активности.
Таким образом, в настоящее время имеется довольно большой выбор диагностических методов, позволяющих установить диагноз остеопороза на разных стадиях, а также эффективных лекарственных препаратов, влияющих на различные звенья патогенеза остеопороза, способных уменьшить или купировать клинически выраженные симптомы заболевания, а также предупредить развитие переломов.