Мелкоочаговая и перивентрикулярная лейкоэнцефалопатия сосудистого генеза что это такое
Звоните нам по телефону 8 (812) 241-10-46 с 7:00 до 00:00 или оставьте заявку на сайте в любое удобное время
Ваша заявка принята!
Благодарим за обращение.
В ближайшее время с вами свяжется наш специалист.
Лейкоэнцефалопатия – клинические формы, диагностика
Медицинский термин «лейкоэнцефалопатия» применяется для определения группы заболеваний, сопровождающихся поражением белого вещества и ряда глубоких структур головного мозга. Быстрое прогрессирование приводит к формированию старческого слабоумия.
У детей встречаются сосудистые разновидности, врожденные формы с длительным хроническим течением. Сроки выживаемости при этом типе больше по сравнению с многоочаговым аналогом.
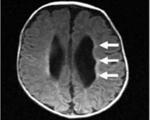
МР-снимок сосудистой лейкоэнцефалопатии
Для отличия патологии от ряда других нейродегенеративных болезней с аналогичными клиническими симптомами разработана классификация по МКБ 10, где четко выделяют формы нозологии.
Что такое лейкоэнцефалопатия головного мозга
Поражение белого вещества мозга обуславливается в большинстве случаев вирусами. Сосудистая, дисциркуляторная формы обусловлены нарушением кровоснабжения определенного участка головного мозга. Хроническая ишемия обуславливает необратимые изменения.
Клинические симптомы болезни чаще возникают при поражении папилломавирусами. Вероятность нозологии у пациентов с ВИЧ менее 6% по данным статистики МРТ головного мозга в СПб.
Формы сосудистого генеза прогрессируют медленно. Хроническое течение заболевания характеризуется постепенным необратимым поражением ткани. Легкая ишемия провоцирует образование небольших некротических участков. Диффузное расположение приводит к неврологическим расстройствам.
Виды лейкоэнцефалопатии
Самой малоопасной формой является очаговая. Формируется хроническими воспалительными процессами сосудистого генеза. Недостаток микроциркуляции определенного отдела мозга провоцирует гипоксию, нехватку кислорода. Гибель зон белого вещества развивается несколько лет.
Агрессивнее протекают морфологические изменения при гипертонической болезни. Увеличение внутричерепного давления обуславливает разрывы мелких капилляров с участками некроза мозговой паренхимы. Разновидность медицинским языком называется «дисциркулярная энцефалопатия». Появляется у людей старше 55 лет.
Прогрессирующая мультифокальная лейкоэнцефалопатия имеет агрессивное течение. Люди при патологии живут не более 5 лет. Летальные исходы связаны с обширными инфарктами, инсультами.
Классификация видов лейкоэнцефалопатии по МКБ 10
Прогрессирующий вид сосудистого генеза (болезнь Бинсвангера) кодируется символами «I67.3». Из классификации болезней десятого пересмотра исключена субкортикальная деменция с кодом «F01.2».
Прогрессирующая мультифокальная (многоочаговая) лейкоэнцефалопатия – «A81.2». К одноименной группе относится фенилкетонурия, болезнь Александера, Канавана. Патологии категории «IA» выделяют по причинам, так как имеют аутоиммунное происхождение – обусловлены повреждением тканей иммуноглобулинами собственного организма. Антитела становятся агрессивными при изменении структуры мембраны или генетической информации клетки под влиянием вирусов, химических, физических факторов.
Рассмотрим полный алгоритм классификации:
Международная классификация десятого пересмотра является действующей. При кодировке диагноза нередко встречается дисциркуляторная энцефалопатия, острая цереброваскулярная недостаточность БДУ ишемия мозга (хроническая).
Клинические симптомы мелкоочаговой лейкоэнцефалопатии
Очаговая симптоматика имеет подострое течение. Начальные стадии болезни выявляются неврологами:
Дифференциальная диагностика очаговых видов проводится для отличия от изменений белого вещества при ВИЧ, деменции. Спинальные очаги протекают без нарушения психических функций. Повреждение белого вещества сопровождается когнитивными расстройствами.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Причина многоочагового повреждения белого вещества – вирус JC, приводящий к распространенному поражению нервной системы. Заболевание развивается на фоне сниженной активности иммунной системы. Антиретровирусное лечение дорогое, поэтому большинство людей погибает.
Прогрессирующая энцефалопатия быстро приводит к разрушению миелина большинства нервных клеток. Изменения необратимы, симптомы постепенно нарастают.
Около 80% населения страны являются носителем полиомавируса человека второго типа, но энцефалопатия не возникает. Только иммунодефициты при СПИДе создают возможности быстрого размножения возбудителя.
Иммунитет пожилых людей не справляется с активность полиомавируса (JC) после иммуномодуляторной или иммуносупрессивной терапии после лечения онкологического новообразования, операций по пересадке органов.
У детей появление патологии наблюдается после начала терапии хронического лимфолейкоза, болезни Ходжкина.
Передается вирус 1С воздушно-капельным или фекально-оральным способом. У большинства населения наблюдается бессимптомное течение. Провоцирующие факторы:
Магнитно-резонансная томография – единственный способ, позволяющий выявить патологические очаги внутри белого вещества. После появления нарушения зрения, дизартрии, гемипареза, афазии неврологи смогут предположить диагноз. Окончательная верификации возможна только после микроскопического обследования биоптатов головного мозга – участки ткани, взятые из места повреждения.
Дисциркулярная энцефалопатия
Хроническое прогрессирующее течение цереброваскулярной патологии сопровождается диффузными многоочаговыми изменениями, приводящими к гемипарезам, ишемическому инсульту, множественным нейропсихологическим и неврологическим расстройствам.
Прогрессирование дисциркуляторной энцефалопатии связано с дегенерацией тканей, накоплением агрессивных метаболитов.
До использования методов нейровизуализации большую часть причин появления когнитивных расстройств специалисты объясняли дисциркуляторной энцефалопатией. Практика показывает гипердиагностику случаев нозологии. Ядерно-магнитный резонанс указывает только 20% случаев встречаемости очагов белого вещества у пожилых пациентов с сосудистыми заболеваниями.
Основным отличием дисциркулярной разновидности в сравнении с инсультом является поражение не крупных мозговых артерий, а мелких пенетрирующих сосудов, артериол. Диффузные повреждения мелких ветвей вызывает ряд морфологических изменений:
Раннее выявление любой категории предотвращает прогрессирование после назначения правильной поддерживающей терапии.
Особенности перивентрикулярной и резидуальной лейкоэнцефалопатии у детей
Хронический недостаток поступления кислорода, длительная ишемия мозговых тканей приводит к повреждению подкорковых структур, полушарий, мозгового ствола. Патологические очаги обнаруживаются в глубине серого вещества, сопровождаются изменениями подкорковых волокон.
Перивентрикулярная энцефалопатия характеризуется преимущественной локализацией патологических очагов вокруг желудочков мозга.
Резидуальный вид имеет врожденные и приобретенные причины. Провоцирующим фактором у ребенка являются травматические повреждения черепа, воспалительные процессы внутри черепной коробки. Отдельная разновидность – энцефаломиелопатия возникает из-за аномалий строения сосудистой сети мозга.
Симптомы резидуальной энцефалопатии детей:
Практика показывает наличие латентного течения нозологии у новорожденных с весом около четырех килограмм. Клинические симптомы появляются после начала активного кровоснабжения. Случаи появления слабоумия у дошкольников и школьников связаны с травмами черепной коробки.
Сколько живут с энцефалопатией
Длительность жизни определяется клинической формой болезни, скоростью прогрессирования, индивидуальными изменениями организма человека.
Прогрессирующая многоочаговая энцефалопатия сопровождается летальным исходом через 1-3 года после выявления. Поддерживающая терапия увеличивает выживаемость.
Разновидности сосудистого генеза имеют хроническое прогрессирование. Люди с данной разновидностью при грамотной организации лечения живут десятки лет. Сокращает сроки гипертония, выраженные ишемические очаги структуры головного мозга, кровоизлияния внутрь мозга.
Принципы диагностики лейкоэнцефалопатии
Лучшим способом верификации изменений белого и серого вещества головного мозга является МРТ. Лейкоэнцефалопатия локализуется в головном и спинном мозге. На снимках визуализируются участки высокой интенсивности диаметром от трех миллиметров до трех сантиметров неправильной округлой и овальной формы. Расположение очагов в субкортикальных и перивентрикулярных отделах определяет режим Т1 взвешенных последовательностей с дополнительным контрастированием (МР-ангиография). Способ диагностирует атрофию, расширение желудочковых пространств, свежие патологические зоны.
Мультифокальная лейкоэнцефалопатия
МРТ головного мозга при лейкоэнцефалопатии выявляет участки разной интенсивности в мозжечке, стволе, теменно-затылочных и лобных областях. Реже встречается инфратенториальная локализация. Сканирование головного мозга должно сочетаться с обследованием спинномозговой жидкости. Анализ позволяет выявить патологических агентов, являющихся причиной патологии.
Прямое выявление вируса JC, ВИЧ методом ПЦР имеет достоверность близкую к 100%. Если тест отрицательный, подтверждение или исключение диагноза возможно способом биопсии – взятие материала из патологического участка после обнаружения МРТ с трехмерным моделированием.
Обязательна диагностика аутоиммунных состояний, иммунодефицита.
Электронейромиография регистрирует снижение проведения сигнала по слуховым, зрительным, соматосенсорным нервным волокнам. Существует специфические места локализации патологии, выявление которых позволяет предположить патологию с высокой долей вероятности.
Разрушение миелина нервных оболочек, верификация дегенерации аксона – признаки нейродегенеративных процессов. Патологические волны возникают на субклинической стадии до первых выраженных симптомов.
Чтобы выявить патологии вначале развития, следует сделать МРТ. Процедура качественно показывает мягкотканый компонент, насыщенный водой. Жидкость после воздействия магнитным полем начинает резонировать, изменяется радиочастотный сигнал. Регистрация импульса позволяет отобразить графическую картинку на экране монитора после обработки программой.
Звоните нам по телефону 8 (812) 241-10-46 с 7:00 до 00:00 или оставьте заявку на сайте в любое удобное время
Перивентрикулярная лейкомаляция
Перивентрикулярная лейкомаляция — это гипоксически-ишемическая энцефалопатия, характеризующаяся поражением белого вещества головного мозга новорожденных. Состояние чаще возникает у недоношенных, провоцируется патологиями течения беременности и родов, неадекватной респираторной поддержкой в постнатальном периоде. Заболевание проявляется мышечной дистонией, судорожным синдромом, задержкой психомоторного развития. Для диагностики болезни назначается КТ или МРТ мозга, ЭЭГ, допплерография церебральных сосудов. Лечение лейкомаляции включает медикаменты (нейропротекторы, инфузионные растворы, антиконвульсанты), индивидуальный комплекс физиотерапии, массажа, ЛФК.
МКБ-10
Общие сведения
По разным данным, перивентрикулярная лейкомаляция (ПВЛ) встречается у 4,8-9% младенцев, причем среди больных преобладают недоношенные новорожденные (78%). Наибольшая вероятность появления болезни у детей, родившихся на сроке 27-32 недели. По данным аутопсии умерших младенцев, признаки ПВЛ регистрируются чаще — у 50-75%. Заболевание имеет большую значимость в детской неврологии, поскольку может вызывать тяжелые отдаленные последствия, считается ведущей причиной ДЦП.
Причины
Основной этиологический фактор перивентрикулярной лейкомаляции — внутриутробная гипоксия, которая выступает следствием осложнений протекания беременности, материнских факторов риска либо негативного экзогенного воздействия. Также состояние может возникать при перинатальной гипоксии, которая развивается во время родов, в первые дни жизни младенца (при синдроме дыхательных расстройств, врожденных аномалиях сердца и легких, неонатальном сепсисе).
В группе риска наибольшую по численности категорию составляют недоношенные младенцы. Зачастую лейкомаляция выявляется у детей, которое были рождены от матерей с сахарным диабетом, хронической анемией, гипертиреозом либо страдавших от преэклампсии и эклампсии. Состояние возникает при выполнении экстренного кесарева сечения, неадекватном родовспоможении (травмирующие акушерские пособия). Высокая частота лейкомаляции (до 22%) отмечается при сочетании длительного безводного периода с хориоамнионитом у матери.
Патогенез
Поражение головного мозга связано со снижением кровотока в церебральных сосудах, недостаточным поступлением кислорода и питательных ингредиентов. Перивентрикулярная область наиболее чувствительна к этим изменениям, что обусловлено особенностями кровоснабжения, несовершенством процессов ауторегуляции, нейроонтогенетическими особенностями головного мозга у младенцев.
Недоношенные намного чаще страдают лейкомаляцией, поскольку у них на фоне гипоксии не увеличивается церебральный кровоток, как это бывает у рожденных в срок младенцев. В результате этого резко уменьшается кровоток в зоне между вентрикулофугальными и вентрикулопетальными артериями, быстро формируется гиперкапния и ацидоз. Расстройства микроциркуляции проявляются стазом, тромбозом, вне- и внутриклеточным отеком белого вещества.
При перивентрикулярной лейкомаляции в конечном итоге происходит некроз отельных участков мозгового вещества, образование кист, избыточное накопление медиаторов воспаления. Поскольку на 28-32 неделях в норме происходит активная миелинизация белого вещества, а в условиях гипоксии этот процесс не может происходить, недоношенные новорожденные впоследствии имеют серьезные органические поражения ЦНС.
Формирование ПВЛ возможно не только при недостатке кислорода, но и при гипероксии — при проведении ИВЛ, оказании других видов респираторной поддержки. При избыточном поступлении кислорода повышается рН крови в мозговой ткани, что вызывает рефлекторный спазм сосудов, затруднение венозного оттока. Также кислород активизирует процессы свободнорадикального церебрального повреждения.
Симптомы
Как правило, перивентрикулярная лейкомаляция формируется антенатально или на протяжении первых часов после рождения ребенка, поэтому начальные признаки заметны уже в родильном доме, особенно если младенец рожден недоношенным. При обширном повреждении белого вещества происходят нарушения сознания по типу летаргии или комы, однако возможна обратная симптоматика — повышенная возбудимость, оживление безусловных рефлексов, судорожный синдром.
Типичным проявлением патологии являются изменения тонуса мышц. На первом месяце жизни преобладает слабость мускулатуры ног в сочетании с нормальным формированием мышц верхних конечностей. У недоношенных новорожденных часто отмечается тотальная мышечная гипотония. Такие нарушения сохраняются в среднем до 6 месяцев, после чего они сменяются спастическими явлениями — повышением тонуса мускулатуры нижних конечностей, оживлением коленных рефлексов.
Течение перивентрикулярной лейкомаляции имеет неравномерный характер: периоды обострения симптоматики сменяются «мнимым благополучием», когда ребенок развивается относительно нормально. Затем происходит задержка формирования моторных навыков, развиваются различные сенсорные нарушения, дизартрия. 66% детей, особенно недоношенные, страдают от снижения остроты зрения вплоть до полной слепоты вследствие атрофии зрительных нервов.
Осложнения
Перивентрикулярные поражения белого вещества — крайне тяжелое состояние. Недоношенные дети с ПВЛ умирают в 50% случаев еще в период новорожденности, у выживших обычно наступает инвалидность с полной дезадаптацией. Пациенты с длительно сохраняющимся судорожными приступами в 85% случаев имеют грубую задержку психомоторного развития. У перенесших ПВЛ в будущем в 1,5 раза чаще встречаются фебрильные судороги, в 27 раз чаще формируется эпилепсия.
При множественных кистах в перивентрикулярной зоне у 80-97% больных (чаще — недоношенных) возникает детский церебральный паралич (ДЦП), который сопровождается глубоким психоречевым отставанием. Развитие заболевания связано с повреждением центральной части внутренней капсулы, средне- и заднелобных сегментов белого вещества полушарий. Также лейкомаляция вызывает микроцефалию (у 42% пациентов), нейросенсорную тугоухость (у 28% больных).
Диагностика
Постановка правильного диагноза в неонатальном периоде затруднена, что объясняется полиморфностью клинической картины, отсутствием патогномоничных симптомов. При физикальном осмотре выявляется асимметрия мышечного тонуса, патологическое усиление рефлексов, на более поздних этапах — спастическая диплегия. Особую настороженность следует проявлять в отношении детей, родившихся недоношенными. В план обследования новорожденных с подозрением на ПВЛ включаются:
Лечение перивентрикулярной лейкомаляции
Терапия перивентрикулярной лейкомаляции представляет собой сложную задачу, учитывая необратимый характер повреждений белого вещества, частое сочетание гипоксически-ишемической энцефалопатии с поражениями других систем организма у недоношенных. Медикаментозное лечение подбирается на основе ведущих синдромов болезни и включает следующие группы препаратов:
Учитывая высокую частоту резидуальных неврологических явлений, рекомендовано восстановительное лечение. Чтобы улучшить двигательные способности, назначаются курсы массажа, физиотерапии, лечебной физкультуры. Для развития речевых навыков требуются коррекционные занятия у логопеда, дефектолога. Детям с поражением органов чувств нужна помощь тифлопедагога, сурдопедагога. Пациентам с ДЦП необходимы специальные ходунки, костыли, инвалидные коляски.
Прогноз и профилактика
В большинстве случаев лейкомаляция отличается неблагоприятным течением, отличается высоким уровнем смертности во время младенчества. Для выживших детей прогноз напрямую зависит от тяжести органического дефекта перивентрикулярной зоны, своевременности и полноты проведенного лечения. Профилактика ПВЛ включает рациональное ведение беременности, предупреждение родового травматизма, соблюдение протоколов при респираторной поддержке в роддоме, усиленный контроль за развитием недоношенных.
Прогрессирующая многоочаговая лейкоэнцефалопатия
Прогрессирующая многоочаговая лейкоэнцефалопатия (син.: прогрессирующая субкортикальная энцефалопатия, PML) является демиелинизирующей болезнью ЦНС, вызванной реактивацией вируса JC (JCV) у иммуннологически скомпрометированных пациентов, включая пациентов после трансплантации, со злокачественными новообразованиями системы кроветворения или СПИДом. С созданием и совершенствованием высокоактивной антиретровирусной терапии (ВААРТ) заболеваемость и распространенность прогрессирующей многоочаговой лейкоэнцефалопатии уменьшились в несколько раз. Тем не менее патология продолжает встречаться и должна рассматриваться в качестве одного из дифференциальных диагнозов при симптомах поражения ЦНС у ВИЧ инфицированных пациентов.
Недавно, о развитии прогрессирующей многоочаговой лейкоэнцефалопатии сообщалось у пациентов с аутоиммуннными болезнями, у которых проводилась иммуносупрессивная терапия. Несмотря на прекращение иммуносупрессии.
Патогенез (что происходит?) во время Прогрессирующей многоочаговой лейкоэнцефалопатии:
В полушариях большого мозга, мозговом стволе и мозжечке обнаруживают множественные очаги демиелинизации с максимальной плотностью на границе между белым и серым веществом. В основном поражаются олигодендроглиоциты.
Симптомы Прогрессирующей многоочаговой лейкоэнцефалопатии:
Течение и прогноз
Обычно трудно установить момент начала заболевания, особенно если оно развивается на фоне тяжёлого соматического недуга. Течение прогрессирующее, заканчивается летальным исходом. Может протекать остро, приводя к смерти в течение 1 мес.
Диагностика Прогрессирующей многоочаговой лейкоэнцефалопатии:
При ЭЭГ практически всегда выявляется локальное или генерализованное замедление ритма, иногда еще до появления изменений при КТ.
Спинномозговая жидкость чаще не изменена, иногда слегка повышена концентрация белка или IgG, менее чем у четверти больных выявляется цитоз, преимущественно лимфоцитарный и не превышающий 25 в мкл.
При обнаружении олигоклональных иммуноглобулинов, выраженного цитоза, наличия нейтрофилов либо эритроцитов в С спинномозговой жидкости необходимо исключить рассеянный склероз, острый геморрагический лейкоэнцефалит, СПИД-дементный синдром и ВИЧ-миелопатию, менингоэнцефалит, вызванный вирусом varicella-zoster, постинфекционный и поствакцинальный энцефаломиелит.
Окончательный диагноз ставится на основании биопсии или аутопсии. В ткани мозга можно выявить антигены вируса JC (иммуноцитохимически) и ДНК вируса (методами флюоресцентной гибридизации in situ или ПЦР), но они обнаруживаются в ткани мозга и у здоровых людей. Около 80-90% людей среднего возраста имеют антитела к вирусу JC. Он может находиться в мозге или других тканях в латентном состоянии и реактивироваться при ослаблении иммунитета. С другой стороны, возможно развитие прогрессирующей многоочаговой лейкоэнцефалопатии у лиц с ослабленным иммунитетом при первом контакте с вирусом; об этом свидетельствует тот факт, что 10-20% больных на момент установления диагноза серонегативны.
Новые данные в этом отношении могут быть получены при широком применении ПЦР.
Лечение Прогрессирующей многоочаговой лейкоэнцефалопатии:
Общее согласие относительно терапии прогрессирующей многоочаговой лейкоэнцефалопатии пока еще не достигнуто.
Появлялись отдельные сообщения о стабилизации и даже улучшении состояния при лечении цитарабином в/в или интратекально в комбинации с интерфероном а либо без него. Однако проведенное Национальным институтом здоровья кооперированное испытание не подтвердило эффективности цитарабина в сочетании с антиретровирусными препаратами (по сравнению с лечением только антиретровирусными препаратами) при прогрессирующей мультифокальной лейкоэнцефалопатии на фоне ВИЧ-инфекции.
Цидофовир, обладающей анти-JCV активностью in vitro, является наиболее эффективной терапией полиомавирусной болезни у мышей. Несколько сообщений предположили его потенциальную терапевтическую выгоду, принимая во внимание, что другие сообщения не показали клинической эффективности.
Поскольку прогрессирующая многоочаговая лейкоэнцефалопатия скорее является последствием реактивации JCV, чем острой инфекции, в идеале, лекарственное средство должно предотвращать повторную инфекцию глиальных клеток. Недавно, Atwood с коллегами продемонстрировали, что JCV использует серотониновый рецептор 5HT2A, чтобы инфицировать глиальные клетки человека. Антидепрессант миртазапин, который является антагонистом 5HT2A, способен пересекать гематоэнцефалический барьер, связывать существенное количество рецепторов 5HT2A и блокировать репликацию JCV in vitro.
К каким докторам следует обращаться если у Вас Прогрессирующая многоочаговая лейкоэнцефалопатия:
Что такое энцефалопатия и чем она опасна?
Что такое энцефалопатия?

Энцефалопатия бывает врожденной и приобретенной. В каждом случае причинами заболевания становятся разные факторы, но их объединяет устойчивое нарушение мозгового кровообращения.
В случае с новорожденными детьми наличие заболевания не всегда становится очевидным. Как правило, диагноз ставят ближе к году при наличии специфической симптоматики. У взрослых людей широко распространены патологии, вызванные сосудистыми нарушениями. К примеру, при атеросклерозе уменьшается просвет сосудов в результате отложения на их стенках липидов. Приток крови к мозгу снижается, развивается ишемия. В сложных случаях просвет сосуда перекрывается кровяным сгустком или холестериновой бляшкой, появляется инсульт, в результате которого отмирают клетки головного мозга.

У каждой разновидности заболевания свои специфические признаки и методы терапии. По этой причине важно вовремя обратиться к врачу, чтобы пройти диагностику и лечение. Проявления нарушений зависят от того, какая область головного мозга поражена.
Сосудистая энцефалопатия. Возникает в результате нарушений кровоснабжения головного мозга и кислородного голодания клеток. Патология может иметь атеросклеротический или гипертонический характер. В первом случае в кровеносных сосудах присутствуют атеросклеротические бляшки, а во втором отмечается повышенное артериальное давление с осложнением в виде отека головного мозга.
Травматическая. В этом случае энцефалопатия развивается как результат перенесенной черепно-мозговой травмы. При заболевании могут отмечаться дегенеративные, дистрофические, рубцовые изменения тканей головного мозга. Чаще всего патология наблюдается у спортсменов, водителей и пассажиров транспортных средств, а также новорожденных детей.
Лучевая. Заболевание может стать следствием воздействия на головной мозг ионизирующего излучения. Такая разновидность энцефалопатии может наблюдаться у специалистов, участвующих в устранении последствий радиационных аварий, а также у тех, кто работает с соответствующим оборудованием.
Метаболическая (токсическая). Поражение головного мозга может быть вызвано интоксикацией организма на фоне печеночной недостаточности, сахарного диабета, отравления угарным газом, солями тяжелых металлов и пр. Токсическое отравление также приводит к тяжелым неврологическим нарушениям.
Воспалительная. Чаще всего речь идет о воспалительных процессах в стенках кровеносных сосудов. Выраженность и специфика проявлений зависят от пораженной области.
Вакцинная. Это редкая разновидность неврологического расстройства, которое появляется в ответ на введение вакцины. Чаще всего реакция наблюдается на препараты от коклюша.
Дисциркуляторная. Нарушение работы головного мозга возникает из-за постепенно усиливающейся недостаточности кровоснабжения. Дисциркуляторная энцефалопатия напрямую влияет на когнитивные способности и неврологические расстройства.
Резидуальная энцефалопатия (остаточная). В головном мозге происходит структурное изменение тканей вследствие перенесенных ранее травм, ишемической болезни, инфекций.
Губчатая. Эта разновидность энцефалопатии объединяет тяжелые заболевания, при которых мозг превращается в губчатое тело. Среди них можно выделить синдром Гетсмана-Штрауслера-Шейнкера, болезнь Крейтцфельда-Якоба и др.

Для заболевания характерно разнообразие клинических проявлений, которые зависят от причин, вызвавших нарушения работы головного мозга. Энцефалопатия может иметь острое и хроническое течение.
Во втором случае признаки нарушения работы головного мозга проявляются постепенно в виде головных болей, забывчивости, эмоциональной нестабильности.
Болезнь в своем развитии проходит несколько стадий, для которых характерны следующие проявления:

Современные методы обследования позволяют установить локализацию, характер патологии, механизм ее появления. Диагностика может включать:
Анализы крови для определения уровня гормонов, липидов, холестерина, сахара и других элементов, которые могут указывать на развитие дисциркуляторной энцефалопатии.
Реоэнцефалографию (РЭГ) для измерения кровотока в головном мозге, определения эластичности и напряжения стенок сосудов.
Магнитно-резонансную томографию для анализа морфологических изменений тканей головного мозга. МРТ позволяет дифференцировать энцефалографию от других заболеваний нервной системы: болезни Альцгеймера, инсульта, опухолей и др.
Ультразвуковую допплерографию для определения скорости кровотока в отдельном кровеносном сосуде и уточнения местоположения атеросклеротической бляшки. Дает информацию о состоянии церебрального кровообращения.
Можно ли вылечить энцефалопатию?

Заболевание требует длительной курсовой терапии и наблюдения у врача-невролога. Для успешного лечения и устранения симптомов болезни первостепенное значение имеет диагностика причин ее появления.
Острая энцефалопатия является показанием к срочной госпитализации и проведению дезинтоксикационной терапии в условиях стационара. Хроническая форма патологии требует соблюдения определенной диеты и приема лекарств по назначению врача 2?3 раза в год.

Лекарства от гипертонии требуют строгого соблюдения графика приема, как правило, 2?3 раза в сутки. Многим пациентам требуется пожизненное употребление препаратов для нормализации артериального давления. Дозировку и разновидность лекарства должен назначать лечащий врач, поскольку каждое из них действует с различной интенсивностью и по-разному выводится из организма.
Современные гипотензивные лекарства делятся на следующие группы:
ингибиторы АПФ (ангиотензинпревращающего фермента);
прямые ингибиторы ренина;
комбинированные и другие препараты.
Для улучшения обмена веществ головного мозга назначаются «Кавинтон», «Вазобрал», «Коринфар», «Целипрол», «Никошпан», «Пикамилон» и другие препараты различных групп.
Лекарства помогают восстановить мозговое кровообращение и благодаря этому устранить такие симптомы, как:

головная боль и головокружения;
нарушение координации движений;
проблемы с памятью;
перепады настроения и пр.
Основные группы препаратов для улучшения мозгового кровообращения:
корректоры микроциркуляции крови и др.
При энцефалопатии схема лечения разрабатывается индивидуально для каждого пациента с учетом данных лабораторных и инструментальных исследований. Практически все препараты для лечения хронической формы заболевания отпускаются в аптеках по рецепту врача. Помимо перечисленных групп лекарств, пациенту могут быть назначены противосудорожные, антидепрессантные, антиагреганты и другие средства.
Последствия и осложнения энцефалопатии
Длительное откладывание лечения приводит к обширному повреждению головного мозга. По мере усугубления заболевания у пациента могут отмечаться:
постоянные головные боли;
ухудшение зрения и слуха;
расстройства координации движений;
тремор конечностей, тик, судороги;
расстройство половой функции;
вегетососудистая дистония и многое другое в зависимости от области поражения мозга.

Для успешного лечения, устранения симптоматики болезни и предотвращения дегенеративных процессов в головном мозге пациенту рекомендуется:
регулярно заниматься спортом для поддержания организма в тонусе.
При своевременном обращении к врачу и обнаружении энцефалопатии на ранних стадиях прогноз положительный. Эффективность лечения во многом будет зависеть от причин патологии. Тяжелые сердечно-сосудистые (ишемия, инсульт, инфаркт) и неврологические (остеохондроз, черепно-мозговые травмы) заболевания могут потребовать пожизненной курсовой терапии. В каждом случае программу лечения и профилактики должен составлять лечащий врач.