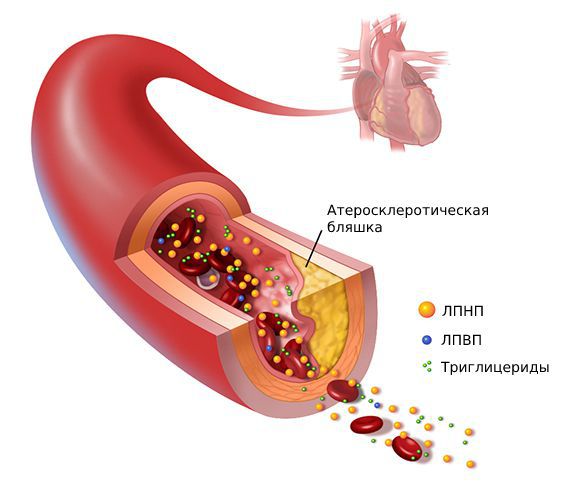
ПРИНЦИПЫ ЛЕЧЕНИЯ нарушений липидного обмена
Необходимость коррекции нарушений липидного обмена в настоящее время не вызывает сомнений.
Необходимость коррекции нарушений липидного обмена в настоящее время не вызывает сомнений. Многочисленными исследованиями, проведенными до начала 90-х годов, доказана возможность снижения уровня холестерина (ХС), триглицеридов (ТГ) и нормализации показателей липидного обмена на фоне гипохолестеринемической терапии.
Но всегда ли выраженное снижение общего холестерина (ОХ) и холестерина липопротеидов низкой плотности (ХС-ЛПНП) способствует улучшению жизненного прогноза?
В исследовании CARE было показано, что снижение ХС-ЛПНП ниже уровня 3,2 ммоль/л не влекло за собой дальнейшего снижения уровня смертности. В то же время, согласно исследованию POST-CABGT, куда включались больные после операции аортокоронарного шунтирования (АКШ), при снижении холестерина ЛПНП до уровня менее 2,6 ммоль/л (по сравнению с больными с уровнем 3,4-3,5 ммоль/л) необходимость в повторных операциях АКШ сокращается на 29%. Аналогичные результаты были получены в ходе исследования CARS, куда включались больные с ИБС, относительно нормальным уровнем ОХ (от 4,1 до 5,6 ммоль/л) и средним уровнем ХС-ЛПНП (3,17 ммоль/л). В настоящее время целью гипохолестеринемической терапии при вторичной профилактике ИБС европейские кардиологи считают достижение уровня холестерина ЛПНП менее 3,0 ммоль/л, а американские — менее 2,6 ммоль/л.
Показана эффективность как медикаментозных, так и немедикаментозных методов коррекции уровня дислипидемий. При этом любую коррекцию следует начинать с устранения факторов риска, способствующих прогрессированию атеросклероза, таких как курение, гиподинамия, а также с нормализации индекса массы тела.
В случаях возникновения дислипидемии на фоне таких заболеваний, как гипотиреоз, нефротический синдром и др., необходимо прежде всего начать лечение основного заболевания.
 |
| Рисунок. Нормализация уровня липопротеидов в крови позволяет уменьшить потребность в хирургическом лечении |
Одним из основных методов немедикаментозного лечения является соблюдение диеты с ограничением употребления жиров животного происхождения и легкоусваиваемых углеводов, ограничение калорийности питания. В ходе исследования Veterans Administrations больным была предписана диета с увеличенным содержанием полиненасыщенных жирных кислот и уменьшенным содержанием животных жиров (по сравнению с пациентами, соблюдавшими стандартную североамериканскую диету). Диетотерапия на протяжении восьми лет привела к снижению уровня ОХ на 12,7% и уменьшению частоты развития инфарктов миокарда (ИМ) на 20%. При этом не было отмечено снижения общей смертности в какой-либо из групп больных. В исследовании Finnish Mental Hospital Study за шестилетний период наблюдения у 450 больных обоего пола в возрасте 34—64 лет на фоне диеты с низким содержанием холестерина отмечено снижение его уровня в крови на 15%. При этом достижение среднего уровня ОХ в 5,8 ммоль/л не вызывало достоверного снижения общей смертности или смертности от сердечно-сосудистых заболеваний. В исследовании DART, включавшем более 2000 больных, средний возраст которых был 56,5 лет, соблюдение диеты на протяжении двух лет повлекло за собой недостоверное снижение уровня общей смертности и смертности от ИБС. Однако ишемические события (нефатальные ИМ) встречались даже чаще в группе больных, соблюдавших диету. Наиболее крупное исследование Minnesota Coronary Survey, включавшее около 5000 пациентов обоего пола и любого возраста со средним исходным уровнем ОХ 5,3 ммоль/л, выявило, что соблюдение только гипохолестериновой диеты привело к снижению уровня ОХ на 14,5% за 4,5 года по сравнению с контрольной группой, придерживавшейся стандартной диеты. Это исследование также не показало уменьшения развития сердечно-сосудистых заболеваний и снижения общей смертности.
На наш взгляд, лечение больных с гиперхолестеринемией и гипертриглицеридемией необходимо во всех случаях начинать с устранения факторов риска и назначения гипохолестеринемической диеты. При этом, если диета эффективна, то рассматривать ее в качестве монотерапии можно только в том случае, если больной действительно в состоянии соблюдать диету в течение всей оставшейся жизни. Однако больным с ИБС в период обострения заболевания и при наличии выраженной гиперхолестеринемии показано, наряду с соблюдением диеты, одновременное назначение гипохолестеринемических препаратов в адекватных дозах. Нормализация уровня показателей липидного обмена только на фоне диеты у таких больных не представляется возможной, а несвоевременное начало лечения может привести к развитию неблагоприятных осложнений.
При отсутствии «острой» ситуации неэффективность немедикаментозной терапии в течение трех месяцев является показанием к подключению медикаментозной терапии. Следует отметить, что применение гиполипидемических препаратов, к какому бы классу они ни относились, ни в коем случае не означает отказа от соблюдения диеты. Наоборот, любая гипохолестеринемическая терапия будет эффективна при условии соблюдения диеты.
В настоящее время используются пять основных классов лекарственных средств, применяемых с учетом механизма их действия, эффективности и наличия побочных эффектов, а также противопоказаний при том или ином типе дислипидемии.
I Статины.
II Никотиновая кислота и ее производные.
III Фибраты.
IV Секвестранты желчных кислот.
V Антиоксиданты.
На сегодняшний день влияние на общую смертность, смертность от сердечно-сосудистых заболеваний и риск развития сердечно-сосудистых осложнений доказано только для препаратов из группы статинов. Действие этих препаратов основано на ингибировании фермента 3-гидрокси-3-метилглутарил-коэнзим-А (ГМГ-ко-А)-редуктазы. Благодаря торможению биосинтеза холестерина в печени и кишечнике статины уменьшают внутриклеточные запасы холестерина. Это вызывает образование повышенного количества рецепторов к ЛПНП и ускоряет удаление их из плазмы.
Другие механизмы действия статинов на эндотелий сосудов, агрегацию тромбоцитов окончательно не изучены.
Эффект статинов преимущественно направлен на снижение уровня холестерина ЛПНП и общего холестерина. В работах последних лет показано, что применение высоких доз статинов может заметно снижать уровень триглицеридов, и конкурировать с эффектом фибратов.
На сегодняшний день в России зарегистрированы следующие препараты из группы статинов:
По данным W. C. Roberts (1997), доза симвастатина в 10 мг приблизительно эквивалентна 20 мг ловастатина или правастатина и 40 мг флювастатина. Согласно его исследованиям, двукратное повышение дозы статинов по отношению к начальной дозе приводит к дополнительному снижению ОХ приблизительно на 5% и ХС-ЛПНП на 7%. При этом повышение уровня холестерина липопротеидов высокой плотности (ХС-ЛПВП) не зависит от увеличения дозы препарата.
Препараты из группы статинов используются для первичной и вторичной профилактики ИБС. Под вторичной профилактикой понимают применение препаратов у больных с доказанной ИБС.
Нам представляется, что наибольшая эффективность при назначении статинов должна определяться не только по уровню исходных показателей липидного обмена, но и по сочетанию суммарного риска развития сердечно-сосудистых осложнений и клиническому течению заболевания. Так, у больных с острым коронарным синдромом клинический эффект применения статинов может быть более выраженным, чем у больных со стабильной стенокардией, а тактика должна быть более агрессивной. Однако эти выводы основаны на нашем практическом опыте, они не получили пока подтверждения в ходе многоцентровых рандомизированных исследований.
Статины, так же как аспирин и β-блокаторы, относятся к средствам, влияющим на прогноз заболевания у больных с ИБС.
Эффективность применения статинов доказана также в ходе исследований, посвященных первичной профилактике.
Исследования 4S, CARE, LIPID, WOSCOPS, AFCAPS/TEXCAPS и другие демонстрируют действенность терапии статинами для вторичной и первичной профилактики ИБС. При этом влияние статинов на «конечные точки» при вторичной профилактике более выражено и экономически более оправданно. Поэтому применение статинов у больных с диагностированной ИБС в сочетании с дислипидемиями может быть рекомендовано всем больным. Эффективность терапии статинами выше в группе больных с более выраженными нарушениями липидного обмена. Развитие «коронарных событий» у ряда больных ИБС на фоне нормальных значений показателей липидного обмена указывает на многофакторность генеза этих осложнений и подчеркивает значение не только уровня дислипидемии, но и совокупности ряда факторов, важнейшими из которых являются клинические проявления обострения заболевания.
Одной из возможных причин эффективности гипохолестеринемических препаратов в профилактике ИБС является продемонстрированная в ряде работ их способность к замедлению прогрессирования и даже возможность регресса атеросклеротического процесса. Эти эффекты изучались путем измерения диаметра сосудов с помощью артериографии или внутрисосудистого ультразвукового исследования.
В исследовании MAAS у больных с ИБС лечение симвастатином в дозе 20 мг в течение четырех лет позволило выявить статистически достоверное уменьшение развития новых стенозов коронарных артерий и регресс уже имевшихся коронарных стенозов; просвет сосудов увеличивался от 0,06 до 0,17 мм при наличии исходного стеноза более 50%.
Замедление прогрессирования или регресс атеросклероза достигаются благодаря интенсивной и агрессивной гипохолестеринемической терапии при значительном снижении уровня ХС-ЛПНП. Наибольшей гипохолестеринемической активностью в одинаковой дозировке обладают симвастатин и аторвастатин. В исследовании SMAC применение аторвастатина и симвастатина в дозе 10-20 мг в сутки позволило почти у 50% больных с ИБС и исходным уровнем ХС-ЛПНП от 4,2 до 7,8 ммоль/л достичь целевого уровня на фоне 52 недель лечения. При этом эффект аторвастатина наступал несколько быстрее, и через 16 недель лечения он был достигнут у 46% больных по сравнению с 27% на фоне лечения симвастатином. К концу года эта разница нивелировалась, составив 50% при лечении аторвастатином и 48% на фоне лечения симвастатином, и была статистически недостоверной. Это исследование показало выраженную гипохолестеринемическую эффективность обоих статинов и примерно одинаковый эффект через год лечения тем и другим препаратами. При этом в большинстве европейских стран стоимость симвастатина была несколько ниже, чем аторвастатина. В данном исследовании не наблюдалось каких-либо серьезных побочных эффектов, потребовавших отмены препаратов.
Другим важным гиполипидемическим средством, используемым для нормализации липидного обмена, является никотиновая кислота и ее производные (ниацин). По мнению В. Парсона, преимущество этой группы препаратов в том, что «они все делают так, как надо». Наряду со снижением уровня ОХ и ХС-ЛПНП препараты этой группы снижают уровень триглицеридов и успешнее, чем любые другие гиполипидемические средства, увеличивают уровень ХС-ЛПВП. Эти препараты обладают и рядом других преимуществ. Например, они снижают уровень липопротеина «а», которому придается большое значение в качестве важного самостоятельного фактора риска развития таких осложнений, как инфаркт и инсульт. Препараты никотиновой кислоты и ее производные уменьшают уровень ЛПНП, воздействуя преимущественно на мелкие, наиболее атерогенные их частицы. Эти лекарственные средства увеличивают уровень ХС-ЛПВП за счет фракции ЛПВП2, которая является наиболее активной в плане удаления липидов из бляшек, и тем самым препятствуют прогрессированию атеросклероза.
В ряде работ показана возможность уменьшения сердечно-сосудистых осложнений и общей смертности при применении ниацина.
В программе сердечно-сосудистых препаратов (США) сравнивался ряд лекарственных средств, изменяющих уровень холестерина. Исследование проводилось у мужчин 30—65 лет, имевших в анамнезе хотя бы один сердечный приступ. Изучалось влияние эстрогенов, тироксина, клофибрата и ниацина. Каждая группа состояла приблизительно из 1100 больных, а группа плацебо была в два раза больше. Предполагаемая продолжительность исследования составляла 5 лет, но для первых двух средств оно было досрочно прекращено в связи с развитием большого количества инфарктов и других осложнений. Клофибрат не оказывал благоприятного воздействия на уровень смертности и количество сердечно-сосудистых осложнений. Таким образом, никотиновая кислота была единственным средством, при применении которого удалось уменьшить число нефатальных инфарктов примерно на 27%, инсультов — на 24%, количество госпитализаций по поводу сердечно-сосудистых осложнений — на 12% и необходимость в хирургическом лечении на сердце и сосудах — на 46%.
Тенденция к снижению смертности, отмечавшаяся за 5 лет наблюдения на фоне приема ниацина, оказалась статистически недостоверной.
Важным преимуществом этой группы лекарственных средств является относительно низкая их стоимость по сравнению с другими гиполипидемическими препаратами. В настоящее время чаще всего применяются медленно высвобождающиеся формы никотиновой кислоты. Они обеспечивают более длительное и постепенное высвобождение активного соединения и обусловливают значительное снижение побочных эффектов. К этим препаратам относятся:
Эффективность этих препаратов также несколько различается. По данным Figge с соавт. (1988), биодоступность препаратов ниацина пролонгированного действия, имеющих восковую матрицу, почти в два раза выше, чем с дозированным высвобождением. Поэтому эффективность эндурацина в дозе 1500 мг в сутки в отношении ХС-ЛПНП, ХС-ЛПВП, по данным Д. Кинана, была даже несколько большей, чем при приеме 3000 мг ниацина с пролонгированным высвобождением.
Крупномасштабные исследования по сравнению характеристик эффективности, дозировки, побочных эффектов различных пролонгированных форм никотиновой кислоты до настоящего времени отсутствуют.
Максимальная суточная доза препаратов никотиновой кислоты не должна превышать 6 г, а для эндурацина — 3 г. Увеличение дозы не привело к улучшению результатов, а количество побочных эффектов при этом может увеличиваться. Общая особенность всех препаратов никотиновой кислоты — это необходимость постепенного повышения дозы под контролем уровня показателей липидного обмена даже при хорошей их переносимости. Чаще всего лечение начинается с дозы 500 мг в сутки в течение недели, затем 500 мг два раза в день в течение еще 1-3 недель, а затем происходит корректирование дозы в зависимости от показателей липидного обмена. Для уменьшения побочных реакций препараты применяют во время еды, ограничивают употребление горячих напитков, а также при появлении первых признаков гиперемии добавляют небольшие дозы аспирина (100—325 мг), что помогает уменьшить эти проявления в первые 3-4 дня до последующего полного их исчезновения.
Наиболее часто встречающиеся побочные эффекты при приеме ниацина — это чувство жара в виде «приливов» и кожный зуд, а также чувство гиперестезии и парестезии; запоры, диарея, головокружение, сердцебиение, нарушение аккомодации, сухость кожных покровов или нарушение ее пигментации. Все эти побочные эффекты составляют от 2 до 7%
(Д. Кинан) и достоверно не отличаются от побочных эффектов в группе плацебо. Обычно для контроля за нежелательными осложнениями со стороны печени каждые четыре недели проводятся биохимические исследования. Появление тошноты, рвоты или других недомоганий требует временной отмены препарата и дополнительного исследования печеночных проб. При этом незначительное повышение уровня АСТ, АЛТ, ЛДГ, ГГТП при лечения ниацином допускается. Кроме печеночных проб, при лечении препаратами никотиновой кислоты должны регулярно контролироваться уровень сахара, мочевой кислоты.
Использование других групп лекарственных препаратов, таких как фибраты, ионообменные смолы (секвестранты желчных кислот) и антиоксиданты, также позволяет в целом ряде случаев улучшить нарушенные показатели липидного обмена. Однако до настоящего времени не получены данные об их влиянии на общую смертность, смертность от сердечно-сосудистых заболеваний, развитие сердечно-сосудистых осложнений, необходимость в хирургических методах лечения, частоту госпитализаций и т. д. Ведущиеся в последнее время крупномасштабные исследования по применению фибратов и антиоксидантов, возможно, позволят более точно определить их роль и место в лечении дислипидемий у широкого контингента пациентов.
По вопросу литературы обращайтесь на кафедру терапии и подростковой медицины РМАПО по тел. (095) 945-48-70
8 мифов о холестерине: ответы на самые важные вопросы
Миф №1. Высокий уровень холестерина не передается по наследству
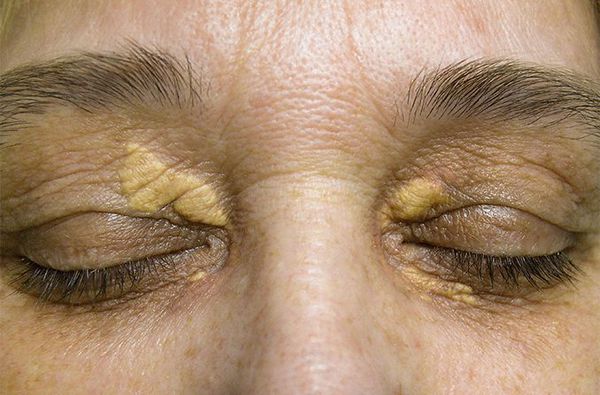
Семейная гиперхолестеринемия — генетическое заболевание, вызванное рядом мутаций в гене рецептора липопротеина низкой плотности на 19-й хромосоме. Этот генетический сбой влияет на способность печени эффективно регулировать уровень «плохого» холестерина, то есть липопротеинов низкой плотности (ЛПНП). Это приводит к повышенным общим показателям холестерина и может спровоцировать риск сердечно-сосудистой катастрофы (инфаркт, инсульт).
Наследуются разные формы заболевания. В случае аутосомно-рецессивного наследования заболеет ребенок, получивший два патологических гена от каждого родителя, и тогда гиперхолестеринемия проявится еще в детском возрасте. Такое состояние ребенка требует обязательного медикаментозного лечения.
При аутосомно-доминантном типе наследования заболевания может быть два варианта проявления болезни. Когда ребенок получает от родителя один патологический ген, заболевание протекает «мягче» и позже проявляется. Когда он наследует два патологических гена, заболевание возникает в раннем детском возрасте и протекает тяжелее.
Кроме этих форм, существуют формы первичной гиперхолестеринемии других типов наследования и приобретенная гиперхолестеринемия. Они легче поддаются лечению.
Миф №2. Холестерин поступает в организм только с пищей
80 % холестерина синтезируется в организме. Поэтому отказ от продуктов, содержащих холестерин, кроме проблем ничего не даст. Ежедневно тело синтезирует примерно 1000 мг холестерина, необходимого для пищеварения, развития клеток, производства витаминов и гормонов.
Повышение уровня холестерина и развитие гиперхолестеринемии возможны при чрезмерном употреблении продуктов с повышенным содержанием насыщенных жиров (сливочное масло, жирное мясо, яйца, сыр) и транс-жиров (жареные продукты, весь фаст-фуд) на фоне нарушений в работе печени.
Миф №3. Холестерин выполняет второстепенную функцию в организме
Холестерин — важнейший компонент жирового обмена и структурная часть гормонов, например, эстрогена и тестостерона, витамина D, желчных кислот, необходимых для переваривания жиров; он используется для построения мембран клеток. В крови холестерин находится в свободном и связанном состоянии с белками. Липопротеины низкой плотности (ЛПНП) — комплексы холестерина с меньшим количеством белка («плохой» холестерин). Их уровень увеличивается в крови в случае нарушений обмена веществ, ведущих к атеросклерозу.
Липопротеины высокой плотности (ЛПВП) — высокобелковые комплексы холестерина («хороший» холестерин) — обладают защитными свойствами для сосудов.
Норма холестерина ЛПВП — 0,-9-1,9 мМ/л. Снижение показателей с 0,9 до 0,78 мМ/л в четыре раза повышает риск развития атеросклероза. Увеличение показателей в большую сторону наблюдается на фоне интенсивной физической активности, под влиянием лекарств, снижающих общий уровень содержания липидов.
Норма холестерина ЛПНП — менее 3,5 мМ/л. Повышение концентрации ЛПНП (выше 4,0 мМ/л) свидетельствует об ожирении, снижении функции щитовидной железы; может быть на фоне приема бета-блокаторов, мочегонных препаратов, контрацептивов. Снижение ниже 3,5 мМ/л возникает в результате голодания, заболеваний легких, анемии, злокачественных новообразований.
Миф № 4. Повышенное содержание холестерина в крови провоцирует атеросклероз
Увеличение концентрации холестерина — гиперхолестеринемия — достоверный факт развития атеросклероза. Высокие риски атеросклероза коронарных артерий наблюдаются уже при величинах свыше 5,2-6,5 ммоль/л (200-300 мг/дл) — это пограничная зона или зона риска. Показатели 6,5-8,0 ммоль/л свидетельствуют об умеренной, а свыше 8,0 ммоль/л о выраженной гиперхолестеринемии. Безопасным считается уровень менее 5,2 ммоль/л (200 мг/дл). В этом случае риск атеросклероза минимальный.
Миф №5. Гиперхолестеринемия не лечится
Гиперхолестеринемия лечится, в том числе семейная. Для этого применяют комплексные методы терапии. В первую очередь назначают статины, фибраты – специальные липидосодержащие препараты, которые уменьшают количество холестерина в крови, тем самым снижая риск осложнений, возможных при атеросклерозе. Из немедикаментозных методов применяют диету и физические нагрузки для нормализации веса и профилактики ожирения, отказ от вредных привычек (употребление алкоголя, курение).
Миф №6. Занятия спортом могут понизить уровень «плохого» холестерина
Если риск развития сердечно-сосудистых заболеваний и гиперхолестеринемии по семейной линии минимальный, то уменьшить показатели «плохого» холестерина помогут занятия фитнесом. Так, например, было доказано, что через три недели занятий у женщин с диабетом II типа уровень липопротеинов низкой плотности (ЛПНП) снизился на 21%, а уровень триглицеридов — на 18%.
Однако не стоит экспериментировать с физическими нагрузками, если у вас диагностированы стенокардия, заболевания периферических артерий, высокие уровни «плохого» холестерина. В этом случае в первую очередь рекомендован прием лекарственных препаратов, а потом уже зарядка.
Миф №7. Существуют продукты, снижающие уровень холестерина в крови
При повышенном риске развития гиперхолестеринемии разумно ограничить до физиологического минимума продукты, содержащие насыщенные жиры (жирные сорта мяса, сливочное масло, яйца, сыр). Это действительно может привести к снижению уровня общего холестерина в крови. Однако многие заменяют насыщенные жиры полиненасыщенными. Доказано, например, что омега-6 жирные кислоты понижают уровень «хорошего» холестерина (ЛПВП). Они содержатся в маслах: льняном, виноградных косточек, кунжутном, арахисовом, кукурузном. Многие считают эти виды масел более полезными, чем подсолнечное. На самом деле, здоровая альтернатива – это оливковое масло, которое помогает снизить уровень холестерина и ЛПНП, не снижая уровень «хороших» ЛПВП. Таким же эффектом обладают морская рыба жирных сортов и оливки.
Миф №8. До 40 лет анализы на холестерин можно не делать
Контролировать уровень холестерина, ЛПВП, ЛПНП, триглицеридов необходимо с 25 лет. Малоподвижный образ жизни, нездоровые перекусы, пристрастие к курению, алкоголю, который оказывает повреждающее действие на печень, могут приводить к повышению уровня холестерина. Важно понимать, что гиперхолестеринемия, уровень более 5,2 ммоль/л, в четыре раза повышает риск развития атеросклероза, ишемической болезни сердца, артериальной гипертензии.
Чтобы пройти обследование и узнать, в норме ли показатели липидов, в СИТИЛАБ можно выполнить комплексные профили тестов:
Он рекомендуется всем, но особенно тем, у кого есть лишний вес.
В состав профиля входят 8 показателей, в том числе общий холестерин, ЛПВН, ЛПНП, а также триглицериды, липопротеин А, аполипротеин А1 и B и индекс атерогенности, который отражает баланс между «плохим» и «хорошим» холестерином.
Что такое гиперлипопротеинемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 24 года.
Определение болезни. Причины заболевания
Это состояние является частным случаем дислипидемии.
Заболевание может долго протекать без симптомов и выявляться случайно после сдачи анализов. При длительном течении болезни развивается атеросклероз, который приводит к сужению сосудов. Симптомы зависят от того, какие артерии поражены:
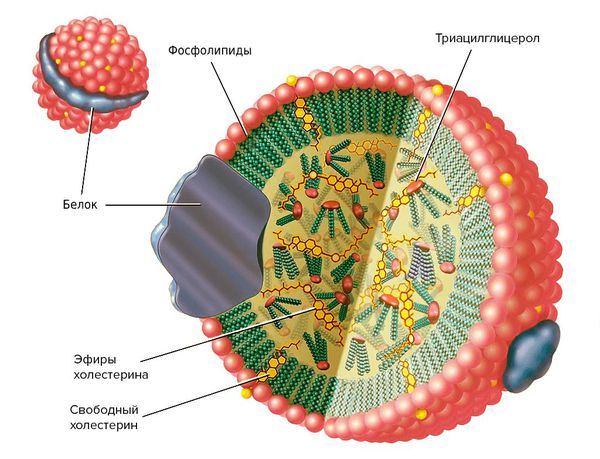
Липопротеины — это растворимые в воде частицы, состоящие из жиров (липидов) и белков (апопротеинов). Они очень важны для организма, поскольку переносят витамины, гормоны и жиры, которые поступают с пищей и синтезируются в печени.
Распространённость
Причины гиперлипопротеинемии
Гиперлипопротеинемии бывают первичными и вторичными. Первичные формы имеют врождённую природу, но встречаются довольно редко: ими страдают 0,25 % населения.
К врождённым гиперлипидемиям относятся:
Вторичные гиперлипопротеинемии обусловлены различными заболеваниями, приёмом некоторых лекарств и неправильным образом жизни.
Наиболее часто заболевание развивается при сахарном диабете, хронической почечной недостаточности, нефротическом синдроме, гипотиреозе, ожирении, желчнокаменной болезни, холестазе, анорексии, частичной или полной потере жировой ткани (липодистрофии), болезнях накопления гликогена, сильном стрессе, сепсисе, беременности, остром гепатите, системной красной волчанке и лимфоме.
Лекарства, которые могут привести к гиперлипопротеинемии:
К развитию гиперлипопротеинемии часто приводит неправильный образ жизни на фоне хронических заболеваний. К неблагоприятным факторам относятся:
Также важно отметить причины, из-за которых снижается уровень ЛПВП. Помимо курения, к ним относятся недостаточное питание и ожирение. Концентрация защитных липопротеинов может уменьшаться при приёме бета-блокаторов и анаболических стероидов.
Уровень общего холестерина может быть выше нормы и у здоровых людей, например при неправильной подготовке к анализу крови и во время беременности.
Гиперлипопротеинемия при беременности
У беременных женщин уровень общего холестерина повышается в 1,5–2 раза. Он резко возрастает в начале II триместра, когда активно формируется плацента. Холестерин — это основа для её клеток, поэтому чем больше срок беременности, тем выше его уровень.
Симптомы гиперлипопротеинемии
Гиперлипопротеинемия может длительное время протекать бессимптомно. Повышенный уровень вредных липидов выявляется при анализах, но клинические симптомы долго не возникают.
При врождённых гиперлипопротеинемиях, вызванных генетическими факторами, симптомы появляются рано. Уровень холестерина при врождённых формах болезни всегда выше 6,5 ммоль/л. Он колеблется от 7 до 13 ммоль/л и выше.
Симптомы первичной гиперлипопротеинемии
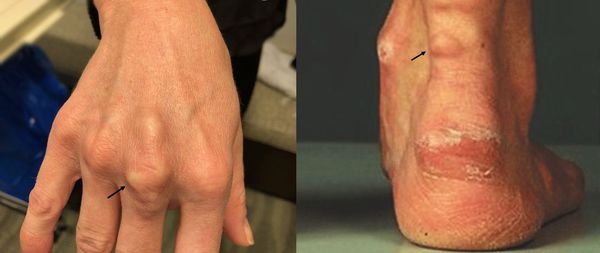
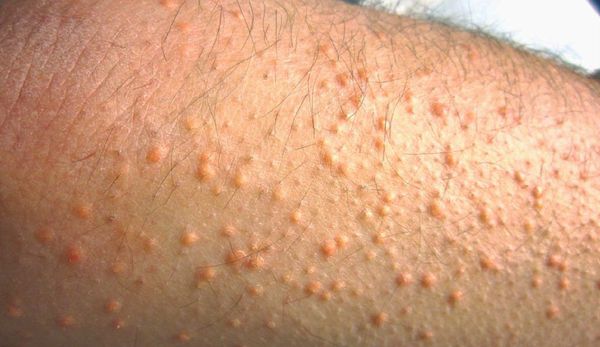
К характерным проявлениям гомозиготной семейной гиперхолестеринемии, при которой человек наследует дефектный ген от обоих родителей, относятся:
При семейной гипертриглицеридемии в крови повышается уровень триглицеридов (до 2,8–8,5 ммоль/л) и липопротеинов очень низкой плотности.
Симптомы вторичной гиперлипопротеинемии
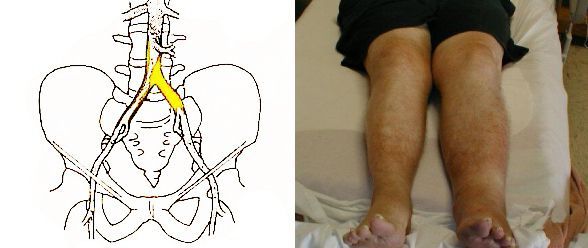
При вторичных гиперлипопротеинемиях симптомы зависят от расположения поражённых атеросклерозом артерий, степени и количества вовлечённых сосудов.
Долгое время уровень вредных липопротеинов растёт, а содержание защитных липопротеинов снижается, но симптомы отсутствуют. Они появляются по мере развития атеросклероза.
К таким признакам относятся:
В зависимости от того, какие артерии повреждены атеросклерозом, возникают следующие симптомы:
Патогенез гиперлипопротеинемии
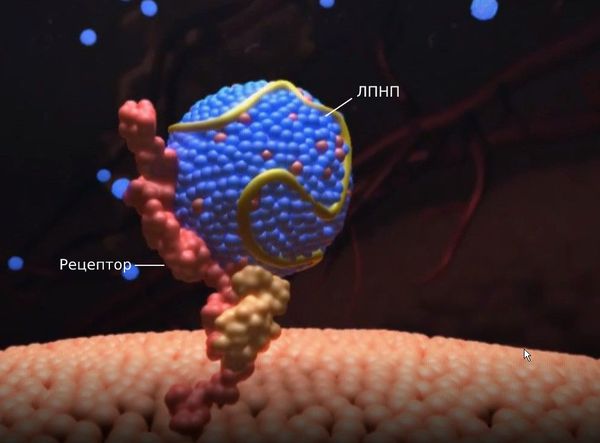
Первичные гиперлипопротеинемии вызваны мутациями в генах, которые ответственны за образование и работу рецепторов к липопротеинам низкой плотности. При гетерозиготной форме семейной гиперхолестеринемии ЛПНП-рецепторы могут быть наполовину полноценными, а при гомозиготной форме — практически полностью отсутствовать. Из-за этого дефекта рецепторы не захватывают липопротеины, они хуже распадаются и не выводятся из организма, поэтому их уровень в крови растёт.
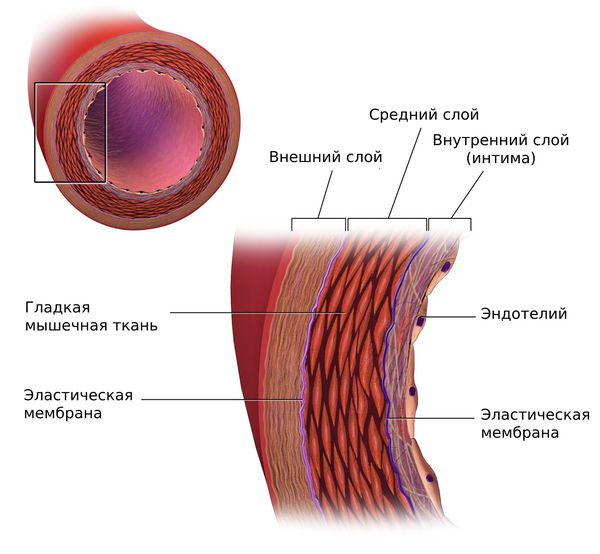
При вторичных гиперлипопротеинемиях повреждается внутренняя оболочка артерий и в неё активно проникают липопротеины.
Липопротеины подразделяются на два вида:
Атерогенность зависит от размеров и физико-химических свойств липопротеиновых частиц.
Липопротеины очень низкой плотности и липопротеины низкой плотности (ЛПОНП и ЛПНП) являются атерогенными и проникают во внутреннюю оболочку артерий (интиму) при повреждении эндотелия.
Дисфункцию эндотелия артерий вызывают:
Под влиянием этих факторов эндотелий разрыхляется и истончается. Расширяются щели между клетками, возникает отёк, клетки и волокнистые структуры внутренней оболочки артерий разъединяются, и частицы атерогенных липопротеинов проникают в интиму артерий.
Затем к этим частицам присоединяется глюкоза. Процесс модификации липопротеинов называется гликозилированием, или гликированием. Он особенно интенсивен при сахарном диабете и избытке глюкозы в крови. В результате нарушается взаимодействие ЛПНП с рецепторами клеток, замедляется распад липопротеинов и, следовательно, развивается гиперлипопротеинемия. Гликирование защитных ЛПВП ускоряет их распад.
Второй путь модификации липопротеинов низкой плотности — пероксидация, или перекисное окисление. Это важнейший фактор развития атеросклероза. В организме постоянно образуются свободные радикалы: ионы, атомы или молекулы с одним неспаренным электроном на своей орбите. Поскольку у них есть свободное место для электрона, они стремятся отнять его у других молекул. Так окисляются любые соединения, с которыми они соприкасаются. Пероксидация ЛПНП делает их высокоатерогенными.
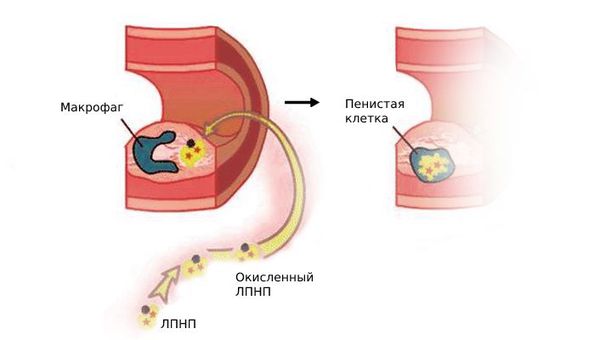
Следующий этап атерогенеза — пропитывание интимы артерий циркулирующими лейкоцитами (моноцитами), которые трансформируются в макрофаги. Они захватывают модифицированные ЛПНП, содержание холестерина в макрофагах быстро нарастает, и они превращаются в пенистые клетки.
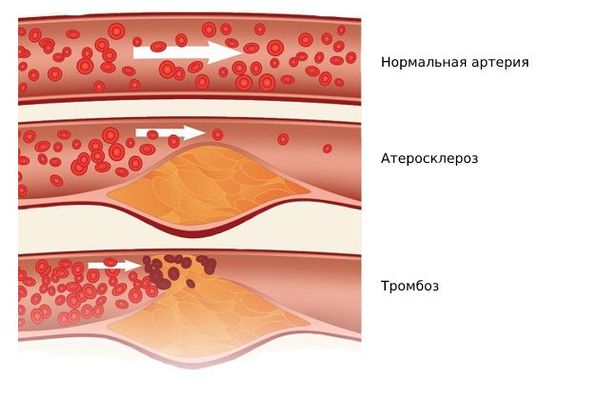
Пенистые клетки остаются в интиме артерий и погибают. При этом они выделяют накопленный холестерин, который образует липидные пятна и полоски, а затем атеросклеротические бляшки.
Одним из наиболее серьёзных осложнений атеросклероза является тромбоз в области бляшки — частичная или полная закупорка артерии тромбом. Образованию тромба предшествуют надрывы и разрывы фиброзной покрышки бляшки, а также повреждение эндотелия самой бляшкой. Иногда атеросклеротическая бляшка становится источником эмболий, при которых её оторвавшийся кусочек закупоривает какой-либо сосуд.
Осложнением атеросклеротической бляшки также является атерокальциноз — отложение солей кальция в стенке сосудов.
Классификация и стадии развития гиперлипопротеинемии
Наиболее распространена классификация липопротеинов в зависимости от плотности:
По участию в развитии атеросклероза липопротеины подразделяются на три класса:
Типы гиперлипопротеинемии
Гиперлипопротеинемии подразделяются на следующие типы:
Также широко применяется классификация гиперлипопротеинемий, предложенная Фредриксоном и соавторами в 1967 году:
Осложнения гиперлипопротеинемии
Диагностика гиперлипопротеинемии
Диагностика гиперлипопротеинемий состоит из осмотра, лабораторных исследований и инструментальных методов.
Осмотр
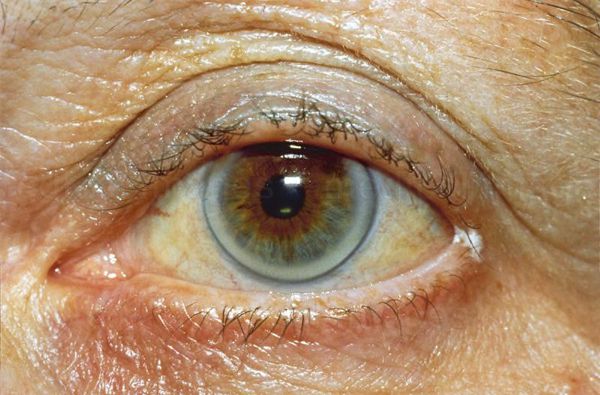
При осмотре врач обращает внимание на признаки, указывающие на нарушение обмена липидов:
Измерение артериального давления
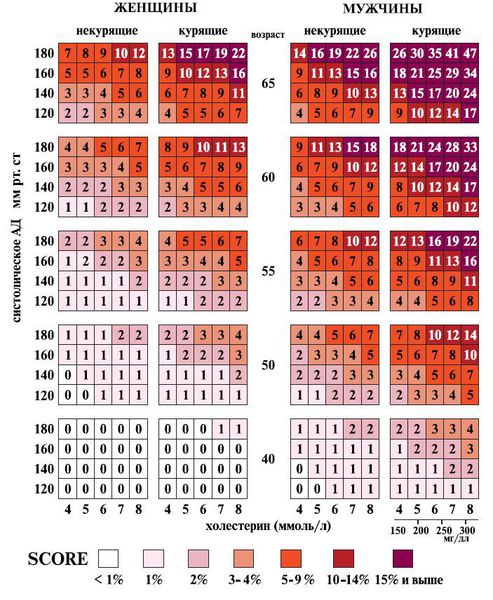
Шкала SCORE — это тест-калькулятор для оценки сердечно-сосудистого риска.
Сердечно-сосудистый риск зависит от сочетания следующих факторов:
По шкале SCORE пациенты попадают в категории низкого, умеренного, высокого и очень высокого риска.
Полученное значение показывает вероятность смерти от сердечно-сосудистого заболевания в ближайшие 10 лет.
Также всем пациентам необходимо проверить состояние печени. Для этого исследуется уровень печёночных ферментов (АСАТ, АЛАТ). Анализ позволяет определить, можно ли назначать статины — препараты для снижения уровня липопротеинов.
Не менее важно проверить состояние щитовидной железы. Для этого исследуется уровень тиреотропного гормона (ТТГ), так как гипотиреоз может быть причиной нарушений липидного обмена и требует коррекции.
Также при гиперлипопротеинемии необходимо определить уровень глюкозы в крови, поскольку сахарный диабет способствует быстрому развитию атеросклероза.
Инструментальные методы диагностики
Для выявления атеросклероза используются:
Лечение гиперлипопротеинемии
Диета
Если у пациента нет симптомов, то лечение начинают со специальной диеты. Коррекция питания позволяет уменьшить уровень холестерина на 5–10 %.
Важно помнить, что холестерин не только поступает извне, но и образуется в организме. Поэтому полностью отказываться от продуктов, содержащих жиры, не стоит.
Медикаментозное лечение
При сердечно-сосудистых заболеваниях, сахарном диабете, хронической болезни почек и высоком риске по шкале SCORE показан приём препаратов, снижающих холестерин. Однако в ряде случаев пациентам даже с умеренным риском может потребоваться медикаментозная терапия. Она поможет уменьшить вероятность развития атеросклероза.
Группы препаратов для лечения гиперлипопротеинемии:
Статины
Статины (Аторвастатин, Розувастатин, Питавастатин) — это наиболее эффективные средства для снижения холестерина. Они блокируют фермент, который участвует в его образовании и тем самым подавляет выработку холестерина в печени. Статины снижают содержание липопротеинов низкой плотности (ЛПНП) и триглицеридов (ТГ).
Статины предотвращают развитие атеросклероза коронарных и церебральных артерий, а при длительном приёме уменьшают размер бляшек в сосудах. Эти препараты необходимы пациентам с гиперлипопротеинемией и атеросклерозом для профилактики инфаркта миокарда и инсульта.
Перед тем, как начать принимать статины, необходимо определить липидный профиль, а также проверить состояние печени по содержанию в крови печёночных ферментов (АСАТ, АЛАТ). Статины применяют в безопасных дозировках до достижения целевых уровней ЛПНП. Дозировка зависит от кардиоваскулярного риска пациента.
Для оценки безопасности и эффективности назначенной дозы через месяц после начала приёма необходимо повторно провести анализы на липидный профиль, АСАТ и АЛАТ. Эффект проявляется в течение первой недели от начала лечения. Через две недели он составляет 90 % от максимального действия. Наибольший эффект достигается к четвёртой неделе и затем остаётся постоянным.
Если целевой уровень ЛПНП достигнут и препарат не влияет отрицательно на печень, то статин в данной дозировке применяют длительно. Липидный профиль, АСАТ и АЛАТ контролируют через каждые 3–6 месяцев. При повышении печёночных ферментов выше трёх норм препарат перестают применять.
Помимо снижения холестерина, статины положительно влияют на состояние внутренней оболочки артерий, стабилизируют атеросклеротические бляшки и улучшают текучесть крови.
Статины обычно хорошо переносятся, но у некоторых пациентов возникают побочные эффекты, например боль в мышцах. Принимать препараты следует под постоянным контролем врача, вовремя корректировать их дозу или использовать в комбинации с другими лекарствами.
Фибраты
Фибраты (Фенофибрат) стимулируют активность фермента липопротеинлипазы и тем самым ускоряют распад липопротеинов. Они снижают не только холестерин, но и триглицериды (ТГ). Это препараты выбора у больных с сахарным диабетом, у которых чаще всего повышены ТГ.
Ингибиторы всасывания холестерина в кишечнике
Секвестранты желчных кислот
Секвестранты (Холестирамин, Колестипол) — ионообменные смолы, которые не дают желчным кислотам всасываться в кишечнике. Истощение запасов этих кислот активирует их синтез из холестерина в печени. Применяются у пациентов с холестазом.
Приём препаратов данной группы часто вызывает побочные эффекты: метеоризм, задержку стула, тошноту, боль или дискомфорт в верхнем отделе живота, что ограничивает их применение.
Моноклональные антитела
N-3 жирные кислоты
Гиполипидемическую терапию важно назначать вовремя, чтобы предотвратить развитие атеросклероза и его осложнений.
Прогноз. Профилактика
При ранней диагностике гиперлипопротеинемии и своевременном снижении уровня атерогенных липопротеинов прогноз благоприятный.
Заболевание может долго протекать без симптомов и выявиться только при профилактическом исследовании, поэтому необходимо регулярно определять липидный профиль. Это поможет избежать атеросклероза и его серьёзных осложнений: инфаркта миокарда, инсульта и т. д.
Если дислипидемия диагностирована при развившемся атеросклерозе, то следует изменить питание и начать медикаментозное лечение. Если удаётся добиться целевых уровней липидов в крови, то прогноз благоприятный. В таком случае сердечно-сосудистый риск значительно снижается. Пациенту необходимо следовать рекомендациям врача и регулярно делать липидограмму.
Прогноз неблагоприятный при значительном повышении уровня липидов в крови, сопутствующих заболеваниях, таких как артериальная гипертензия, сахарный диабет, хроническая болезнь почек и осложнения атеросклероза. Такие пациенты находятся в группах высокого и очень высокого риска с большой смертностью.
Профилактика гиперлипопротеинемии
Цель первичной профилактики — уменьшить влияние возможных причин гиперлипопротеинемии. Для этого нужно правильно питаться, не курить, больше двигаться и по возможности исключить препараты, нарушающие обмен липидов.
Также для профилактики атеросклероза следует: