Лимфодиссекция (лимфаденэктомия)
Лимфодиссекция и лимфаденэктомия в современной онкологии считаются взаимозаменяемыми терминами, обозначающими хирургическое удаление лимфатических узлов при злокачественном процессе. В последние годы шире употребляется термин лимфодиссекция, который полнее отражает техническую суть операции — удаление единым блоком группы лимфоузлов с окружающей клетчаткой.
Показания к лимфодиссекции
Лимфодиссекция — стандартная манипуляция при хирургическом лечении рака любой локализации, при некоторых злокачественных процессах брюшной полости и забрюшинного пространства обязательно выполняется вместе с операцией на пораженном первичной опухолью органе, то есть это один из этапов радикального хирургического лечения.
Цель лимфаденэктомии — удаление пораженных злокачественными клетками лимфатических узлов. С одной стороны, это полноценное лечение с ликвидацией метастаза в лимфоузле, с другой — диагностическая процедура, определяющая степень ракового поражения для оптимального планирования дальнейшего лечения.
Лимфаденэктомия с удалением поверхностно располагающихся лимфатических коллекторов, к примеру, в паху, в подмышке или на шее не проходит бесследно, осложняясь застоем лимфы ниже места операции — лимфедемой. Вызванные лимфедемой физические страдания, особенно нарушение движений конечности, не оправданы, если в лимфоузлах не было метастазов и лимфаденэктомия проводилась с профилактической целью.
Во избежание избыточного хирургического лечения в виде лимфаденэктомии при отсутствии метастатического поражения, сегодня выполняется биопсия сторожевого лимфоузла. Если срочное гистологическое исследование во время операции выявляет раковые клетки, то лимфоузлы удаляются. При отсутствии раковых клеток лимфоколлектор не трогают.
От биопсии сторожевого лимфоузла часто отказываются по техническим соображениям: нет специалиста, невозможно провести срочное морфологическое исследование, качество анестезии не позволяет. В международной клинике Медика24 всегда есть всё необходимое для высокотехнологичного лечения.
Наши врачи вам помогут
При каких заболеваниях выполняется лимфаденэктомия
Необходимость иссечения лимфоколлекторов зависит от степени распространения первичной опухоли и её прогностических характеристик, то есть от агрессивности рака.
Манипуляция не нужна при практически не метастазирующих новообразованиях, например, при базальноклеточном раке кожи, и при поверхностных «ранних» раках, в подавляющем большинстве не осложняющихся метастазированием.
При раке молочной железы, плоскоклеточной карциноме кожи, меланоме, новообразованиях головы лимфаденэктомия выполняется только при метастазах, диагностируемых при биопсии сторожевого лимфоузла. Свободные от раковых клеток лимфоколлекторы не трогают, во избежание развития лимфедемы.
При немелкоклеточной карциноме удаление лимфоузлов средостения с обеих сторон входит в стандартный объём радикального лечения. При технической невозможности лимфаденэктомии вследствие прорастания метастазов в органы средостения, случай признается неоперабельным. Поэтому в процессе дооперационной диагностики необходимо точно определиться с возможностью выполнения лимфодиссекции, чтобы не подвергать пациента напрасному вмешательству, когда «разрезали, посмотрели и зашили».
При панкреатической карциноме лимфодиссекция тоже неотъемлемой этап радикальной операции на поджелудочной железе, при сомнениях в возможности удаления метастазов пациенту назначается только консервативное лечение.
При раке желудка лимфодиссекция нескольких групп лимфатических узлов, располагающихся в разных анатомических зонах, считается стандартным вмешательством, выполняемым одновременно с удалением желудка. Рассчитана вероятность наличия метастазов в зависимости от глубины внедрения рака в стенку желудка, то есть от стадии. При поверхностной — «ранней» карциноме только у 3% больных раковые клетки находят в ближайшей к желудку группе лимфоузлов, при 1 стадии — у каждого десятого. При 2 стадии — у каждого третьего больного метастазы поражают лимфатические группы уже нескольких анатомических зон, при 3 стадии — у 90%. Исходя из стадии заболевания выполняется разное вмешательство на желудке — резекция или полное удаление, также различается и объём лимфаденэктомии.
По аналогичным принципам проводится лимфодиссекция и при злокачественных процессах мочеполовой системы.
Виды лимфаденэктомии
По объему вмешательства лимфодиссекцию разделяют на региональную, то есть удаление ближайшей группы узлов, селективную — выборочную, расширенную — несколько уровней лимфатических коллекторов.
В зависимости от уровня удаляемой группы лимфатических узлов лимфодиссекции подразделяют на варианты с литерой «D» и цифрами от 1 до 4. Лимфодиссекция D1 — удаление ближайшего к органу лимфоколлектора, D4 — иссечение самой удаленной группы лимфатических узлов. Классификация используется при новообразованиях внутренних органов, для каждого злокачественного заболевания разработана отдельная градация уровней и стандарт лимфодиссекции.
Описание операции
Лимфатические узлы удаляются по определенным онкологическим канонам, гарантирующим максимальную «чистоту» остающихся тканей от раковых клеток:
Техника лимфодиссекции при удалении поверхностных лимфоколлекторов включает рассечение кожи, отделение скальпелем от прилежащих мышечных массивов всей жировой клетчатки вместе с лимфоузлами, перевязку и пересечение сосудов, и зашивание операционной раны.
Внутри брюшной, грудной или тазовой полости последовательно, но также единым блоком удаляется пораженный опухолью орган и внутренняя клетчатка с лимфоузлами. Всё удаленное отправляется на гистологическое исследование.
Метастатическое поражение шейных лимфатических узлов
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
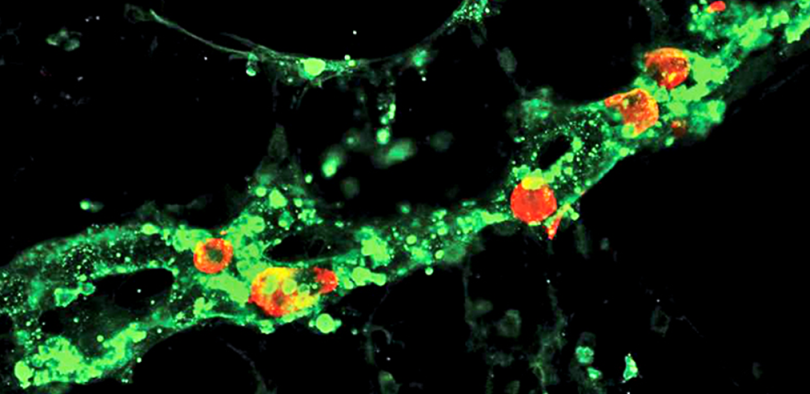
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
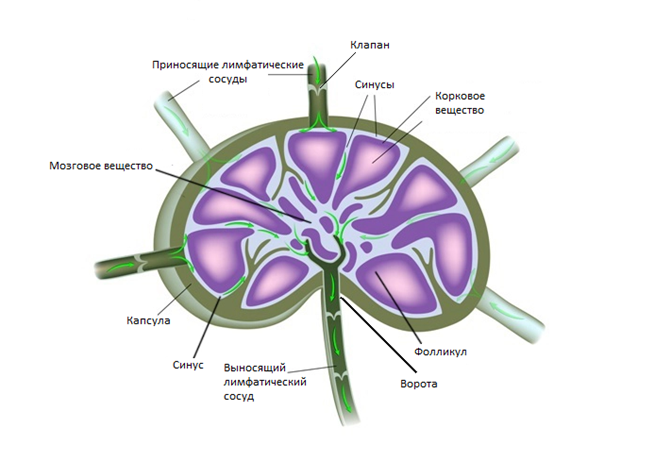
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы – место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.
Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
Ценность МРТ – превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз – критерии, общие для протоколов исследования КТ и МРТ.
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
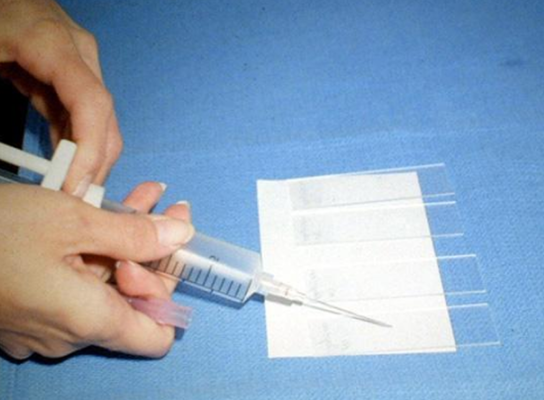 | 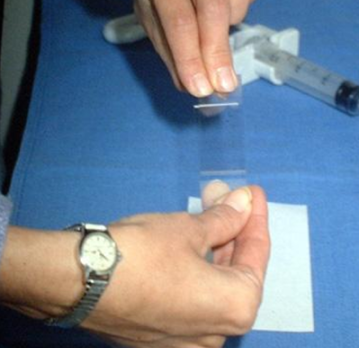 |
| Процесс приготовления предметных стекол для цитологического исследования. Материалом служит содержимое шприца после выполнения тонкоигольной аспирационной биопсии | |
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
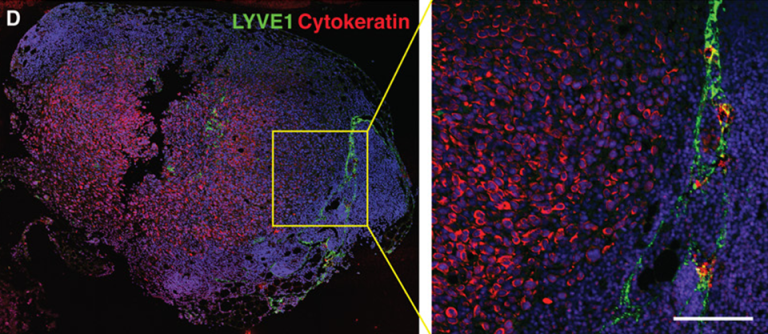
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) – маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1–2 года осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяца, на сроке 3–5 лет – один раз в 6–12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
Авторская публикация:
Амиров Николай Сергеевич
Клинический ординатор НМИЦ онкологии им. Н.Н. Петрова
Под научной редакцией:
Раджабова З.А.
Заведующий отделением опухолей головы и шеи
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, научный сотрудник, кандидат медицинских наук, доцент
Лимфаденэктомия
Лимфаденэктомия (лимфодиссекция, удаление лимфатических узлов) означает оперативное удаление лимфатических узлов, которое производится, как правило, в рамках резекции злокачественной опухоли c диагностической и/или терапевтической целью.
Когда и как выполняется лимфаденэктомия при различных онкологических заболеваниях:
Во всех случаях лимфаденэктомия дает важную информацию относительно стадии опухоли и прогнозе лечения.
Терапевтический эффект лимфаденэктомии
Сегодня можно утверждать, что сопутствующая лимфаденэктомия улучшает прогноз лечения при таких видах рака как:
Биопсия сторожевых узлов
В настоящее время перед проведением радикальной диссекции лимфатических узлов проводится так называемая биопсия сторожевых узлов. Сторожевыми называют первые узлы на пути распространения опухоли по лимфатических протокам. Сторожевой узел служит своеобразным индикатором, если он не поражен опухолью, это означает что вероятность ее распространения в следующие лимфатические узлы ничтожно мала. Однако в случае поражения сторожевого узла, выполняется радикальное удаление лимфатических узлов.
Перед проведением биопсии сторожевых узлов, проводится их маркировка красящим или радиоактивным вещевом и помощью сцинтиграфии лимфатических узлов определяется их точное месторасположение.
Способы проведения лимфаденэктомии
Как правило, лимфаденэктомия проводится во время основной операции опухоли. Однако, в случае отдельного оперативного вмешательства процедура может быть проведена миниинвазивно, например, лапароскопически.
Возможные последствия лимфаденэктомии
Наиболее частым осложнением лимфаденэктомии является лимфостаз – застой жидкости в межклеточных пространствах, который вызывается плохим оттоком лимфы по лимфатическим сосудам. Чем больше лимфатических узлов удалено, тем выше риск возникновения лимфостаза.
Анализ лимфогенного метастазирования рака толстой кишки I-III стадии по результатам D3 лимфодиссекции
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, отделение колопроктологии с хирургией тазового дна, отделение патологоанатомическое, г. Москва Первый московский медицинский университет им. И.М. Сеченова, лаборатория электронной микроскопии и иммуногистохимии, г. Москва
Многие исследования демонстрируют, что улучшение результатов лечения колоректального рака, произошедшее в последнее время, достоверно связано с изменением техники выполнения оперативных вмешательств. Целью работы было определение особенностей лимфогенного метастазирования рака толстой кишки I-III стадии среди группы пациентов, проживающих, на территории России, на основании изучения лимфатических, узлов, полученных, из удаленных, препаратов после радикальной резекции с расширенной лимфодиссекцией.
В данное проспективное исследование включены последовательно пролеченные больные колоректальным раком без отдаленных, метастазов, которым была выполнена радикальная операция с D3 лимфодиссекций.
Среднее число лимфатических, узлов, которое может быть выделено из препарата колоректального рака у пациента из российской популяции, составляет 39 штук. Среднее значение индекса метастазирования (0,13) в изученной группе больных, невелико, что является подтверждением большого объема лимфодиссекции и может иметь существенное прогностическое значение.
Введение
Прогресс в лечении рака толстой кишки, отмеченный за последние три десятилетия, стал наиболее значимым событием в области тарапии солидных новообразований брюшной полости. К удивлению специалистов, улучшение эффективности лечебных протоколов в основном было достигнуто в результате стандартизации хирургических пособий, хотя весомую роль в снижении числа местных рецидивов и лечении отдаленных метастазов злокачественных опухолей ободочной и особенно прямой кишки играет применение лучевой и химитерапии, а также их комбиниции. В странах с эффективной системой оказания специализированной помощи, основанной на тесном взаимодействии хирургов, радиологов и химиотерапевтов, частота местных рецидивов снизилась до уровня ниже 10%, а канцерспецифич-ная пятилетняя выживаемость находится на уровне 70% [11]. Между тем, большинство специалистов не считает эти цифры окончательными, полагая, что превзойти данные показатели позволит более прецизионная стратификация больных, построенная на основе изучения различных факторов прогноза течения заболевания и подбора индивидуальной программы лечения. В этой связи данные о местном характере роста новообразований толстой кишки и их распространении по лимфатической системе у больных без клинических и инструментальных признаков гематогенной и перитонеальной диссе-минации на основе Международной классификации опухолей человека ТNМ явлются необходимым элементом в цепи поиска такого рода прогностических критериев. При этом «идеальной» (с определенными ограничениями) является ситуация, когда объектом изучения станут все группы лимфатических узлов, потенциально опасных для поражения, включая апикальные.
Целью настоящего исследования было определение особенностей лимфогенного метастази-рования неметастатического рака толстой кишки у пациентов, проживающих на территории РФ, на основании изучения лимфатических узлов, полученных из удаленных препаратов после радикальной резекции с расширенной лимфодиссекцией.
Материалы и методы
Методы набора материала для исследования
Данное проспективное контролируемое исследование проведено на базе отделения колопроктологии с хирургией тазового дна Российского научного центра хирургии им. акад. Б.В. Петровского РАМН. Морфологическая часть работы проведена в отделении патоморфологии того же центра и лаборатории электронной микроскопии и иммуногистохимии Первого московского медицинского университета им. И.М. Сеченова.
В исследование включены последовательно пролеченные больные в соответствии со следующими критериями включения: гистологически подтвержденный аденогенный рак толстой кишки; отсутствие отдаленных метастазов и перитонеальной диссеминации по данным пред- и интраоперацион-ного исследования; отсутствие лучевой, химио- и/ или химиолучевой терапии в анамнезе; выполнение открытого (нелапароскопического) радикального оперативного вмешательства с D3 лимфодиссекцией; подписание информированного согласия для участие в исследовании. Критериями исключения больных из исследования являлись: первичномножественный характер опухолевого поражения; наличие соматических заболеваний в стадии декомпенсации; наличие или появление у больных причин, препятствующих проведению наблюдения в отдаленном послеоперационном периоде.
Локализацию опухоли в ободочной кишке определяли по данным ирригоскопии. В случае расположения опухоли в бассейне верхней брыжеечной артерии (восходящая и поперечно-ободочная кишки) считали, что опухоль расположена в правой половине ободочной кишки. Под левосторонней локализацией опухоли понимали ее расположение от селезеночного изгиба до ректосигмоидного перехода. Локализацию опухоли в прямой кишке определяли по расположению ее нижнего полюса от 0 до 18 см по тубусу ректоскопа.
Методика выполнения D3 лимфодиссекции при раке толстой кишки
В практике отделения внедрена концепция хирургического лечения злокачественных опухолей толстой кишки различной локализации, основанная на принципах удаления сегмента кишки, несущего опухоль вместе с путями лимфооттока вплоть до зоны апикальных лимфоузлов. При этом важной особенностью выделения удаляемого сегмента кишки является сохранение его собственной фасции (мезоректальной или мезоколической фасции), что обозначается терминами «мезоректумэктомия» и «мезоколонэктомия».
Отдельное внимание уделяется принципу «notouch» (не трогая), предполагающему соблюдение этапности действий при выполнении оперативного приема: первым этапом выполняли перевязку сосудов, питающих участок кишки, пораженный злокачественным процессом, затем производили лим-фодиссекцию, пересекали кишку проксимальнее и дистальнее новообразования в соотвествии с принципами онкологического радикализма и только после этого выделяли сегмент кишки с опухолью и удаляли его.
После выполнения срединной лапаротомии и коррекции доступа с использованием ретрактор-ной системы выполняли ревизию органов брюшной полости и малого таза с целью исключения перитонеальной диссеминации и отдаленных метастазов. Дополнительно выполняли ультразвуковое исследование печени с помощью интраоперационного конвексного УЗ-датчика с частотой 3,5-5 МГц. При отсутствии данных за генерализацию опухолевого процесса приступали к выполнению радикального вмешательства.
Методы морфологического исследования удаленного препарата
При расположении опухоли в слепой кишке к лимфатическим узлам первого порядка (парако-лическим) относили те из них, которые располагались вдоль кишечной стенки и краевого сосуда на удалении до 10 см в обоих направлениях от краев опухоли. К лимфатическим узлам второго порядка (промежуточным) относили узлы, расположенные вдоль подвздошно-ободочной артерии или вдоль правой ободочной артерии (в случае ее наличия) на протяжении от ствола ВБА до аркадных артериальных дуг. Лимфатические узлы обозначались как лимфоузлы третьего порядка (или апикальные) в случае их локализации в области устья правой ободочной и подвздошно-ободочной артерий, а также в непосредственной близости от ствола ВБА.
При расположении опухоли в правой половине ободочной кишки параколическими считались лимфоузлы, расположенные вдоль кишечной стенки и краевого сосуда на удалении до 10 см в оральном и анальном направлении от краев опухоли. К лимфатическим узлам второго порядка относили узлы, расположенные вдоль правой ободочной артерии и подвздошно-ободочной артерии на их протяжении от ствола ВБА до аркадных артериальных дуг. Лимфатические узлы обозначались как апикальные при их локализации в области устья правой ободочной и подвздошно-ободочной артерий, а также в непосредственной близости от ствола ВБА.
После фиксации лимфоузлы и ткани опухоли подвергались проводке по стандартной методике и заливались в парафин. После проводки из парафиновых блоков изготавливали срезы 3-4 мкм. Для определения характера роста опухоли, гистологического типа, степени ее дифференцировки и уровня инвазии, а также морфологических особенностей регионарных метастазов изучали парафиновые срезы, окрашенные гематоксилином и эозином.
На основании гистологического изучения препарата определялась окончательная (патоморфологическая) стадия заболевания в соответствии с классификацией опухолей по системе TNM 6 издания [1]. У каждого пациента III стадии болезни (с найденными метастатически пораженными регионарными лимфатическими узлами) был определен индекс метастазирования (Им), который рассчитывался как отношение числа лимфатических узлов, содержащих опухоль, к общему числу найденных в препарате лимфатических узлов. Были выделены квартили (первый, второй, третий) значений метастатического индекса, на основании которых эти пациенты разделены на четыре группы: при значении ИМ менее первого квартиля, от первого до второго квартиля, от второго до третьего квартиля и больше третьего квартиля.
Клиническая характеристика больных и количество найденных в препарате лимфатических узлов
число найденных лимфатических узлов у одного
лимфатических узлов диаметром
4, была наибольшей среди групп больных раком ППОК и ПК (50% и 43% соответственно).
Доля метастатически пораженных среди всех найденных лимфатических узлов у всех больных раком ППОК составила лишь 1,9%, что незначительно меньше этого показателя при раке ЛПОК (2,8%, р=0,36) и достоверно меньше, чем при раке ПК (4,8%, р=0,011). Среднее значение индекса метастазирования среди пациентов с III стадией заболевания было наименьшим при локализации опухоли в ППОК (0,07±0,04), незначительно большее среднее значение этого индекса отмечено при расположении опухоли в ЛПОК (0,09±0,07) и наибольшее его среднее значение получено у больных раком ПК (0,16±0,13). Среднее значение ИМ в общей когорте пациентов составило 0,13±0,11 (0,03-0,38). При изучении распределения пациентов по квартилям индекса метастазирования отмечается, что у всех больных раком ППОК III стадии значение ИМ меньше значения третьего квартиля ( 0,2 было отмечено лишь у 7 пациентов (27%), среди которых нет ни одного больного раком ППОК.
Результаты гистологического исследования препарата у пациентов с пораженными лимфатическими узлами
Среднее число пораженных лимфатических узлов
Число больных с пораженными лимфатическими узлами первого порядка, чел. (%)
Число больных с пораженными лимфатическими узлами первого и второго порядков, чел. (%)
Число больных с поражением 4 и более лимфатических узлов, чел. (%)
Общая частота поражения лимфатических узлов
Индекс метастазиро-вания, чел.
Обсуждение
В этой связи настоящее сообщение представляет определенный интерес, так как описывает опыт D3-лимфодиссекций при колоректальном раке, выполненных у представителей западной популяции, т.е. пациентов из России. Мы не встречали публикаций в русскоязычной литературе, в которых были бы подробно описаны варианты поражения путей лимфооттока от злокачественной опухоли ободочной или прямой кишок на основании изучения удаленного препарата в ходе радикальной резекции с расширенной лимфодиссекцией. Поэтому одной из целей работы было привести подробное описание методики выполнения D3 лимфодиссекции при колоректальном раке различной локализации. Кроме того, является уместным проведение сравнения особенностей лимфогенного метастазирования между пациентами из России (представителями западной цивилизации) и представителями восточной популяции.
Представленный в настоящей работе материал по распределению найденных в препарате лимфатических узлов по порядкам поражения может быть полезным для построения теоретической модели эффективности расширенной лимфодиссекции по сравнению с ограниченной лимфодиссекцией. Если провести анализ числа лимфатических узлов в зависимости от их удаления от первичной опухоли в нашей выборке больных колоректальным раком (в среднем 16 лимфатических узлов первого порядка, 18 лимфатических узлов второго порядка и 5 лимфатических узлов третьего порядка), то становится очевидным, что при ограничении объема лимфо-диссекции до уровня D2 общее число найденных лимфатических узлов сократится в среднем на 5, а при дальнейшем сокращении объема лимфодиссекции разница в количестве исследованных лимфатических узлов по сравнению с D3 лимфодиссекцией может достигать 15-20 штук. Если учесть, что в среднем частота поражения лимфатических узлов только второго и третьего порядков в сумме составляет около 10%, а эффективность D3 лимфодиссекции составляет порядка 60%, то можно предположить улучшение онкологической эффективности лечения на 6% только за счет хирургической компоненты. Однако, для подтверждения или опровержения этого необходимо проведение проспективного рандомизированного исследования.
Выводы
1. Среднее число лимфатических узлов, которое может быть выделено из препарата колоректального рака у пациента, проживающего на территории РФ, составляет 39 штук, при этом более половины из них имеют диаметр менее 5 мм.
2. В брыжейке правой половины ободочной кишки в среднем обнаружен 61 лимфатический узел, что значительно превышает число лимфатических узлов, которые были найдены в брыжейке левой половины ободочной кишки (30 штук) или в мезоректальной клетчатке и брыжейке прямой кишки (37 штук).
3. Среднее значение индекса метастазирования (0,13) в изученной группе больных невелико, что является подтверждением большого объема лимфодиссекции и может иметь существенное прогностическое значение.