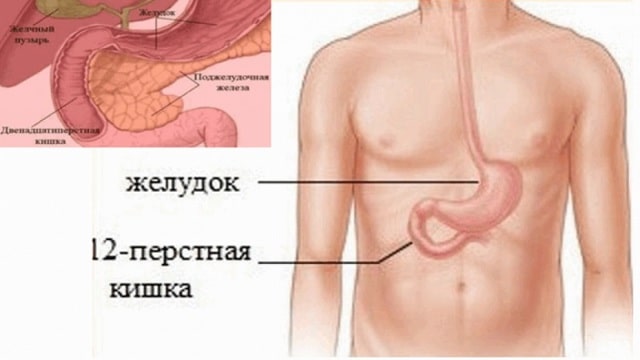
Доброкачественные опухоли 12-перстной кишки: от диагностики до хирургического лечения
Доброкачественные опухоли 12-перстной кишки можно разделить на несколько групп. Первая – эпителиальные полипы. Эти новообразования вызывают у человека чувство дискомфорта, боль и спазмы после принятия пищи. Для ранней диагностики людям с патологиями ЖКТ необходимо ежегодно проходить фиброгастродуоденоскопию, которая дает более детальную информацию чем гастроскопия. Сами по себе полипы не опасны, но несут угрозу перехода в злокачественную опухоль посредством малигнизации. Поэтому при выявлении железистых полипов их необходимо удалить с обязательным проведением гистологического исследования.
Вторая группа – аденомы 12-перстной кишки, которые также относятся к предраковым состояниям, хотя злокачественной трансформации подвергаются гораздо реже, чем полипы. Аденомы вызывают болевой синдром, чувство тяжести в желудке. Увеличиваясь в размерах, нарушают прохождение пищи, перекрывают отток желчи, провоцируя желтушность кожных покровов. Аденомы диагностируются методами фиброгастроскопии и компьютерной томографии и также подлежат обязательному удалению.
Третья группа – сосудистые опухоли подслизистого слоя – гемангиомы. Они крайне редко подвергаются злокачественной трансформации, но их травматизация при прохождении пищи и под воздействием агрессивной кислотной среды 12-перстной кишки нередко провоцирует кровотечение. Гемангиомы подлежат эндоскопической резекции или склерозированию; в крайних случаях – удалению лапароскопическим или открытым способом.
В отдельную группу можно выделить гастроинтестинальные и нейроэндокринные опухоли. Эти новообразования имеют очень короткий путь перехода из доброкачественных в злокачественные. Диагноз ставится при биопсии и под контролем иммуногистохимических исследований. Опухоль исследуется целиком, поскольку в одной части может быть группа клеток доброкачественного генеза, в другой части – злокачественного.
Что касается размеров опухолей, полипы редко превышают 2 см; аденомы бывают разные – от 3 мм до 15 см. Недавно в моей практике встретилась уникальная по размерам гастроинтестинальная опухоль весом 16,7 кг. Она была расположена на границе желудка и 12-перстной кишки, то есть росла снаружи органа, внутрь брюшной полости. Этой пациентке многие врачи рекомендовали оперативное вмешательство, но она услышала только одного, который когда-то сказал: «Если не мешает, ничего страшного – опухоль доброкачественная». У нее были боли, она регулярно принимала обезболивающие препараты, живот был огромный – больше чем на поздних сроках беременности. В итоге, когда она уже практически не могла наклоняться, решилась на операцию. Мы сделали биопсию и результат показал наличие злокачественных клеток. Несмотря на гигантский вес опухоли, мы не выявили поражения ни в одном из 36 лимфоузлов. Прогноз для жизни пациентки – хороший.
Следует подчеркнуть, что до операции мы обязательно выясняем, злокачественная или доброкачественная опухоль: это необходимо для определения объема подлежащих удалению тканей. Если опухоль доброкачественная, нет необходимости в удалении лимфатических узлов, что положительным образом влияет на объем резекции желудка и 12-перстной кишки: он уменьшается в 2-3 раза. А это влияет на качество и продолжительность жизни человека.
СПРАВОЧНО
Роман Викторович Ищенко – хирург, онколог. Специализация: злокачественные опухоли органов брюшной полости, легких, трахеи и плевры, кардиоонкология (лечение злокачественных опухолей у пациентов с сердечно-сосудистыми заболеваниями).
Консультирует пациентов в ФНКЦ ФМБА России (Москва). Записаться на очный прием можно на сайте врача или по телефону +7(495)971-71-72.
Подробнее о порядке госпитализации в московские клиники можно узнать на сервисе социального проекта «Здоров Я».
Рак двенадцатиперстной кишки
Рак двенадцатиперстной кишки — это злокачественная опухоль, образующаяся на слизистой оболочке, а также железистых тканях кишечника. Различается первичная и вторичная формы рака. В первом случае очаг опухоли находится в двенадцатиперстной кишки, а во втором рак распространяется из других органов. Это заболевание встречается у представителей обоих полов. Наиболее часто — после 55 лет.
Акции
Оперативные вмешательства со скидкой 7%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Рак двенадцатиперстной кишки – это злокачественный процесс с образованием опухоли, локализованной в области начального отдела тонкой кишки. По данным наблюдений двенадцатиперстная кишка несколько чаще страдает от злокачественного перерождения в сравнении с другими отделами тонкого кишечника. Но в целом, рак 12-перстной кишки достаточно редко встречающаяся опухоль – около 0,5-3% от всех раковых поражений пищеварительного тракта и до 45% от всех опухолей тонкой кишки.
Средний возраст болеющих приходится на 40-60 лет, частота возникновения у женщин либо мужчин практически одинаковая. Как первичная опухоль она проявляется редко, в основном имеет форму вторичного, метастатического поражения, возникающего при других заболеваниях – опухоли желудка либо кишечника с метастазами.
Причины и факторы риска
Относительно причин развития онкологии в области двенадцатиперстной кишки мнения экспертов расходятся. Есть данные о том, что причины возникновения рака этой локализации сходны с причинами опухолей желудка.
Предполагают, что есть связь с длительно текущей инфекцией, вызванной H.Pilori, кислотоустойчивыми бактериями. Язвенные дефекты, спровоцированные этим микроорганизмом, возникают чаще, чем в области желудка. Они возникают у 8 из 10 пациентов, в то время как в желудке только у 6 из 10 людей. Дуоденальные язвы чаще бывают у женщин, хотя встречаемость рака у них равна таковой у мужчин. Есть публикации о связи рака с ожирением, особенностями питания, включая некоторые национальные кухни мира.
Злокачественные опухоли двенадцатиперстной кишки могут возникать на фоне определенных провоцирующих факторов. К ним относятся:
Кроме того, одними из факторов риска называют вирусные инфекции, диабет, панкреатит. Имеет значение и неблагоприятная наследственность.
Рак двенадцатиперстной кишки: основные симптомы и признаки
Типичные симптомы рака двенадцатиперстной кишки практически не выявляются на ранних стадиях. Заболевание достаточно длительное время может протекать бессимптомно. Определить опухоль в это время можно случайно, при проведении обследований по поводу других заболеваний. В более поздней стадии возможны боли при раке двенадцатиперстной кишки. Но и они не всегда настораживают пациента, так как могут быть приняты за признаки несварения или переедания. Боль имеет тупой и разлитой характер, обычно она локализуется в верхней части живота, под ребрами или подложечкой. Возможно появление болезненных ощущений в ночные часы или после длительного голодания. По мере прогрессирования болезни может возникать интоксикация продуктами распада опухоли. Это проявляется потерей веса, резкой бледностью, постоянной слабостью.
Проявления рака во многом зависят от стадии рака, размера очага и дополнительных патологий, осложняющих состояние. На поздних стадиях рак может себя проявлять следующими признаками:
Если ткань опухоли распадается, повреждаются сосуды и открывается кровотечение, возможно появление черного стула.
Классификация рака 12-перстной кишки
Примерно 80% всех опухолей составляет экзокринный рак. Основная его форма – аденокарцинома. Реже возникает недифференцированная форма экзокринного рака. Чаще всего этот тип поражает перипапиллярный отдел кишки, опухоль циркулярно прорастает стенку, сужая ее просвет, что приводит к кишечной непроходимости. Реже возникает экзофитный рост с развитием кровотечения. Возможно развитие как одиночной, так и множественных первичных образований.
Около 5% составляют эндокринные опухоли (апудомы). Они могут быть в форме карциноида, инсулиномы, випомы, гастриномы, глюкагономы. Они обычно определяются в средней трети кишки. Растут медленно, инфильтрируют ткани.
Также возможно развитие неэпителиальных опухолей. Самой частой из них считается лейомиосаркома, достигающая размеров в 8 см и более. Реже бывает фибросаркома, достигающая 3 см, которая может иметь низкую и высокую дифференцировку. Также возможны злокачественные невриномы, ганглионейробластомы или нейрофибросаркомы, особенно часто они встречаются у детей.
Из сосудистых опухолей наиболее часто регистрируется лимфосаркома, стоящая на втором месте после экзокринного рака.
Стадии
Онкологами выделяется 4 стадии рака данной локализации. Они различаются по размерам опухолевого очага и распространению на соседние ткани:
По классификации TNM оценивается тяжесть ракового поражения двенадцатиперстной кишки на основании трех критериев.
Т – это первичная опухоль может иметь 4 степени:
Поражение лимфоузлов обозначается следующими стадиями.
Для определения распространенности опухоли используют классификацию М0 и М1. В нулевой стадии отдаленных метастазов нет, в первой – рак 12-перстной кишки дал отдаленные метастазы.
Диагностика
Основа диагностики – это инструментальные обследования. Выполняется дуоденоскопия с забором биопсии для определения природы опухоли, а также проводится рентген кишечника. Дополнительно проводят УЗИ органов брюшной полости, чтобы определить прорастание опухоли в сосуды, поджелудочную железу, поражение лимфоузлов, печени и скопление жидкости в животе (развитие асцита).
Ангиография помогает определить особенности кровоснабжения опухоли, что важно для оперативного ее удаления, обнаружения мелких метастазов в печень. Также важны анализы крови, мочи на уровень гастрина и серотонина.
Лечение рака двенадцатиперстной кишки
Обычно терапия рака двенадцатиперстной кишки включает в себя комбинацию операции с химиотерапевтическим и лучевым методами. Это позволяет максимально полно удалить первичный очаг опухоли и не допустить распространения метастазов на соседние органы, предотвращает рецидив онкологии.
Химиотерапию проводят с применением тщательно подобранных цитостатических препаратов, применяемых перед оперативным вмешательством, чтобы уменьшить размеры опухоли, и после него, чтобы полностью подавить оставшиеся клетки. Применение этого метода сопряжено с множеством побочных эффектов, поэтому за состоянием пациента тщательно следят врачи.
При хирургическом вмешательстве происходит полное удаление пораженной части кишки в пределах здоровых тканей. Операцию назначают лицам моложе 75 лет, при начальных стадиях болезни. При терминальных стадиях рака операцию не назначают.
При лучевой терапии применяется ионизирующее излучение, направленное на опухолевый очаг. Лучи подавляют рост опухоли, приводят к гибели клеток. Это помогает предотвратить распространение метастазов, а также повторный рост рака. Лучевую терапию проводят на любой стадии процесса.
Рак двенадцатиперстной кишки: прогнозы
При ежегодной диспансеризации и профилактических осмотрах можно выявить рак на ранней стадии. В первой стадии выживает после полноценного лечения до 98% пациентов. Они могут полностью вылечиться, имеют благоприятные прогнозы для жизни и здоровья.
Во второй стадии рака выживаемость на протяжении 5 лет достигает 70-90%, к третьей стадии она снижается до 40-70%, но прогнозы неблагоприятные, возможна инвалидность. На четвертой стадии выживает на протяжении 5 лет не более 30% больных. Болезнь лечится крайне тяжело.
Профилактика рака 12-перстной кишки
Основа профилактики опухолевых процессов в кишечнике – это здоровое питание, отказ от вредных привычек, регулярное проведение обследований у врача, своевременное лечение любых расстройств пищеварения.
Лейомиома 12 ти перстной кишки что это такое
Двенадцатиперстная кишка (лат. duodénum) — начальный отдел тонкой кишки, следующий сразу после привратника желудка. Продолжением двенадцатиперстной кишки является тощая кишка.
12-ти перстная кишка (ДПК) получила своё название из-за того, что её длина около двенадцати поперечников пальцев руки.
Двенадцатиперстная кишка имеет несколько отделов:
Назначение 12-ти перстной кишки
Двенадцатиперстная кишка выполняет секреторную, моторную и эвакуаторную функции. Дуоденальный сок вырабатывается бокаловидными клетками и дуоденальными железами. В двенадцатиперстную кишку поступают сок поджелудочной железы и желчь, обеспечивающие, начавшееся в желудке, переваривание пищи.
Виды опухолей ДПК
К опухолям ДПК относятся:
Рак двенадцатиперстной кишки
ДПК чаще поражается раком по сравнению с другими отделами тонкой кишки, однако заболеваемость раком двенадцатиперстной кишки низкая и составляет 0,05-3,5% в структуре злокачественных опухолей желудочно-кишечного тракта и не более 45% в структуре новообразований тонкой кишки.
Пик заболеваемости приходится на возраст 40-60 лет.
В России частота заболеваемости среди мужчин и женщин одинакова.
Факторы риска
Факторы риска развития рака двенадцатиперстной кишки:
Экзокринный рак ДПК
Экзокринный рак ДПК встречается в 80% случаев всех первичных злокачественных опухолей двенадцатиперстной кишки.
Основной формой экзокринного рака двенадцатиперстной кишки является аденокарцинома. Чаще всего экзокринный рак поражает среднюю треть двенадцатиперстной кишки – в 62-78% случаев.
Развитие заболевания и симптомы
Заболевание развивается сравнительно медленно. Опухоль циркулярно поражает стенки кишки, вызывая сужение ее просвета, в результате чего возникает кишечная непроходимость.
Реже опухоль имеет вид экзофитно (снаружи) растущего узла. В этом случае первым проявлением заболевания может быть внутрикишечное кровотечение. Кровотечения также высоко вероятны при первично-язвенной форме рака двенадцатиперстной кишки. Реже опухоли двенадцатиперстной кишки вызывают механическую желтуху.
Приблизительно у 10-30% больных во время установления диагноза уже имеются метастазы в регионарные (близлежащие к опухоли) лимфатические узлы.
Опухоль может поражать головку поджелудочной железы, забрюшинную область, нервные сплетения, что проявляется болевым синдромом.
При раке ДПК довольно часто встречаются множественные первичные опухоли.
Злокачественные опухоли нейроэндокринного происхождения, апудомы
На долю нейроэндокринных опухолей (НО) приходится не более 5% всех злокачественных новообразований двенадцатиперстной кишки.
В двенадцатиперстной кишке встречаются следующие злокачественные нейроэндокринные опухоли:
Функциональная (гормональная) активность нейроэндокринных опухолей прежде всего оценивается по клиническим проявлениям. Однако, клинические проявления гормональной активности опухоли требуют лабораторного подтверждения, т.е. обнаружения гормонов и других биологически активных веществ в крови или их метаболитов в моче.
Апудомы длительное время могут не выходить за пределы подслизистого слоя двенадцатиперстной кишки. По мере увеличения размеров опухоли появляются черты инфильтрирующего роста и клинические симптомы.
Прочие опухоли двенадцатиперстной кишки
Так же в ДПК встречаются следующие опухоли:
Диагностика опухолей двенадцатиперстной кишки
Для диагностики проводится комплекс исследований, включающий:
Лечение опухолей 12-ти перстной кишки
Лечение злокачественных опухолей двенадцатиперстной кишки – хирургическое, заключается в удалении пораженного органа с опухолью.
Объем вмешательства зависит от размеров и распространенности опухоли. Так же применяется химиолучевая терапия в зависимости от типа и клеточного строения опухоли.
Лечение в отделении торакоабдоминальной хирургии и онкологии РНЦХ проводится по программам ОМС, ДМС, ВМП, а также на платной основе. Наше отделение — это высококвалифицированные хирурги, современное оборудование, комфортные условия стационара и внимательный персонал.
Читайте, как попасть на лечение в отделение торакоабдоминальной хирургии и онкологии РНЦХ.
Для записи на консультацию позвоните по телефонам:
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Лейомиома 12 ти перстной кишки что это такое
Институт хирургии им. А.В. Вишневского Министерства здравоохранения и социального развития РФ
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского, Москва
Подслизистые новообразования желудочно-кишечного тракта в эндоскопической практике
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2010;(2): 51-59
Старков Ю. Г., Солодинина Е. Н., Новожилова А. В. Подслизистые новообразования желудочно-кишечного тракта в эндоскопической практике. Хирургия. Журнал им. Н.И. Пирогова. 2010;(2):51-59.
Starkov Iu G, Solodinina E N, Novozhilova A V. Submucosal neoplasms of gastrointestinal tract in endoscopic practice. Khirurgiya. 2010;(2):51-59.
Институт хирургии им. А.В. Вишневского Министерства здравоохранения и социального развития РФ
Институт хирургии им. А.В. Вишневского Министерства здравоохранения и социального развития РФ
Институт хирургии им. А.В. Вишневского, Москва
Институт хирургии им. А.В. Вишневского, Москва
Длительное время подслизистые новообразования трактовались хирургами и эндоскопистами как доброкачественные и в большинстве подлежащие динамическому наблюдению. Исключение составляли новообразования больших размеров, которые имели клинические проявления и вынуждали хирургов к оперативному вмешательству. Подслизистые новообразования наиболее часто выявляются при эндоскопическом или при рентгенологическом исследовании желудочно-кишечного тракта. При рентгенологическом исследовании данные образования выглядят как пристеночно расположенные дефекты наполнения округлой или овоидной формы. Однако данное исследование не позволяет провести дифференциальную диагностику между образованием стенки полого органа и экстраорганно расположенным патологическим очагом. Наиболее эффективным методом диагностики подслизистых опухолей до последнего времени оставалось эндоскопическое исследование, при котором визуализируются округлой или овоидной формы образования, деформирующие просвет органа и покрытые в большинстве наблюдений неизмененной слизистой. По косвенным эндоскопическим признакам можно предположить, что данное образование исходит из стенки полого органа, однако четкие критерии, позволяющие провести дифференциальную диагностику между подслизистым образованием и экстраорганной компрессией, отсутствуют. По данным литературы, чувствительность и специфичность рутинного эндоскопического исследования в дифференциальной диагностике между подслизистыми образованиями и экстраорганной компрессией составляют 87 и 29% соответственно [51]. Также визуальное эндоскопическое исследование не дает ответа на вопрос о структуре образования и не позволяет определить, из какого именно слоя стенки полого органа оно происходит. С учетом локализации биопсия по стандартной методике при эндоскопическом исследовании также не дает возможности установить гистологическую природу этих новообразований [8]. Другие неинвазивные лучевые методы диагностики (КТ, УЗИ, МРТ) еще менее чувствительны [40], так как в большинстве наблюдений небольшие подслизистые образования этими методами не выявляются. Возможности диагностики и дифференциальной диагностики неэпителиальных опухолей и неопухолевых образований стенки желудочно-кишечного тракта значительно расширяет эндоскопическая ультрасонография. Этот метод позволяет не только достоверно различать образования стенки и экстраорганные структуры, но и определять слой, из которого происходит новообразование, а оценивая его эхогенную характеристику, четко дифференцировать неэпителиальные опухоли и неопухолевые образования желудочно-кишечного тракта. При морфологическом исследовании становится ясно, что подслизистые образования включают кисты, дистопию ткани поджелудочной железы и целую группу неэпителиальных опухолей мышечного, неврогенного и сосудистого происхождения [48].
В последние годы интерес к неэпителиальным опухолям желудочно-кишечного тракта значительно возрос, активно изучаются визуальные и лучевые характеристики этих новообразований, их гистологическое строение, проводятся исследования результатов хирургического и химиотерапевтического лечения пациентов с различными подслизистыми новообразованиями желудочно-кишечного тракта. Своей задачей в данном обзоре мы видим необходимость дать информацию для эндоскопистов и врачей других специальностей о том, каковы могут быть возможные варианты безобидных с виду подслизистых новообразований, так как только своевременная дифференциальная диагностика служит основой решения тактических вопросов.
Гастроинтестинальные стромальные опухоли являются наиболее распространенными среди неэпителиальных опухолей желудочно-кишечного тракта и составляют до 1% всех злокачественных опухолей этой локализации [7, 12, 18, 38, 51, 53]. Эти новообразования ранее расценивались как лейомиомы, лейомиобластомы и лейомиосаркомы, однако иммуногистохимические исследования показали их особую природу [27].
Еще в 1960 г. J. Martin и соавт. [33] опубликовали сообщение о 6 наблюдениях «интрамуральных мышечных опухолей» желудка и предположили мышечное происхождение этих «странных» опухолей [27]. Двумя годами позже A. Stout [55] ввел термин «лейомиобластома» для описания группы «причудливых» миогенных опухолей желудка. В течение двух десятков лет авторы использовали различные названия для удобства описания веретеноклеточных и эпителиоидных опухолей, встречающихся во всех отделах желудочно-кишечного тракта. Первыми термин «гастроинтестинальная стромальная опухоль» (ГИСО) ввели M. Mazur и H. Clark в 1983 г. как компромиссный для описания опухолей с не вполне понятной дифференцировкой [35]. Для этих опухолей характерной была двойственность их фенотипа: гладкомышечный и нейрогенный.
Наиболее часто встречаются веретеноклеточный (62%), эпителиоидный (17%) и смешанный (21%) гистологические варианты строения ГИСО [1]. Несмотря на различные варианты гистологического строения, все ГИСО считаются потенциально злокачественными [1, 12, 26]. Даже после радикального удаления опухоли (макро- и микроскопически в пределах здоровых тканей) частота рецидивов достигает 30-50%, проявляясь либо метастазами в печень, либо местным рецидивом (метастазы по брюшине). Особенно неблагоприятен прогноз при опухолях тонкой кишки, когда средний уровень выживаемости составляет около 20 мес [41]. Основными путями генерализации гастроинтестинальной стромальной опухоли является метастазирование в печень и распространение по брюшине. Лимфогенное метастазирование для опухоли не характерно [12, 23]. В настоящее время для определения степени злокачественности ГИСО пользуются критериями, предложенными C. Fletcher и соавт. [18] и M. Miettinen и соавт. [38], по которым высокий риск определяется размером опухоли более 5 см, количеством митозов более 5 в 50 полях зрения при увеличении 400 и инвазией опухолью слизистой. Иммуногистохимическим маркером степени злокачественности опухоли является также индекс экспрессии Ki-67, который достоверно возрастает выше 10% в опухолях высокого риска [68].
При эндоскопическом исследовании опухоли могут выявляться в виде образований округлой или овоидной формы; небольшие образования покрыты неизмененной слизистой, однако нередко можно выявить ее изъязвление над опухолью, что служит прогностически неблагоприятным фактором относительно злокачественности образования и может стать источником желудочно-кишечных кровотечений с развитием анемии, в 50% наблюдений это является поводом для обращения пациентов к врачу и причиной выявления ГИСО [21]. При эндосонографическом исследовании ГИСО визуализируется как гипоэхогенное образование, которое в зависимости от степени злокачественности может иметь как гомогенную, так и гетерогенную структуру и исходить из мышечной пластинки слизистой или мышечного слоя стенки органа [25].
В дифференциально-диагностическом ряду с гастроинтестинальными опухолями находятся мезенхимальные опухоли и другие новообразования, локализующиеся в стенке пищеварительной трубки и покрытые неизмененной слизистой. Наиболее часто гастроинтестинальную опухоль приходится дифференцировать с истинными гладкомышечными опухолями, липомой, шванномой, нейроэндокринной опухолью, эктопированной поджелудочной железой. Такие образования, как воспалительная миофибробластическая опухоль, воспалительный фиброзный полип, гранулярно-клеточные опухоли, нейрофиброма, сосудистые опухоли и метастазы в стенке желудочно-кишечного тракта, встречаются крайне редко и имеют небольшое практическое значение в дифференциальной диагностике.
Нейроэндокринные опухоли желудочно-кишечного тракта развиваются в органах, производных от передней кишки эмбриона (пищевод, желудок и двенадцатиперстная кишка), и составляют до 5-8% всех нейроэндокринных опухолей. При локализации в верхних отделах желудочно-кишечного тракта обычно гормонально не активны и выявляются случайно при эндоскопическом исследовании или при оперативных вмешательствах по поводу других заболеваний [19]. Гистологически опухоль представлена в виде гнездных скоплений мелких клеток с круглыми ядрами или в виде тяжей опухолевых клеток, соединенных трабекулами. Образование обычно локализуется во II (мышечной пластинке слизистой) или III (подслизистом) эхо-слое, покрыто неизмененной слизистой, однако иногда покрывающая слизистая может изъязвляться, что также является причиной кровотечений [39]. Нейроэндокринные опухоли обладают определенным злокачественным потенциалом, и чем больше размер опухоли, тем выше риск метастазирования, поэтому при образованиях размером более 2 см рекомендуется их удаление [34].
Другие сосудистые опухоли: гломусная опухоль (гломус-ангиома) состоит из щелевидных сосудов, выстланных эндотелием и окруженных муфтами из эпителиоидных (гломусных) клеток; лимфангиома развивается из лимфатических сосудов, разрастающихся в разных направлениях и образующих узел или диффузное утолщение стенки органа. На разрезе опухоль состоит из полостей разной величины, заполненных лимфой. Эти опухоли имеют доброкачественное течение и при наличии клинической симптоматики могут быть удалены эндоскопически [53].
Эктопированная поджелудочная железа обычно выявляется случайно при эндоскопии, оперативных вмешательствах или на аутопсии. По данным литературы, она встречается у 1 из 500 больных, оперированных по поводу заболеваний верхних отделов желудочно-кишечного тракта. На аутопсии эктопированная поджелудочная железа выявляется в 6-14% случаев [25]. Новообразование имеет строение, характерное для поджелудочной железы, нередко на слизистой, покрывающей образование, можно визуализировать устье выводного протока. В большинстве наблюдений клиническая симптоматика отсутствует, однако возможно развитие осложнений в виде воспаления, кистозной трансформации, изъязвления, кровотечения, обтурации просвета кишки и малигнизации, что оправдывает ее удаление [48].
Обобщая изложенное выше, можно сделать заключение, что современные тенденции в лечении подслизистых новообразований желудочно-кишечного тракта сводятся к следующему алгоритму: при небольших доброкачественных бессимптомных опухолях, таких как лейомиома, шваннома, липома, гранулярно-клеточная опухоль и сосудистые опухоли, проводится динамическое наблюдение, условно доброкачественные и симптоматические доброкачественные опухоли подлежат удалению преимущественно из малоинвазивного эндолюминального доступа [16, 48, 53, 63]. При злокачественных опухолях, к которым относят и солитарные ГИСО, большинство авторов склоняются к необходимости резекции органа из лапаротомного, лапароскопического или лапароскопического трансгастрального доступа [10, 12, 23, 32, 41].
Такой дифференцированный подход к лечебной тактике при подслизистых образованиях предъявляет высокие требования к дооперационной диагностике. Эндосонография открывает новые возможности точной диагностики подслизистых образований. Первым рубежом диагностики является разграничение образований стенки и экстраорганных опухолей, деформирующих просвет полого органа [62]. Наибольшие трудности встречаются при дупликационных кистах, которые часто, особенно при расположении на задней стенке желудка, трактуются диагностами как кистозные опухоли поджелудочной железы [56]. Помимо доказательства связи образования со стенкой органа перед эндосонографией ставится задача установить предположительный диагноз, характер образования и его локализацию относительно слоев стенки полого органа, на основании чего можно косвенно судить о характере поражения (табл. 2) [25].
Совокупность этих данных играет немаловажную роль в определении лечебной тактики и метода удаления опухоли в каждом конкретном наблюдении. Основными характеристиками опухоли, определяемыми при эндосонографии, являются размер образования, эхогенность, внутреннее строение, четкость контура и слой, из которого она исходит [43, 61].
M. Miettinen и соавт. [38] на большом клиническом материале показали, что мелкие, до 2 см, ГИСО не имели метастазов, что позволяет отнести небольшой размер опухоли к прогностически благоприятным факторам. Для удобства оценки риска злокачественности опухоли L. Palazzo и соавт. [45] выделили 3 основных критерия: неровность контура опухоли, наличие в ней анэхогенных зон и увеличение регионарных лимфоузлов (последний критерий не актуален для ГИСО). Авторы отмечают, что чувствительность и специфичность каждого из этих признаков составляет 91 и 88% соответственно, достигая 100% при наличии двух признаков из трех.
В большинстве наблюдений для окончательного определения гистологического характера опухоли необходимо получение ткани опухоли для проведения гистологического и иммуногистохимического исследований. Возможности щипцовой биопсии при подслизистых образованиях значительно ограничены, а выполнение резекции части опухоли для ее гистологического исследования чревато такими осложнениями, как кровотечение из опухоли и диссеминация процесса. Транскутанная биопсия сложна при образованиях небольшого размера и может привести к диссеминации процесса, поэтому ее следует использовать только при крупных, нерезектабельных опухолях для подбора химиотерапии [14]. Тонкоигольная пункция и аспирационная биопсия под контролем эндосонографии открыли новые возможности для морфологического и иммуногистохимического анализа подслизистых новообразований. По мнению P. Chatzipantelis и соавт. [13] и M. Gu и соавт. [24], с внедрением этого метода ГИСО стали диагностировать значительно чаще. Метод позволяет получить материал для гистологического и иммуногистохимического исследований в 60-80% наблюдений [20, 60]. Многие исследователи предпочитают проведение микроскопического исследования непосредственно в операционной для первичной оценки результативности биопсии и при недостаточном количестве материала прибегают к повторной пункции и аспирационной биопсии, что позволяет достигать 100% эффективности манипуляции [8]. По данным P. Chatzipantelis и соавт. [13], гистологическая верификация диагноза при анализе мазка в операционной достигала 82,4%, в 17,6% наблюдений потребовалось проведение иммуногистохимического исследования фиксированного материала. По данным разных авторов, диагностическая точность аспирационной биопсии под контролем эндоскопического УЗИ составляет от 91 до 100% [7, 8, 30].
Подводя итог изложенному, хотелось бы еще раз подчеркнуть, что подслизистые новообразования являются широкой группой заболеваний, которая требует серьезного обследования, дифференциальной диагностики и лечения с использованием современных эндоскопических методов. В связи с выделением потенциально злокачественных гастроинтестинальных стромальных опухолей, которые считаются самыми распространенными неэпителиальными опухолями желудочно-кишечного тракта, и трудностью проведения дифференциальной диагностики их с другими неэпителиальными опухолями подход к ведению и лечению таких пациентов на сегодняшний день изменился. При выявлении во время эндоскопического исследования подслизистых новообразований необходимо дифференцировать их от сдавления органа извне с помощью других уточняющих методов исследования, таких как УЗИ, КТ, МРТ. Однако самым точным методом диагностики, позволяющим определить органную принадлежность опухоли и слой стенки полого органа, из которого она исходит, является эндосонография, данные которой определяют выбор метода лечения подслизистых новообразований желудочно-кишечного тракта.
Мы считаем, что выявленные подслизистые образования необходимо удалять с последующими гистологическим и иммуногистохимическим исследованиями. Исключения составляют диссеминированные формы ГИСО, при которых необходимо проведение комплексного лечения в специализированных стационарах. Вместе с тем при наличии мелких бессимптомных образований, не имеющих признаков злокачественности, особенно исходящих из мышечной оболочки пищевода, возможно динамическое наблюдение. При этом мы руководствуемся тем, что ГИСО для пищевода наименее характерны, а радикальное удаление опухоли, исходящей из мышечного слоя, требует резекции стенки органа, т.е. торакоскопии или торакотомии. Таким образом, имеется несоответствие риска оперативного вмешательства и риска прогрессирования заболевания. При выборе хирургического доступа необходимо руководствоваться размером опухоли, ее распространенностью за пределы органа и наличием признаков злокачественности. Пограничные опухоли или вызывающие те или иные жалобы у пациентов подлежат удалению по возможности из малоинвазивного доступа. Способ удаления следует выбирать, принимая во внимание слой стенки органа, из которой исходит опухоль. При локализации опухоли в мышечной пластинке слизистой или в подслизистом слое предпочтение следует отдавать эндоскопическим методам лечения. Если опухоль исходит из мышечного слоя, необходимо выполнять лапароскопическую резекцию. При наличии признаков злокачественности, выявляемых при эндосонографии, следует производить операцию лапаротомным способом, используя широкую резекцию с лимфаденэктомией.
В заключение хотелось бы сказать, что благодаря появлению такого метода эндоскопического исследования, как эндосонография, подход к диагностике и лечению пациентов с подслизистыми образованиями желудочно-кишечного тракта претерпел значительные изменения. Точность в постановке верного диагноза увеличилась в разы, что обусловливает улучшение исходов лечения данной группы пациентов.